(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПИРАЗОЛО- l,2-b -ФТАЛАЗИН-1,5-(1ОН)-ДИОНА
1
Изобретение относится к способу получения новых гетероциклических соединений, обладающих ценными фармакологическими свойствами.
Способ основан на известной реакции взаимодействия фталазина с соединениями, содержащими активный атом галогена.
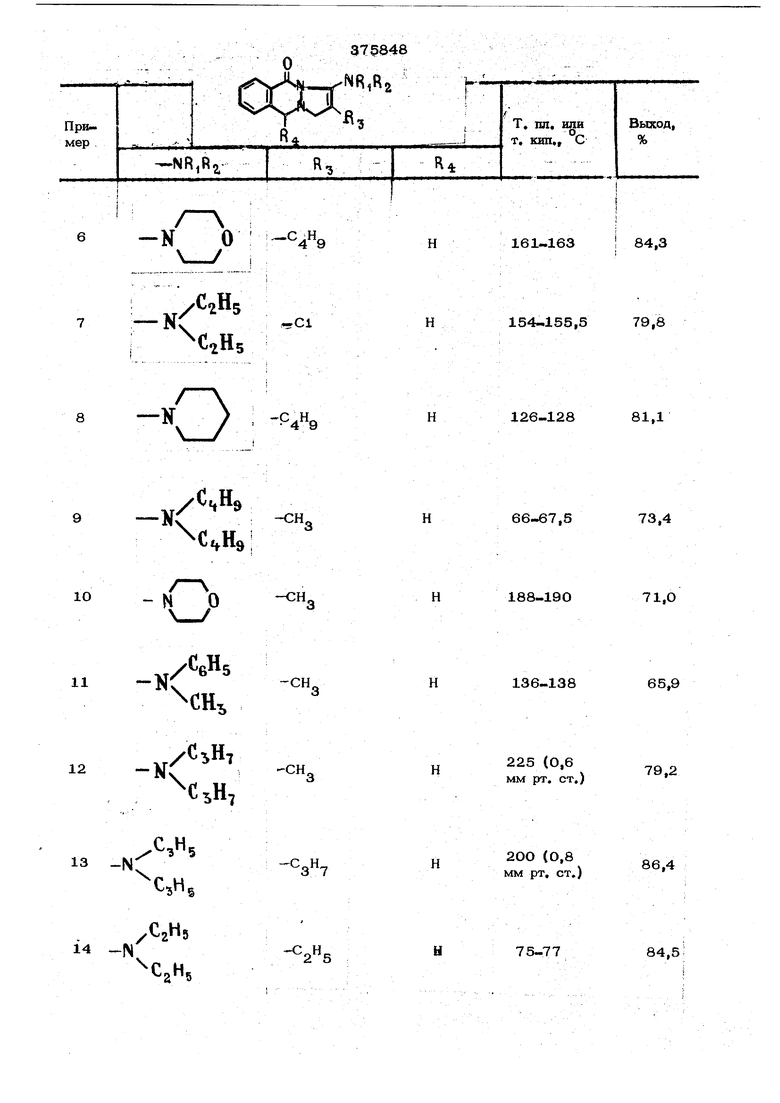
Описываемый способ получения производных пиразоло- 1,2-ЬЗ -4 алазин 1,5-(1ОН)-диона общей формулы I
N KjH.
Нг) вместе с соседним атомом азота образуют гетероциклическое кольцо, с li-2 гетеро- атомами;
атом водорода, галоид, низший алкил, арил или ашшради- кал; Яд- атом водорода, низший алкил
или арилрадикал.
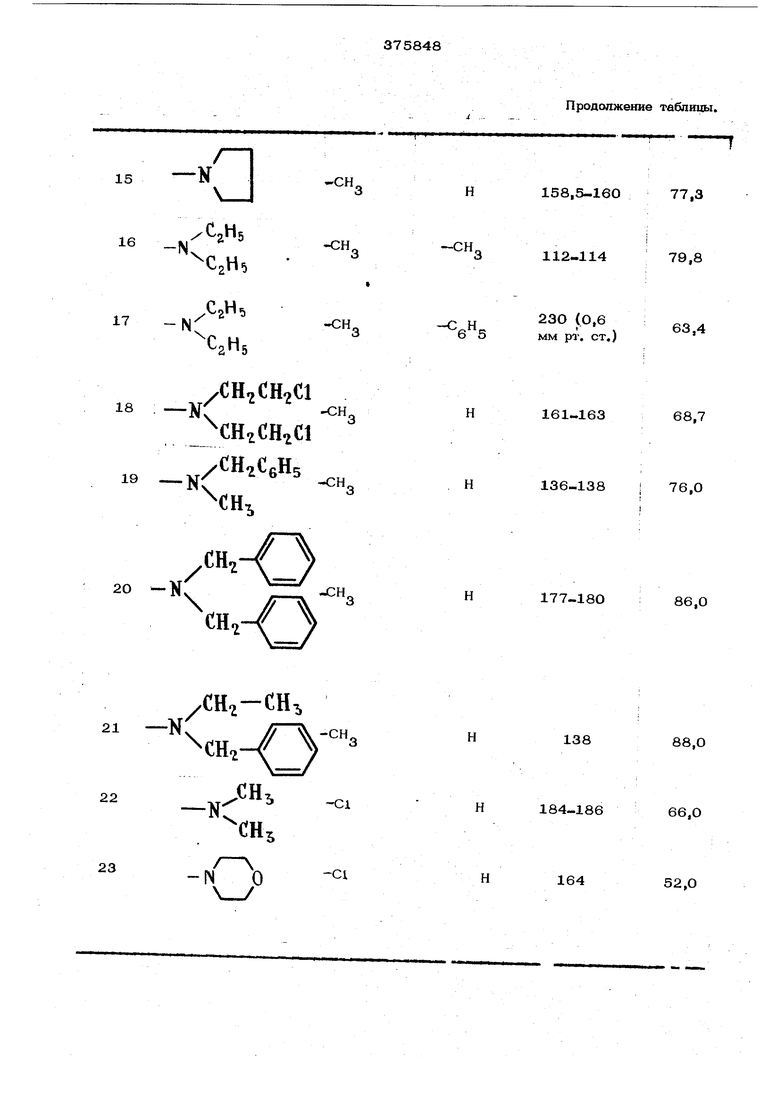
Способ заключается в том, что производные 3,4-дигидро-1(2Н)-фталазинона общей формущд; II
О
,где R. Fl - каждый означает атом водорода, низший алкил, галоид (низший) алкил, аралкил, арил и ацилрадикал или
где Яд- имеет приведенные вьпие значения, подвергают взаимодействию с эквимолярным количеством производного ацилхлорангидри- да карбоновой кислоты формулы 111 где R , R Rl имеют приведенные выше для радикалов R R. и R соответётв ющие значения, кроме атома водорода и ашшрадикал Процесс обьдчно проводят при комнатной температуре в инертном оргатзшёск ы. растворителе в присутствии третичного амина. В зависимости от применяемого адшшюрангидри ца время реакции может быть различным, в основном оно колеблется от 2 до 6 час. . В качестве растворителей применяют бензол, толуол, ксилол и другие ненасыщенные углеводороды, эфиры - диоксан и тетрагидрофуран. Предпочитаемыми третичными аминами являются три (низшие)ал- киламкны - триметиламин, триэтиламин, можно также применять и другие алифатические амины - трио-( -гидроксиэтил)- амин или гетероциклические амины - шшерадин или морфолин. Полученные по вышеописанному методу пиразолфталазиноны можно по желанию под вергать дальнейшей обработке, для того чтобы модифицировать связанные с пяти томным кольцом группы заместителей, Эти модификации проводят известными методами, например, подвергая соединение фо1 мулы I, где R сэбозначает.хяор. мягкой о ...: ;.-- .-: . - /- гидрогенизации, желательно при юэлшатной температуре и атмосферноТГдавлении, в пр сутствии катализатора - палладий на угле, получают соответстаующий 2-лезамещенны пиразолфталазинон. Его можно ацилировать в положении 1 при помощи обьмнохю ацили рующего средства как хлорангидрид карбоновой кислоты. При гидрогенизации N -бензиламиноипи N , N -дибензиламинопроизводного формулы I в более сильных условиях бензи остатки отщепляются. Предпочтительно гидрогенизацию ведут в растворе низшего спирта при температуре 50-1ОО°С, под давлением 1О,-йО атм и в присутствии палладия на угле в качестве катализатора. Свободные аминосоединения можно далее подвергать ацилированйЪ11о обычным мето дам, получая таким образом ацетиламиноили диацетиламинопроизводные. Пиразолофталаз1шоны, полученные описанными методами, приведены ниже. 2-Метш1-3-дипентиламино-1Н-пиразоло- 1,2-ьЗ -фталазин-1,5-( ЮН )-дион. 2-чметнл-3-ди-трет -пентипамино-IH- пиразоло- Г1,2-Ь -4|талазин-1,5-.(1ОН)-. дион, 2-фенил-3-дйбутияамино-1Н-.пиразал& 1,2-bJ -фталазин-1,5-(1ОН).ион, 2-4 ени№-3 пирролидино-1Н-пиразоло-. - 1,2-Ь -фталазин-1,5-(1ОН)-чДион, 2-фенил 3-пииеридино-.1Н« 11фазоло-. 1,2-Ь -фталазин-1,5-(1ОН)-дион, )енщ&-3 4ъ1Орфолино -1Н-лиразоло- 1,2-ЬЗ -Фталазин-1,5-(1ОН)-дион, 2-хлор-5.ипрошшаминО|-1Н-4шразолс. 1,2-.ь1 -4талазин-1,5-(1ОН)н1ион, 2-хпор-Зчхибутнламино- Н-лиразоло l,2-t; -фталазин-1,5-(1ОН)ион, 2-хлор-3-{ N -фени№- N -метиламино)1Н-пиразоло- 1,2-ЬЗ -4талазин-1,5-(1ОН). дион, 2-ошо; -пирролидино-1Н-пиразоло- 1,2-ьЗ Н)талазин-1,5«.(1ОН)-дион, 2-хло1 - 1орфолино-1Н-пиразоло- 1,2-Ь -фталазш1-1,5-{1ОН)-дион,; 2-метил-3-пиперидино ч1ОрМетип-1Н- . пиразрло- 1,2-Ь -4 талазин-1,5-(1ОН)- i дион, 2-хлор-3-диэтшшмино-1О-метш1-1Н-пиразоло- 1,2-ьЗ -4)талазин-1,5-(1ОН) 2-хлор-3-пирролидино-1О-метил-1Н- .пиразоло- Г 1, -фг лазин-1,5-(ЮН)- 2-метш -3-пипервдино-1О-фенил-1Н- ; пиразоло- 1,2-ЬЗ -фталазино-1,5-(1ОН)-дион, 2-метшь-3 1иэтиламино-10-4еншь-1Н- -пиразоло- 1,2-1)3 -фталазино-1,5-i (10Н)-дион,i 2 ijyioi -пирррладино- О-фенил-1Н- пиразоло- 1,2-ь -фталазин-1,(1ОН)- -дион. Пример 1. 2-Метшь-3-диэтилам но-1Н-пиразол1 - Г 1,2-ьП Ц)талазин-1,5-(1ОН)-дион. К раствору 98,5 г 3,4-дигидpo-l(2H)-фтaлaзинoнa и 157,7 г триэтиламина в 4,6ОО мл безводного толуола, предварительно охлажденного до О С, медленно прибав- ляют в течение ЗО мин 163 г 2-(с| хлор- Л-диэтиламинометилиден)-пропионил- хлорида в 5ОО мл безводного) толуола. Teivt пературу повышают до комнатной и реак;ционную смесь перемешивают в течение 2 час, затем отфильтровывают, промывают три раза водой и сушат над сульфатом нат- рия. Растворитель отгоняют в вакууме и -1...-- - .--... . . I . статок кристаллизуют из ацетона. Выход 132,4 г (69,6 % )2-.метил-3-диэтш1амиО-1Н-пиразоло- 1,2-bJ -фталазин-1,5-( iOH )-дйона; т. пл. 12 5-12 7 .
б6
Пример 2. 2-Бутип-3-диэт1Июмино-: ., Пример 4. 2-Бути}иЗ- иметш1а-1Н-пиразоло-Г1,2-Ь1 Ч талази -1,5-йино-1Н-пиразоло- 1,2-Ь -фталазин-(10Н)-дион.11,5-(10НМион.
14,8 г 3,4 игидро-1(2Н)-фталазинонаПо описанному в примере 1 способу,
растворяют в смеси 29 млтриэтиламнна и1 Sприменяя 12,7 г 3 4 игкдро-1(2Н).300 мл безводного диокрана и подвергают i- алазинона и 19,30 г а-(а-ослор-0
заимодёйствию УзЗ г 2-|1-хпор-о1-Диэтип--диметш1аминометш1вден)-капрохлоркда,
минометилиден -капроилхлорЙда в 100 мл получают 20,1 г (78,2%) :2-бугил- безводного толуола при по описан--Диметкламино.1Н-«иразоло- 1,2-5 HOKiy/B примере 1 способу. Выход 24,5 г Ю H-ana3im-l,5-{lOH)-AHOH; т.пл. 114,5(75,0%) 2-бутш1 -3-диэтиламино-1Н-пиразо-L с г, о
Г 1 о +,П л 1 с tif Tj Пример 5. 2-4 енил-3-диметш1а-.
ло- 1 1,2-Dj -фталазин-1,5-(1ОН)-дио- „ г -i о т л.
- - An Ьл мино-1Н-пиразоло- I 1,2-Ь | -фталазинна; т. пл. 190 С (0,6 мм рт. ст.). ,, с Пон п„гчн uj -чПример 3. 2-Метил-3 иэтш1ами--1,&-Ыин; ион.
lu г 1 о t.-i i 1 г- 15По описанному в примере 1 способу,
но-1Н-пиразоло- Г 1,2-Ь J -фталазин-1,5- .„, ои -i/ou
-(1ОН)-.пион t J применяя 19,1 г 3,4 аигидро-1(2Н)п /1 «; i-фталазиноца и 45 г 2-(о( -хлор-q -диПо описанному в примере 1 способу,
применяя 14,8 г 3,4 игидро-1(2Н)-метиламинометилиден)-2.4енилацетюш1о.талазинона g. 18,2 г 2-(а ор-а- .ЖиГЙ Н Н-пи оЙ -диметиламинометилиден;-прошюнилхлрри- - J
да получают 20,8 г (81,0%) 2-метил -3--фталазин-1,5-(1ОН)дион;т.пл,, 152-153
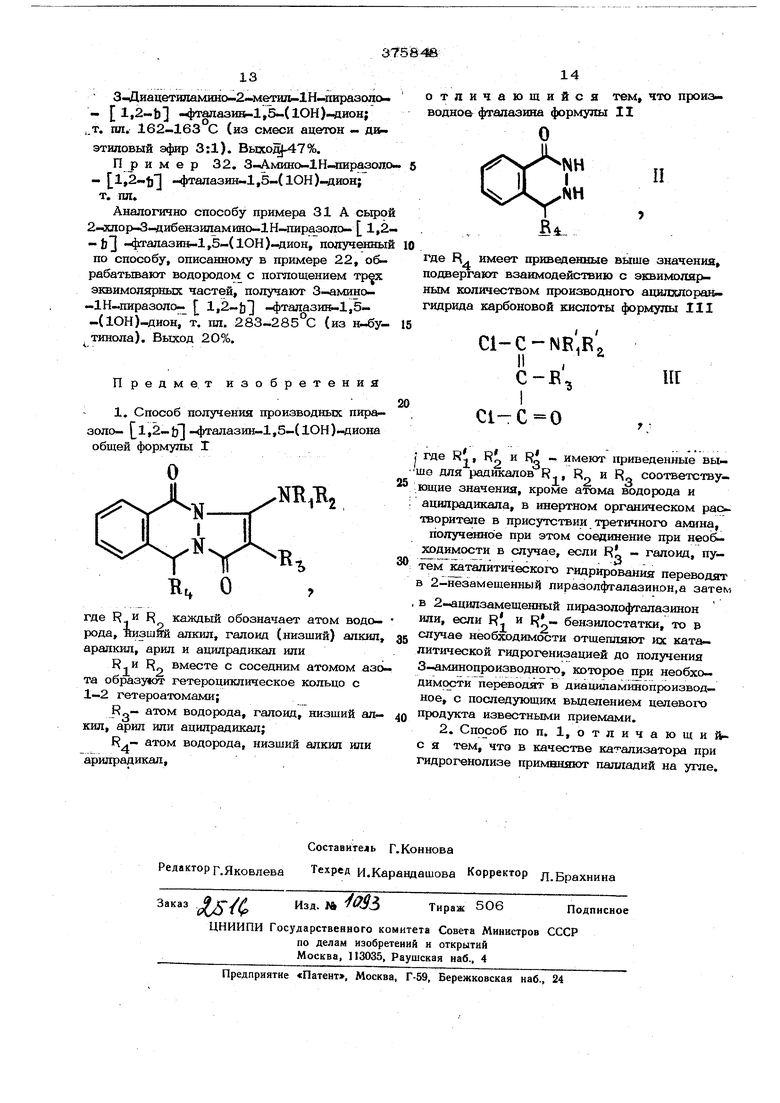
-диметиламино-1Н-пиразоло- 1,2-и -В таблипе приведены соединения, полу- i -фталазин-1,5-(юн)-дион; т.пл. 142-144С. ченные по описанному в примере 1 способу.
375848
О
8
н
126-12881,1



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных индола или их солей | 1970 |
|
SU444362A1 |
| Способ получения фталазино /2,3-в/ фталазин-5(14н),12(7н)диона | 1974 |
|
SU520916A3 |
| Способ получения производных хинолина,их солей или их изомеров | 1974 |
|
SU535034A3 |
| Способ получения трициклических пиридонпроизводных | 1988 |
|
SU1598879A3 |
| 7-Амино-3-замещенный метил- @ -цефем-4-карбоновая кислота в качестве промежуточных продуктов в синтезе 7-ациламидоцефалоспоринов,проявляющих антибактериальные свойства | 1983 |
|
SU1350166A1 |
| Способ получения производных бензодиазепина или их солянокислых солей | 1981 |
|
SU1170971A3 |
| Способ получения 4-(бициклогетероциклилметил)пиперидинов или их фармацевтически приемлемых солей присоединения кислот | 1985 |
|
SU1396964A3 |
| Способ получения производных бензопирана или их солей | 1978 |
|
SU741797A3 |
| Способ получения конденсированных производных пиразоло[3,4- @ ]пиримидина | 1988 |
|
SU1739850A3 |
| Способ получения тиено(1,5) бензодиазепинов или их солей | 1974 |
|
SU629879A3 |

,,
Ж-сн.
9
1О
-сн.
- N О
/СпНе V/
N
-сн.
СН,
12
13 N
14 -IS
н
66-67,5
73,4
н
188-19О
71,0
н
136-138
65,9
79,2
86,4
84,5;
20 N
-сн.
сн.
/ сн,
-N
-сн.
,сн
-С1
-N
.
сн
23
IN ОПродолжение таблицы.
н
177-180
86,0
н138
88,0
Н184-186
Н
164
52,0 Пример 24. 3-Диэтиламино-1Н-пиразопо- 1,2-.Ь фталазин-1,5-{1ОН 1,5 г 2-«лор-3-лиэтипамино-1Н-1Шразо , л 4b,. --- .f Г 1.2-bl -фталазшь-1,5-(10Н)-диона .„„ растворяют в 150 МП ледяной уксусной кислоть и обрабатьтают водородом в npifrсутствии 0,75 г 1О%-ного палладия на угле в качестве катализатора, затем смес фильтруют и фильтрат вьшаривают в вакууме досуха. Остаток, состоящий из 3-ди этиламино-1Н-гафазолр- 1,2-Ь -фтала зшь-1,5-(1ОН)-днона, кристаллизуют из ацетона. Выход 1,18 г (88,7%); т.пл. 135-137°С. Прим е р ы 25 и 26. Соединения получают по способу, описанному в пример 24. Получают 3-диметиламино-1Н-пира- золо- 1,2-ьЗ н алазш.1,5-(юн)- -дион, т. пл, 171-173 С (из ацетона). Выход 85%. 3-Морфолино-1Н-пиразоло- 1,2-Ь1 -фталазин-1,5-(1ОН)-дион; т. пл. 235238 С (из этанола). Выход 87%. Пример 27. 2.-Ацетил-3.иэтил„,„,„ 1 иг -1 л -1 , амино-1Н-пиразоло- | 1,2-Ь| -фталазин1 ч ( г,I J j«,b-V-i- nу-ДИОН 4 г 3 иэтипамино-1Н-пиразоло- 1,2 -Ь -фталазин-1,5-(1ОН)-диона ацилируют в течение iVs час в 8 мл ацетилхлорида. Затем избыток второго реагента отгоняют в вакууме, остаток растворзаиют в 200 stn бензола и бензольный раствор промьшают сначала 1О%-ным водным раствором бикарбонааа натрия, затем водой. Органическую фдзу отделяют, сушат над сульфатом натрия и бензол дистиллируют в вакууме. Остаток, состоящий из 2-ац. Т1Ц1-3-диэтш1амино-1Н-пиразоло- 1,2- ь -фталазин 1,5-( ЮН )-йнона перекристаллизовываю - из метанола. Выход 3,7 г (8О,0 т. пл. 174-176 С. Пример 28. 2-Ацетил-З-диметип амино-1Н-пиразоло- 1,2-Ь -фталазин-1,5-(10Н)-дион. j По описанному в примере 27 способу, исходя из 3-диметиламино-1Н-пиразоло- - (1,2-Ь1 -фталазин-1,5-( ЮН)-диона, получают 2-ацетил -3-.диметиламино-1Н-пиразоло- 1,2-ьЗ -фталазин-1,5- -(1ОН).. гш. 201-2О4°С (из ме.танола). Выход 63%. Пример 29. А. 2-Метш1-3-метш1|амино-1Н-пиразоло- 1,2-ь -фталазш -1,5-(10Н)-дион. 6,6 V 2-метш1-3-( N -бензил- -метиламино)-1Н-пиразоло- j 1,2-b -фта лазин-1,5-(1ОН)-диона раствЬряют в 1ОО, МП этанола и обрабатьтают водородом в течение 7 час при 75 С, давлении 35 в присутствии 0,8 г палла гттугт TIQ mrtf VQV VQf lTTtr4fl«TV knft (f дня на угле как катализатора. Затем смесь фильтруют и раствор концентрируют досу- Jxa в вакууме. Остаток перекристаллизо- вывают из метанола, получая 3,1 г (64,ДО) ;2-метизь-3-метипамино-1 И-пиразол 1,2- -|| -фталазивь-1,5-(1ОН)-диона; т. пл. 207-2О9°С. Б. 2-Метил-3-( N -ацетил- N -метил)амино 1Н-1Шразоло- 1,2-tfj -фталазин-1,5-(1ОН)н1ион. Соответствующее З-ЬГ -ацетшшроизводное получают путем обра- ботки полученного в п. А соединения хлор ангидридом или ангидридом уксусной кисло:.ты в присутствии избытка триэтиламина ; обычным методом; т. пл. 216-218 С (из ацетона). Выход 85%. ПримерЗО. А. 3-Этш1амино-2-метил-1Н-пиразоло- { 1,;2-Ь -ч|)Талазин-1,5-(1ОН)-дион. Соединения получают по описанному в примере 29 способу. З-Этил- амино-2-метия-1Н-пиразоло- Г 1,2-hi - ,-t,-./i/, «фталазин-1,5-(1ОН)-дион плавится при Q1 - 151-152 С (из этанола). Выход 79%. Б. 3-( N -ацетил-N -этил)-амино-2-метш1-1Н-ииразоло- 1,2-Ь1 -фталазин-1,5-(1ОН)-дион. 3-( N -ацетил-N -этил)-амино-2-метш1-1Н-пиразоло- 1,2-й -фгалазин-1,5-(1ОН)-дион плавится при 151-154 С (из ацетона). Выход 91%. Пример 31. А. З-Амино-2-метшь1Н-пиразоло- 1,2-ЬЗ -фталазин-1,5-( ЮН)-дион. Аналогично способу, описанному в примере 29, З-дибензиламино-2- -мет1ш-1Н-пиразр1 ки L -фталазин-1,5-(1ОН).4йирк. обрабйТРЫйают водородом в течение;7: ар 1ри 100°С и давлении в 5О атм (поглощается две эквимолярные части водорода) и получают 3-амино-2-метил-1Н-пиразоло- 1,2-ьЗ -фталазин-1,5-(ЮН)-дион;т. пл. 241-245°С (из этанола). Выход 75%. Б.. 3-Ацетиламино-2-метил-1 Н-пиразо- о- 1,2-Ь1 - } талазш1-1,5-(1ОН)-дион и 3-диацетиламино-2-метил-1 Н-пиразоло- -|lli2-tj -4талазин-1,5-(1ОН)-дио1и 3-Ацетиламино- и З-диацетиламинопразводные получают обработкой оцлой или двумя соответственно частями ацетш1хло- рида и избытком триэтиламина. 3-Ацетил амино-2-метил-1Н-пиразило- 1,2-Ь -«Ьтелазин-1,5-(1ОН)-днон; .пл, 220-222°С (из ацетона). Вых.зд 41)%. -3 иацетиламино-2-.метшь-1Н- иразопо-. - l,2-.b -ч})талази -1,5-(1ОН)-лион; ,.т. пп. 162-163°С (из смеси ацетон - диэтиловый эфир 3:1). Выход}-47%. Пример 32. 3-Амино.1Н-пиразоло ,2-lj -фталазин-1,5-(1ОН).ион; Аналогично способу примера 31 А сыро 2-.;г Лор-3-дибензиламино-1Н-пиразоло- 1,2 -frl -фталазин-13-(1ОН)-дион, полученны по способу, описанному в примере 22, обрабатывают водородом с поглощением ЭКВИМОЛ5ФНЫХ частей, получают 3-амино-Ш-пиразоло- 1,2-Ь1 -фтал зи -1,5-(1ОН)-дион, т. пл. 283-285 С (из н-бутинола). Выход 20%. Предмет изобретения 1. Способ получения производных пиразоло- 1,2-Ь -фталазин-1,5-(1ОН).иона общей формулы Г где R и F каждый обозначает атом водо- рода, низший алкил, галоид (низший) алкил аралкил, арил и ацилрадикал или F вместе с соседним атомом азо та образуют гетероциклическое кольцо с 1-2 гетероатомами; атом водорода, галоид, низший ал- кил, арил или ацилрадикал; атом водорода, низший алкил или арилрадикал,. о т л ичающийся тем, что производное фталазина формулы II где R. имеет приведенные В1лше значения, подвергают взаимодействию с эквкмопярным количеством производногх) ацилхпоран- гидрида карбоновой кислоты формулы III , II , С -В-5 где R , R и R - имеют приведенные выо для радикалов R, R и f{ соответствующие значения, кроме атома водорода и ацилрадикала, в инертном органическом растворителе в присутствии третичного амина, полученное при этом соединение при нео&. ходимости в случае, если R - галоид, пу- - - .... ii тем каталитического гидрирования переводят в 2-незамещенный пиразолфталазинон.а затек в 2-йцилзамещенный пиразолофталазинон или, если R и R - бензилостатки, то в случае необходимости отщепляют их каталитической гидрогенизацией до получения 3-аминопроизводно1Х), которое при необхо- димехзти переводят в диациламинопроизвод- ное, с последующим вьщелением целевого продукта известными приемами. 2. Способ по п. 1,отличающи{ с я тем, что в качестве катализатора при гидрогенолизе применяют палладий на угле.
Даты
1973-01-01—Публикация