Изобретение относится к области получения новых производных изоксазола, имеющих улучшенные .свойства по сравнению с соединениями аналогичного действия, нрименяемымн В фармацевтической промышленности.
Предлагается основанный на широко известной реакции реакционноспособного производного кислоты с азотсодержащим соединением, например с мочевиной, способ .получения нроизводных изоксазола общей формулы I
CH-C-CO-N-СII II ,Сч/К
R, Y
к:Г о
где RI и R2 -атом водорода, аякил или щиклоалкил, имеющие не более И атомов углерода (например, .метил, этил, изопропйл, трег-бутил, амил, циклопропил, щиклогексил, адамантил, октил);
Ra и R. - атом водорода, алкил или циклоалкил, имеющие «е более 11 атомов углерода (например, метил, этил, изопропил, трет-бутил, амил, циклопропил, циклогексил, адамантил, октил), арил, имеющий -не более 15 атомов углерода (напри-мер, фенил, толил, нафтил), аралкил, имеющий не более 20 атомов углерода (например, бензил, фенетил, яаф/А,
тил, метил), илн группа -N;
вместе
R.
образуют гетероциклическую группу, которая молчат содержать другой атом азота н/илн кислорода;
Y - ОКСО-, Т1ИОКСО- или иминогруппа.
Способ заключается в том, что реакционноспособное проивводное изоксазолилкарбоновой кислоты общей формулы П
сн-с-сох
г ii (И)
нГ V
где X - остаток аниона карбоновой кислоты, такой как атом галогена (хлор, бром, йод), алкокси- или арилоксигруппа (метокси-, ЭТОКСИ-, паранитрофеноксигруппа), или остаток ангидрида (ацетоксигруппа);
RI имеет указанные значения,
подвергают взаимодействию с соединением общей формулы III
TJ
HNR-f-C-NC (Ш)
Ri
Y
3
где R2, Rs, R:i, Y имеют указанные значения.
Продесс по описываемому способу осуществляют при реакднн походного соедппепня формулы (II) с пропзводным мочевпны формулы (1П) прп О-150°С, лучше npci iO-90G, в инертном растворителе. К пригодпым инертным растворптелям относятся иизшпе €ннрты жнрното ряда (например, метанол, этанол, изопропанол), низшие галоидалканы (напрпмер, хлордстын метплеп, хлороформ, хлоршстый этилен, четыреххлористып углерод), ароматпческне углеводороды (например, гексан, петролейный эфир, цпклогексан), ароматпческие третичные основаиня (например, ииридин, пиколдн, коллиднн), диметилформамид, диметнлсульфокспд и гексаметилфосфамнд. Для ускорения конденсации можио применять соответсвующие добавки, например, алкоголяты щелочных металлов (метилат натрия, этилат .калия), алифатиче.ские третичные ампны (например, триэтиламин), ароматические третичные основания (например, пиридии, лутидни) и соли щеиточных металлов (дапример, бикарбонат натрия, ацетат лития, карбоиат кальция). Реакцию можно проводить обычным способом, как при получении уреида.
Реакция кон.аенсации может протекать легко с образованием эффективного дроизводного 3-изоксазолилуреида формулы (I) С хород1им выходом.
Исходную реакционную форму изоксазол-Зкарбоновой кислоты можно получить, иаиример, нрн 1,3-диполярном циклодрисоединении винилэтилового э(фи|ра нли виниладетата к алкилхлорокеиМинацетату в нрисутствии триалкиламина и последующем удалеии1И этанола или уксусной кислоты, соответственно, или при реакции конденсадии сложного эфира 2,4-дикетоалифатической кдслоты с гпдроксиламином в условиях замыкания кольца с последующим преобразованием полученного продукта в желаемую активную форму.
Пример 1. К суснеизии 5-метилпзоксазол-3-карбоновой кислоты (130 вес. ч.) в бензоле (1000 об. ч.) добавляют хлористый тонил (150 вес. ч.) « пиридин (10 об. ч.) прп непрерывном перемешивании, поддерживая температуру ниже 20°С. Полученную смесь ностененно нагревают и кипятят с обратным холодильником в течение 3 час. Затем для удаления растворителя и оставшегося реагеита смесь выпаривают досуха при пониженном давлении; остаток обрабатывают холодным бензолом (500 об. ч.) и фильтруют.
К полученному раствору хлорангидрида 5-метилизоксазол-З-карбоновой кислоты в бензоле в течение 1 часа при перемешивании и
Отношение частей к объемным такое же, как отношение грамма к миллилитру.
охлаждении льдом прикапывают раствор N-изoпpoпилмolleвипы (85 вес. ч.). С.:есь выде))живают п|Л1 20С и течение 12 час, liaijiCвают до и выпаршкиот досуха п) v.oпнжепном давленнн. Остаток об)аиатывг11(гг холодной водой (1000 об. ч.) и получают сырой продукт в виде К-(5-: етил-3-изокСазолнЛкарбонил -К-нзопропилмочевины (110 вес. ч.). Этот продукт перекристаллизовываю из
смеси хлористого метилеиа и бензола и получают бесцветные иглы с теми. ил. 164-165°С. ИК-спектр (нужол): 3315, 3280, 1685- 1697 cм-. Пример 2. Реакцию -проводят апалогпчпо при.меру I с заменой изопропплмочсч/ипы бутилмочевииой. Получают N- (5-метил-З-изоксазолилкарбонил)-N- бутилмочевину в ви.че бесцветных призм с темп. пл. 139-ИО С. ИК-сиектр (нужол) : 1696 ).
Пример 3. Реакцию проводят аналогично примеру 1 с заменой изопроп-ллмочевины диклогексилмочевииой. Получают N- (5-мет 1л3-изоксазолилкарбонил) - N-диклогексил.мочевииу в форме бесцветных пластинок с
темп. пл. 180-180,5°С (перекристаллизоваи из метадола). ИК-спектр(1ужол):
1690 64j-i().
Пример 4. К раствору эт ;лата цатрия (75 вес. ч.) в безводном этаполе (500 об. ч.)
добавляют при перемешивании и охлаждении хлоргидрат гуанидииа (96 вес. ч.) и получают этанольный раствор свободного гуапидпна. К этому раствору в течение 2 час при перемешивании и 40°С добавляют раствор этил-5метилизоксазол-3-карбоксилата (135 вес. ч.) в водном этаноле (200 об. ч.). Получениую смесь выдерживают в течение 12 час при 20°С. Выпавшие в осадок кристаллы отфильтровывают, промывают иебольшИ М количестBOjM воды и перекристаллизовывают из этанола. Получают 1-(5-метил-3-изоксазол1Илкарбо|иил)-гуанидиц в виде бесцветных призм с темд. пл. 192-192,5°С с разложением. ИК-спектр (пужол) ; 1652 с.и-()Пример 5. Реакцию проводят аналогично примеру 1 с заменой изолропилмочевины свободной мочевиной в толуоле при 80-ПО°С. Получают N- (5-метил - 3 - дзоксазолилкарбонил)-мочевииу в виде бесцветных игол с темп.
пл. 238,5°С с разложением. ИК-спектр (нужол): 1701, 1663 см.
Пример 6. Реакцию нроводят аналогично примеру 5 с заменой мочевины тиомочевиной. Получают N- (5-метил-З-изоксазолилкарбонил)-тиомочевИНу в виде бесцветных игол с темп. пл. 218-218,5°С е разложением. ИК-спектр (нужол) : 1699, 1610 ().
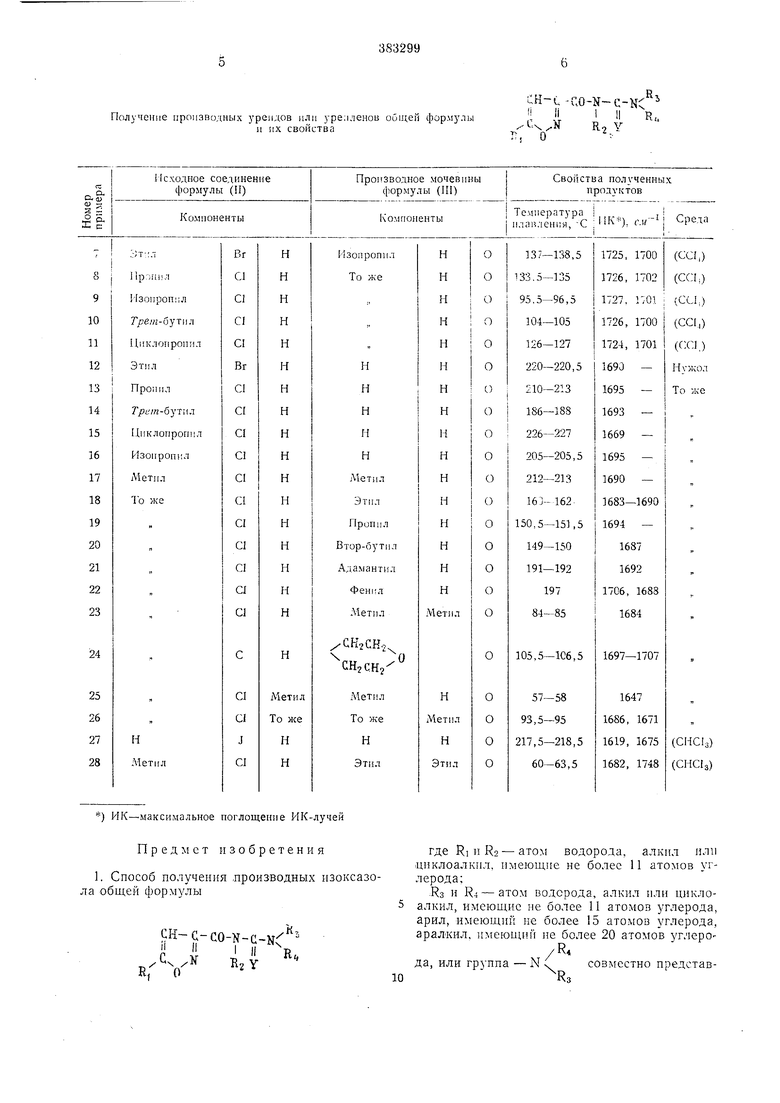
П р и м е р ы 7-28. Реакцию проводят аналогично примеру 5. Получают соответствующие
дроизводные уреидов или уреиленов, указанные в таблнде.
Получение производных урендов или уре: лено1з общей формулы
и их свойства
-CO-N-C-NC
J.J i «
R2 Y
м О


) ИК-максимальное поглощение ИК-лучей
Предмет изобретения
cH-c-co-K-cV
srV «
где RiiiRo -атом водорода, алкил или |циклоалк11л, имеющие не более 11 атомов углерода;
.Rs и R4 - атом водорода, алкил или циклоалкил, имеюи1ие не более 11 атомов углерода,
арил, имеющий не более 15 атомов углерода,
араЛКил, имеющий не более 20 атомов углероR4
Ссовместно представда, или группа - N
Нз ляют собой гетероциклическую группу, которая может иметь еще ато.л азота и/или кислорода;Y - окео-, тиоксо- или иминогруппа, отличающийся.тем,, что реакционноспособное ироизв(нре,..1зЪксазЬлкарбоновой киелоты -; :йюб1це№|) -. ..,.Ш|1Шй с-аох S.. А .:- нГ сГ где RI имеет указанные значения; X - анионный остаток карбоновой кислоты, такой как атом галогена, алкоксн- или арнлоксагруппа, или остаток ангидрида, такой как ацетоксигруппа, .подвергают взаимодействию с производным мочевины общей формулы HNRrC N: II в которой Rs, Кз, R4, Y имеют указанные значения, с последующим выделением продуктов известным способом. 2. Способ по п. 1, отличающийся тем, что процесс ведут в среде органического растворителя. 3. Способ по п. 1, отличающийся тем, что процесс ведут при 20-90°С.

Авторы
Даты
1973-01-01—Публикация