Изобретение относится к способу получения новых производных фенилуксусной кислоты общей формулы I С - СООН где X - атом кислорода или серы, R - линейный или разветвленный алкилиден, содержащий от 1 до 4 атомов углерода, Hal- атОМ хлора, брома или фтора, а также сложных эфиров этих 1кнслот 1или их солей, которые обладают ценными фармакологическими свойствами и могут быть попользованы В медицине в качестве фарма цевтических 1преиаратов. Известен юпособ получения галоидпроизеодных фенилуксусной кислоты взаимодействием галоидзамещенного ;бензилгалогенида/ с ии-( анидом щелочного металла и последующим гидролизом лолученного нитрила до галоидзамещенной фенилуксусной кислоты. Однако в литературе отсутствуют данные о получении соединений общей формулы I, обладающих Ценными фармакологическими свойства мп. Предлагается способ получения новых производных фенилуксусной кислоты общей формулы I, а также сложных эфиров этих кислот или их солей, заключающ 1Йся в том, что, соединение общей формулы И где X имеет вышеуказанное значение, подвергают адетилированию -ироизводным кислоты RI-СООН, где RI-линейный или разветвленный ал;кильный радикал, содержащий от I до 4 атомов углерода, в присутствии кислоты Льюиса и полученное три этом соединение формупы III
обрабатывают нитрующим реагентом с получением соединения формулы IY
CO-R,
где Х - атом кислорода или ато-м окисленной серы,
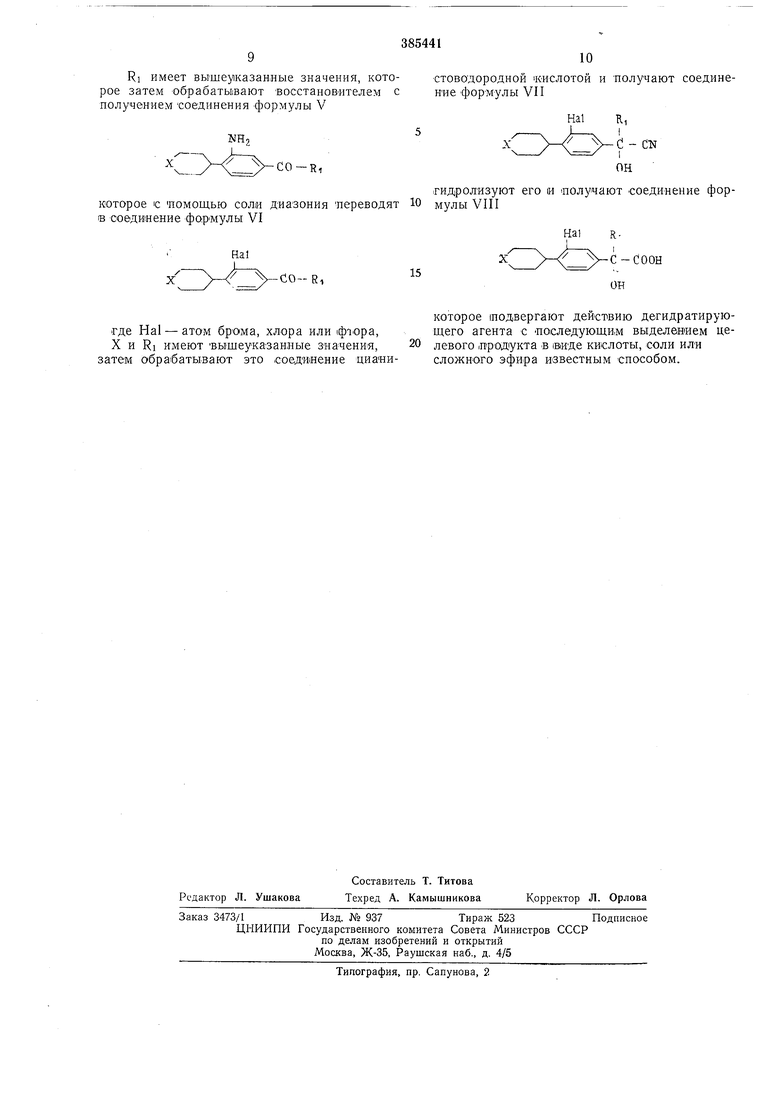
RI имеет вышеуказанные значения, которое затем обрабатывают воостановителел с получением соединения формулы V
«оторое с (ПОМОЩЬЮ соли диазония переводят в соединение формулы VI
лде Hal - атом брома, хлора или фтора,
X и RI имеют вышеуказанные значения,
затем обрабатывают это галоидированное
шроизводиое цианистоводородной кислотой и
получают соединение формулы VII
В качестве ацетилирующего средства предпочтительно используют .ПрОИЗВОДИОС КИСЛОТЫ
RI-СООН, как-то хлорид, бромид или ангидрид кислоты.
Реа-кцию цианистоводородной Кислоты с соединением формулы VI проводят в присутствии третичного основания, например пиридина или лутиднна. Переводциангидрииа формулы VII в соответствующую кислоту -формулы VIII путем гидролиза может быть произведен в одну или в две стадии с Выделен-ием иромежуточноО:бразовавщвгося амида.
Последнюю стадию способа - дегидратацию кислоты формулы VIII для получения
соответствующей а-алкилидеикислоты формулы I - осуществляют при помощи дегидратирующего средства, например серной кислоты, фосфорной кислоты, фосфорного ангидрида или, предпочтительно, п-толуолсульфокислоты.
Целевой продукт выделяют -в виде кислоты, соли или сложного эфира. Перевод 1кислот в соответствующие соли или сложные эфиры осуществляют по известным способам, независийЮ от того желают ли получить соль с минеральным оонованием, в частности едким натром или едким «али, или с органическим осиованием, например триэтиламином.
Для получения сложного эфира этих кислот предпочтительно используют диазометан в -качестве реагента этерификации.
Пример. Получение а-метилен-4-(4-тетрагидропиранил) -3-хлорфенилуксусной кислоHal
Ri
- С - CIS ОН
гидролизуют его и получают кислое соединение |формулы VIII
которое подвергают действию дегидратирующего агента с последующи м выделением целевого (Продукта в виде кислоты, соли или сложного эфира известным способом.
В качестве КИслоты Льюиса предпочтительно используют хлористый алюминий, хлористый цинк, хлористое (IV) олово или треххлористый бор.
В качестве нитрующего реагента можно применять концентрированную азотную кислоту, но предпочтительна смесь азотной и серной кислот.
В качестве восстановителя можно употреблять металл, 1как-то: железо, олово или цинк в присутствии водного раствора кислоты, например соляяой иди уксуоиОЙ. Предпочтительно употребляют двуххлористое олово и коицентри.рованеую соляную кислоту.
ты.
А. 4- (4-Тетрагидропиранил) -ацетофенон. В 450 см хлористого металена при 10°С вводят в вЗВещенном состоянии 189 г хлористого алюминия, а затем в течение 5 мин прибавляют 45 см хлористого ацетила.
Далее постеиенно ириливают раствор 90 г 4-|фенилтетрагидрОпираиа в 250 см хлористото метилена и,, нажоиец, 90 см хлористого метилена; перемещивают 2 час при 10°С, а затем - 4 час при -комнатной температуре. После этого вносят 144 см соляной кислоты в 820 см воды, дакантируют органический слой, водный слой экстрагируют хлористым метиленом, соединенные органические слои промывают водой, а затем насыщенным водным раствором кислого углекислого натрия и, наконец, водой. Далее сущат над сернокислым натрием и вЫПаривают досуха в вакууме. Остато раствОряют в теплом состо-яниив 115 сж
изопроиилового эфира, морозят в течение ночи, фильтруют 1ПОД разрежением, осадок промывают ледяпым изопропиловым эфиром и сущат в вакууме. Получают 81,2 г 4-(4-тетрагидрацираиил)-а,цетофенона (выход 72%),
плавящегося при 79-80°С, который употребляют в следующей фазе.
Для анализа соединение лерекристаллизовывают в изопропиловом эфире при нагревании и на холоду: 4-(4-тетрагидропираиил)ащетофенон имеет вид бесцветных кристаллов.
растворимых в метиловом спирте и в хлористом метилене, нерастворимых -в воде, .плавящихся при 80°С.
Анализ: CisHieOs. Мол. вес 204,26.
Вычислено, %: С 76,44; Н 7,90.
Найдеио, %: С 76,2; Н 7,5.
Спектр ЯМР подтверждает положение ларагру1п1пы СОСНз. ИК-Спектр - хлороформ: присутствие с отряженного кетона при 1679 см, СОСНз при 1360 ел-, ароматического соединения при 1608 и 1573 см-.
Б. 4-(4-Тетрагидрапиранил) - 3-нитроацетофенон.
В 100 см серной .кислоты растворяют 20 г 4-(4-тетрагидропиранил)-ацетофенона и охлаждают раствор до -10°С; .прибавляют 20 см азотной (кислоты (плотность 1,49) в течение 2 час, выдерживают 1 час 15 мин При - 10°С, выливают раствор в смесь воды со льдом при перемешивании и в атмосфере азота. Осадок экстрагируют хлористы.м .метиле«ом, оргаи-ические слои «промывают водой, насыщенным водным раствором кислого углекислого натрия и затем водой до нейтральности 1промывных вод, После чего сушат над сернокислым натрием и выпаривают в вакууме досуха. Получают 23,18 г сырого 4-(4-тетрагидропиранил) - 3-нитроацетофенона (.выход 95%), плавящегося шри теМПературе около 70°С.
Для анализа 2,4 г соединения лерекристаллизовывают в метаноле ири нагревании и на холоду, Получают 1,15 г 4-(4-тетрагидропиранил)-3-нитроа1цетофеноиа. Соединение имеет вид светло-1коричневых кристаллов, растворимых в горячем состоянии в хлороформе, хлористом метилене и спиртах, нерастворимых в воде, Плавящихся, при 78°С.
Анализ: Ci3Hi5NO4. Мол. вес 249,26.
Вычислено, %: С 62,64; Н 6,07; N 5,62.
Найдено, %: С 62,6; Н 5,9; N 5,5.
ИК-спектр - хлороформ:присутствие
СОСНз При 1696 NO2 ;при 1534 и 1357 , а также ароматического соединения, замещенного гетероатомом.
В. 4- (4-Тетрагидропираиил) -З-аминоащетофенон.
В 290 см соляной кислоты вводят во взвешенном состоянии 35 г 4-(4-тетрагидропиранил)-3-нитроацетофенона, -прибавляют 98 г двухлористого олова и .реакционную смеюсь нагревают 1При 60°С в течение 6 час. Затем оставляют для остывания до комнатной температуры и оставляют на ночь .при перемешивании, .после чего обра|батывают льдом в течение 30 мин, фильтруют ПОД разрежением. О.статок промывают во.дой и вводят во взвешенном состоянии в 300 см 2 и. едкого патра, выдерживают 4 час при перемешивании при 25°С, фильтруют иод разрежением, inpoмывают ВО.ДОЙ и сушат в вакууме. Получают 24,7 г 4-(4-тетрагидропиранил)-3-аминоацетофенона, плавящегосяПри 164°С, который употребляют в следующей фазе.
Для анализа .перекристаллизовывают 820 мг соединения в метаноле в горячем и холодиом состоянии. Получают 570 мг 4-(4-тетрапидропира«ил)-3-аминоацетофенона в виде охровых- кристаллов, растворимых .в горячем состоянии в хлороформе и спиртах, нерастворимых в воде, плавящихся лри 164°С, Анализ: Ci3Hi7NO2. Мол. вес 219,17.
Вычислено, %: С 71,20; Н 7,82; N 6,39. Найдено, %: С 71,1; Н 7,5; N 6,7. ИК-сиектр - хлороформ: присутствие NH2 при 3475 и 3395 , СОСНз при 1675 и 1357 сл-1.
Г. 4- (4-Тетрагидропиранил) -3-хлориетофенон.
В трехгорлую колбу вводят смесь, состоящ-ую из 1440 см воды и 900 см соляной кислоты, которую -охлаждают до 10°С, и к ней прибавляют 89,8 г 4-(4-тетрагидропиранил)З-аминоацетофенона, массу охлаждают до 5°С и приливают раствор 29,25 г нитрита натрия
в 55 см воды; перемещивают 30 мин, поддерживая температуру 5°С, медленно добавляют раствор 119 г однохлористой меди в 2070 см соляной кислоты и оставляют реакционную смесь при комнатной температуре на ночь при
перемешивании, затем фильтруют под разрежением, промывают осадок водой и сушат в вакууме. Получают 71,76 г сырого 4-(4-тетрагидропиранил)-3-хлора цетофенона, плавящегося При 57°С, который очищают шерекристаллизацией в изопропиловом эфире, в горячем и в холодном состоянии.
Таким образом, получают 46,4 г чистого соединения, которое имеет вид ох.ровых кристаллов, ра.створимых в спи.ртах и в .хлороформе, нерастворимых в воде, плавящихся при 59°С (выход 47%). Концентрируя маточные растворы, дополнительно собирают 7,7 г тро.дукта, т. пл. 59°С. выход (общий) 55%. Анализ: Ci3Hi5ClO2. Мол. вес 238,71.
Вычислено, %: С 65,41; Н 6,33; С1 14,85. Найдено, %: С 65,2; Н 6,2; С1 14,5. ИК-опектр - хлорофор.м: присутствие сопряженного кетона при 1688 , СОСНз при 1356 , а также ароматического соеди.нени я.
Аналогично по известным способам, исходя ИЗ 4-(4-тетрагидропиранИл)-3-аминоа1цетофенона получают - разложением соответствующего бромистого диазоиия бромистой
медью (I) - 4-(4-тетрагидропираиил)-3-бромащетофенон; термическим -разложением соответствующего фторбората диазония - 4-(4тетрагиДропиранил)-3-фторацетофенон.
Д. а-Окси-а- метил-4 - (4 - тетрагидропиранил) -З-хлорфенилацетамид.
5 см безводной цианистоводородной кислоты охлаждают до 0°С, .прибавляют раствор 5 г 4-(4-тетрагидро.пирапил) - 3-хлорацетофенона в 5 см пиридина и теремещивают 16 час 1П|ри 5°С, затем приливают 55 см концентрированной соляной 1К1И1СЛОТЫ, 25 см эфира, после чего теропуакают хлористый водород (газ) в течение 24 час при комиатной температуре, Перемешивая. Далее массу выливают в смесь воды со льдом, остаток экстрагируют эфиром, содержащим 10% хлористого метилена, раствор 1пр1омывают водой, насыщенным водным раствором кислого углекислого натрия и снова водой до Нейтральности иромывиых вод, сушат «ад серНО кислым натрием и выпаривают досуха в вакууме. Остаток превращают в тестообразное состояние в 50 слг изопролилового эфира, перемешивают до полной кристаллизации при комнатной температуре и фильтруют под разрежением. Осадок промывают мзопрапиловым эфиром и сушат в вакууме. Получают 2,7 г а-окси-а-метил-4-(4-тетрагидр0пира1нил)-3-хлор фбнилацетамида в виде кристаллов, раст1воримых в спиртах, малорастворимых в хлористом метилене, нерастворимых в воде, плавящихся при 135°С. Это соединение применяют в следующей фазе. ИК-Опектр - вазелиновое масло: прИСутствие карбонила при 1680 еж-, ароматического соединения, поглощение около 3 мк (OH)NH. Е. сб-Окси-а-метил - 4- (4-тетрагидрапиранил) -З-хлорфенилуксусная -кислота. 3.4 г едкого натра растворяют в 34 см воды И 34 см эта-нола, прибавляют 2,7 г а-оксиа-метил - 4 - (4 - тетрагидрапиранил) - 3 - хлорфенилащетамида и нагревают с обратным холодильником 18 час. Эта-нол перегоияют при атмосферном давлении, фильтруют в горячем виде, Оставляют раствор для охлаждения до комнатной температуры и доводят рН до 1 45 см 2 н. соляной кислоты, затем четыре раза экстрагируют хлорпстым метиленом осевшую фракцию, промывают водой хлорметиленовые слои до нейтральности ирОМЫвных вод, сушат над сернокислым натрием И выпаривают досуха в вакууме. Получают 2,7 г а-оксиа-метил-4 - (4-тетрагиД|роТ1иранил) - 3-хлорфенилукСусной кислоты в виде бесцветных кристаллов, растворимых в горячем Виде в спиртах, малорастворимых в хлороформе, нерастворимых в воде, Плавящихся лри 167°С. Для анализа продукт перекристаллизовывают в этаноле в горячем и холодном :виде: точка нлавления не изменяется. Анализ: CuHieCU. Мол. вес 284,74. Вычислено, %: С 59,05; Н 6,02; С1 12,45. Найдено, %: С 58,8; Н 6,1; С1 12,6. ИК-Опектр - вазелиновое -масло: присутстВИе ароматического соединения, .карбонила при 1731 с./и-1, поглощение в полосе ОН. Ж. Метилен-4 - (4-тетрагидрапиранил)-3хларфенилуксусная кислота. Смесь, Состоящую из 1,9 г а-акси-а-метил-4(4-тетрагидропиранил) - 3-хлорфеннлуксусной кислоты и 0,45 2 л-толуолсульфо1юислоты в 190 см толуола нагревают с обратным холодильником в аппарате с азеотрапным отделением воды 5 час. Затем реакционную массу доводят до комнатной температуры, промывают водой толуолыный слой, сушат над сернокисльм натрием и вьтаривают досуха в вакууме. Остаток превращают IB тестообразное состояние в 30 сж изопроиилового эфира При перемешивании, замораживают в течение 1 час, фильтруют под разрежением и сушат в вакууме. Получают 1,7 г а-метилен-4(4 - тетрагидрО пиранил) - 3 - хлорфенилуксусной кислоты в виде бесцветных кристаллов,, растворимых в хлорофор.ме и в спиртах в горячем состоянии, нерастворимых в воде, плавящихся при 149°С. MiK-C neKTp - хлороформ: отсутствие - ОН, присутствие ири 891 см. при ,1617 сл-1. iO р е д м е т и з о б р е т е н и я Способ получения производных феНИлуксусной кислоты общей формулы I V- С- СООН где, X - атом кислорода или серы, R - линейный или разветвленный алкилиден, содержащий от 1 до 4 атомов углерода, Hal - атом хлора, брома или фтора, а так}ке сложных эфиров этих кислот или их солей, отличающийся тем, что соединение общей форМулы II оде X имеет выщеуказанное значение, подверГают ацетилированию производным кислоты RI-СООН, где Ri - линейный или разветвленный алкильный радикал, Содаржащий от 1 до 4 атомов углерода, в присутствии кислоты ЛьЮИса, и |полученное при этом соединение формулы III rV- iO--R, обрабатывают нитрующим реагеито-м с получением соединения формулы IV де Xi - атом -кислорода илй атом окисленной серы. Ri имеет вышеуказанные значения, которое затем обрабаты/вают восстанов«телем с получением соединения формулы V «Нг
-СО-R, ноторое с ПОМОЩЬЮ соля диазония переводят Ю IB соединение формулы VI
где Hal - атом брома, хлора или фюра,
X и RI имеют вышеуказанные Значения,
затем обрабатывают это соедияение цианиОН
которое шодвергают действию дегидратирующего агента с Последующим выделением це20 левого продукта в ииДе кислоты, соли или сложного эфира известным способом. стоводородной кислотой и получают соединение формулы VII Hal R, х VC-CN гидролизуют его и получают соединение формулы VIII Hal R.





Авторы
Даты
1973-01-01—Публикация