в пр|исут,ст,вии акцептора фторводорода с последующим выделением целевого продукта известнЫМ способом.
Применяемые в ка:чест1ве исходных веществ производные угольной и Kaip6oHOBof ки.слот общей фор.мулы II большей частью известны и TIX можно получать известным образом, «аеример путем .взаимодействия галогелидов угольной :ИЛИ .карбоновой кислоты с алшиаком аминами. Таким образом многие подпадающие под общую формулу II .производные мочевины можно получать известным |0бразоам из 1пер1вичных амипов « изоцианатов, например следующие изоцианаты: п-трифторметилфепили:зоцианат, п. - нитрофеНИлизодиа.нат, метилизоциапат, изодро-пилизоциа.нат, г/ ег-бутилизоцианат, циклогексилизоцианат, аллнлизоц.ианат, р-хлорэтилнзоцианат, фепилизоцианат, о-нитрофенилизоцианат, /г-нитрофенилизоцианат, г-нит рофенилизоцианат, о-хлорфепилизоцианат, м- хлорфенилизоцианат, 3,4-дихлорфенилизодианат, п-хлорфенилнзоциаиат, р-нафтилизоциаиат, бензилизоцианат, стеарилизоцианат, |3-цианоэТИлизоцианат, этилизоциапат, н-пропилизоцианат, м-бутилизоциапат, изобутилизоцианат, 2-этил-гексилизоциаиат, додецилизоцианат, тетрадецилизоцианат, п-мето:ксифенилизоцианат, «-метил меркаптофенилизоцианат.
В качестве ;прн,мер01в для первич ных аминов, Кроме аминов, (которые являются исходНЫЛ1И веществами указа нных «зоциа натов, годятся также следующие амины для .получения соедилений формулы II: 2-аминопиридип, 2аминотиазол, 2-амннобензтиазол, 2-амино-1метилциклогексан, гексагидробеизиламин, 2хлораНИЛ|Ин, 3-нит|роанилин, 2-хлор-4-.нитроанил«н, 5-хлор-2-а,мИНотолуол, 4-хлор-З-аминобепзотрифторид, 1-ами.но-2-фе.пилэтап-2-амино-1-изопропилбензол, 5-амино-1,2,4-триметилбензол, 5,б,7,8-тетраГИ|Дронафтила1МИп-(1), 3,5дихлоранилин, 2,4,5-трихлораннлИН, 2,4-дихлоранилин, 2,3-дихлорапилин, 2,5-дпхлоранилин, 3-хлоранилин, 4-хлоранилип, 4-хлор-2-нитроанплин, апилин, 2-нитроанилин, 4-нитроанилин, 5-хлор - 2 - нитроанилин, 4 - хлор3-нитроапилин, 3 - хлор - 4 - нитроанилип, 4,6Лихлор-2-питроанилин, 2,5 - дихлор - 4 - питроапилин, 2,6-дихлор-4-нитроанилин, 2-амипотолуол, З-хлор-2-аминотолуол, 4-хлор-2-амипотолуол, 5 - нитро-4-амино-1,3-диметилбензол, 6 - нитро - 4 - амино - 1, 3 - диметилбепзол, 5-амино - 1,3 - диметилбензол, 5-амино-1,3-бастрифторметилбензол, 2-амино-1,4-диметилбензол, 2-ами«о-1-мет1ил-3-этилбеизол, 6-амино1.2,4-триметилбензол, 2-амипо-1,3,5-триметилбензол, 2-ами:но-1,3-диэтилбензол, 4-амино1,3-димет1Ил-5-этилбензол, 4-а.мино-1-метил-3,5диэтилбензол, 2-амино-1,3-диизо(пропнлбензол, 5,6,7,8-тетрагидоонафтиламин-(2), р-бром-этилам.ин, 1-циано-1-фенилэтиламин, 1-цпапо-1-метилэтиламин, 5-хлор-2 - аминобензотрифторнд, 6-хлор-2-аминотолуол, 4,5-дихлор-2-аминотолуол, 3-.пп:тро-2-а ми но толуол, 4-Н Итро-2-ам111нотолуол, 5-нитро-2-аминотолуол, 6-нитро-2-ам«нотолуол, 4-хлор-5-н1гг1ро-2-аминотолуол, 3аминотолуол, 4-хлор-З-аминотолуол, 6-хлор-Заминотолуол, 4,6-дихлор-З-аминотолуол, 4-ам: нотолуол, 2-хлор-4-амИнотолуол, 2-.нитро-4а.минотолуол, З-нитро-4-аминотолуол, 2-амино1-этилбензол, 1-амино-1-фепилэтан, 2,3-анметил анилин, 2,6-диметилар1клнн, 3,4-диметиланилин, 2,4-диметиланилин.
Подпадающие под формулу II гуанидины, .мер 2-аМИнобеизи.мидазол, 2- а1Мино-(|карбометокси)-бензимпдазол, /г-хлор фенил им ;1доN, КТ-д1иэтилмочеви.ну, можно получать известным образом.
ПрИ.мепяемый в 1качестве исходного .вещест1за :перфтор-2,5-диазагекса-2,4-д11е:н формулы III известен.
Процесс можно вести з П;р сутствии разбавителя.
В качестве разбавителя годятся все .инертиые органические растворители. К ним принадлел ат .преимущественно углеводороды - бензин, бензол, толуол; нитрилы - ащето.нитрил; хлорированные углеводоро.ды - метилеихлорид, хлороформ и хлорбензол. В :качестве связывающего кислоту вещества можно при1менять все обычные овязывающие кислоту средства - щелочные карбонаты, щелочные бикарбонаты; трет-ампны - триэтиламин, диметиланилин. Преи.муществе«но применяемые -на практике акцепторы фторводорода - щелоч ные фтори.ды, среди которых прежде всего фторид натрия.
Тем::1ературы реакции можно :варьировать в шир01ких пределах (от Niimyc 50 - до плюс 120°С, преимущественно от м.инус 30 до -плюс 9.).
Для проведения способа согласно изобретению на 1 моль сое|Динения согласно формуле II вводят 1 моль iпepфтop-2,5-диaзaгeкса-2,4-дие.на формулы III, щелочной фторид применяют в избытке (приблизительно 3- 4 моль), однако возможно отклонение максимально на 20 вес. % ниже илИ выше указанного количественного соотношения без значительного уменьшения выхода.
Целесообразно перфтор-2,5-диазагекса-2.4диен Прикапывать к суспензии, состоящей т исхо.дного .материала, органического растворителя и фторводородного акцептора. Затем полученный продукт отфильтровывают от сЬтор1ида, сгущаютИ перекристаллизовывают. Другой способ обработки за1К.лючается .в том, что к реакционной смеси добавляют водуиобразова.вшийся остаток, з случае необходимости, .перекписталлизовывают.
Пример 1. К 9 г (0,1 моль) N. N-диметилмочевины и 15 г (0,36 моль) фториаа натрия в 150 мл бензола цри температуре 50°С прикапывают 23 г (0,1 моль) перфтор-2,5-.диазагекса-2,4-Д1иена. Дополнительно -перемешивают приблизительно в течение 30 мин с о5ратньш .холодильником, отфильтровывают от гидрофторида натрия п фтошгла натрия и сгу1цают фильтрат в вакууме. После лерекристаллизации из простого эфира.пентана получают
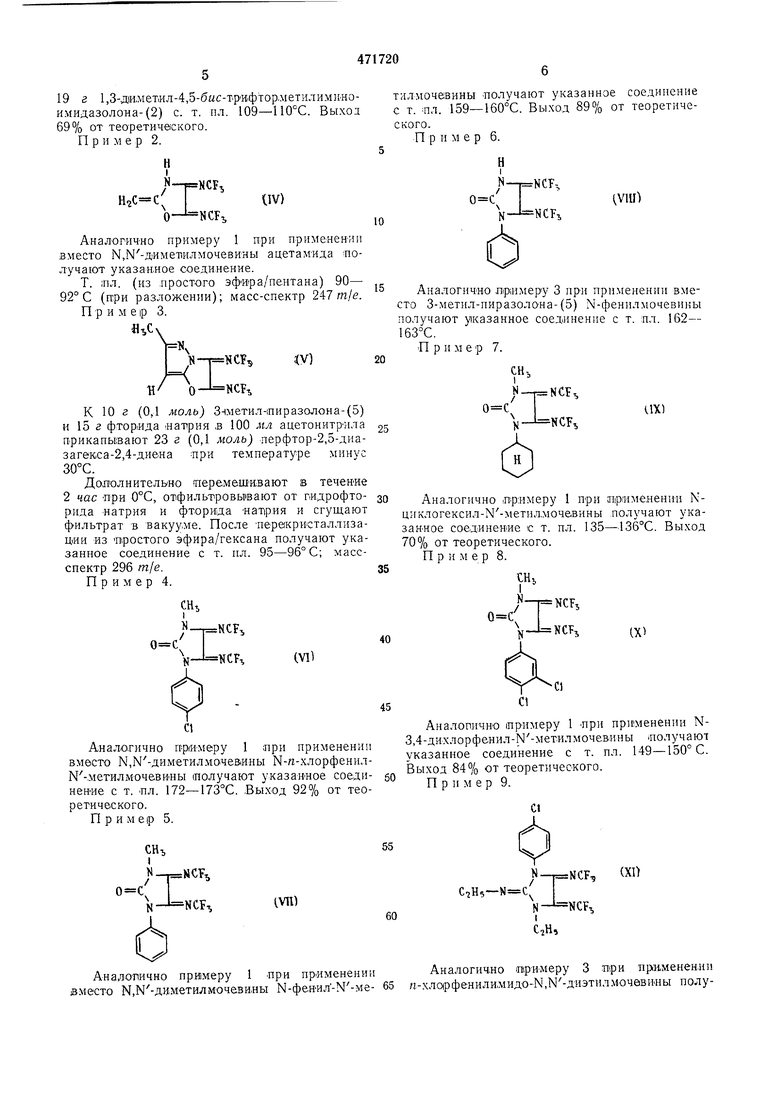
19 г 1,3-Д1И,метал-4,5-б«с-трИфтор,метилим1шоимидазолона-(2) с. т. пл. 109-110°С. Выход 69% от теоретического. Пример 2.
тлл.мочевины Получают указанное соединение с т. пл. 159-1бО°С. Бы.ход 89% от теоретического.
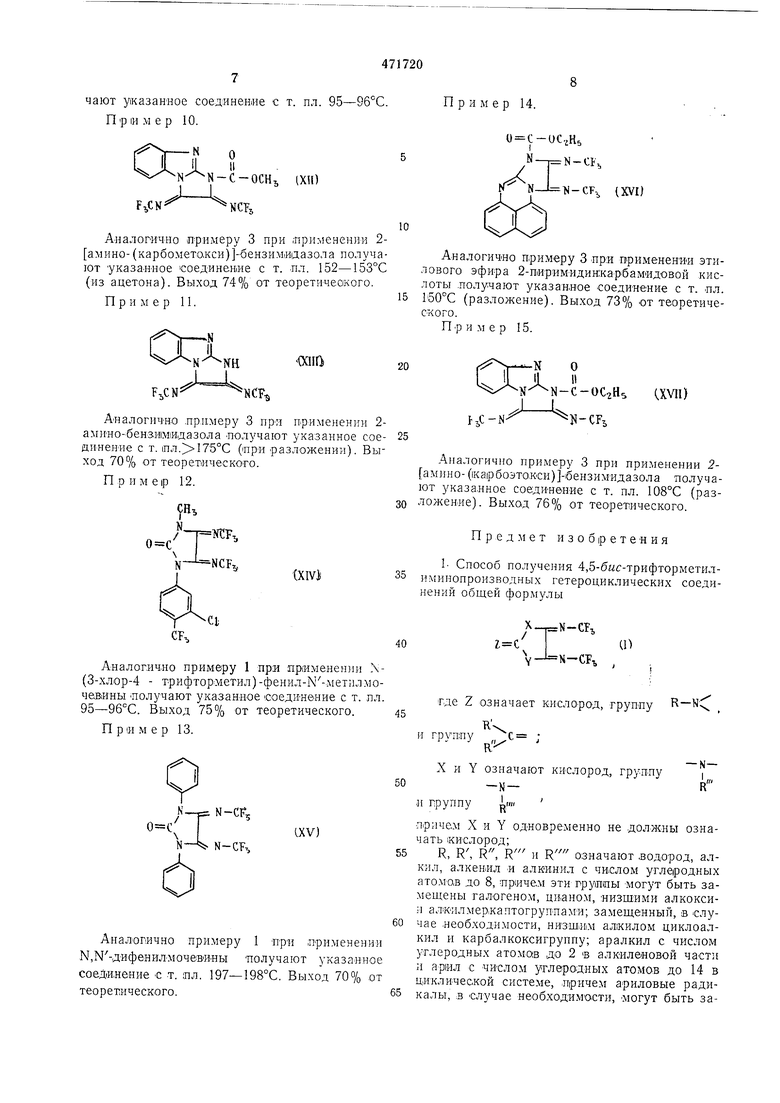
П р и м е р 6.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных пиперазина или пиперидина или их солей | 1977 |
|
SU683621A3 |
| СПОСОБ ПОЛУЧЕНИЯ САЛИЦИЛАНИЛИДА | 1970 |
|
SU281285A1 |
| Способ получения замещенных 2,6-динитробензоламинов | 1979 |
|
SU990080A3 |
| Способ получения производных акриловой кислоты | 1985 |
|
SU1395139A3 |
| Способ получения производных 1-(4-феноксифенил)-1,3,5-триазина | 1973 |
|
SU489333A3 |
| Способ получения алканоиланилида или его аммониевых солей | 1986 |
|
SU1528343A3 |
| Способ получения производных имилазо-(4,5-в)-пиридина | 1974 |
|
SU535908A3 |
| Способ получения полиеновых соединений или их солей | 1975 |
|
SU623515A3 |
| Способ получения тиено(3,2-д) пиримидинов | 1972 |
|
SU461506A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2-АНИЛИНОНИКОТИНО- ВОЙ или N-ФЕНИЛАНТРАНИЛОВОИ КИСЛОТ ИЛИ ИХ СОЛЕЙ | 1973 |
|
SU365884A1 |

Аналогично примеру 1 при применении вместо М,Ы-димет1илмочевины ацетамида получают указанное соединение.
Т. ;пл. (из .простого эфИра/пентана) 90- 92° С (п:ри разложении); масс-спектр 247/п/е.
При м е ip 3.
«ьС
У)
,
NCP,,
К 10 г (0,1 моль) Знметил-1Пиразолона-(5) и 15 г фторида натрия ,в 100 лгл ацетонитрила прикапывают 23 г (0,1 моль) перфтор-2,5-диазагекса-2,4-диена ири температуре минус
зо°с.
Дополнительно перемешивают в течение 2 час при 0°С, отфильтровывают от гидрофторида «атрия и фторида яатрия и сгущают фильтрат в вакууме. После -перекристаллизации из Простого эфира/гексана получают указанное соединение с т. пл. 95-96° С; массспектр 296 т/е.
Пример 4.
Аналогично при.меру 3 прИ применении вместо 3-метил-пиразолОна-(5) N-фенилмочевины получают указанное соединение с т. лл 162- 163Т.
П р и м е р 7.
сн,,
N--, NCF
UX)
NCFb
Аналогично Пр:имеру I при лр1име.нении Nциклогексил-Ы-метил.мочевины .получают указанное соединение с т. пл. 135-136°С. Выход 70% от теоретического.
Пример 8. Аналогично прЯМеру 1 при применении вместо ,Ы-диметил.мо чев1Ины К-/г-.хлорфенилМ-,метилмочеБИНы (получают указанное соеди- бО нение с т. .пл. 172-173°С. Выход 92% от теоретического. Пример 5.
(VII)
С, Аналогично примеру 1 при применении N3,4-дихлорфенил-Ы-метил мочевины «получают указанное соединение с т. пл. 149-150° С. Выход 84% от теоретического. Пример 9.
Аналопично примеру 1 при применении вместо Ы,Ы-диметилмочеви,ны Ы-фенил-М-ме- 65
Аналогично тримеру 3 при 11р1И,менен.ии п-хло(рфенили,мидо-Ы,Ы-диэтилмочввш1ы получают указанное соединение с т. пл. 95-96°С. Пример 10. Гл 8 N- N-CОСИ, (ХИ) Аналогично примеру 3 при .-применении 2 амино-(карбометол си)-бензиМ|И дазола получают указанное 1соединен1ие с т. пл. 152-153°С (из ацетона). Вы.ход 74% от теоретичеакого. Пример 11. АНалогнЧНО .примеру 3 прЯ иримеиении 2амиНО-бенви1М1Идазола получают указанное соединение с т. 1Пл.175°С (при разложении). Выход 70% от теоретического. П р и м е ip 12. (xm Аналогично примеру 1 при применении X(3-хл|Ор-4 - трифтор:метил)-фенил-К-метилмочевины получают указанное соедипепие с т. лл. 95-Эб С. Выход 75% от теоретического. Пример 13. N-% N-CF, Аналогично примеру 1 при примене К ,М-дифениЛМОчевИпы получают указан соединение € т. пл. . Выход 70% теоретического. Пример 14. 0 C-UC.jH5 NАналогичйо примеру 3 .пр:и применении этиового эфира 2-пиримидин;карбамидовой кислоты .получают указанное соединение с т. пл. 150°С (разложение). Выход 73% от теоретического. При м ер 15. Аналогично примеру 3 при применении 2 амино- (1ка|рбоэто,КСи)- бензимидазола получают указа.иное соединение с т. пл. 108°С (разложение). Выход 76% от теоретического. Предмет изобретения I- Способ получения 4,5-быс-трифторметилиминопроизводных гетероциклических соединений общей формулы r :N-Cr,, Ч-СТ где Z означает кислород, группу R-Ni и группу с ; R X И Y означают кислород, группу и группуj. лричем X и Y одновременно не .должны означать кислород; R, R, R, R и R означают .водород, алкил, алкепил и алнинил с числом углеродных ато,мо,в до 8, причем эти группы могут быть замещены галогено.м, цпано.м, иизшими алкоксии алкилмер.каптогруппам:и; замещенный, в случае .необходимости, низш пм алкилом циклоалкил и карбалкоксигруппу; аралкил с числом углеродных атомов до 2 в алкиле«овой част;1 л арил с числом углеродных атомов до 14 в циклической системе, причем ариловые радикалы, в случае необходимости, -могут быть замещены галогеном, циа-ном, нитрогрутпой. низшим алкилом и галоидным алкилом, низшей алкокси- и алкилмер1каптогруппой; 5- 7-членные гетероциклы «ли такие радикалы, которые могут связывать Z с X или Y при образо вании 5-7-членного кольца (гетероциклы М01гут быть аннелироваиы также с бензольным кольцом, .которое, в случае «еобходилюспи, частично также может быть гидрировано; крОМе того, гетероциклы могут быть замещены галогеном, цианом, нитрогруплой и низшим алкилом),
отличающийся те.м, что соединение общей фор1мулы
л-н
an
.
Y-Н
10
где Z, X и Y имеют указанные значения, иодБе|ргают взаимодействию с перфтор-2,5Хиазагекса-2,4-диеном формулы
СЬь
(ПП
у
MF
в присутств;ии акцептора фторводорода, с последующим выделением целевого продукта известным способом.


Авторы
Даты
1975-05-25—Публикация
1971-12-14—Подача