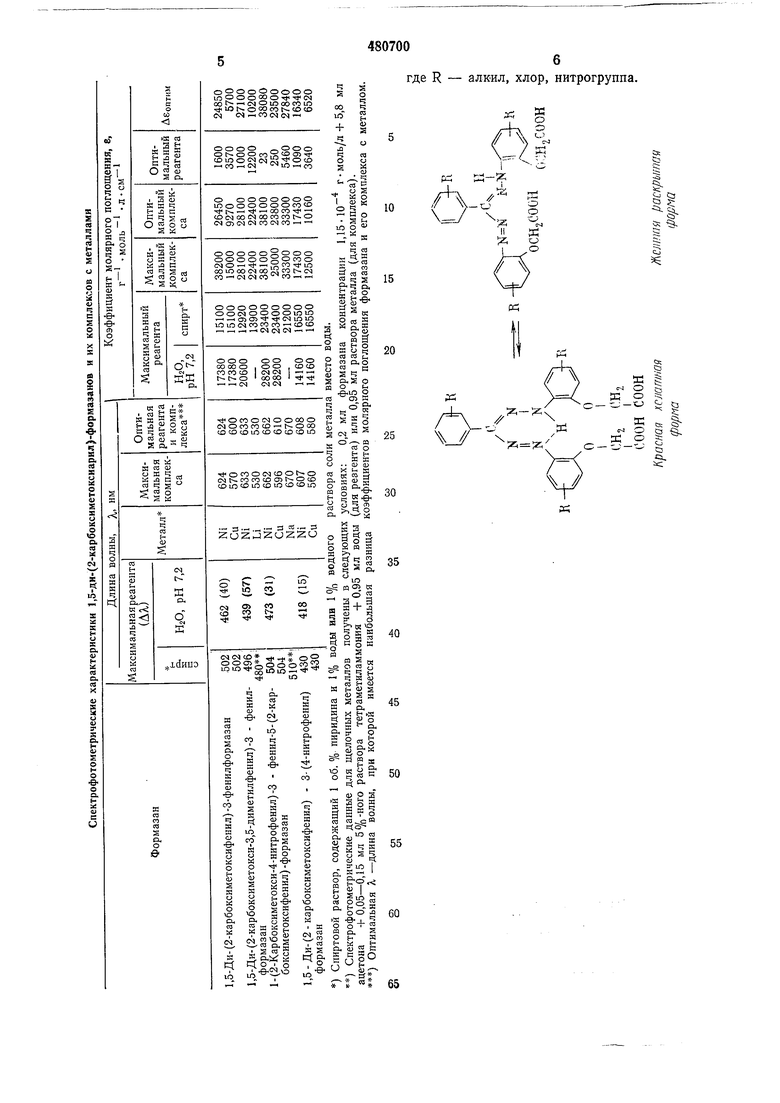
где R - алкил, хлор, нитрогруппа.
Отличие структуры данной группы формазанов от известных формазанов состоит в том, что в ортоположении к формазановой тетразогруппе находятся две карбоксиметоксигруппы.
1,5-ди- (2-карбоксиметоксиарил) - формазаны являются интенсивно окрашенными соединениями с высоким коэффициентом молярного поглощения в видимой области спектра, способными к образованию комплексов с металлами с сильным батохромным сдвигом и углублением окраски образующихся комплексов (см. таблицу в коцце описания).
Эта способность формазанов дает возможность использовать их в ряде разделов химии, например в аналитической химии и гистохимии.
Так, новые 1,5-ди-(2 - карбоксиметоксиарил)-формазаны способны образовывать комплексы с щелочными металлами с новым, батохромным эффектом. 1,5-ди-(2-карбоксиметоксиарил)-Формазаны способны образовывать комплексы с никелем и медью с сильным батохромным эффектом при ,2 при гистохимическом окрашивании биологических тканей в отличие от известных формазановых комплексов с никелем или медью.
Предлагаемую новую группу формазанов получают сочетанием диазотированной 2-аминоарилуксусной кислоты с 2-карбоксиметоксиарилгидразоном фенилглиоксалевой кислоты в среде пиридина или с 2-карбоксиметоксиарилгидразоном арилальдегида в среде тетрагидрофурана и спиртового раствора едкого кали, причем сочетание гидразонов арилальдегидов не идет в пиридине, а сочетание гидразонов фенилглиоксалевой кислоты не идет в тетрагидрофуране и спиртовой щелочи.
Пример 1. Получение 1,5-ди-(2-карбоксиметоксифенил)-3-фенилформазана.
Растворяют 5,4 г (0,017 моль) 2-карбоксиметоксифенилгидразона фенилглиоксалевой кислоты в 60 мл пиридина в трехгорлой колбе емкостью 250 мл, снабженной ртутным затвором с мешалкой, барбатером для пропускания азота и капель..ой воронкой. В течение 20 мин через раствор гидразона пропускают азот и при интенсивном размешивании прибавляют по каплям диазораствор, полученный заранее при диазотировании 3,3 г (0,017 моль) натриевой соли 2-аминофеноксиуксусной кислоты в смеси 20 мл воды и 1,1 г нитрита натрия, которое протекает при быстром добавлении 7,5 мл концентрированной соляной кислоты при -2° С. Реакционную массу размешивают 1,5 ч, вливают ее в 600 мл 2%-ной соляной кислоты. Выпавший осадок отфильтровывают, переосаждают из ацетона 1%-ной соляной кислотой (выход 6 г, 79%) и из этанола водой, сушат в вакуум-эксикаторе над твердым еджим кали. Формазан представляет собой темно-красные кристаллы с золотистым блеском с т. пл. 185-186° С. Выход продукта 4,8 г (63%).
Найдено, %: С61,42, 61,39; Н4,57, 4,37; N 12,98, 12,90.
С2зН2оМ4Об.
Вычислено, %: С61,62; Н4,50; N12,49.
Пример 2. Получение 1,5-ди-(2-карбоксиметокси-3,5-диметил) -3-фенилформазана.
Синтез проводят, как в примере 1 сочетанием 2-карбоксиметокси-3,5-диметилфенилгидразона фенилглиоксалевой кислоты с диазотнрованной 2-амино-4,6-диметилфеноксиуксусной кислотой. Выход 32%, темно-бордоые блестящие кристаллы с т. пл. 174-175° С.
Найдено, %: С 64,89, 64,97; Н 5,82, 5,84,; N11,06, 11,28.
C27H28N4O6.
Вычислено, %: С64,53; Н5,61; N11,10.
Пример 3. Получение 1-(2-карбоксиметокси-4-нитрофенил) - 3 - фенил-5 - (2- карбоксиметаксифенил)-формазана.
Синтез проводят сочетанием 2-карбоксиметоксифенилгидразона фенилглиоксалевой кислоты с диазотированной 2-амино-5-нитрофеноксиуксусной кислотой в условиях, описанных в примере 1.
Выход 59%, темно-коричневые с зеленым блеском (Кристаллы с т. пл. 207-207,5° С.
Найдено, %: С56,12; 56,40; Н3,95, 3,93; N 13,99, 13,95.
C23Hi9N5O8.
Вычислено, %: С55,98; Н3,88; N14,19.
Пример 4. Получение 1,5-ди-(2-карбоксиметаксифенил)-3- .(4-нитрофенил) - формазана.
Растворяют 6,2 г (0,02 моль) 2-карбоксиметоксифенилгидразона 4-нитробензальдегида в 50 мл тетрагидрофурана, добавляют 5,6 г (0,01 моль) едкого кали в 30 мл метанола и при -2 С при интенсивном размешивании но
каплям добавляЮТ диазосоединение, полученное, как в примере 1 из 3,8 г (0,02 моль) нитрита натрия в 20 мл воды и 8 мл соляной кислоты. Размешивают 2 ч при 0° С, поддерл ивают рН реакционной смеси не менее 7. Продукт выделяют добавлением в реакционную массу 200 мл 2%-ной соляной кислоты, отфильтровывают и переосаждают из ацетона 1%-ной соляной кислотой (с активированным углем).
Выход 3,6 г (37%), т.пл. 166-167°С, красные кристаллики.
Найдено, %: С56,28, 56,45; Н3,90, 3,91.
C23Hi9N508.
Вычислено, %: С 55,98; Н 3,88.
Предмет изобретения
Сексадентатные реагенты на металлы 1,5ди- (2-карбоксиметоксиарил) -формазаны общей формулы

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 1,5-ди-(2-карбоксиметоксиарил)-3-арилформазина | 1975 |
|
SU536212A1 |
| 4-Амино-2,3-дигидро-1,4-бензоксазин-3-оны в качестве полупродуктов для синтеза 2-карбоксиметоксиарилгидразонов и 1,5 -ди- (2-карбоксиметоксиарил) формазанов и способ их получения | 1976 |
|
SU612932A1 |
| 1,5-Ди(2-карбоксиметоксифенил)3-цианформазан в качестве красителя-реагента на скандий | 1975 |
|
SU595347A1 |
| Аминоарилформазан в качестве промежуточного продукта в синтезе макроциклов | 1975 |
|
SU538012A1 |
| 16,17-Дигидро-7-фенил-5Н,15Н-ди @ 2,(12)-нитробензо @ 1,11,4,5,7,8 @ -диоксатетраазациклотетрадецин в качестве хромогенного реагента для определения лития | 1982 |
|
SU1057500A1 |
| ФОТОТРОПНЫЕ ВЕЩЕСТВА | 1969 |
|
SU241442A1 |
| СПОСОБ ПОЛУЧЕНИЯ 1,5-ДИБЕНЗАЗОЛИЛ-З-АЛКИЛФОРМАЗЛНОВ | 1967 |
|
SU199900A1 |
| 16,17-Дигидро-2,12-динитро-5Н,7Н,15Н-дибензо (в, @ ) (1,11,4,5,7,8)-диоксатетраазациклотетрадецин в качестве хромогенного реагента для определения лития и способ его получения | 1986 |
|
SU1432058A1 |
| Кислородосодержащие циклоформазаны систем три-, тетра- или гексадецина и способ их получения | 1977 |
|
SU682517A1 |
| Способ получения реактивной бумаги | 1981 |
|
SU1178819A1 |


Авторы
Даты
1975-08-15—Публикация
1973-06-18—Подача