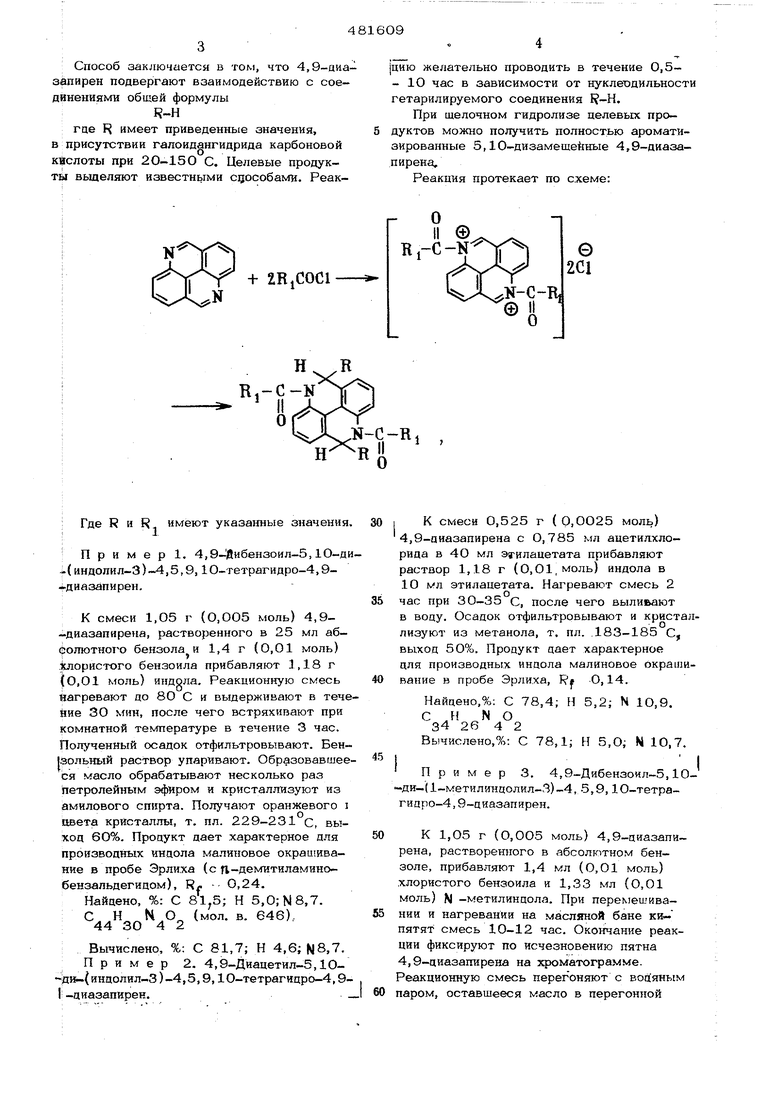
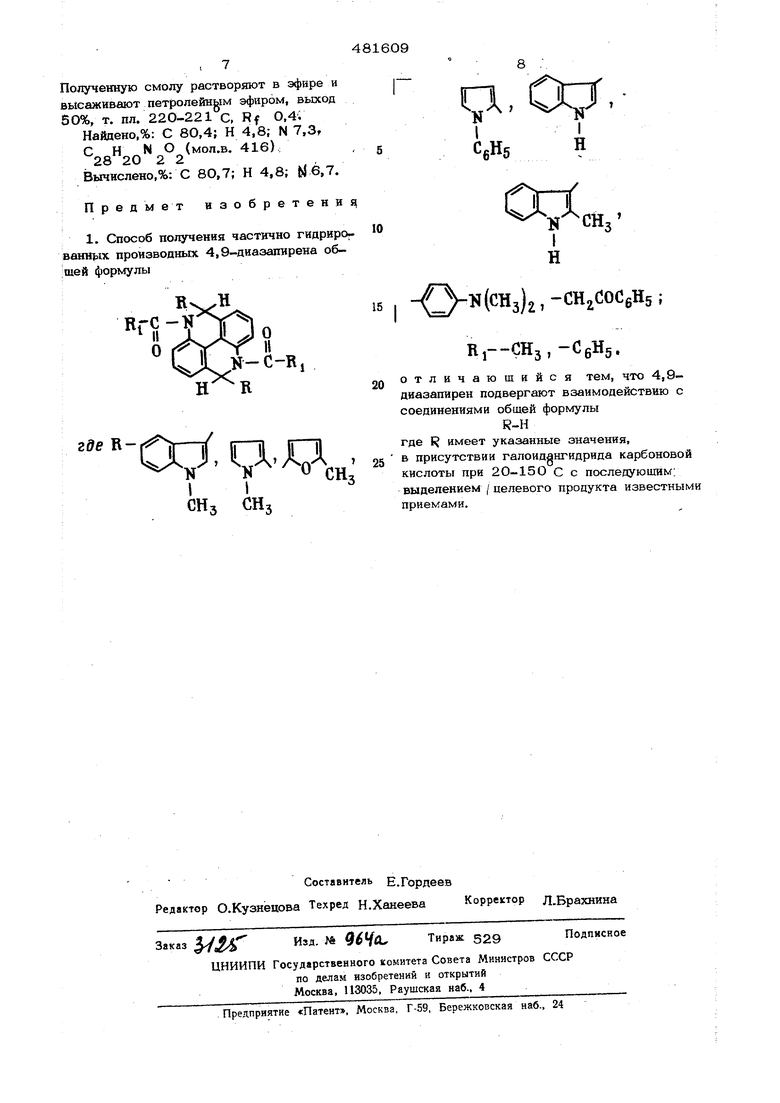
Способ заключается в том, что 4,9-аиазапирен подвергают взаимодействию с соединениями общей формулы R-H
где R имеет приведенные значения, в присутствии галоидангидрида карбоновой кислоты при 2 0-15 О С. Целевые продукты вьщеляют известными сцособами. РеакN
+ 2R,COC1
цию желательно проводить в течение 0,5- - 10 час в зависимости от нуклетэдильности гетарилнруемого соединения R-H.
При щелочном гидролизе целевых продуктов можно получить полностью ароматизированные 5,10-дизамещейные 4,9-диазапирена.
Реакция протекает по схеме:
RJ-C N
2С1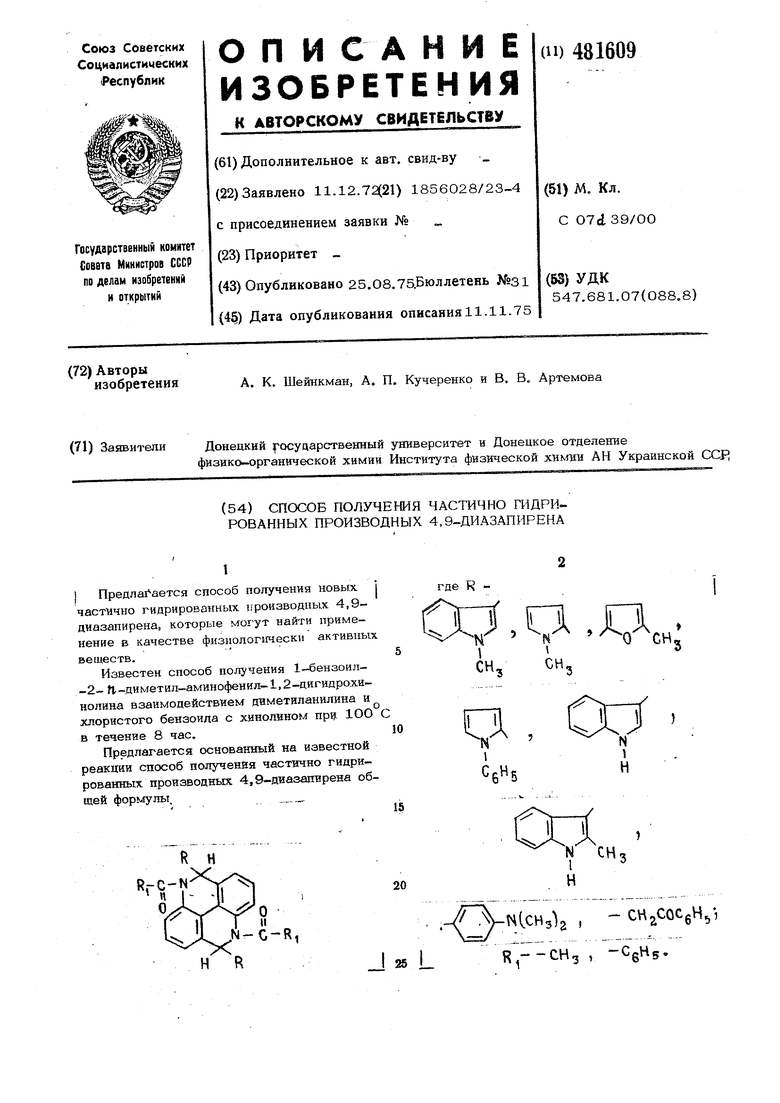

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2-замещенных перимидина | 1973 |
|
SU504770A1 |
| Способ получения имидов карбоновых кислот, их право-или левовращающих изомеров или их солей | 1975 |
|
SU665803A3 |
| Способ получения производных м-диоксан-5-метиламина | 1975 |
|
SU663305A3 |
| Способ получения производных хиназолина | 1974 |
|
SU523090A1 |
| Способ получения галогенпроизводных 5н-пиридо (2,3- @ ) или 5н-пиримидо (4,5- @ ) (1,4) тиазинов | 1974 |
|
SU534073A1 |
| Способ получения (арилалкил) алкановых кислот | 1978 |
|
SU884568A3 |
| Способ получения гетероциклических производных амидов о-фенилендиамина | 1972 |
|
SU455096A1 |
| Способ получения замещенных трихлорацетамидинов или их солей | 1976 |
|
SU633471A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЧАСТИЧНО ГИДРИРОВАННЫХ N,N'-ДИAЦИJ]ЬHЫX ПРОИЗВОДНЫХдихинолилов и диизохинолилов | 1971 |
|
SU414258A1 |
| Способ получения 2,6-диэтинилпиперазинов | 1973 |
|
SU492518A1 |

Где R и R имеют указанные значения Пример. 4,9- ибензоил-5,1О-д Ц индолил-3)4,5,9,1О-тетрагидро-4,9-диазапирен, К смеси 1,О5 г {О,О05 моль) 4,9-диазапирена, растворенного в 25 мл аб- фолютного бензола и 1,4 г (0,01 моль) .1шористого бензоила прибавляют 1,18 г (О,О1 моль) индола. Реакционную смесь нагревают до 8О С и выдерживают в теч йие ЗО мин, после чего встряхивают при комнатной температуре в течение 3 час. Полученный осадок отфильтровывают. Бен зольный раствор упаривают. Образовавшее ся масло обрабатывают несколько раз петролейным эфиром и кристаллизуют из амилового спирта. Получают оранжевого цвета кристаллы, т. пл. 229-231 с, выход 6О%. Продукт дает характерное для производных индола малиновое окрашивание в пробе Эрлиха (с ц-демитиламинобензальдегидом), R- - 0,24. Найдено, %: С 81,5; Н 5,0; N8,7. Вычислено, %: С 81,7; Н 4,6; N8,7. Пример 2. 4,9-Диацетил-5,10-ди-(индолил-3)-4,5,9,1О-тетрагидро-4,9 I -циазапирен. К смеси 0,525 г ( 0,ОО25 моль) 4,9-аиазапирена с 0,785 мл ацетилхлорида в 4О мл эгилацетата прибавляют раствор 1,18 г (0,01, моль) индола в 10 мл этилацетата. Нагревают смесь 2 час при 30-35 С, после чего выливают в воду. Осадок отфильтровывают и кристаллизуют из метанола, т, пл. .183-185 С, выход 5О%. Продукт дает характерное для производных индола малиновое окрашивание в пробе Эрлиха, R 0,14. Найдено,%: С 78,4; Н 5,2; N 1О,9. С Н N О 34 26 42 Вычислено,%: С 78,1; Н 5,0; N 1О,7. Пример 3. 4,9-Дибензоил-5,10ди-.(1-метилиндолил-3)-4, 5,9,1О-тетра гидро-4,9-диазапирен. К 1,О5 г (О, О Об моль) 4,9-диазапи рена, растворенного в абсолютном бензоле, прибавляют 1,4 мл (0,01 моль) хлористого бензоила и 1,33 мл (0,О1 моль) М -метилиндола. При перемешивании и нагревании на масляной бане кипятят смесь 10-12 час. Окончание реакции фиксируют по исчезновению пятна 4,9-диазапирена на хроматограмме. Реакционную смесь перегоняют с воцяным паром, оставшееся масло в перегонной |колбе растворяют в метаноле и высаживают воцой. Полученный осацок 4,9-аи6ензоил-5ДО-ди-{ N -метилинаои -)-4,5,9,1О - тетрагидро-4,9 аиазапирена кристаллизуют из метанола, т. пл. 160о161 С, выход 45%, Rr . 0,75. Найцено,%: С 82,9; Н 5,0; М ..8,6. С Н N О 46 33 42 Вычислено,%: С 82,9; Н 4,9; N..8,4. Пример 4. 4,9-Дибензоил-5,1О д и- (2-метилиндолил-З) -, 5,9,10-тетра - я ро-4,9-аиазапирен. Соединение получают аналогично. Обра вавшееся масло растворяют в хлороформе и высаживают петролейным эфиром. Получают осадок сиреневого цвета, выход 45% т. пл. 175-176 С; Rr 0,17. С Н N О 46 33 4 2 Найдено,%: С 82,1; Н 5,3; N 8,6. Вычислено,%: С 82,9; Н 4,9; N 8,4. П р и м е р 5. 4,9-Дибёнзоил 5,10ци-( N -метилпирролил-2)-4,5,9,10-тетра гидро-4,9-диазаг1ирен. Растворяют 1,О5 г (О,ОО5 моль) 4,9 -диазапирена в 25 мл абсолютного бензол прибавляют 1,4 мл (0,01 моль) хлористо бензоила и нагревают смесь до кипения, после чего приливают 0,99 мл (0,О1 мо N -метилпиррола. Реакцио1гаую смесь кип тят на масляной бане в течение 11 час. За ходом реакции следят по хроматограмм По окончании реакции смесь перегоняют с воцяным паром. Оставшееся масло раство ряют в эфире и высаживают петролейным эфиром. Получазот светлый осадок, выход 5О%, т.пл. 155-157 С, Re О,66. Найцено,%: С 79,2; Н 5,3; N 9,5. С Н N О 38 30 4 2 Вычисле1Ю,%: С 79,4; Н 5,3; N 9,7.
Пример 6. 4,9.-(1ибензоил-5,10.. .-ди( 1-фенилпирролил-2 Х4,5,9,1О.-тетрагицро-4,9-аиазапирен.
Смесь 1,О5 г (0,005 моль) 4,9-диазапирена в 25 мл бензола, 1,4 мл (0,01 моль) .хлористого бензоила и О,72 г N фенилпиррола греют на масляной бане Ю12 час при 11D-120 С. Реакционную массу перегоняют с водяным паром. Оставшееся масло обрабатьгоают эфиром и высаживают петролейным эфиром. Получают белый осадок 4,9-дибензоил-ди-( N -фенилПример 9. Взаимодействие 4,9циазапирена с ацетофеионом.
1,05 г (0,ОО5 моль) 4,9-ana3an ipeна растворяют в 25 мл абсолютного бензола и приливают 1,4 мл (0,О1 моль) .хлористого бензоила. К подогретоьлу до 5О С раствору добавляют 1,34 мл ( 0,01 моль) ацетофенона. Смесь нагревают на масляной бане до кипения и кипятят в течение 14 час. За .хрдом реакц следят по хроматограмме. Реакционную смесь перегоняют с водяным паром. ирролил 2)-4,5,9,10 тетрагидро-4,9- иазапирена, выход 40%, т. пл. 146-148 С f ОД8. Найдено,%: С 82,1; Н 4,9; N8,0. С Н N О 48 34 4 2 Вьгчислено,%-. С 82, 4,9; N 8,0. Пример 7. 4-Бензоил-5-(2-ме- илфуроил 5)-4,5 дигидро-4,9-диазапирен. 1,05 г {0,005 моль) 4,9-диазапирена астворяют в 25 мл абсолютного бензола, риливают 1,4 мл (0,01 моль) хлористого eH3ovma и 0,89 мл (0.01 моль) сильваIна. Опыт проводят в токе азота. Реакционную (умесь греют в течение 10 час при 1ОО С на масляной бане. За ходом реакции следят по хроматограмме. После окон- чания реакции смесь перегоняют с водяным паром, получают масло, которое растворяют в ацетоне и высаживают водой, выпадает белый осадок, выход 35%, т. пл. 220-222°с, R -0,27. Найдено,%: С 80,О; Н N 7,3. С Н NO 26 18 2 2 Вычислено,%: С 80,0; Н 4,6; N7,2. П р и м е р 8. 4,9-Дибензоил-5,10ди-( П-диметиламшюфенил)-4,5,9,10тетрахИцро-4,9-циазапирен. Смесь 1,05 г (0,О05 моль) 4,9-диазапирена в 25 мл абсолютного бензола с 1,4 мл (0,О1 моль) хлористого бензоила и 1,29 мл (0,01 моль) диметиланилина греют ДО час на масляной бане при 110 - 12О С. Затем реакционную массу пере1-х няют с водяным паром. Остаъ , ишеся масло растворяют в эфире и выса- жи.вают петролейным эфиром, выход 51%, т. пл. 155-157°С, RC 0,66. Иайде1Ю,%: С 8О,5; Н 5,7; N 8,6. С Н NO (мол.в. 654) 44 38 4 2 Вычислено,%: С 80,7;. Н 5,8; N 8,5.
Полученную смолу раствор$пот в эфире и высаживают петролейным эфиром, выход 5О%, т. пл. 220-221 С, Rf О,4; Найдено,%: С 80,4; Н 4,8; N 7,3,
Вычислено,%: С 80,7; Н 4,8; js|6,7.
Предмет изобретени

Авторы
Даты
1975-08-25—Публикация
1972-12-11—Подача