(54) СПОСОБ ПОЛУЧЕНИЯ ПО/ ИАЗОСОЕДИНеШЯ


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ крашения или печати природных,синтетических полиамидов или натуральной кожи | 1980 |
|
SU1168098A3 |
| Способ крашения текстильного материала из шерстяных или синтетических полиамидных волокон | 1974 |
|
SU556734A3 |
| Способ получения бензтиазолового азокрасителя | 1972 |
|
SU470971A3 |
| СПОСОБ ПОЛУЧЕНИЯ АЗОКРАСЙТЁЛЕЙ | 1971 |
|
SU298127A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДИСАЗОКРАСИТЕЛЯ | 1969 |
|
SU416954A3 |
| Способ получения пиразолового моноазокрасителя | 1973 |
|
SU537631A3 |
| СПОСОБ ПОЛУЧЕНИЯ РЕАКТИВНОГО МОНОАЗОКРАСИТЕЛЯ | 1971 |
|
SU296322A1 |
| Способ получения орто-окси-азокрасителей | 1927 |
|
SU13989A1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОАЗОКРАСИТЕЛЕЙ | 1968 |
|
SU209323A1 |
| СПОСОБ ПОЛУЧЕНИЯ МОНОАЗОКРАСИТЕЛЕЙ | 1969 |
|
SU252223A1 |

1
Изобретение относится к получению новых азокрасителей, в частности к способу получения полиазосоединения, которое может быть использовано для крашения текстильных материалов,преимущественно кожи.
Известен способ получения полиазокрасителя для кожи формулы
N
$05Н
Способ состоит в сочетании предварительно продиазотированного аминосоединения с азосоставляющей бензольного ряда.
Недостатком красителя, полученного по известному способу, является его канцеро™ гениость, а также низкая красящая способность по отношению к рубленой коже. I
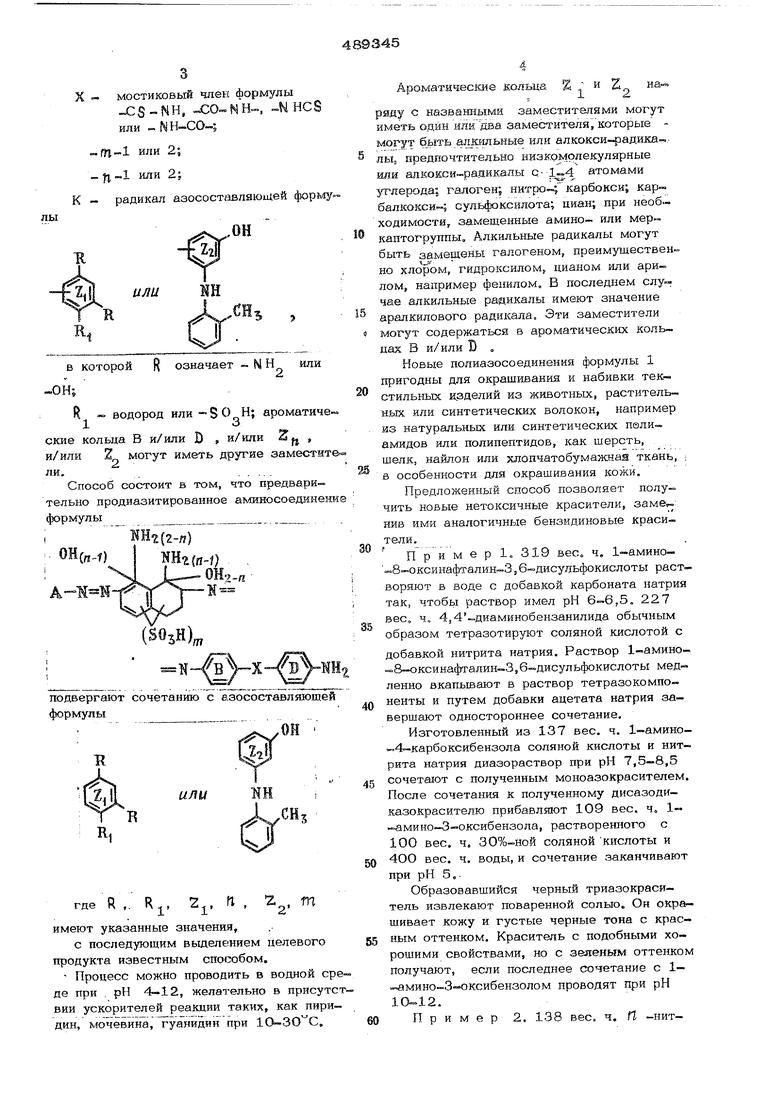
Предлат ается способ получения полиазосоединения; обшей формулы
(-« онап-п} г(п-1)
N
()
-/В
где А - незамещенный ф ениловый радикал или фениловый радикал, замещенный низкомолекуляр- ной алкильной, алкоксиS - алкильной, -COOH,-SO Н,о
-WO , гидроксильной группой, галогеном, или при необходимости аминогруппой сульфокислоты или карбоновой кислоты, или алкиламино-, ариламино- или ациламиногруппой;
X - мостикоБый член формулы
CS-NH, -CO-.NH-, -Ы HCS или -NH-CO-i
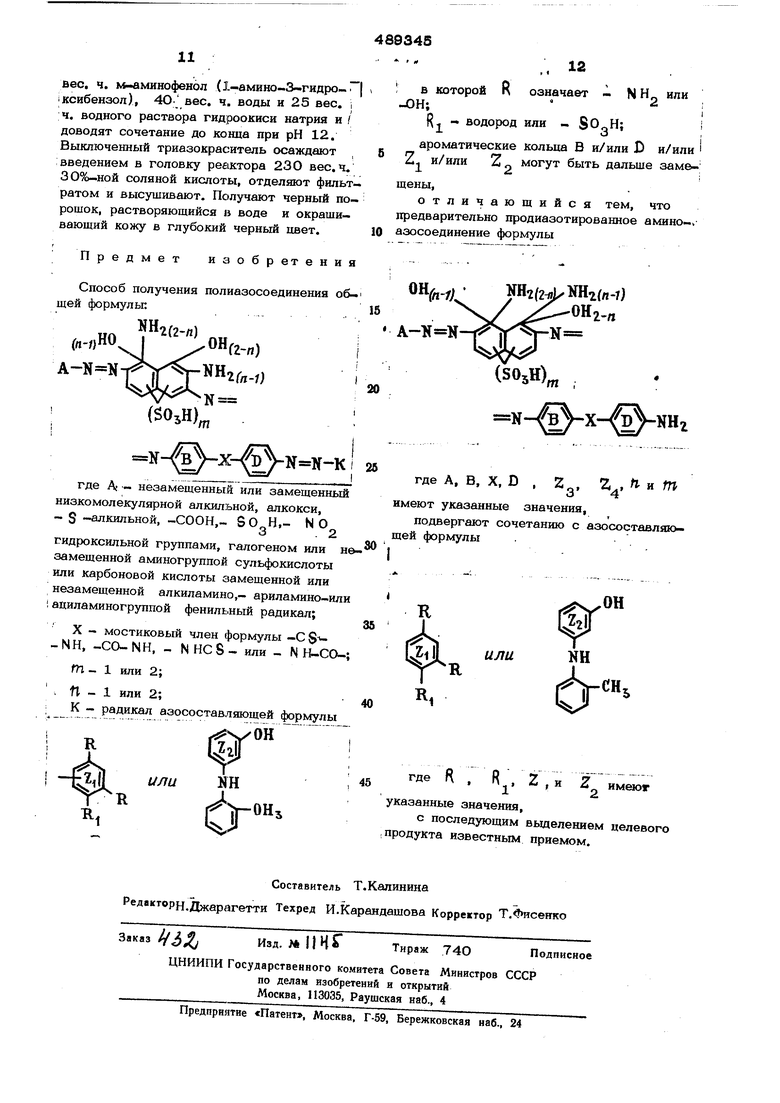
-m-i или 2; fl-l или 2-. К - радикал азосост;звляюи1ей форму.лы
или
в которой R означает -. N Н или -ОН;
R - водород или - S о Н; ароматичеIо
ские кольца В и/или D , и/или fj ,
и/или Z могут иметь другие заместители.
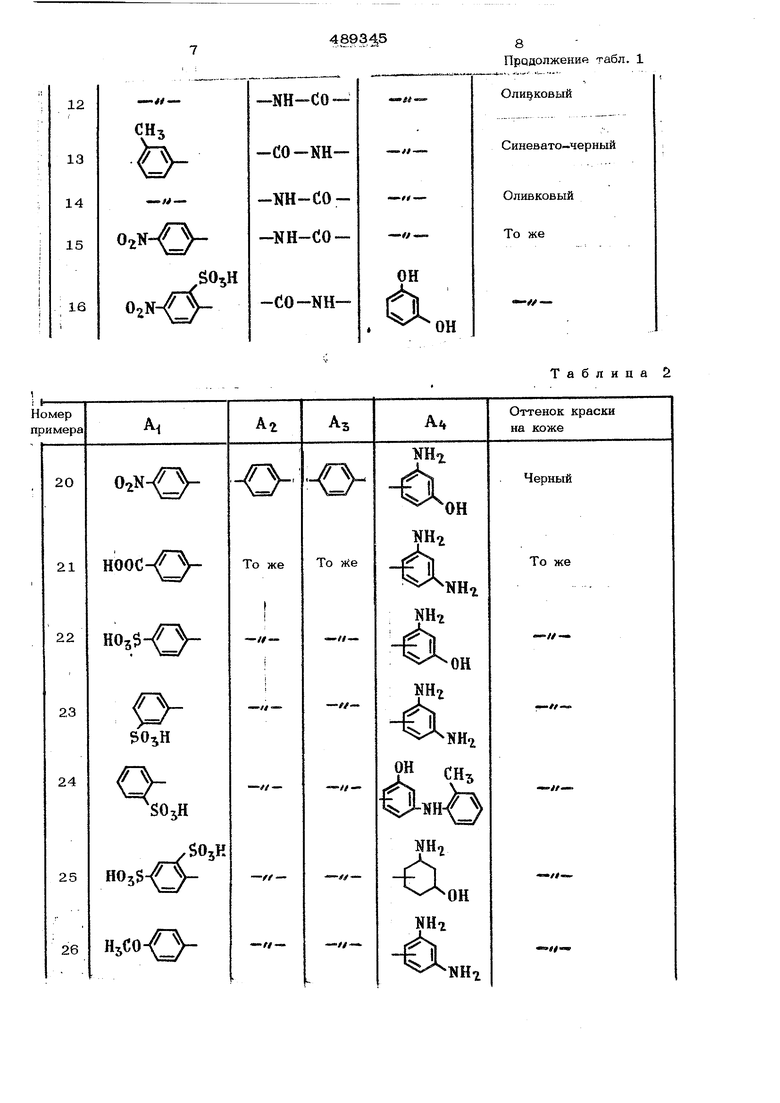
Способ состоит в том, что предварительно продиазитированное аминосоединеш-ie формулы
КН2(2-/г)
Щп-1)тг(п-1)
,-«
A- M-fnfV™N-
Ч(
(SOjH)
сочетанию с е.зосоставляющей
Y
или
где R ,. R ,
fl
-Г I
имеют указанные значения,
с последующим вьвделением целевого продукта известным спо«Х)бом,
Процесс можно проводить в водной среде при . рН 4-12, желательно в присутствии ускорителей реакции таких, как пиридин, мочевина, гуаяидин при lO-SO C.
Ароматические кольца и и Z. нас названными заместителями могут иметь один или два заместитеяя,которые MorjfT бь1ть алкнльные или алкокси- адика-,.лы предпочтительно низкомолекулярные или алкокси-радйкалы Q- 1„4 атомами углерода; галоген; нитро™; карбокси; кар- балкокси-; сульфоксилота; ииан; при необходимости, замещенные амино- или меркаптогруппы, Алкильные радикалы могут быть замешены галогеном, преимущественно хлором, гидроксилом, цианом или арилом, например фепйлом В последнем слу™ чае алкильные радикалы имеют значение
« аралкилового радикала, Зти заместители могут содержаться в ароматических кольцах В и/или D „
Новые полиазосоединения формулы 1 пригодны для окрашивания и набивки тек стильных изделий из животных, растительных или синтетических волокон, например из натуральных или синтетических пели- амидов или полипептидов, как шерсть, шелк, найлон или хлопчатобумажнан ткань, ; в особенности для окрашивания .
Предложенный способ позволяет получить новые нетоксичные красители, заме нив ими аналогичные бензидиновые красители.
Пример. 319 вес. ч. 1 амино 8-оксинафталин--35б- дисудьфокислоты растворяют в воде с добавкой карбоната патрия так, чтобы раствор имел рН 6-6,5. 227 вес, ч. 4,4-диаминобензанилида обычным образом тетразотируют соляной кислотой с добавкой нитрита натрия. Раствор 1-амино- .8--оксинафталин-3,6-дисульфокислоты медленно вкапьшают в раствор тетразокомпоненты и путем добавки ацетата натрия завершают одностороннее сочетание.
Изготовленный из 137 вес. ч. 1-амино- -.4-карбоксибензола соляной кислоты и нитрита натрия диазораствор при рН 7,5-8,5 сочетают с полученным моноазокрасителем. После сочетания к полученному дисазоди- казокрасителю прибавляют 109 вес. ч. 1«ймино 3-оксибензола, растворенного с 100 вес. ч, 30%-ной соляной кислоты и 40О вес. ч. воды, и сочетание заканчивают при рН 5,.
Образовавшийся черный триазокраси- тель извлекают поваренной солью. Он окрашивает кожу и густые черные тона с красным оттенком. Краситель с подобными хорошими свойствами, но с зеленым оттенком получают, если последнее сочетание с 1- мино-3-оксибензолом проводят при рН 10-12.
Пример 2. 138 вес. ч, П -нитроанилина диазотируют обычным образом с нитратом натрия и соляной кислотой. В раствор диазония впивают нейтральный расутвор, состояший из 309 .вес. ч. 1 амино-.8-.гидрок;си-нафталин-3,6-.дисульфоновой кислоты в воде таким образом, что значение рН реакционного раствора не превышает, 2,3,
После сочетания в моноазокраситель добавляют соединение диазония, полученного из 173 вес. ч. 1-аминобензол-4-суль- фоновой кислоты, нитрата натрия и соляной кислоты при рН 9,5, сочетают в диаз краситель. После сочетания диазокрасйтель нагревают до 40° и восстанавливают i нитрогруппу 117 сульфида ;натрия при рН В этот диазоамино краситель добавляют 185,5 вес. ч„ 4-нит робензоилхлорида и конденсируют добавлением гидроокиси натрия до наступления щелочной реакции. После конденсации в краситель добавляют 17 вес. ч. сульфида натрия и радуцируют нитрогруппу. Установлением значения рН-7 и добавлением хлорида натрия изолируют краситель, который размещают в воде, с соляной кисло
той устанав;7ивают конго-соленым и диазо- тируют добавлением нитрита натрия.
В диазотированный краситель добавляют раствор, состоящий из 1О9 вес. ч, 1-амино-3 гидроксибензола и воды и гид- роокиси натрия и сочетают при рН 9.
Оставшийся триазокраситель изолируют хлоридом натрия. Он представляет собой темный олив ков о-зеленый порошок, хорошо растворяющийся в воде и прочно окрашивагюший кожу.
в табл. 1 указано структурное строение красителей, полученных по примерам 3-16 и соответствующих формуле
N
Н0з$- $05Н
N N-К,
где А, X и К имеют указанные зна
чения.
Таблица i
Таблица S
,j
-/#«
27
W28
Г29
30
Иро юлжение табл. 2
#rf.
.jj.
#Черный с зеленоватым OTTeiiKOM
To же
To же
31
To
же
O.K32
To же
33
.// -
34
Черный с зеленоватым оттенком
То же
| Черный
В табл. 2 указано структурное строение красителей, полученных по примерам и соответствующих формуле
щк он
чЖ-хЦ 2
W
где А, А„, А и Ад имеют указан-
ныв в таблице значения,
Пример 3, 22,7 вес. ч. 4,4-: -диаминобензанилида {4-аминобензоил-4-аминоанилид) тетразуют с 60 вес. ч..
ЗО%-ной соляной кислоты, ЗО вес. ч. льда и 13,8 вес. ч. нитрита натрия, К соединению тетразония нри О-5 прика- пьшают нейтральны.й раствор, состоящий из 31,9 вес. ч. 1-амино-8-1идрокси-нафта-. лин-3,6 дисуль4юновой кислоты и 100 вес, ч. воды, всыпанием бикарбоната натрия при рН 2-2,6 заканчивают одностороннее сочетание.: После реакции диазосоеди- нение из 17,3 вес. ч. 1-амииобензол-сульфоновой кислоты добавл5пот в моиоазокраситель и прикапьшанием водой гидроокиси натрия при рН 6-7 доводят реакцию до конца.
В образовави1ийся диазокраситель доб 1вляют раствор, состоящий из 1О,9
Авторы
Даты
1975-10-25—Публикация
1973-02-13—Подача