лотным анионом, можно выделить свободное основание. Пол ченные таким образом основанря можно внойь перевести в те же или другие .
В -качестве ккслоты обычно применяют соляную, бромистоводородную, йодистоводородную, азотную, серную или сернистую, фосфорную, уксусную, молочную, лимонную, винную, янтарную, малеиновую и глюконовую.
Полученные соединения содержат асимметрический атом углерода. Таким образом, каждая структура содержит две энантиоморфкые формы с точно одинаковыми химическими и физическими свойствами, отличающиеся лишь направлением вращения плоскости поляризованного луча. Разделение подобной пары на оптически активные изомеры можно осуществить известными методами.
Среди полученных соединений следует особенно отметить:
2 - оксиметил - 3-окси-6-(Г-окси-2-изопропиламиноэтил) -пиридин;
2 - оксиметил - 3-окси-6-(1-окси-2-т;7ет-бутиламиноэтил) -пиридин;
2 - оксиметил - 3-окси-6-{1-окси-2- 3 -(«метоксифенил)-Г-метилпропиламино - этил}пиридин;
2 - оксиметил - 3-окси-6-{1-окси-2- 2 -(поксифенил)-Г-метилэтиламино -этил} - пиридин;
2 - оксиметил - 3-оксн-6-{1-окси-2- 2 -(лметоксифенил) - Г-метилэтиламино - этил}пиридин;
2 - оксиметил - 3-окси-6-{Г-окси-2- 3 - (поксифенил) - Г-метилпропиламино -этил}-пиридин.
Пример 1. Дигидрохлорид 2-оксиметил-Зокси-6-(Г-окси-2- изопропиламиноэтил) - пиридина.
В раствор 6,6 г 2-фенил-6-(Г-окси-2-изопропиламиноэтил)-4Н-ж-диоксино {5,4-в) пиридина в 150 мл метанола приливают 40 мл 1,0 н. метанольного раствора хлористого водорода и 50 мл воды. Раствор нагревают в течение 7 ч при 50°С, затем упаривают под вакуумом до объема примерно в 30 мл. Медленно приливают диэтиловый эфир, выпадает дигидрохлорид. Продукт очищают дополнительной перекристаллизацией из метанола - эфира.
Пример 2. Дигидрохлорид 2-оксиметил-Зокси-6-(Г-окси-2-изопропиламиноэтил) - пиридина.
В раствор 3,1 г 2,2-диметил-6-(1-окси-2изопропиламиноэтил)-4Н-Л1 - диоксино (5,4-в) пиридина в 50 мл метанола вносят 23 мл 1,0 н. метанольного раствора хлористого володора и 0,30 мл воды. Раствор нагревают в течение 7 ч при 50°С, затем упаривают под вакуумом до объема в 10 мл. Медленно приливают диэтиловый эфир, выпадает Дигидрохлорид. Его очищают перекристаллизацией из метанола -
эфира. Продукт плавится при 186°С с разложением.
Пример 3. Дигидрохлорид 2-оксиметил-Зокси-6-(1-окси-2-т/7ет-бутиламиноэтил) - пиридина.
Смещивают 3,3 г дигидрохлорида 2-фенил-6(Г-окси-2-г/7ет-бутиламиноэтил) - 4Н-л{-диоксино (5,4-в) пиридина, 30 мл метанола, 0,40мл воды, 1 каплю концентрированной соляной кислоты и нагревают в течение 7 ч при 50°С. Затем раствор охлаждают до 25°С и приливают 100 мл диэтилового эфира, выпадает целевой продукт. Его очищают перекристаллизацией из метанола- эфира. Он плавится при 182°С с разложением.
Пример 4. Дигидрохлорид 2-оксиметил-Зокси-(Г-окси-2-т/7ег-бутиламиноэтил) - пиридина.
Загружают 4 г дигидрохлорида 2,2-диметил6-(Г-окси-2-г/зег-бутиламиноэтил) - 4Н-лг-диоксино (5,4-в) пиридина, 30 мл метанола, 0,5 мл воды и 2 капли концентрированной соляной
кислоты и нагревают в течение 7 ч при 50°С. Раствор охлаждают до 20°С и медленно приливают 100 мл диэтилового эфира, выпадает целевой продукт, который перекристаллизовывают из метанола-эфира. Продукт плавится
при 182°С с разложением.
Пример 5. Исходя из 2-фенил-6-(1-окси2-аминоэтил)-4П-ж-диоксипо (5,4-в) пиридинов аналогично получают соединения со следующими значениями радикалов:
RIRI
СбН5СН2С(СНз)2- СбН5СН(С2Н5)СН2СН2-3,4-(СН202)- 3-НОСбН4(СН2)зСН(СНз)СбНзС.Н2- СНз- СПз(СН2)2СНСНз
(СНз; мССП2цикло-СзНбЦИКЛО-С7П133,4-(СНзО)2СбПзСН24-ПОСбН.1СП2СП(СНз)Пример 6. Исходя из 2,2-диметил-6-(Гокси-2-аминоэтил)-4П-ж-диоксино (5,4-в) пиридинов получают соединения со следующими значениями радикалов:
RI
RI
СНз-CeHsCHjн-СзН7-4-СНзОСбН4(СН2)2Н-С4Н9-СбН5(СН2)4(СНз)зССН2-2-СНзОСбН4(СН2)2(С2Н5)2СН-3,4-(СН2О2)СбНзСН2цикло-СзНб-4-НОСбН4 (СН2) зСН (СНз) цикло-СбН,,-3-СНзОСбН4 (СН2) зСН (СИз) ЦИКЛО-С7Н13-3,4-(СНзО)2СбНзСН2СН(СНз)Формула изобретения
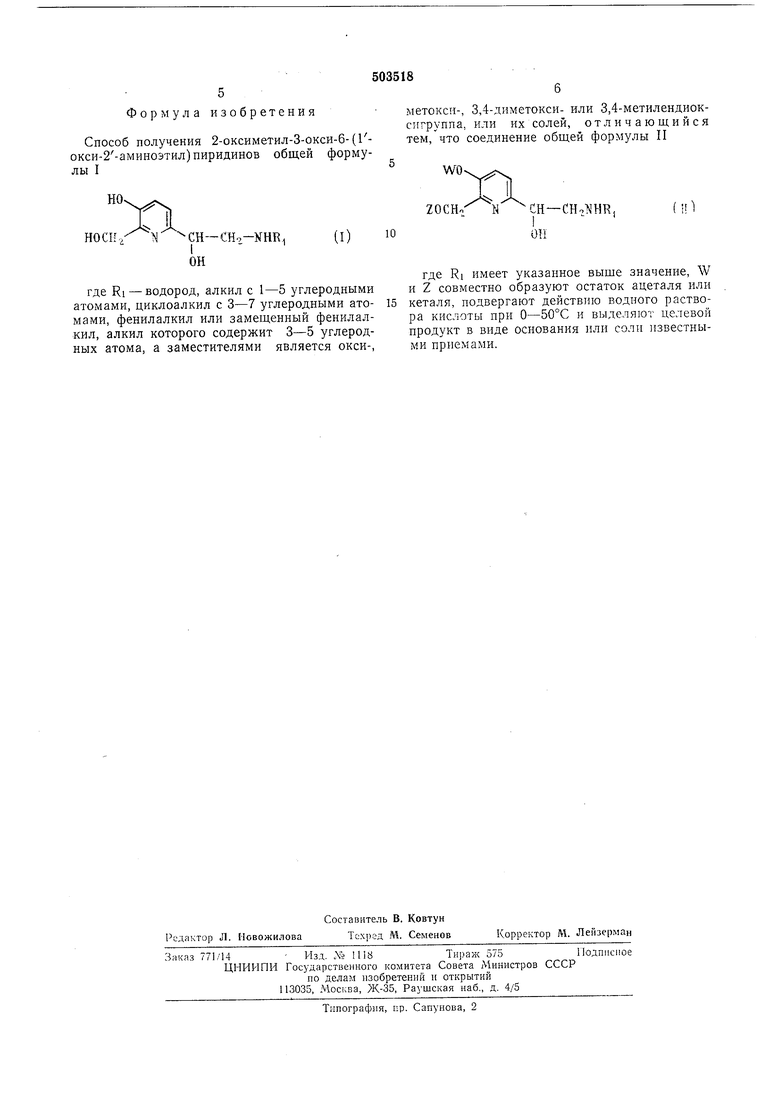
Способ получения 2-оксиметил-3-окси-6-(1окси-2-аминоэтил)пиридинов общей формулы I
НО
НОСИ СН-СНг-NHR.,
(I) ОН
где RI - водород, алкил с 1-5 углеродными атомами, циклоалкил с 3-7 углеродными атомами, фенилалкил или замещенный фенилалкил, алкил которого содержит 3-5 углеродных атома, а заместителями является окси-.
метокси-, 3,4-диметокси- или 3,4-метилендиоксигруппа, или их солей, отличающийся тем, что соединение общей формулы II
WO
N СН-CH.NHRj
ZOCH
ОН
где RI имеет указанное выше значение, W и Z совместно образуют остаток ацеталя или кеталя, подвергают действию водного раствора кислоты при О-50°С и выделяют целевой продукт в виде основания или соли известными приемами.



Авторы
Даты
1976-02-15—Публикация
1973-09-12—Подача