C-NRj-CHe-CHrN -ННа
и.
R.

| название | год | авторы | номер документа |
|---|---|---|---|
| Производные 3-карбамоил-1-тиаизохроман-1,1-диоксида или их соли, проявляющие психотропную активность | 1974 |
|
SU559923A1 |
| Способ получения четвертичных аммониевых солей производных 3-(3"-аминопропилкарбамоил)-1,1-диоксо-1тиаизохромана | 1973 |
|
SU512207A1 |
| Способ получения производных 3-карболкокси1-тиа-изохроман-1,1-диоксидов | 1970 |
|
SU493960A3 |
| Способ получения производных 1тио-1,1-диоксидаизохромана | 1970 |
|
SU523900A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3-КАРБАЛКОКСИ-1-ТИАИЗОХРОМАН-1,1-ДИОКСИДА | 1973 |
|
SU390719A1 |
| ВОВСОЮЭНАЯ JШШ111-Ти[ШЧГ1.'--ЯВМБЛИОТЕНЛ | 1972 |
|
SU328578A1 |
| Способ получения производных 4-амино-2-пиперидинхиназолина или их солей | 1980 |
|
SU953982A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 3-КАРБОКСИ-1-ТИА-ИЗОХРОМАН-1,1-ДИОКСИДОВ | 1973 |
|
SU400103A1 |
| ПРОИЗВОДНЫЕ 4-ФЕНИЛМЕТИЛ-1Н-ИНДОЛА В ВИДЕ ЭНАНТИОМЕРОВ, РАЦЕМАТОВ ИЛИ ДИАСТЕРЕОИЗОМЕРОВ ИЛИ В ВИДЕ КИСЛОТНО-АДДИТИВНЫХ СОЛЕЙ, ОБЛАДАЮЩИЕ АНТИАРИТМИЧЕСКОЙ ИЛИ АНТИКАЛЬЦИЕВОЙ АКТИВНОСТЬЮ | 1992 |
|
RU2067576C1 |
| ПРОИЗВОДНЫЕ ХИНОЛИНА И ХИНАЗОЛИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2130934C1 |

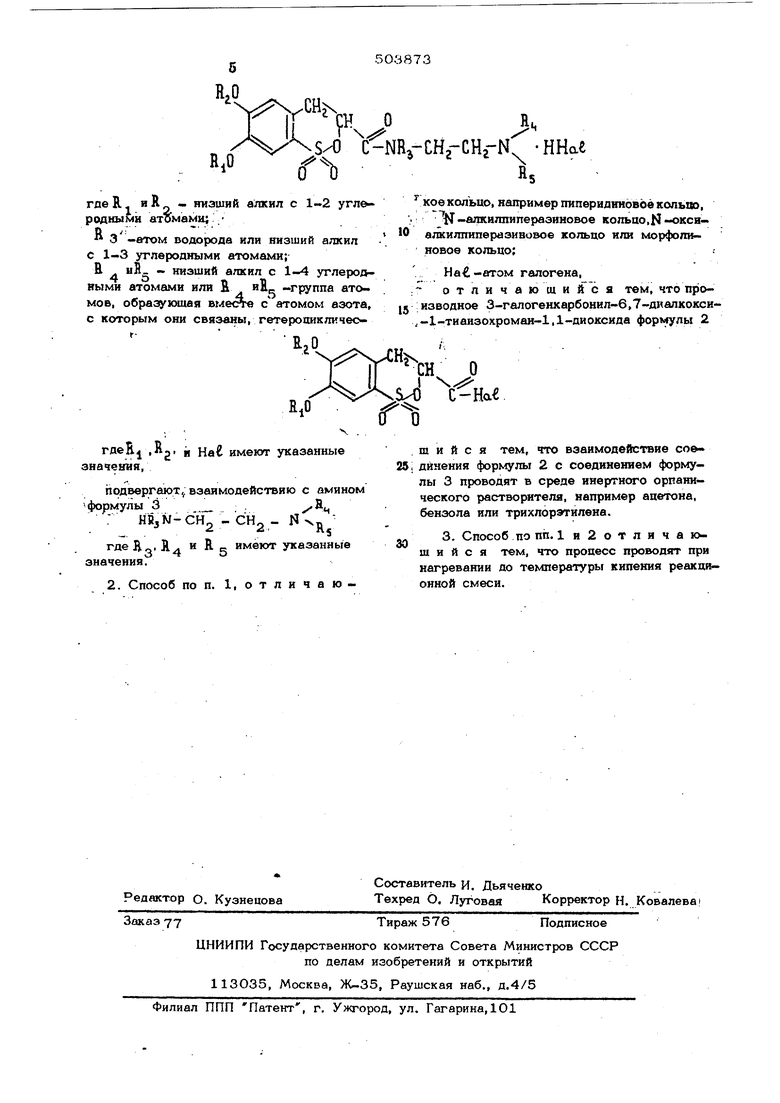
гдеН и В. - низший алкил с 1 - 2 углеродными атомами;
R атом водорода или низший алкил
с 1 - 3 углеродными ат омами;
ц и Rj- низший алкил с 1 - 4 угле родными атомами или R . и R.-группа атомов, образующая вместе с атомом азо-. та, с которым они связйиы, гетероциклическое кольцо, например пиперидиновое колыю.-алкилпиперазиновое кольцо, Н - .. - ксиалкилпиперазиновое кольцо или мор фолиновое кольцо;
На-Ё. -атом галогена.
Эти соединения обладают больи1ей физиологической активностью по сравнению с ближайшими аналогами подобного дей-
.СТБИЯ.
Способ основан на реакции взаимодействия 3-хлоркарбонил-6,7-диалкокси-1- . -ти ат1:зрхроман-1,1-диоксида с первичными или вторичными алифатическими амине ми.
Предлагаемый способ заключается в том, что производное 3-галогенкарбонил- -Ъ,7 диалкокси-1-тиаиэохрома -1,1-днокси яа формулы 2 ;н о SH) 0 где R. , R 2 имеют указанные значения, подвергают взаимодействию с амином форк1улы 3 HfijN -fflj,-CHj-N, гдеЯ. Кц и R, имеют указанные значения.-/ В качестве аминов используют, например, 2-диэтиламиноэтиламин, 2-диизобути аминоэтиламин, 2-пиперидиноэтиламин, 2- -морфолиноэтилеи лин, 2-диэтилaминoэтил-. -N-кзoпpoпилaмин и 2-.пиперидиноэтИгь. - N-метиламин. При Еэанмодействик соединения формулы 2 с аминами формулы 3 исходные компоненты .берут в эквимолярном количестве, причем реакцию предпочтительно проводить в среде инертного органического растворите ля, например ацетона, бензола или трихло{ этилена, при температуре от комнатной до температуры кипения реакционной смеси. Полученный продукт очишают перекристаллизацией из органического растворителя, например из метилового спирта, этилового спирта.; или из смеси различных спиртов. П р и м е р . К охлажденной смеси, содержащей 6,1 г 3-хяоркарбонил-6,7-ди- метокси-1-тиаизохромап-1,1-диоксида и 30 мл ацетона, прибавляют при перемешивании раствор, приготовленный из 2,3 г 2-диэтиламиноэтиламина и 20 мл ацетона После перемешивания реакционной смеси при комнатной температуре в течение 1,5 час выделившуюся в осадок солянокислую соль 3-(2-диэтиламиноэтилкарбамоил)-6,7 -диметокси- 1-тиаиэохроман-1,1-диоксида отфильтровывают, промывают ацетоном и сушат. Выход продукта составляет 7,8 г (92,2% от теоретического). Неочищенный продукт перЬкристаллизовывают из абсолют кого этилового спирта т. пл. полученного продукта составляет 147,5-153,3 С. Найдено,%: С 4J,88; Н 6,77;N6,38; 5 7,66. С„Н„,,Н„0„3- НС€ (мол. в. 422.9). J. / iiO «i D Вычислено;%:С 48,28; Н 6,43;Ne.62; , S7,57. Аналогичным способом получают и друсоединения. 3-(2-Ш{изoбyтилaминoэтилкap aмoил)- 7-диметокси-1-тиаиэохроман-1 ,1-диок, хлоргидрат, плавится при 117-125 С. Найдено,%: С 5Я,46; Н 7,5O;N5,97; 5 6.89. С И N„05- НС€ 44ill 34 2 Ь, л. в. 479,1). Вычислено,%: С 52,6; Н 7,36;N 5,85; S6, 70. 3-(2 -Диэтилaминoэтил-N-изoпpoпилбамойл )-6,7-диметокси-1-тиаизозфоман1-диоксид, хлоргидрат, плавится при 2-184°С. Найдено,%: С 51, 76; Н 7,45;N6,04; S 7.07. С И N OS- нее (мол. в. 465,0) Вычйсле1Ю. С 51.66; Н 7,15;N6,02; jS 6,90. 3-(2 -пиперидинеэтилкарбамоил)-6.7- метокси-1-тиаизохроман-1,1-диоксид, оргидрат, плавится при 179,5-186°С. Найдено,%: С 49.67; Н 6,48;Нб,22: S 7.36. (мол. в. 435,0) Вычислено,%: С 49,7О; Н 6,26;Кб,44,,S 7,37. 3-(2 -Морфолиноэтилкарбамоил)-6,7иметокси-1-тиаизохроман-1,1-диоксид, оргидрат, плавится при 195-198°С. Найдено,%: 0465.75; Н 5,96;N6,15; S 7.Р9. (мол. в. 436,9). Вычислено,.%: С 46,73; Н 5,77;N6,41; S 7,34. 3-(2 -пипepидинoэтил-N-мeтилкapбaил)-6,7-диметокси-1-тиаизохроман-1,1-; иоксид, хлоргидрат, плавится при 155О°С. Найдено,%: С Н 6,66;N6,08; 5 6,83. C,H.. -нее (мол.в. 449,0) 19 2tt 2 о Вь1числено,%: С 50,83; Н 6,,24; S7.14. Формула изобретения 1. Способ получения Ы,Н-Дизамещенны}, роизводных, 3-( 2 -аминоэтилкарбамоил ),7-диатжокси- -тиаизохромап-1,1-ди- сида (}хэрмулы 1
V/°
S/0 с НВгСНг(f
где В. и R - низший алхил с 1-2 угл&родными атомами; .
ВуГ V
Э -атом водорода или низший алкил
с 1-3 углеродными атомами;
R ИЙ- - ииэший алкил с 1-4 углеродными атомами или Ь иЕ -группа атомов, обра; юшая вместе с атомом азота, с которым они связаны, гeтepoшIкличec-
гдеЯ .Rg- и На имеют указанные ,
подвергают взаимодействию с амином формулы 3 .
: нйзМ-сн - сн - f R
гдеЯ,. а и R
имеют указанные
значения,
коекольцо, например пипериднновоё колыю, , -алкилпиперазиновое кольцо,N-окси10 алкилпиперазивовое кольцо или морфопиновое кольцо;
На€|-атом галогена,
: отличаюшиСся тем, что проJ5 изводное 3-галогешсарбонил-6,7-диалкокси 1-тиаизохромаи-1,1-диоксида формулы 2
сн о
.5И)
Г
о
ш и и с я тем, что взаимодействие со&« дйнения формулы 2 с соединением формулы 3 проводят в среде инертного орпанического растворителя, например ацетона, бензола или трихлорэтилена.

Авторы
Даты
1976-02-25—Публикация
1973-08-29—Подача