Как правило, алкил и ал.коксил представляют собой низшие алкил и алкоксил.
Для защиты гидрокснльных групп обычно используют пропзводные ацила, циклические ацетали и кетали. Ацильные группы омыляют преимущественно щелочами, а циклические ацетали или кетали отщепляют преимущественно с помощью муравьиной кислоты или разбавленных ми 1еральных кислот.
Перевод це.тевых соединений, с которых Кз - аллОлСил, в соединения, в которых - гидроксил, проводят щелочным омылением; соединения, в которых Rs - амино- или алкиламнногруппа, получают при обработке аммиаком или алкиламинами.
Из фармакологически приемлемых солей можно назвать соли соляной, серной, фосфорной, бромистоводородной, уксусной, .молочной, лимоипой, яблочной, салициловой, малоновой, малеиновой или янтарной кислоты.
П р и м е р. N(6)-(3 - Этоксикарбопилбензил)-аденозин.
:К суспензии 2,6 г аденозина в 50 мл N,Nдиметилацетамида при 70° С постепеино .прибавляют 7,5 г этилового эфира 3-бромметилбензойной кислоты. Через 1 час образуется прозрачный раствор, который выдерживают 24 часа при 70° С, выливают в 200 мл эфира и выпавший маслянистый осадок растворяют в воде. К водному слою прибавляют 68 лм 0,1 н. едкого натра, экстрагируют эфиром, экстракт высушивают и выпаривают, остаток перекристаллизовывают из небольшого количества этилового спирта и получают 1,3 г (30%) целевого продукта, т. пл. 132-135° С.
Аналогичным образом получают:
N(6)-(3-Этoкcикapбoнил-2 - метилбензил)аденозин, т. пл. 1-38-139° С
N(6)-(4 - Мето,ксикарбонилфенэтил)-аденозин, т. пл. 183-184° С
N(S)-{4 - Этоксикарбонилбензил)-2 - хлораденозин, т. пл. 188-190° С
N{6)-(3 - Метоксикарбонилбензил)-адеиозин, т. пл. 95-97° С, выход 85%
N(6)-(2 - Этоксикарбонилбензил)аденозин, т. пл.105-107° С, выход 47%
N(6) - (4 - Этоксикарбонилбензил)-адеиозин, т. пл. 151 -153° С, выход 70%
N(6) - (3 - Изопропоксикарбонилбензил)аденозин, т. пл. 81-83° С, выход 64%
N(6)-(5 - Это-кси карбопил-2-метилбензил)аденозин, т. пл. 164-165° С, выход 59%
N(6) - (3 - Этоксикарбоиилфенэтил)-аденозин, т. пл. 137-138° С, выход 65%
N(6)-(4 - Этокср карбонилфенэтил)-аденозин, т. пл. 176-177° С, выход 62%
N(6)-(4 - Этоксикарбонил-2-метилбензил)аденозин, т. пл. 150-15ГС, выход 65%
N(6)-(3 - Этоксикарбонилбеизил)-2 - хлораденозия, т. лл. 167-169°С, выход 30%
N (6) - (4 - Метоксикарбонилфенэтил) - 2 хлорадеиозин, т. пл. С, выход 74%
N (6) - (3-Этоксикарбонилбензил) -2-бромаденозин, т. пл. 163-165° С, выход 68%
N(6)-(4 - Этоксикарбонилфенэтил)-4-бромаденозин, т. пл. 174-176° С, выход 65%
N(6)-(3 - Этоксикарбонилбензил)-2-оксиаденозин, т. пл. 168-170° С, выход 18% N(6)-(2 - Этоксикарбонилфеиэтил) - аденозин, т. пл. 107-109° С, выход 23%
N(6)-(4 - Карбоксибензил)-аденозин, т. пл. 250-251° С
N(6)-(3 - Карбокси-2-метилбензил)-аденоЗИН, т. пл. 204-206° С
N(6)-(2 - Карбоксибензил)-аденозин, т. пл. 150-151° С, выход 17,5%
Ni6)-(3 - Карбожсибензил)-аденозин, т. пл. 240° С (разл.), выход 84%
N(6)-(5 - Карбокси-2-метилбензил)-аденозин, т. пл. 274° С (разл.), выход 95%
Т(6)-(3-Карбоксифенэтил)-аденозип, т. пл. 205°С (разл.), выход 70%
М(6)-(4-Карбоксифенэтил)-адеиозин, т. пл. 207-208° С, выход 85%
N(6)-(4 - Карбокси-2-метилбе.нзил)-аденозин, т. пл. 263° С (разл.), выход 86%
N(6)-(3 - Карбоксибензил)-2 - хлораденозин, т. пл. 250° С (разл.), выход 40% N(6)-(3-|Карбамоилбенэил)-аденозин, т. пл. 225° С
N(6)-(3 - Карбамоилфенэтил) - аденозин, т. пл. 162-164° С
N(6)-(2-Карбамоилбензил)-аденозин, т. пл. 130° С (разл.), выход 22,5%
N(6)-(4 - Карбамоилбензил)-2 - хлораденозин, т. пл. 190-192° С
N (6)-(4-Карбамоилбензил)-аденозин, т. пл. 181-4 83° С, выход 80%
N(6)-(5 - Карбамоил-2-метилбензил)-аденозин, т. пл. 220-222° С, выход 59%
N (6)-(4-Карбамоилфенэтил)-аденозин, т. пл. 203-,204° С, выход 44%
N(6)-(3 - Карбамоил-2-метилбензил)-адеКОЗИН, т. пл. 235-237°С, выход 40%
N(6)-(4 - Карбамоил-2 - метилбензил)-аденозии, т. пл. 144-146° С, выход 71%
N(6)-(4-Карбамоилфенэтил)-2 - хлораденозин, т. пл. 135-138°С, выход 27% N(6).-(4 - Карбамоилбензил)-2-бромаденозии, т. пл. 210-212° С, выход 64%
N(6)-(4 - Карбамоилбензил)-2 - оксиаденозин, т. пл. 185-188° С, выход 14% N(6) - (2 - Метиламинокарбонилбензил)аденозин, т. пл. 114-И 5° С
N(6)-(3 - Метиламинокарбонилфенэтил) аденозин, т. пл. С
N(6)-(3 - Метиламииокарбонилбензил)-аденозин, т. пл. 158-.160° С, выход 90%
N(6)-(4 - Метиламинокарбоиилбензил)-аденозин, т. пл. 165-167° С, выход 83%
N(6)-(3 - Метиламинокарбонил-2 - метилбензил)-аденозин, т. пл. 192-194° С, выход 30%
N(6) - (4 - Метиламинокарбонилфенэтил)адеиозин, т. лл. .С, выход 53%
N(6)-(4 - Метиламинокарбонилфенэтил)-2бромаденозин, т. пл. 186-187° С, выход 40%.
Формула изобретения
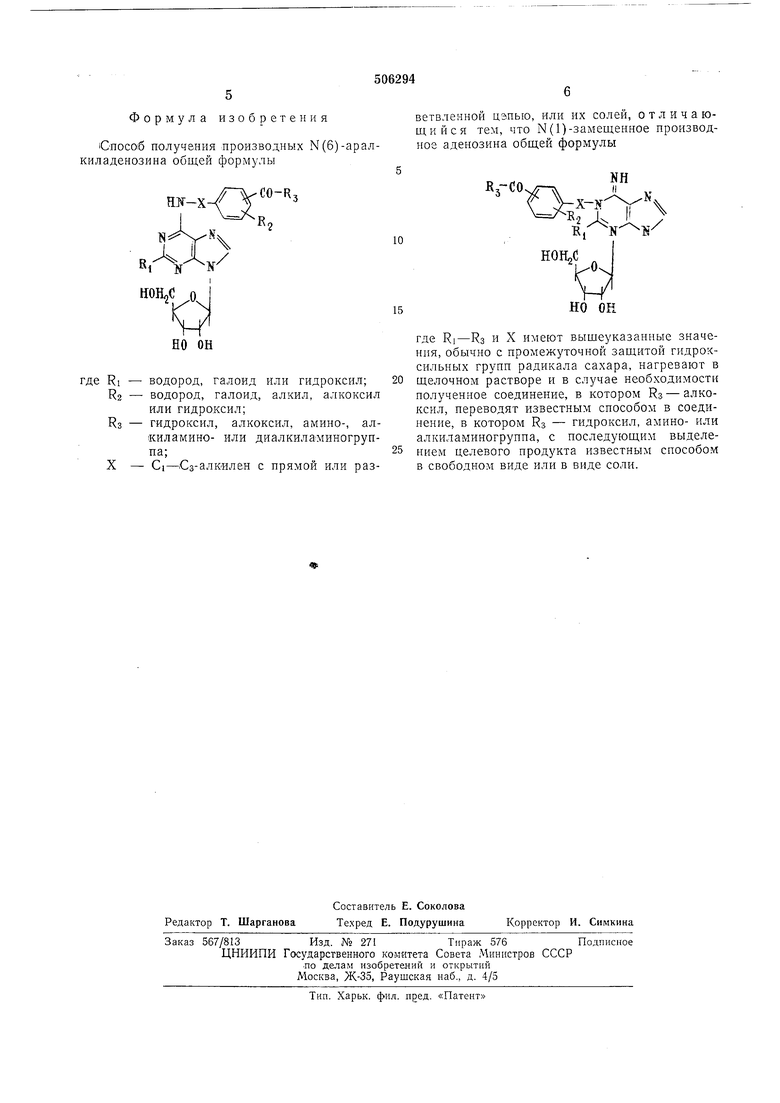
Cnocoi6 получ&ния производных Н(6)-аралкиладенозина общей формулы
ветвленной цэпью, или их солеи, о т л и ч а гощи йен тем, что N(1)-замещенное производное аденозина общей формулы
CO-Rj
НЖRo
S
о I
W
но он
е RI
водород, галоид или гидроксил;
R2
водород, галоид, алкил, алкоксил
или гидроксил;
Кз
гидроксил, алкоксил, амино-, алкиламино- или диалкила миногруппа;
Ci-Сз-алкиле.н с прямой или разX
НО ОК
где RI-Нз и X имеют вышеуказанные значения, обычно с промежуточной защитой гидроксильных групп радикала сахара, нагревают в щелочном растворе и в случае необходимости полученное соединение, в котором Ra - алкоксил, переводят известным способом в соединение, в котором RS - гидроксил, амино- или алкиламиногруппа, с последующим выделением целевого продукта известным способом в свободном виде или в виде соли.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения (6)-аралкиладенозина | 1971 |
|
SU469253A3 |
| Способ получения (6)замещенных производных аденозина | 1972 |
|
SU539532A3 |
| Способ получения производных аденозина | 1973 |
|
SU515454A3 |
| Способ получения производных аденозина | 1973 |
|
SU576955A3 |
| Способ получения /6//-дизамещенных производных аденозина" | 1973 |
|
SU515459A3 |
| Способ получения производных бензиламина или их солей | 1975 |
|
SU521838A3 |
| Способ получения производных бензиламина или их солей | 1975 |
|
SU543341A3 |
| Способ получения производных аденозина | 1971 |
|
SU444368A1 |
| Способ получения глюкозамина или его солей | 1977 |
|
SU747430A3 |
| Способ получения производных бензиламина или их солей | 1975 |
|
SU528866A3 |


Авторы
Даты
1976-03-05—Публикация
1971-11-30—Подача