1
Изобретение относится к способу получеюш новых производных пиперазина, обладающих биопогической активностью и проявляюищх улучшенные по сравнению с их ближайш:1ми юшлюгами.
В органической XHNem восстановительное амкиированж альдегидов в присутствии водорода над палладиевым или платиновым катализатором.
Описывается основанный на известной реакции способ получения новых производных пиперазина обшей формулып
K--/N-f . (Т
где R - атом водорода, низшая алкильная нли алкокоигруппа или атом галогена;
R - одна из групп а мета- или пара-положения формулы -CHRi-Q A, CHRi-A, -Q-CHRj-CHRi-Q-A, причем А означает радикал формулы
/ л, i 1
-чг -f «
где Q - неразветвленную или разветвленную алкиленовую цень с --4 атомами углерода;
ft) - атом водорода, оксигрутш, низшая ajiкоксигруппа или rpjTHBO-CQ-Rj.
R, - атом водорода или метильная группа;
Вз и Й4 одинаковы шш различны и обозначают атом водорода, шзшую алкильную или алкоксигруппу, атом галогена или грифторметильную группу или вместе взятые означают приконденсированное алифатическое или аромат 1ческое Г1ятиили шестичленное кольцо;
RJ-низшая алкильная группа, которая может быть замещена атомом галогена, окси- или шзшан алкокси-, амино-, моно- или дналкиламиногруппа;
атом водорода или низший веразветвленный или разветвленный алкильный, алкенильный, алкиннльньй, оксиалкильний шш диалкиламиноалкильный радикал или аралкштьный радикал.
Под алкияьиым или алкокснрадикалом шш
НИ31ШМ алкильным и низишм алкоксирадикалом следует noHHvraTb радикалы в общем с 1-4, предпочтительно 1-2, атомами углерода.
Предпочтительными атомами галогена являются
атом хлора, брома.
Способ получения {цюнэводных пиперазина общей формулы I зуктачаатся в восстановительном амишфовшшн соеданення общей формулы О
Iе
R
ы
в с-с«1
где R и1| имеют указанные значения;
Rg означает одну из групп в мета- или пара-положении -СНО-, -CHRi-С Н. О- и - -CHR3-CHRi-CnH2p.jO, где R, и Ra имеют указа1шыв значения, н ij. означает 1,2 или 4, с. ам1шом общей формулы Г-А, где А имеет указанloiie значения, в присутствии водорода в катализатора гидрогенизации.
Исходные продукты щт осущесхвлевия едлагаемого способа часгачно описаны или могут быть получены о1ьгшыми методами сгаггеза.
Приме р 1.
/-л
- CH CU-lf N
где Z означает радикал.
10 г 1 - (4 - илшдазолиданон - 2 ил фенил) - 2 - оксопропана с 8,1 г 2 - метилфешошшеразина в 100 мл метанола в присутствю 1 г Р10гпри60Сй 5 атм гидрируют до поглощешя рассчитанного ко личестда водорода. После удаления катализатор отгоияют метанол и остаток с ацетонитрилом доводят до {фисгаллмзации. Из основания с небольшим количеством метанола путем добавки концентрированной соляной кислоты получают гидрохлорид. имеющий Г.Ш1. 299-301° С и кристаллизующийся в виде моногидрата.
Выход 74% от теоретического.
Ио примеру 1 получают нижеследующие производаые пнперизина общей формулы Т (где Z имеет указанное значение):
- 4 Ишщазолидинон - (2) - илфеизтил - 4 (3 ) - пиперазнн;
m-CH,-ir CHiCBj-llf
C,Hj
лжтаносупьфонат 1 - (4 - (3 - метилимидазолидинш
-(2) - ил - фенэтил - 4(2 - метилфе1п«)) шшеразина; т.ш1. 196°C выход 69% от теоретического;
гидрохлорид 1 - 4 - (3 - п - бутилимвдазолидинон - (2) - ил) фенэтил - 4 - (2 метилфенил) шшеразнна; т.пл. 283°С; выход 65% от теоретического;
гидрохлорид - (1 - (4 - имидазолидинон - (2) - илфенил) - 1 - едетилоксиэтил - 4 - (2 метилфенил) - пиперазина, т.пл. 310° С (разложение) ; выход от 49% теоретического;
гидрохлорид 1 - {1 - (4 - имидазолидинон - (2)
-илфенил) - метшпсарбамоилоксиэгил 4 - (2 меишфеннл) - пияеразина; т.пл. (разложеняе); в1ход 50% от теоретического;
метаносульфонат 1 - 1 - (4 - имидазолидийон (2) - нлфенил) - 1 - этоксиэгал - 4 - (2 мйтилфенил) - пиперазииа; т.пл. 214° С (разложение); выход 54% от теоретического.
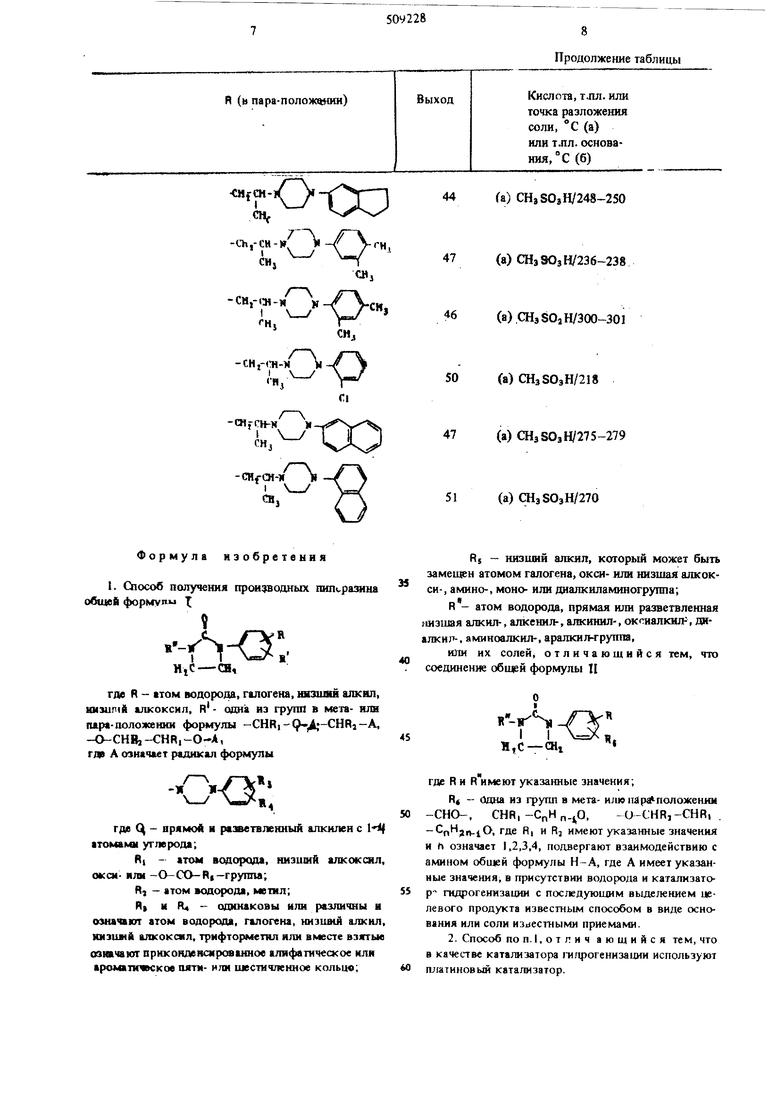
Соединения формулы 1, где R и R означают атомы водорода, представлены в таблице.
По примеру 1 получают соединения общей формулы 1, перечисленные ниже.
Метаносульфонат I - {4 - (3 - бензилимидазолидинон) - 2 - ил (фенэтил)- 4 - метилфенил шшеразина, выход 64%, т.пл. 194-195°С;
Дигидрохлорид 1 - 14 - 3 - (2 - димегиламиноэтил) - имидазолидинон - (2) - ил - фензтил - 4 (2 - метилфенил) - пкперазина, выход 60%, т.пл. ЗОЯ°С (разложение);
Дигидрохлорид 1 - 4 - 3 - (3 - диметиламинопропил) - имидазодидинон - (2) - ил - фензтил - 4
-(2 - метилфенил) - шшеразина, т.Ш1. 309° С (разложение), выход 58%;
Гидрохлорид 1 - 4 - (3 - зтиламидазолидиноп (2) - ил - фенэтил) - 4 - (2 - метилфенил) пиперазина, выход 70%, т.пл. 286° С;
Гидрохлорид 1 - 4 - (3 - аллипимидазолидинон - (2) - ил - фенэтил - 4 - (2 - метилфенил) I шшеразина, выход 44%, т.пл.г287°С (разложение); Метаносульфонат J - (4,- (3 - пропаргил- , имидазолидинон - (2) - ил) - фенэтил - 4 - фенилпкперазина, выход 41%, т.пл. 232-233°С;
Сульфат I - 1 - (4 - имидазоЯидинон - (2) илфеннл - 1н - бутилкарбамоилоксиэтил-4-У2 метилфеню - пиперазина; т.пл. (разложение) ; выход 54%.
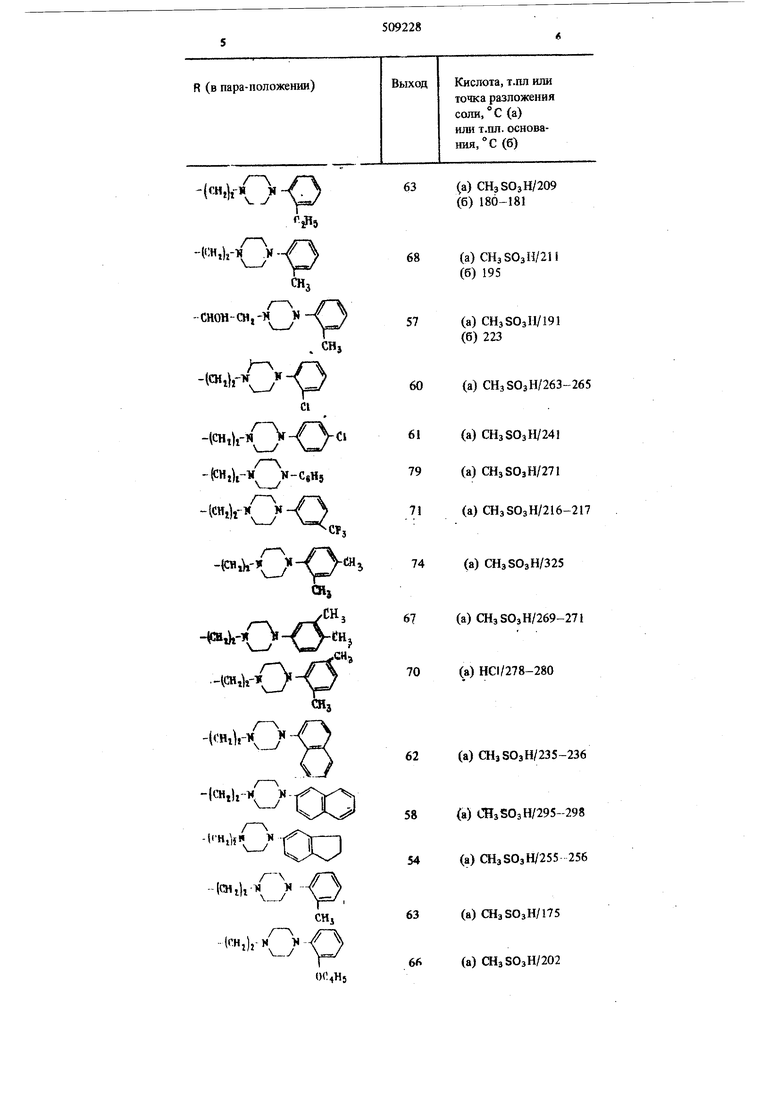
R (в пара-положении)
-(-н,},-1ГЛ
Г -СНОИ-СН,М
. CHj
- ь-О-р
(Ч
-lCHi)fK
Кислота, Т.Ш1 или точка разложения соли, С (а) или т.пл. основания, с (6)
63(а) СНз50зН/209
(6) 180-181
68(а) СНз50зИ/211
(б) 195
57(а) СНз80зШ191
(6)223
60(а) СНз50зН/263-265
61(а) СНз80зН/241
79(а) СНз80зН/271
71(а) СНз80зН/216-217
74(а) СНэ80зН/325
67(а)СНз80зН/269-271
70(а) HCI/278-280
-(
62(а) СНз8ОзН/235-236
-icH,)
-(. «
V.7 С
CHj
(CHi)j-M )
00.4H5
58(а) СНз50зН/295-298
54(а) СНз80зН/255 256
63(а) СНз80зН/175
66(а) Шз8ОзН/202

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения фенилимидазолидинонов | 1972 |
|
SU493067A3 |
| СПОСОБ ПОЛУЧЕНИЯ ФЕНИЛИМИДАЗОЛИДИНОНОВ | 1972 |
|
SU453839A3 |
| Способ получения производных пиперазина | 1973 |
|
SU503516A3 |
| Способ получения фенилимидазолидинонов | 1973 |
|
SU492085A3 |
| Способ получения фенилимидазолидинонов | 1973 |
|
SU498907A3 |
| Способ получения производных пиперазина | 1973 |
|
SU505358A3 |
| Способ получения производных кумарина | 1971 |
|
SU461494A3 |
| Способ получения карбостирильных производных | 1981 |
|
SU1367857A3 |
| Способ получения производных бензодиазепинона или их солей | 1978 |
|
SU772484A3 |
| Способ получения сульфонамидов алкилфенилкарбоновых кислот | 1981 |
|
SU1088664A3 |


Авторы
Даты
1976-03-30—Публикация
1973-11-14—Подача