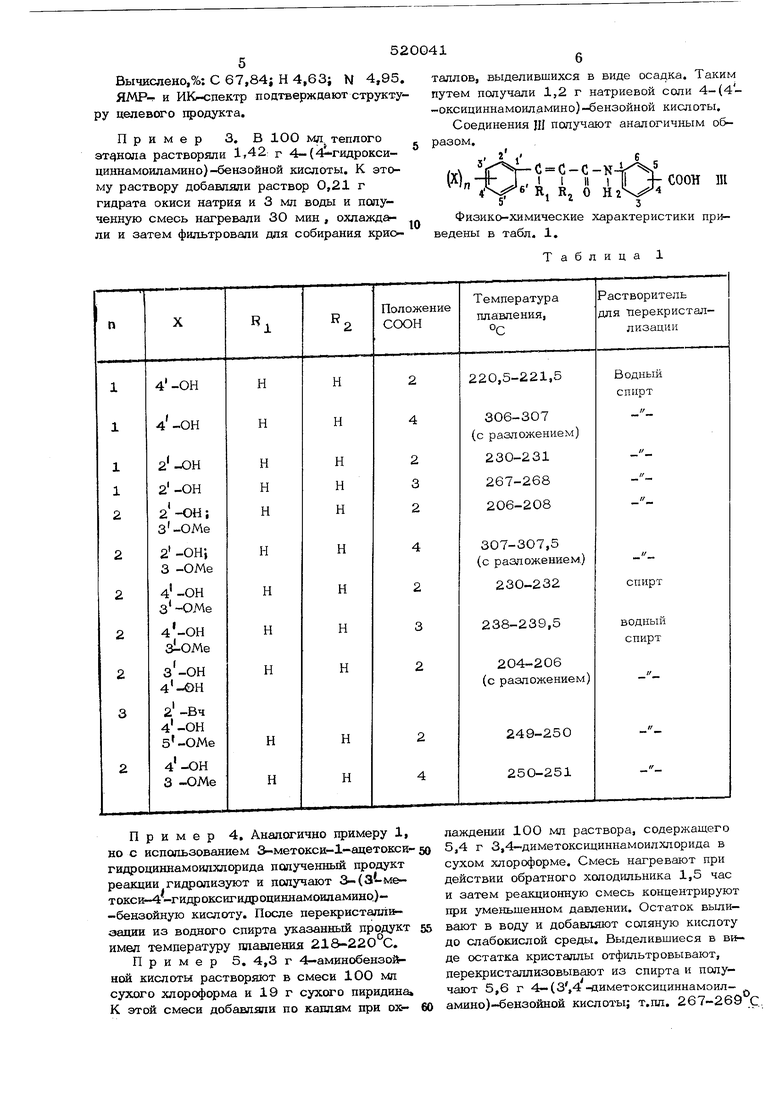
где ff., , Rq, Ц,, X, -13 - вышеуказан ные значения, i - оксигруппа, галоген или ангидрид кислоты формулыI/ , или смешанный ангидрид с другой кислотой, или ее галоидангидридом, например бензсшсульфонилхлоридом, или оксиалкил, подвергают взаимодействию с аминобензойной кислотой с последующим выделением целевого продукта в свободном виде или в виде соли. Получаемые соединения формулы I обладают-лучшими свойствами (физиологически активными), по сраБнению с цикиагл-ойл-аминобензойной кислотой, Арома7ичс-;; ас карбоновые кислотЫз обдадшотдие ; ной связью имеют два изомера: цкс- и транс-форму, В качестье исходнькх ;рс -/;атических карбоновых кислот формулы 13 могут быть испапьзованы такие, как ,, 3или 4-метил, этил- пропил™, гидрокси-s метокси, этокси-, или хлор-f бром-, или фторгидрокоричная кислота| 2,3-диметщ1гид коричная кислота; 3,4-метилендиоксигидрокоричная кислота; о -метил-4-этилгидро коричная кислота или g -этщ1 2 ХторгядрО коричная кислота, а таюке гфименяют арсх матические ненасыщешаю карбоновые кисло ты, такие как 2-, 3- или -Ф-проинл-, бутна гидрокси-, пропокси, хлор--5 бром-з или фторкоричную кислоту, 2-метил-3-этил- ил 3,4-диметнпкоричную кислоту и (, В качестве аминобензойной кислоты, воз можно использовать, антраннловую кислотуг 1 - аминобензойную кислоту или -п-аминобензойную кислотус В случае галоидпроизводных кислот целесообразно вести взаимодействие с аминобен зойной кислотой в среде инертного растворителя, В качестве инертного растворителя используют гиороформ, метипешшорид, ац тон, бензол, толуол, тетрагйдрофуран, дйоксан или диметилформамид. Процесс целесообразно проводить путем растворения аминобензойной кислоты и смеси сухого хлороформа и сухого пиридина, взятых в количествах 5-40 и 2-15-кратном избытке по отношению к количеству исходного соеди нения формулы Л , Последнее добавляют к раствору аминобензойной кислоты в сухом хлороформе при охлаждении и перемешивани а затем нагревают всю реакционную смесь с обратным холодильником в течение необх димого времени. Далее продукт реакции концентрируют :фи уменьшении давления и остаток вьшиваю « в воду. Полученную водную смесь слегка подкисляют добавлением соляной кислоты. Выделившиеся в виде осадка кристаллы от фильтровывают и перекристаллизовывают из адлежашего органического растворителя. В случае, когда исходным соединением формулы И является ароматическая карбоновая кислота, то в этом соединении целесообразно защищать гидроксильную группу ацилированием уксусной кислотой. По окончании синтеза эту группу можно удалить любым известным приемом. Образовавшееся соединение J , несущее карбоксильную группу, можно превратить в его соль, пригодную в физиологическом от ношении с применением обычного способа, Напрг.(мер,5 водный раствор гидрата окиси натрия Б зкви.aлeкyлstpнoм количестве .мо itei бь;.ть добавлен к спиртовому раствору соединения общей формулы Г и смесь нагретаК числу физиологически приемлемых солей следует отнести щелочные (калийная и литиевая соль), щелочноземельные (магниевая и кальциевая соль), аминные (пипери- диновая, триэтансяаминовая и диэтиламиноэтиламиновая), а также -аммонийную соль. Данное изобретение поясняется пример&ми, причем температуры плавления целевых продуктов .приводятся без корректировки. Пример 1, В смеси 20 мл сухого хлороформа и 10 мл сухого пиридина растворяют 2,6 г 4-аминобензойной кислоты, К этой смеси добавляют по каплям при охлаждении 20 мл сухого хлороформа, содержащего 3,2 г 4-ацетоксициннамоилхлорида, Смесь нагревают при действии обратнсго холодильника 2 часа, затем реакционную смесь концентрируют при уменьшенном давлениИо Остаток выливают в воду и после этого добавляют соляную кислоту до слабокислой среды. Кристаллы, выделившиеся в виде осадка, отфильтровывают и перекристаллизовывают из спирта. Получают 2,9 г 4- (4 -ацетоксициннамош1амино)-бензойной кислоты. Температура плавления 305-307 С (с разложением). Пример 2. Cмecь2,7г4-(4 aцeтoкcициннaмoилaминo) -бензойной кислоты и 5 О мл 10%-ного водного раствора окиси натрия нагревают 1 час, охлаждают и затем слегка подкисляют соляной кислотой. Выделившиеся в виде осадка кристаллы отфильтровывают и перекристаллизовывают из водного спирта. Получают 1,75 г 4-(4-оксициннамоиламино)-бензойной кислоты, имеющей температуру пл-авления С (с разложением), Найдено,%: С 67,69; Н 4,56; ,72. 1б 13 4 Вычислено,%: С 67,84; Н 4,63; N 4,95. ЯМР. и ИКг-спектр подтверждают структуру целевого продукта. Пример 3. В 100 мл теплого этанола растворяли 1,42 г 4-(гидроксициннамоиламино)-бензойной кислоты. К этому раствору добавляли раствор 0,21 г гидрата окиси натрия и 3 мл воды и полученную смесь нагревали 30 мин , охлаждали и затем фильтровали для собирания криоталлов, выделившихся в виде осадка. Таким путем получали 1,2 г натриевой соли 4-(4-оксициннамоиламино) -бензойной кислоты. Соединения Ш получают аналогичным образом. Tysi.iJ A,U7W° и Физико-химические характеристики приведены в табл. 1. Таблица 1

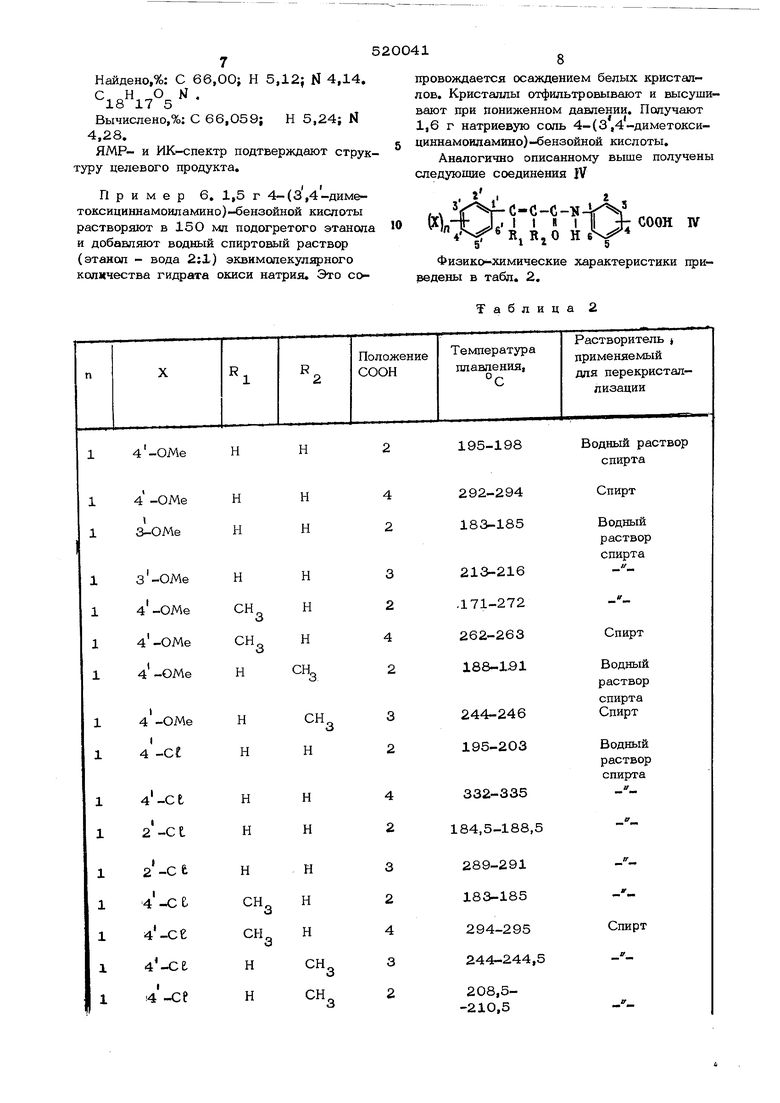



Пример 4, Аналогично примеру 1, но с использованием 3-метокси-1-адетоксигидроциннамоилхлорида псотученный продукт реакции гидролизуют и получают 3-(3-метокси 4 -гидроксигидроциннамоиламино)-бензойную кислоту. После перекристаллизации из водного спирта указанный продукт имел температуру плавления 218-220°С р и м е р 5. 4,3 г 4-.аминобензо ной кислоты растворяют в смеси 100 мл сухого хлороформа и 19 г сухого пиридина К этой смеси добавляли по каплям при охлаждении 100 мл раствора, содержащего 5,4 г 3,4 диметоксициннамоилхлорида в сухом хлороформе. Смесь нагревают при действии обратного холод1шьника 1,5 час и затем реакционную смесь концентрируют при уменьшенном давлении. Остаток выливают в воду и добавляют соляную кислоту до слабокислой среды. Выделившиеся в виде остатка кристаллы отфильтровывают, перекристаллиаовывают из спирта и получают 5,6 г 4-(3,4 чдиметоксициннамоиламино)-бензойной кислоты; т.пл. 267-269°С НайденоД: С 66,00; Н 5,12; Ы 4,14. Вычислено,%; С 66,059; Н 5,24; Ы t,io. 4,28. ЯМР- и ИК-спектр подтверждают струкly целевого продукта. Пример 6. 1,5 г 4-(з,4-диме520041 провождается осаждением белых кристаллов. Кристаллы отфильтровывают и высушивают при Пониженном давлении. Получают Ii6 г натриевую саль 4-(з,4-диметоксиВДНнамоипамино)-бензойной кислоты. Аналогично описанному выше получены следуюпше соединбния JV
520041
10
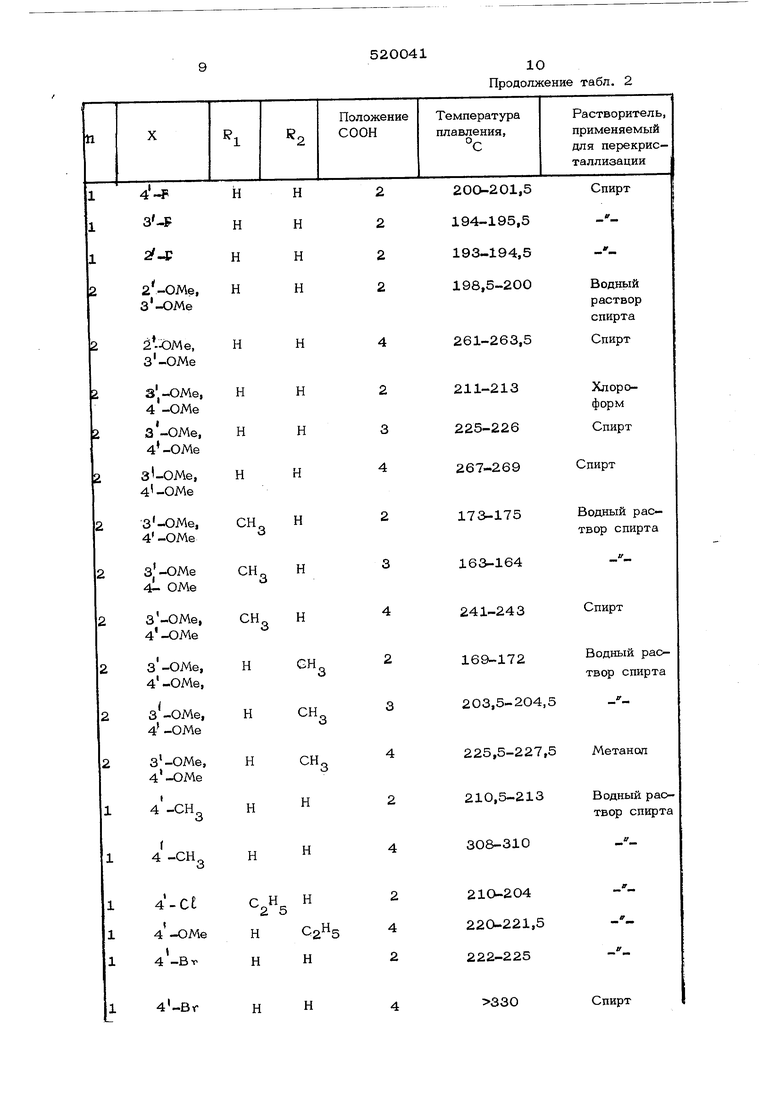
Продолжение табл, 2
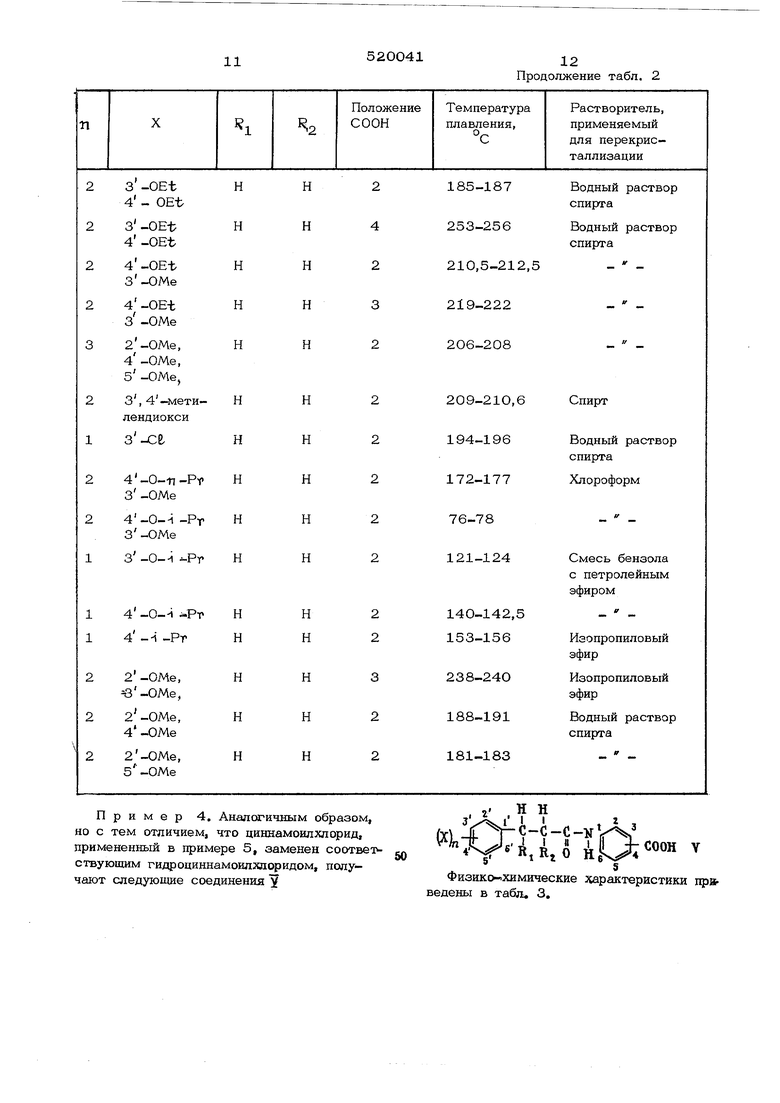
Пример 4, Аналогичным образом, но с тем отличием, что циннамоилхлорид, примененный в примере 5, заменен соотвегствующим гидроциннамоилхлоридом, получают следуюпще соединения Y
5,. Н Н .3
lkeUi°«
I 1 т - п
Физико-.химические адрактеристики приведены в табл. 3.
13
Пример 7. 4 г 3,4-диметоксикоричной кислоты растворяют в 20 .мл сухого пиридина. К полученному раствору добавляют при охлаждении льдом и перемешивании 2 г бензолсульфонилхлорида. Образуется красно-оранжевый осадок. Реакционную смесь перемешивают около 1 час, затем при охлаждении льдом добавляют 2 г метилантранилата. Далее, смесь перемешивают 2 час при комнатной температуре для заверщения реакции.
По окончании реакции реакционную смесь концентрируют и остаток растворяют в 10мл хлороформа. Раствор промывают сначала 10%-ным водным раствором гидрата окиси натрия. 1и%-ным водным раствором соляной кисло ты и в заключение водой. После удаления хлороформа перегонкой получают кристаллы сложного метилового эфираЫ -(3,4-диметоксициннамоип)-антраниловой кислоты,
Пример 8, Продукт, полученный в примере 7, растворяют в 10 мл xaopt форма, К полученному раствору добавляют 10 мл водного раствора гидрата ОКИСИ натрия и смесь подогревают до 50 С (для обеспечения гищмзлиза сложноэфирной гругшы). После окончания реакции, органзаческую фазу отделяю-., промывают водой и перегоняют для удаления растворителя. Получают 2,1 г (выход 48%) целевого Щ)дукта Я -(3, 4-диметокснциннамош1)-антраниловой кислоты. Этот продукт имел температуру плавления 211-213 С,
П р и мер 9, 2 г 3,4-диметоксикоричной кислоты растворяют в смеси 20 мл сухого днметилформамида и 1,5 г триэтила- ммка„ К этому раствору добавляют при охла ждении льдом и перемешивании 1,1 г этилхлоркарбоната и выдерживают в течение 1 ч
520041
14 Таблица 3
Кэтой смеси добавляют 10 мл диметилфор-мамида, содержащего 1,5 г аминобензойной кислоты, и перемешивают смесь в течение 2час, По завершении реакции, жидкую реакционную смесь концентрируют примерно до половины первоначального бъема и выливают в водный раствор соляной кислоты. Выделившиеся в виде осадка кристаллы отделяют фильтрованием, промывенот водой и перекристаллизовывают из эквимолекулярной смеси этанола с водой, получают 3-(3 , 4 -диметоксициннамоиламино) -бензойную кислоту с 50%-ным выходом, имеющую температуру плавления 225-226 С.
Пример 10, К смеси 20 мл сухого диоксана и 0,7 г сухого пиридина добавляют 2 г 3,4-диметоксикоричной кислоты, 1,6 г хлорокиси фосфора (хлорангидрида фосфорной кислоты) и 1,6 г метилантранилата. Смесь нагревают при действии обратного холодильника 2 час для обеспечения проведения реакции. По окончании реакции реакционную смесь концентрируют и остаток растворяют при нагревании в этаноле и затем охлаждают, выделившиеся кристаллы отфильтровывают и обрабатывают аналогично примеру 7 (для обеспечения гидролиза сложноафирной группы). После перекристаллизации продукта из хлороформа получают 2 г N -(3 , 4 --диметоксициннамокл)-антраниловую кислоту, имеющую температуру плавления 211-213°С,
Формула изобретения
Способ получения амидов ароматических кацбоновых кислот или их солей общей формулы I
15
соон
где RJ и Rj ьодород или совместно представляют двойную связь;
RJ и ц -водород или алкил С - С ;
X - одинаковые или различные и npejjставляют собой оксигруппу, галоид, алкил С - С{, или алкоксил С - Сц ;
f - целое число 1-3, причем, если X означает две алкильных или алкоксильных группы, то они могут совместно образовывать кольцо, отличающийся тем, что кислоту или ее производное формулы 1(
16
С-С-С-2
О
где RJ, Rg, RJ, Нц, X; ц-вышеуказанные значения;
- оксигруппа, галоген или ангидрид кислоты фор мулы II или смешанный ангидрид с другой кислотой или ее галоидангидридом, например бензолсульфонилхлоридом, или оксиалкил, подвергают взаимодействию с аминобензойной кислотой с последующим выделением целевого продукта в свободном виде или в виде соли.
Авторы
Даты
1976-06-30—Публикация
1974-01-17—Подача