Изобретение относится к способу получе ния новых пенициллинов, имеющих большое значение в медицинской практике и обладаю щих улучшенными качествами и широким спектром действия. Известнь способы пол че1-1кя пазличных замещенных ампициллина, имеющих алифа1-и ческие, аралифатические и гетероциклическ заместители по аминогруппе. Предлагаемый способ отличается от известного тем, что 6-аминопенициллановую кислоту подвергают взаимодействию с изме ненными в карбоксильной группе различными производными карбоновой кислоты. едлагается способ получения пеницилобщей формулы 1 Z-NH-CH-CO-NH-CH-CH II/ С-N. / / сн о е л - труппа NHC N-y-N -NI I -а/ 2 R.-X-N y-NX N N I1 VQ/ 1. TJ, X-N-y-N I 1, где X - группа у - группа ОS IIII -с- , -сN-S (| арил IIII -С- , группа G-G-GIIЧСКили-С- CO - с & & -С -N-C- (с) I I II & К && I Q группа & I j (С) -CIG GN-(C)G G G G -C-CO-C - ,-(C)-C C-CII I Оили I &&&& / GG / (f /7 (c), -c VZic)II Оили I G-Q.Q.GGGгде J - неразветвленный или разветвленный алкильный радикал с 5 углеродными атомами;G- - водород или R, причем стрелка в двухвалентном промежуточном звене Ч показывает, что вызываемое двумя свободными валентностями этого промежуточного звена соединение двух атомов дол/кно произойти не любым, а указанным стрелкой образом;Н. - алкил с числом углеродных атомов до 10, циклоалкил с числом углеродных атомов до 10, алкенил с числом углеродных атомов до 10 и циклоалкенил с числом углеродных атомов до 10, винил, арилвинил, МОНО-, ди- и тригалоген- низший алкил, - ,арил,-ЫН-, арилнизший алкил - амино, алкоксил с числом углеродных атомов до 8, аралкоксил с числом углеродных атомов до 8, циклоалкоксил с числом углеродных атомов до 7, арилоксигруппа , группа , R-S-V-, , R-0-CO-V-, HjN-CO-V-, R.-MH CO-V-, (13) N-CO-V Только Б том случае, если X одновременно не означает -SOj. «,/((«2) / г ..(он.).-, S,., « -/И/ ХТ / & о R, А , где V - двухвалентный органический радикал с 1-3 атомами углерода; каждый - водород, нитро-, нитрил, , CR) N-CO- -CO-NHR- O-tO-, Тг-СО-О- 2-,R-0-, H,N-SOa xjiC|j, 5pOM, йод, фтор или грифторметил, при чем R, имеет указанное значение; U - целое число от О до 2; R и R каяедый - водород, алкил и алкенил, каяадый с числом углеродных атомов до 8, винил, аллил, пропенил, циклоалкил и циклоалкенил, каждый с числом углеродных атомов до 8, винил, аллил, пропенил циклоалкил и пиклоалкенил, каждый с числом углеродных атомов до 6, моно-, ди- и тригалоген низший алкил или арил; В - группа формулы С1 7-Rg - водород, галоген, R, , 12-3-, R-SO-, -R-SOg.-, нитро, (R) -, R-CO-NH-, HQ,R-CO-0-, причем R имеет указанное значение; 2 - группа -СС или-СС. С - асимметричный атом углерода или их солей. Способ заключается в том, что б-аминопенициллановую кислоту подвергают взаимодействию с функциональным производным кар боновой кислоты общей формулы III А -Z NH - СООН I В где А, Z 8 i4 С имеют указанные значения, в безводном или водусодержащем растворителе в присутствии основания, обычно при температуре приблизительно от-7Одо + 5О°С, предпочтительно от -5О до . В случае взаимодействия 6-аминопенициллановой кислоты с измененными в карбоксильной группе карбоновыми кислотами формулы III реакция может быть проведена в водусодержащих растворителях при РН 2-9 предпочтительно при рН 2-3 или 6,5-8,5. При превращении карбоновой кислоты формулы 111 в измененные в карбоксильной группе Карбоновые кислоты этой же формулы в качестве исходных соединений можно также применять соли общей формулы Ilia илислож силиловые эфкры общей формулы Шб в A-2-NH-CH-COO M Me Шо Б A-Z -NH-CH -COD-SL-I.. В А -Z-NH-CH-COO X -Z -NH-CH-CQO где Л, 2, В, R,,,R,,, R имеют указанные значения; - катион щелочных или щелочноземельметаллов или катион злемекта алюминия; П - целое число от 1 ;;о 3, Карбоновые кислоты обще): фор;-,1уль; 1П их соли формулы Ша, илп лх сложные иловые эфиры формулы IllC; и/.и мойшо вращать в измененные в карбо;,.сильной ппе Карбоновые кислоты фоол1улы Ш, подгая их взаимодейстВ1;ю приблизктелвно с ольэкв. соединений обип;х фюомул I W ы-к,. Р ivi .CHg C.H2.s где R имеет указанное значение; Т „ имеет то же значение, что и или 1) ачает фенил; ц - двухвалентный органический ради CH)2Vr(Wa}s- Аи -(CHaV-O-t aVi W - галоген. При применении соединений формул Ш и 1Па в водусодержащем или безводном .ническом растворителе, а при применен единений формулы IU6 или в - в безвод или свободном от гидроксильных групп /дифферентном органическом растворител присутствии или в отсутствии основания температуре от -7 О до +30 , предпочт тельно при -5О - О С. При этом и при следующей реакции взаимодействия с соед нием формулы 11 целесообразно проводить цию в присутствии приблизительно 1 МОЛЬ оксисоединений общих или специальных мул YIII, Villa и б: /СО-СН2 HO-N C CO-CH2 УШа где и - радикал -CsN и/ или -COQщий алкил. С другой стороны, карбоновые кислот общей формулы lit,их соли (Ilia) ил их сложные силиловые эфиры (11(6 или в гут быть превращены в измененные в к боксильной группе карбоновые кислоты что подвергают их взаимодействию приб зительно с 1 мольэкв. соединений обще формулы IX или ХХаилис 0,5-1,0 моль-э соединений общей формулы X или Ха: И/ 13 W-CH N х С N „ W (1Ъ Н 13 Ч имеют указанны значения, в присутствии 1 МОЛЬЭКВ. (по отнощ нию к карбоновым кислотам общей форму лы Ш) М -оксисоединений YIL1, УШа или б, в случае применения соединений Ш илиШав водусодержащем или безводном органическом растворителе, а в случае применения соединений Ц1б или в - в безводном или свободном от гидроксильных групп индифферентном органическом растворителе в присутствиии или отсутствии основания при температуре от -70 до +ЗО С, предпочтительно при температуре от -50 до О С. В случае, если у асимметричного атома углерода С имеется оптическая активность, возможную рацемизацию в этом месте можно предотвращать тем, что при превращении карбоновых кислот или их солей, или их сложных силиловых эфиров или в в измененные в карбоксильной группе карбоновые кислоты не применяют никаких органических оснований или используют только сравнительно слабые органические основания (N -метилморфолин, N -этилморфолин, N,M -диэтиланилин, пиридин), или неорганические основания, или буферные смеси. Кроме того, карбоновые кислоты общей формулы Ш могут быть превращены в измененные в карбоксильной группе карбоновые кислоты тем, что соединения общей формулы УШ где 1 имеет указанное значение, превращают в безводном индифферентном органическом растворителе в присутствии по меньшей мере 1 моль-экв. служащего уловителем капель кислоты органического основания при температуре приблизительно от -4О до +25 С с 1 МОЛЬЭКВ. тионилхлорида с образованием 1 мольэкв. основного гидрохлорида в неизвестные промежуточные соединения, а последние без изоляции подвергают взаимодействию с 1 мольЭкв. карбоновых кислот общей формулы Ш или 1 МОЛЬЭКВ. соединений общих формул Ilia,б,в в присутствии дополнительного моль-эквивалента основания, причем не добавляется никакое основание или вводится основание в количестве до 1 моль-экв. при температуре приблизительно от -40 до +30°С. При этом получают измененные в карбоксильной группе карбоновые кислоты общей формулы XI /Q A-H-NH-CH-C и k где А, г , 5 , С и иимеют указанные значения. Кроме того, карбоновые кислоты общей формулы ГЦ можно превращать в измененные в карбоксильной группе карбоновые кислоты общей формулы ХГ тем, Что в присутствии приблизительно 1 моль-экв.соединений общей формулы УШ подвергают их азаимодействию приблизительно с 1 мольэкв карбодиимида в растворителе. При взаимодействии б-аминопеницИллановоЦ кислоты с измененными в карбоксильной группе карбоновыми кислотами формулы Ш 6-аминопеницилЛановую кислоту применяют предпочтительно в виде раствора ее соли в кислоте или основании. Пригодными растворителями для этого являются, например, вода или смеси иа воды и смешивающихся с водой органических растворителей, например тетрагидрофурана, диметилсульфоксида или триамида гексаметилфосфорной кислоты. Пригодными кислотами являются, например, соляная, серная и фосфорная кислоты. Для превращения 6-аминопенициллановой кислоты в растворенную в одном из названных растворителей соль основания в качестве пригодных для этой цели оснований можно применять, например, такие неорганические основания, как карбонат, гидроокись, бикарбонат натрия, соответствующие соединения калия или кальция, окись кальция, окись магния, карбонат магния или буферные смеси, а также такие органические основания, как N -метилморфолин, 14 -этилпиперидин, М -диметиланилин, пиридин, триэтиламин. Для получения раствора 6-амиаопенициллановой кислоты в безводной ореде в качестве растворителя особенно пригоден хлороформ или дихлорметан, а для солеобразования в качестве основания пригодны, например, триэтиламин, диэтиламин, N -этилпиперидин, N -этилморфолин и пиридин. При взаимодействии с измененными в карбоксильной группе карбоновыми кислотами соли 6-аминопенициллановой кислоты не должны быть полностью растворены Они частично могут находиться в качестве суспензии.
При реакции взаимодействия измененных в карбоксильной группе карбоновых кислот формулы Щ с 6-аминопенициллановой кислотой компоненты реакции применяются обычно в эквимолекулярных количествах. Может быть целесообразно использование одного компонента реакции в избытке для облегчения очистки или получения в чистом виде же.шемого пенициллина и повышения выхода
Количество оснований, добавляемых при взаимодействии измененных в карбоксильной группе карбоновых кислот общей формулы Щ с 6-аминопенициллановой кислотой, определяется, например, необходимым регулированием определенного значения рН. Если измерение и регулирование значения рН не производятся, или невозможны, или бессмыС ленны из-за отсутствия достаточного количества воды в разбавителе в случае применения 6-аминопенициллановой кислоты и безводной реакционной среды, используют приблизительно 1,5-2,5 моль-экв. основания. Количество добавляемой при реакции кислоты определяется, например, поддержанием определенного значения рН или определенной области рН. Обычно выгодно реакцию взаимодействия измененных в карбоксильной группе карбоновых кислот Ш с 6-аминопенициллановой кислотой вести при максимально пониженных температурах. Это позволяет получить более чистые продукты, улучшить вы0ход и предохранить имеющуюся у асимметричного атома углерода С оптическую активность от рацемизации. Если при этой реакции исходят из силиловых соединений, то применяют предпочтительно только такие
6 органические растворители, которые не содержат никаких групп К-Н и 0-Н например, дихлорметан, хлороформ, тетрагидрофуран, диоксан, диэтиловый эфир, ацетонитрил, бензол, ацетон или диметилформамид. Если
0 при реакции взаимодействия карбоновых кислот, их солей или их силиловых соединений с соединениями общих формул W , V ,У1 или П добавляют основания, то для этого пригодны практически все основания, которые достаточно индифферентны по отношению
S к ацилирующим средствам и, в случае применения силиловых соединений, не содержат никаких групп Н j предпочтительно никаких групп О-Н-И N-H.
о
При получении производных карбоновых кислот общей формулы XI исходят из соединений общей формулы УШ, которые в таких растворителях, как ацетон, тетрагидрофуран, диоксан, дихлорметан, хлороформ, бензол,
5 сложный этиловый эфир уксусной кислоты, Д1 этиловый эфир или диметилформамид, в присутствии одного моль-эквизалента основания, например триэтиламина гшрвдина, хинолина t -мет лфорфолина, H,N -диметиланилина при температуре от -40 до +25 С превращаются с 1 МОЛЬЭКВ. тионилхлорида в неизвестное промежуточное соединение и без выделения в присутствии дополнительного моль-эквивалента того же основания и В тех же растворителях подвергаются взаимодействию с 1 моль-экв. карбоновых кислот, или без дополнительного добавления оснований, или с основаниями в количестве до 1 МОЛЬЭКВ. при температуре от -4Одо+ЗО°С с 1 МОЛЬЭКВ. солей или силиловых соединений. Соединения общей формулы XI можно при необходимости и после удаления образовавшегося в течение реакции и выделивщегс ся основного гидрохлорида отделять упариванием растворителя и очишать кристаллизацией иа индифферентных растворителей или, если получаемое вещество не кристаллическое, кратковременной промывкой, например, эфирного или бензольного раствора водным
i; ;rnoi)OM iHKai rOHr(t н/сгрия щя; акг.1МЧПьчо iinfiH KPn bix TOMiiopaTyiiix.
С : щп --т1 ft -.u.fKT.TKffi в iieiiHUHJiJiHHax предолоно 1одометриче(;ким методом. Все писанные вешестпя покд.л-гв.кчи COOTDOTCTуюишй их строению ИК- спектр. Спектры или пеииииллинов наблюдались в раство« CDjOB ; указанные в примерах сигналы ;оотп тству.,от шкало ТГ и строению исслеуемо ix пенициллина.
При обработке результатов анализа учитывалось содержание воды в пеницнллинах.
Экспериментальная часть
Пример 1.
А. Натрий и-(/.(3-метилсульфонилимидазолвдин-2-OH-l-ил) -карбонапамино -бензилпенициллина. 6,8 вес.ч. 1) (З-метилсульфонилимидазолид ИН-2-ОН-1 -ил) -карбониламино} -фенилуксусной кислоты растворяют в 4О об ..ч. хлористого метилена с добавкой небольшого количества тетрагидрофурана, охлаждают до -4О°С и смешивают при интенсивном размешиван ВИ с 2,0 вес .ч. W -метилморфояина. Затем при интенсивном размешивании однократным вливанием добавляют раствор 3,75 вес.ч. хлорида тетраметнлхлорфор дамидяния в 15 об.ч. хлористотх) метилена, также охлалодетгаый до -4О С, перемешивают в течение 5 мин при -4О С, а потом соед5шявот с охлажденным до О°С (рН 2,5) раствором 4,7 вес.ч. 6- аминопенициллановой кислоты в ЗО об.ч. 8О%-ного водного тетрагидрофурана. Добавлением дополнительного Ы -мётилморфолина поддерживают значение рН смесв 2,5, Размешивают в течение ЗО мин без охлаждений, причем значение рН не изменяют. После этого добавляют 4О об.ч. воды, затем устанавливают значение рН до 7, хлористый метилен и тетрагидрофурак отделяют во вращающемся выпарном аппарате, раствор извлекают однократно при покюши 5О об.ч. уксусного эфира, а на водную фазу подают слой свежего уксу ского эфира. При размешивании и (охлаждении льдом подкисляют разведенной сопяной кислотой до значения рН 1,5, отделяют уксусный эфир дважды извлекают водную фазу при помощи уксусного эфира, промывают соединенные органические фазы водой и сушат над Потом фильтруют, смешивают с 2О об.ч. молярного раствора из 2-этнлгексаноат;а натрия в содержащем метанол эфире, упаривают в вакууме почти досуха, остаток растворяют в необходимом количестве метанола и производят оса- сдение натриевой соли пенициллина добавлением в 1О раз большего количества ;абсолютного эфира при встряхивании. Отсапывают, тщательно 1ромывают абсолютным
эфи)оок1 II высушивают в ипкуумр)ом эксиклторе нл,и РЗ DS- . Выход 84%.
С .одержанпе -лактпма 74%. .Вычн.л. но, ;.: С 43,4 Н 4,8N 11,3
S10,4
Найдено, %; С 43,4 Н 5,4 N 11,3 51О,3
Полосы ИК-спектра при 3325, 3055, ЗО25, 3002, 2965, 2924, 2865, ,
1738, 1679, 1610.1529, 1398и1171см-1
Сигналы ЯМР при -fS-S -2,8 (5П), 4,4 (1Н), 4,5 (2Н), 3,8 (1Н), 6,15 (4Н), 8.4 (ЗН) и 8,5 ч. на млн. (ЗН)
. 1 }В-(3-метилсульфонилимндазолидин-2-он-1-ял)-карбониламино} -фенилуксусная кислота. 16,6 вес.ч. ()-С-фенилглицина pacTBOpsnoT в 15О об.ч. 5О%-ного водного диоксана; с добавлением достаточноfro количества 2 н, раствора гидроокиси нат- рия. Знгйение рН этого раствора юнижают до 7,5 добавлением 2 н. соляной кислоты, причем аминокислота частично выделяется в высокодисперсном виде. Затем при охлаждении льдом пордиями добавляют 1-ллоркарбонил Зг метилсульфонилим1щазолидона г(2) и поддерживают значение рН при 7,5 путем одновременного введения 2 н. раствора гидроокиси натрия. Без охлаждения размешивают дополнительно до тех пор, по- ка не будет установлено остающееся постояв- ным даже без прибавления щелочи значение рН 7,5 (приблизительно в течение 10 мин).. Затем примешивают 5О об.ч. воды, отгоняют на роторе до половины первоначального
объема и извлекают один раз при помощи 5О об.ч. уксусного после отфильтровывания от непрореагировавшегося С-фенилглицина. Затем подкисляют до значения рН2, извлекают несколько раз при помощи уксусного эфира, соединенные фазы уксусного эфира промывают водой, высушивают над МоГ$0/| отфильтровывают, упаривают досуха и перекристаллизовывают из ацетона /нитромета:на. Т.пл. 25О С. Выход продукта 56%.
Вычислено, %: С 45,7; Н 4,4; N12,3; S9,4.
Найдено, %: С 45,7; Н 4,5; N12,3; 59,2 Полосы ИК-спектра при 3345, 36ОО-23ОО, 1731, 1652, 1538, 121О и (B.Najof ) 1168 см-1
Сигналы ЯМР при Г -1,2 (1Н)-2,55 (5Н), 4,6 (IH), 6,2 (4Н), и 6,6 ч. на млн.(ЗН).
2)D L-).-С (З-метилсульфонилимидазолйдин-2-он-1-ил)-карбониламино -4-хлор- фенилуксусная кислота. Эту карбоновую кислоту получают описанным в примере -1 Б 1Ьпособом из 5,8веч. ч. 4-хлор-С-фенилглицина и 6,8 вес.ч. 1-хлоркарбонил-З-метилсульфонилимидазолидона-(2).
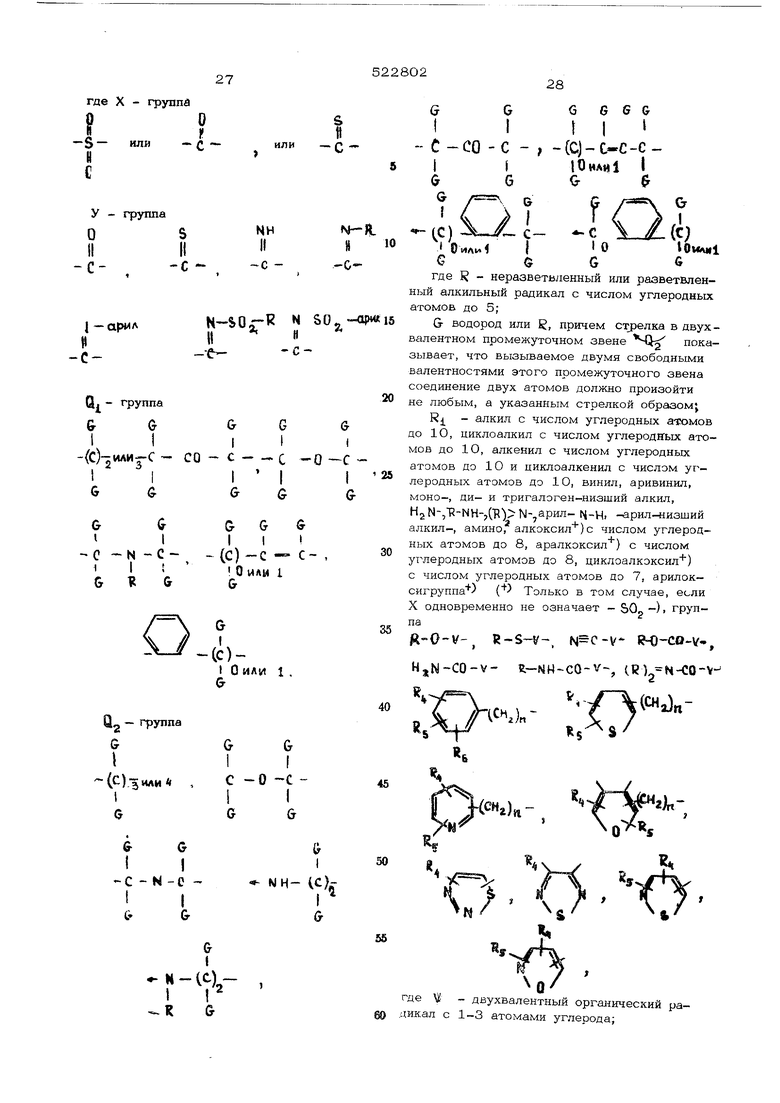
Т.пл. 19О С. Выход продукта Вычислено, %: С 41,6; Н 3,7; С1 9,4 N11,2; S8,5. Найдено, %: С 4О,8; Н 3,7; С1 9,2; Ы 11,1; S8,9. Полосы ИК-спектра при 3700-22ОО, 3310, 1730, 1654, 154О и 1168 см (в „Najoe ). Сигналы ЯМР при Т -1,1 (1Н), 2,55 (4Н), 4,5 (1Н), 6,1 (4Н) и 6,65ч на млн. (ЗН). 3) D, L dC -(3-метилсульфонилимидазолидин-2-он-1-ил)-карбониламино - JL -тиенил-(2) -уксусная кислота. Эту карбоновую кислоту получают описа йым в примере 1Б 1) способом из 5,5 вес с -тиенил-(2)-глицина и 6,8 вес .ч. 1-хлор ка рбонил-3-метилсульфонилимидазолидона-( Выход продукта 88%. Т.пл. около НО С (сырой продукт). Н 3,8; N1 12,1 С 38,0; Вычислено, S18,4. С 38,2; Н 4,8; Н 1О,8; Найдено, %: 517,0. Полосы ИК-спектра при 3600-2200, 3315, 174О, 1725, 1664, 1525 ( и 1170 см-1. Сигналы ЯМР при Т-1,2 (1Н), 2,43,1 (ЗН), 4,2 (1Н), 6,07 (4Н) и 6,67 ч на млн. (ЗН). 4)Ц-с {13-метилсульфонилимидазолидин-2-он-1-ил)-карбониламино -фенилуксусная кислота. Эту кислоту получают описанным в при мере 1 Б 1 способом из 5,3 вес.ч. ( L -С-фенилглицина и 6,8 вес .ч. 1-хлоркарбо нил-3-метилс,пьфснилимидазолидона-( 2). Т.пл. 245 С. Вычислено, %: С 45,7; Н 4,4; N 12,3 59,4. Найдено, %: С 44,9; Н 4,5; N 11,9;S9 ИК-спектры и спектры ЯМР идентичны со спектрами продукта по примеру 1 Б 1. 5)11, U Х. (3-метилсульфонилимид азолидИН-2-ОН-1 -ил) -карбониламино -2,6-дихлорфенилуксусная кислота. Эту кислоту по лучают описанным в примере 1 Б 1 спосо бом из 7,7 вес.4. 2,6-дихлор-С-фенилглиц на и 6,8 вес.ч. 1-хлоркарбонил-З-метилсульфонилимидазолидона ( 2), Т.пл. 260С. Выход продукта 69%. Полосы ИК опектра при 34ОО-2200, 3290, 1742, 1714, 1646, 1580 „Nujg 1522, 1260, 1170, ИЗО, 783 и763см Сигналы ЯМР при Т -0,9 (1Н), 2,4 2,65 (ЗН), 3,4 (1Н), 5,8-6,2 (4Н) и 6,65 ч. на млн. (ЗН). 6) L с (З-апетилимидазолидин-2-он -1-ил)-карбониламино -фенилуксусная кисл та. 2 Эту кислоту получают описанным в примере 1 Б 1 способом из 5,0 вес.ч. ( L )-С-фенилглицина и 5,7 вес.ч. 1-хлоркарбонил-3-ацетилимидазолидона (2), Т.пл. 214 С. Выход продукта 69%. Вычислено, %: С 55,0; И 4,9; Ы 13,8. Найдено, %: С 53,5; Н 5,2; N 13,7. Полосы ИК-спектра) при 3650-2250, „ 3300, 1735, 1665 и 1252СМ-1 (B,,Najo8 ) Сигналы ЯМР при Т -1,0 (1Н) 2,32,8 (5Н), 4,5 (1Н), 6,2 (4Н) и 7,6 ч. на млн. (ЗН). 7)D,L X. (З-ацетилимидазолидин-2-он-1-ил)-карбониламино|-4-хлорфенил уксусная кислота. Эту кислоту получают описанным в примере 1 Б 1) способом из 6,2 вес.ч, D,-U-4-xnop-C-фенилглицина и 5,7 вес.ч. 1-хлоркарбонил-З-ацетилим1щазолидона (2).Т.пл. 194 С. Выход продукта 53%. Н 4,1; С1 10,4; Вычислено, %: С 49,5; М12,4. Найдено, %: С 49,6; Н 4,6; С1 9,4; N12,2. Полосы ИК-спектра при 3700-2300, 3290, 1725, 1685, 1848 и (B.KIujof ) 1252 см-1. Сигналы ЯМР при -IT 0,9 (1Н), 2,55 (4Н), 4,45(1Н), 6,2(4Н) и 7,55 ч. на млн. (ЗН). 8) В, L -оС t( 3-aцeтилимидaзoлидин-2-oн-l-ил)-кapбoнилaминoЗ -4-метилфенилуксусная кислота. Эту кислоту получают описанным в примере 1 Б 1 способом из 5,4 вес.ч. 4-метил-С-фенилглипина и 5,7 вес.ч. 1-хлоркарбонил-3-ацетилимда1азолидона (2). Выход продукта 42%. Полосы ИК-спектра при 36ОО-2200, 3310, 1738, 1712, 1678, 1666 ( в NujoE ) и 1256 см-1. Сигналы ЯМР при Т-1,0 (1Н),2,6(2Н), 2,8 (2Н), 4,-5(1Н), (в ацетоне) 6,2 (4Н), 7,6(ЗН) и 7,7 ч. на млн.(ЗН). $) D , L в | 3-ацетилимидазолидин-2-он-1 -ил) -карбонидаминоД - J., -тиенил- (2) -уксусная кислота. Эту кислоту получают описанным в примере 1 Б 1 способом из 8,6 вес.ч. тиенкл-(2)-уксусной кислоты и 9,5 вес.ч. 1-хлоркарб онил- 3-ацетилимидазолидона (2). Т. пл. 197 С. Выход продукта 62%. Вычислено, %: С 46,3; Н 4,2; N13,5; .§10,3. Найдено, %: С 47,1; Н 4,4; Ы 13,8;S9,7. Полосы ИК-спектра при 3280, ЗО8О, 345О-230О, 1728, 168О, 1652, ( в „MLLJoE ) 1522, 1260 и 705 см ,1(1Н), 2,5Сигналы ЯМР при Т -1 3,2(ЗН), 4,2(1Н), б,2(4Н) и 7,6 ч. на млн.(ЗН). 1О) Л , L о С(3-ацетилимидазолидин -2-он-1-ил)-карбониламино) -2,6-дихлорфенилуксусная кислота. Эту кислоту получают описанным в примере 1 Б 1 способом из 6,7 вес.ч. 2,6-дихлор-С-фенилглицина и 5,3 вес.ч. 1-хло карбонил-3-ацетилимидазолидона (2). Т. пл. 25О С. Выход продукта 74%. Вычислено, %: С 44,9; Н 3,5; С1 19,0 N 11,2. Найдено, %: С 45,2; Н 3,7; С1 18,5; N 11,4 Полосы ИК-спектра при 360О-2200, 3302 1735, 1682, 1625, 1520 (в „MujoM и 1255 см. Сигналы ЯМР при Т -0,7(1Н), 2,32,7(ЗН), 3,4(1Н), 6,2(4Н) и 7,6 ч. на млн.(ЗН). Б. 1-хлоркарбонил-З-метилсульфонилими дазолидсн (2). 16,4 вес.ч. 1-метилсульфонилимидазолидона (2) кипятят в течение трех суток вместе с 27 вес.ч. триметилхлорсилана и 2О вес.ч. триэтиламина в ди- океане. Отфильтровывают от выпавшего три этиламингидрохлорида, смешивают с 11 вес.ч. фосгена и выдерживают в течение ночи при комнатной температуре. Затем упаривают до суха и перекристаллизовывают изкипяш.его ацетона. Выход продукта 70%.Т.пл. 178 С. Вычислено, %: С 26,5; Н 3,1; С1 15,7 Н 3,1; С1 15, N 12,4; S14,1. Найдено, %: С 27,2; Н 3,4; С1 15,3; N 12,0; 514,1. Сигналы ЯМР при Т -5,6-6,2(4Н) и 6,6 ч. на млн.(ЗН). Полосы ИК-спектра при 3010, 1807, 1721, 1360, 1165, 984 и 742 см. Тот же продукт можно также хорошо получить из 1-метил-сульфонилимидазолидона и фосгена в избытке в хлористом метилене в присутствии пиридина. Г. Ы -метилсульфонилимидазолидон-2. Метод 1. К суспензии из 43 вес.ч. имидазолидона-2 в 40О об.ч. сухого тетрагидрофурана при комнатной температуре прикапывают 63 вес.ч. метансудьфохлорида, размешивают в течение часа при 30-4О С и после этого нагревают в .течение часа с об ратным холодильником. Затем отгоняют рас воритель в вакууме и вьщерживают в течевакуумение часа при 60 С у масляного насоса. Ос таток перекристаллизовывают из теплого ацетона. Т.пл. 193 С. Выход продукта 25% Вычислено, С 29,3; Н 4,9; N 17,1; 319,5. Н 5,0; N 17,2; Найдено, %: С 29,О; S19,6. 216 Полосы ИК-спектра при 3250, 3115, 1715, 135О и 1160 . Сигналы ЯМР при Г -2,4(1Н)-6,2(2Н), 6,6(2Н) и 6,8 ч. на млн.(ЗН). Метод 2. К суспензии из 43 вес.ч. имидазолидона-2 в 300 об.ч. сухого тетрагидрофурана в течение 30 мин при размешивании прикапывают 80 вес.ч. метансульфохлорида и 56 вес.ч. триэтиламина, после чего внутренняя температура составляет 354О°С. Перемешивают дополнительно в течение 2 час при 45 С, затем выделяют растворитель в вакууме, получаемый при этом остаток дважды извлекают хлороформом, каждый раз в количестве 150 об .ч., а остающиеся кристаллы перекристаллизовывают из метанола. Выход продукта 49%. Данный продукт соответствует N -метилсульфонилимидазолидону-2 по температуре плавления и ИК-спектру. Пример 2. Патрий В, ( 3-метилсульфонилимидазолидин-2-он-1-ил}-карбониламино -4-хлорбензилпенициллина. Этот пенициллин получают описанным в примере 1 А способом из 7,5 вес.ч. D, L (3-мeтилcyльфoнилимидaзoлидин-2-oн-l-ил)-кapбoнилaминoJ -4-хлорфенилуксусной кислоты 3,75 вес.ч. хлорида тетраметилхлорформамидиния и 4,7 вес .4. 6-аминопенициллановой кислоты. Вместо N -метилморфолина применяют 2,02 вес.ч. триэтиламина. Выход продукта 65%. Содержание j -лактама 62%. Согласно спектру ЯМР, получаемый продукт содержит еще 24% метилсульфонилимидазолидонил-карбониламинохлорфенилуксусной кислоты, которую можно, однако, удалить фракционированным подкислением водного раствора натриевой соли пенициллина. Полосы ИК-спектра при 3310, 176О, 1722, 1670, 1605, и 1170 см-1 (в ,Nuja ) Сигналы ЯМР при Т -2,53 (2Н), 2,67 (2Н), 4,4(1Н)-4,5(2Н). (в метаноле) 5,8 (1Н) 6,1(4Н), 6,65(ЗН), 8,3-8,5 ч. намлн(бН). Пример 3. Натрий D,. C(3-мeтилcyльфoнилимидaзoлидин-2-oн-l-ил)-кapбoriИпамино - е -тиенил-(2)-метилпенидиллина. Этот пенициллин получают описанным в примере 1 А способом из 7,0 вес.ч. D,L-ьit(3-мeтилcyльфoнилим;шaзoлвдин-2-oн-i-ил)-карбониламино -тиенил-(2/-уксусной кислоты, 3,75 вес.ч. хлорща тетраметилхлорформамидиния и 4,8 вес.ч. 6-аминопенициллановой кислоты. Выход продукта 3t:7o. Содержание Ji -лактама 68%. Полосы ИК-спектра при 3310,.1758, 1722. 165О, 1605и 1170 Сигналы ЯМР при Т -2,5-3,1 (ЗН), 4,1-4,6(ЗН), 5,8(1Н), 6,1(4Н), 6,7{ЗН и 8,25-8,5 ч. на млн(бН). Получаемый сырой продукт содержит око ло ,L .(З-метилсульфонилимидаз лидин-2-он-1-ил)- карбониламино - сХ. -ти енил-(2Н)-ацетата натрия, который можно, однако, удалить фракционированным подкислением водного раствора. Пример 4. Натрий L (3-м тилсульфонилимидазолидин-2-OH-l-ил)-карб ниламино -бензилпенициллина. Этот пенициллин получают описанным в примере 1 А способом из 6,8 вес.ч. LЦ 3-метилсульфонилимидазолидин-2-он-1-и капбониламино -фенилуксусной кислоты, 3,75 Бес:л. хлорида тетраметилхлорформам диния и 4,7 вес.4. 6-аминопенициллановой кислоты. Выход продукта 72%. Содержание - лактама 66%. Вычпслено, %: С 44,1; Н 4,7; N 11,5 510,6 Найдено, %: С 43,5; Н 5,5; N11,5; 310,1 При расчете результатов анализа учиты вают содержание воды 3% и содержание 2-этилгексаноата натрия 2%. Полосы ИК-спектра при 331О, 176О, 172 1665, 16О2 и 1168 . Сигналы ЯМР при Г -2,6(5Н), 4,354,8 (ЗН), 5,8 (1Н), 6,2 (4Н), 6,7 (ЗН) и 8,4 ч. на млн. (6Н). Пример 5. Натрий B,L с С(3-метилсульфонилимидазолидин-2-он-1-ил)-карСонилампноЗ -2,6-дихлорбензилпеницилл;|.;;. ,- i -КШ1ЛЛИН получают описанным в пг: .:,.:,ре 1 А способом из 7,0 вес.ч. Д L - - 3-метилс:;...(ьфо : лимид,золидин-2- -2,6-дихлорфенил -он-1-й; - арбонилы.. уксусной кислоть;. 3,2 1ь., -. х:10рида отр метилхлорформамидин i л 4,3 Dec Л 6-ами ы. акцик мо нопенициллановой кисло действия замещенной фенилулсусно- кис.:;,, с хлоридом тетраметилформамидш.л , олнако, в отличие от примера 1 А, проводя, при -2О С. Выход продукта 77%. Содержание Ji-лактама 61,5%. Вычислено, %: С 38,5; Н 4,О; С1 12,2 N 10,0; S 8,7. Найдено, %: С 36,0, Н 4,0; С1 12,6; N 10,5; 59,3. Полосы ИК-спектра при 331О, 1764, 1720, 1678, 16О7, 1512, 1255 и (в „ NU.QM ) 1167 см-1. Сигналы ЯМР при Г -2,5-2,9{ЗН), 3,8(1Н), 4,45(2Н), 5,8(1Н), 6,15(4Н), 6,7(ЗН) и 8,3-8,6 ч. на млн.(бН). Содержание пенициллина 62%, натриевой соли eiC- (3-метилсульфонилимидазолидин)-2-oн-l-ил)-кapбoнилaминoJ -2,6-дихлорфенилуксусной кислоты 30%, 2-этилгексаноата натрия 4,0% и воды 3,6%. Эти содержания получают спектром ЯМР сырого продукта. Фракционированным подкислением водного раствора сырого продукта пенициллина можно получить в чистом виде. Пример 6. А. Натрий . 1(3-ацетилимидазолидин-2-ОН-1 -ил)-карбониламино} -бензилпенициллина. Этот пенициллин получают описанным в примере 1 А способом из 5,0 вес .ч. L - pi. - i(3-aцeтилимидaзoлидин-2-oн-l-ил)-кapбoнилaминo -фенилуксусной кислоты, 3,1 вес.4. хлорида тетраметилхлорформамидиния и 4,3 вес.4. 6-аминопенициллановой кислоты. Выход 74%. Содержание р лактама 75%. Полосы ИК-спектра при 3305, 1765, 1730, 1675, 1605, 1520 и 1258 (в „ Nujoe Сигналы ЯМР при Г -2,4-2,8(5Н), 4,5-4,8(ЗН), 5,8(1Н), 6,22(4Н), 7,5(ЗН) и 8,4 ч. на млн.(бН). Б. 3-Ацетилимидазолидин-2-он-1-карбонилхлорид. Приготовляют смесь из20вес.ч. N -ацетилимидазолидона-2 с 25 вес.ч.триэтиламина и 150 об.ч. сухого бензола и в течение 30 мин при комнатной температуре, размешивая, прибавляют по каплям 27 вес.ч. триметилхлорсилана в 40 об.ч. бензола. Затем в течение 18 час кипятят без доступа влаги с обратным холодильником, после охлаждения отфильтровывают от выпавшего триэтиламингидрохлорида (22 вес.ч. - 1ОО%), который тщательно промывают сухим бензолом. Получаемьш бензольный раствор смешивают при5°Сс раствором из 17 вес.ч. фосгена в 5О об.ч. бензола и выдерживают в течение ночи при 5 С. Затем выделяют растворитель в вакууме, а остаток высушивают у масляного насоса. Пере- кристаллизовывают из смеси ацетон/пентан . Выход продукта 81%. Т.пл. 104 С. Вычислено, %: С 37,7; Н 3,7; С1 18,6; Ы14,7. Найдено, %: С 39,3; Н 4,3; С1 17,7; - 14,7. .юлосы ИК-спектра при 1798, 17 4О, (э9О и 1660 . Сигналы ЯМР при Т -5,65-6,3 1Н и 7,45 ч. на млн.(ЗН). Согласно спекгу, ЯМР, продукт содержит еше 5-10% ацетил--.илазолона, что, однако, не мешает при взаиьдч-д . ии с С-фепилглицином и другими аминокисло- а и (к,-- . примере 1 Б 6). В. N -ацетилимидазолидон-2. К суспензии из 25,8 вес.ч. имидазолона-2 в 350 об.ч. сухого тетрагидрофурана в течение 6О мин при О С прикапывают 23,6 вес.ч. ацетилхлорида в 10О об.ч. тет- рагидрофурана. Размешивают в течение 3 час при комнатной температуре, затем через раствор в течение некоторого времени продувают сухой воздух, удаляют растворитель в вакууме, а остаток перекристаллизовьюают из кнпяоцаго нитрометана. Выход продукта 52%. Т.пл. 188 С. Вычислено, %: С 46,9; Н 6,9; Ы 21,9. Найдено, % : С 47,0; Н 6,2; hl 22,5 Полосы ИК-спектра при 3230, 1730 и 1640 см . Сигналы ЯМР при Т -6,2 (2Н 6,5(2Н), и 7,6 ч. на млн. (ЗН). Пример 7. Натрий I}, I (3-ацетилимидазолид ин-2-OH-l -ил) -карбонила- мино1-4-хлорбензилпенициллина Этот пенициллин получают описанным в примере 1 А способом из 4,0 вес.ч. Hj L-oL- Е(3-йцетилимидазолидин-2-он-1-ил)-карбониламино1 -4-хлорфенилуксусной кислоты, 2,2 вес.ч. хлорщ1а тетраметилхлорформамидиния и 3,25 вес.ч. 6-аминопенициллановой кислоты. Выход продукта 76%. Содержание J пак тама 89%. Полосы ИК-спектра при 331О, 176О, 1730, 1670, 1600, 1518 и (в ,) 1259 см-1. Сигналы ЯМР при Т -2,4-2,9(4Н), 4,4(1Н), 4,5(2Н), 5,8(1Н), 6,2 {4Н), 7,5(ЗН) и 8,3-8,5 ч. на млн.(бН). Пример 8. Натрий Ц, L - o-l -1(3-ацетилимидазолидин-2-oн-l-ил)-кapбoнилaминoJ;-4-мeтилбeнaилпeнициллинa. Этот пенициллин получают описанным в примере 1 А способом из 3,2 вес.ч.Ц L, - с/. -(3-ацетилимидазолидин-2-он-1-ил)-карбониламино| -4--метилфенилуксусной кислоты, 1,9 вес.ч. хлорида тетраметилхлорформамидиния и 2,6 вес.ч. 6-аминопенициллановой кислоты. Выход продукта 45%. Содержание -лактама 83%. Полосы ИК-спектра при ЗЗО5. 176О, 1725, 1672, 16ОО, 1515 и 1255 см-1 (в NujoE ) Сигналы ЯМР при Г -2,6-2,8(4Н), 4,4-4,8(ЗН), 5,8(1Н),. 6,2(4Н), 7,5(ЗН), 7,7(ЗН)и8,3 8,6 ч. на млн.{6Н). Пример 9. Натрий Ц, L - «С. -(3 -ацетилимидазолидин-2-OH-l -ил )-карбонилaминoJ- з -тиенил-(2 )-метилпенициллина. Эт пенициллин получают описанным в примере 1 А способом из 8 вес.ч. - «Л. -(3-ацетилимидазолидин-2-он-1-ил)-карбониламикр|-тиенил-(2 )-уксусной кислоты. 4,9 вес хлорида тетраметилхлорформамидиния и 6,5 вес.ч. 6-аминопенициллановой кислоты. Выход продукта 887о. Содержание 3- -пак тама 87%. Полосы ИК-спектра при 3302, 176О, 1732, 1678, 16О5, 152О, и (з ) 1261 . Сигналы Majoe ЯМР при Г -2,5-3,2 (ЗН), 4,0-4,5 (ЗН), 5,8(1Н), 6,2(4Н), 7,5(ЗН) и 8,2-8,6 ч. на млн.(бН). Пример 10. Натрий ,Ь - «С -(3-ацетилимидазолидин-2-OH-l -ил) -карбонилаMHHoJ-2,6-дихлорбензилпенидиллина. Этот пенициллин получают описанным в примере 1 А способом из 6,5 вес.ч. TlU - «1 -(3-ацетилимидазолидин-2-OH-l -ил) -карбониламино -2,6-дихлорфенилуксусной кислоты3,2 вес:Ч. хлорида тетраметилхлорформамидиния и 4,3 вес.ч. 6-аминопенициллановой кислоты. При этом реакцию взаимодействия замещенной фенилуксусной кислоты с хлоридом тетраметилхлорформамидиния проводят при-10 С. Выход продукта 29%. Содержание Ji -лактама 66%. Полосы ИК-спектра при 331О, 1765, 1735, 1685, 1615, 152О, ( в Nujot) 1265, 1100, 1028 и 8О5 . Сигналы ЯМР при Т -2.7 (ЗН), 3,8(1Н), 4,3-4,6(2Н), 5,8(1Н), 6,2(4Н), 7,5(ЗН) и 8,2-8,6 ч. на млн. (6Н). Согласно спектру ЯМР, сырой продукт содержит еще 27% натрия В,Ь- - - (3-ацетилимидазолидин-2-он-1-ил)-карбониламино -2,6-дихлорфенилуксусной кислоты, которую можно выделить из продукта путем фракционированного подкисления водного раствора. Пример 11. Натрий D.L - Л -(3-этилсульфонилимидазолидин-2-OH-l -ил) -карбoнилaминoJ-бензилпенициллина. -2,9 вес.ч. B,L - X -(3-этилсульфонилимидазолидин-2-он-1-ил)-карбониламино -фенилуксусной кислоты (содержит 1 моль изопропанола и 1 моль в кристалле) растворяют в 30 об.ч. тетрагидрофурана. Затем раствор охлаждают до -30 С и соединяют с охлажденным до -4О С раствором из 1,6 вес.ч. хлорида тетраметилхлорформамидиния в ЗО об.ч. дихлорметана. Затем смесь доводят до -25 С, добавляют 0,9 вес.ч. Ы -метилморфолина и через 3 мин еще охлажденную до -5 С смесь из 2,3 вес.ч. 6-аминопенициллановой кислоты и 25 об.ч. 9О%-ного водного тетрагидрофурана с рН 2,5 обрабатывают приблизительно 10%-ной соляной кислотой. Затем температуру повышаютдо О С и добавлением К -метилморфолина или разведенного натрового щелока рН поддерживают тот же. Через час для поддержания значения рН 2,5 добавления основания больше не нужно. Затем рН устанавливают 7,0,тетрагидрофуран большей частью вьщеляют в вакууме, а остающийся водный раствор извлекают один раз путем встряхивания эфиром (-эфирную фазу удаляют) и после подачи слоя смеси из эфира и уксуса подкисляют . до значения рН 1,5. Органическую фазу отделяют, промывают водой и высушивают в течение часа над при О С. ЗаTfM удаляют вь.1с:у111ИПс1Ю1пее BeuiecTBo и поп помощи сояерж.чшМо метан(;л эфирно1Х) раствора 2-этилгексаноа1-а натрия ;осаждают натриевую соль пеницилпима. Выход продукта 3,2 вес.ч. Содержанке J -лактама81, Сигналы ЯМР при Т -2,4-2,85(5Н), г4,4-4,8(ЗН), 5,8 (1.11), 6,15(4Н), 6,36,7(2Н) и 8,3-8,8 ч. на млн. (9Н) D - Д - {3-этилcyльфoнилимидaзoлнj дин-2-oн-l-ил)-кapбoнилaминoЗ -фенилуксусная кислота. К раствооу 5,5 вес. ч. 3); -бис-триме тилсилил-о4 -аминофенилуксусной кислоты в 40 об .4. тетрахлорметана приблизительно при О С прибавляют 4,5 вес.ч, 3-этилсульфонилимвдазолидин-2-он-1-карбонилхлорида, затем эту смесь вьщерживают в течение 4 час при 20 С, удаляют растворитель, а остаток в ступке тщательно обрабатывают 1 н НСЕ Получаемый твердый продукт отсасывают, промывают водой, высушивают и перекристаллизовывают из изопропанола. Выход продукта 6,О вес.ч. Т.пл. 1О2 С, после повторного затвердевания т. пп. 211 О При расчетй результатов анализа учитывается содержание 1 моля изопропанола и 1 моля Н2О. Вычислено, %: С 47,1; Н 6,3; f49,7;S7,4. НаГщено, %: С 47Д; Н 5,7; Г N 9,7; S 7,6. Сигналы ЯМР при Г;-2,(5н 4.6(1Н), 6,.1(4Н), 6.3-6,7(2Н), и 8,58,7 ч. на млн. (ЗН). З-Этилсульфонилимидазолияин-2-oH-l-карбонилхлорид. Этот продукт получают из З- этилсулфонилимидазплиден-2-она- и фосге на в дихлорметане и в присутствии пирцдин при 2О°С. Т.пл. 174°С. Вычислено, % : С 29,9; Н 3,8; С1 14,8; N 11,6; S 13,3 Найдено, % : С ЗО,1; Н3,8; С1 14,7,-. N 11,8; S13,3. Сигналы ЯМР при f -5,5-6.1 (4Н), 6,2-6,65{2Н)и8.4-8.75 на млн. (ЗН). : . 1 Этилсульфонилимидазолидин 2 -он. Это вещество получают нагреванием молярных количеств имидазолидин-2-она и этилсульфо нилхлорида при 15О-18О С (до окончания выделения HCl). Чистое вещество получаю путем извлечения при помощи горячего бен зола, ацетона и уксусного эфира из сырого продукта и перекристаллизации из ещетона (с добавкой активного угля) Т.пл. 114°С. Вьгаислено, %: С 33,7; Н 5,7; N 15,7; 18,0 Найдено, %: С 33,1; Н 5,7; N 16,3; S17 Сигналы ЯМР при Т -5,9-6,7(бН) н 8,5-8,8 ч. на млн.(ЗН). Г1 р и м е р 12. Натрий D - - С этилсульфонилнмидазолилнн-2-on-1 -пд) -карбоииламнно т-бензилпенилнллнн. 1аствор из 8,6 вес.ч. D -био-Т птметилсилил- еС -аминофенилуксуспой кпслотг в ди хлорметане охлаждают до О С, затем п{Н1 дальнейшем охлаждении прибавляют по капЛям раствор из 7,0 вес.ч. 3-этилсульфонилимидазолидин-2-он-1-карбонилхлори/1а t :15 об.ч. дихлорметана, а после этоrxj выдерживают смесь в течепие ночи при . Потом добавляют раствор 5,0 вес.ч. хлорида тетраметилхлорформамидиния в 13 об.ч. дихлорметана и выдерживают эту смесь в течение часа при О С. Затем реакционную смесь каплями подают в охлажденную до Ю С и доведенную при помощи разведенной ;Соляной кислоты до значения рМ 2,5 суспен|зию из 8,2 вес.ч. 6-аминопенипнллановой «ислоты в;85 об .ч .-лого водного тетрагидрофурана и при этом поддерживают значение рН соответствующей добавкой развепри 2,5. Затем в течение денного часа дополнительно разМещивают при О С и при этом дальнейшим добавлением развеценного натрового щелока поддерживают значение рН 2,5. Затем значение рИ устанавливают 7,0,1 удаляют летучие органические растворители в вакууме и выделяют натриевую соль пенипиллина J описанным в предьщущем примере способом. Выход продукта 8,0 вес.ч. Содержание „ -лактама 58%. Пример 13. Натрий Л-(3 -этилсульфонилимидазолидин-2-он-1-ил)-карбони-. ламино - И -хлорбензилпенициллина. Этот пенициллин получают описанным в .примере 11 способом из 4,5 вес.ч. в L 3л-этилсульфонилимид азолидин-2-он-1 -ил) -карбониламино; - ft. -хлорфенилуксусно и кислоты,; 2,.ч. хлорида тетраметилхлорфор;мамидиния, 1,3 вес.ч. N -метилморфолина ш.3,2 вес.ч. 6-аминопенициллановой кислоты. Соединение с б-г&мйнопенициллановой кислотой производят через 7 мин. Выход продукта 4,4 вес.ч. i Полосы ИК-спектра при ЗЗОО, 1765, 1725, 167О, 16ОО,-152О-1500, 126О, 1165, ИЗО см-1 (в NuLJaP ). ei. - (З-этилсульфонилимидазолидин-2-он-1-Ш1)-карбониламино - Ц -хлорфенилуксусная кислота. К суспензии из 11,0 вес.ч. п -хлор-с( -аминофенилуксусной кислоты в 110 об.ч. 5О/о-ного водного диоксана прибавляют концентрированный натровый щелок до тех пор. пока кислота не будет растворена. Затем г1ри размешивании вводят разведенную соля ную кислоту до тех пор, пока не будет достигнуто значение рН 7,5-8,0. Потом добавляют по порциям 13 вес .4. 3-этилсульф нилимидазолидин-2-он-1-карбонилхлорида приблизительно при О С и при помощи разведенного натрового щелока поддерживают значение рН смеси 7,5-8,0. Затем размещивают дополнительно, пока для поддержания этого значения рН еще необходимо время от времени подавать натровый щелок. При значении рН 6,5 удаляют большое количество диоксана в вакууме, добавляют около 200 об.ч. воды, при значении рН9,0 извлекают один раз при помощи эфира (эфир ный экстракт удаляют), подают слой свежего эфира, и, размешивая, регулируют до значения рН 0,5. После этого органическую фа зу отделяют, промывают,. высушивают и полностью упаривают в вакууме. Остаток растворяют в горячем уксусном эфире, затем добавляют одинаковое количество бензола и петролейного эфира в количестве, как раз достаточном для исчезновения помутнения, и оставляют стоять для кристаллизации. Выход продукта 4,9 вес.ч. Т.пл.168 С. Сигналы ЯМР при Г -2,6(4Н), 4,6(1Н) 6,1(4Н), 6,3-6,7(2Н) и 8,4-8,8 ч. на млн.(ЗН). Полосы ИК-спектра при 33(5), L72O,165O, 1350, 116О см (в NaioC Пример 18. А. Натрий Б,Ь - « -(З-метилсульфонилимидазолидин-2-OH-l-и -карбониламино -4-метилбензилпенициллина. Этот пенициллин получают описанным в примере 1 А способом из 7,0 вес.ч. D, L -(З-метилсульфонилимидазолидин-2-OH-l-ил) -карбониламино -4-метилфенилуксусной кислоты, 3,8 вес.ч. хлорида тетраметилхлорформамидиния и 5,0 вес.ч. 6-аминопенициллановой кислоты. Выход продукта 57% Содержание -лактама 83%. Полосы ИК-спектра при 332О, 1765, 1727, 1674 16О5, 1515, 1255 (в NaioE. ) и 1170 см Сигналы ЯМР при Г -2,65(2Н), 2,83{2Н), 4,3-4,6{ЗН), 5,8{1Н), в,15(4 6,7(ЗН), 7,7(ЗН) и 8,3-8,5 ч. на млн. (6Н). Б. D,L - о4 -(3-метилсульфонилими дазолидин-2-он-1-ил)-карбониламино-4-мети фенилуксусная кислота. Эту карбоновую кис лоту получают описанным в примере 1 Б 1 способом из 11,3 вес.ч. 1-хлоркарбонил-З-метилсульфонилимидазолидона ( 2) и 9,1 вес, D,L -4-(метилфенил)-глицина. Выход продукта 42%. Полосы ИК-спектра при 370 5 2 1540, 15ОО, 1740-1660, 2200, ЗЗОО, ) 1255 и 97О см-1. Сиг(в NUJQ налы ЯМР при Т -1,3(1Н), 2,7(4Н), 4,7(1Н), 6,2(4Н), 6,6(ЗН) и 7,7 ч. на млн.(ЗН). Пример 19. А. Натрий D,L - J -(З-метоксикарбонилимидазолидин-2-oH-l-ил) -карбониламино -4-хлорбензилпенициллина. Этот пенициллин получают описанным в примере 1 А способом из 9 вес .ч. D, L -об -(З-метоксикарбонилимидазолидин-2-OH-l -ил) -карбониламино -4-хлорфенилуксусной кислоты, 4,85 вес.ч. хлорида тетраметилхлорформамидиния и 6,5 вес.ч. 6-аминопенициллановой кислоты. Выход продукта 8О%. Содержание -лактама 85%. Полосы ИК-сп.ектра при ЗЗОО/ЗО5О. 1770, 1742, 1730, 1670, 1605, 1520, 1320, и 1260 см (в Nujo ). Сигналы ЯМР при1: -2,57(2Н), 2,65(2Н), 4,35-4,65 (ЗН), 6,14{4Н), 6,16(ЗН) и 8,3-8,6 ч. на млн.(бН). Б, D, L - оС - f (3-метоксикарбонилимидаЗОЛИДИН-2-ОН-1-ИЛ)-ка;рбониламино -4-хлорфенилуксусная кислота. Эту карбоновую кислоту получают описанным в примере 1 Б 1 способомиз 1О,4вес.ч. 1-хлоркарбонил-З-метоксикарбонилимидазолидона(2) и 10,2 вес.ч. D, L - «i. -(4-хлорфенил)-глицина. Выход продукта 61%. Вычислено, %: С 47,2; Н 4,0; С1 1О,0; N 11.8. Найдено, %; С 47,4; Н 4,5; С1 9,2; N 11,2. Полосы ИК-спектра при 37ОО-225О, 3280, 3060 и 1780-1630 см-1 ( в NLLJO ). Сигналы ЯМР при Г -1,0(1Н), 2,5(4Н), 4,5{1Н), 6,15(4Н) и 6,2О ч. на млн.(ЗН). В. 1-Хлоркарбонил-3-метоксикарбонил- имидазолидон(2). Этот хлорангидрид кар)баминовой кислоты получают описанным в примере 6 5 способом из 8 B.C. ч ( -метоксиарбаыилимидазолидона,-2, 9,7 вес. ч. три- метилхлорсилана, 9 вес.ч. триэтиламина и 6,2 вес.ч. фосгена. Выход продукта 72%. Т.пл. 129°С. Вычислено, %: С 34,6; Н 3,4; С1 17,2; N 13,6. Найдено, %: С 34,8; Н 3,4; С1 17,li N 13,6. Полосы ИК-спектра при 1820, 1737, 169О и 1260 см-1. Т -5,7-6,3(4Н) и Сигналы ЯМР -при 6,1 ч. на млн.{ЗН). Г. К1 -метоксикарбонилимидазолидон-2 . 14,9 вес.ч. N -хлоркарбонилимидазолидона-2 вводят в 7О об.ч. холодного, как лед. 25 течение часа пр метанола и размешивают в комнатной температуре, а затем U течение 40-5О С. После удаления избычаса при точного метанола перекристаллизовывают и ацетона. Выход продукта 55%. Вычислено, %: С 41,6; Н 5,5; N 19,4. Найдено, %: С 41,8; Н 4,8; N 19,2. Полосы ИК-спектра при 332О, 1745, и 1670 см-1. Пример 20. А. Натрий D, L о(- (3-мeтoкcикapбoнили IилaзoлlIдин-2-oн-l-ил)-кapбoнилaминc - oL -тиенил{2 )-метшшенициллина. Этот пенициллин получают описанным в примере 1 Л способом из 8,5 вес.ч. D L- о4 - (3-метоксикпрбонилимил1азолидин-2- -он-1 -ил)-карбониллмино - / -Tiiслил (2 )уксусной кислэты, 5,1 вое.ч. хлорида тетрамети 1хлорфо)м;1милиния ;; 6,9 вес.ч. 6-аминолон;-1Циллс111О1зо 1 кис.поты. Выход продукта 72/о. Содержание ft -лактама 67%. Полосы ИК-спектра при 3310,1773, 1750 1730,1670, 1610, 1520, (в N Uj Q Сигналы ЯМР при 1320 и 1265 СМ Т -2,5-3,2(ЗН), 4,1(1Н), 4,4-4,б(2Н), 5,8(1Н), 6,15(7Н) и 8,3-8,55 ч. на млн.(бН). Согласно спектру ЯМР, сырой продукт содержит еще 23% D, L - о(. -ИЗ -метоксикарбонилимидазолидин-2-он-1-ил)-карбониламиноЗ- (. -тиенил(2 )-уксусной кислоты, которую можно, однако, удалить фракционированным подкислением водного раствора. Б. Т , L - i. - (3-метоксикарбонилимида золидин-2-он-1-ил)-карбониламино - oL -тиенил(2)-уксусная кислота. Эту карбоновую кислоту получают описанным в пример 1 Б 1 способом из 8,8 вес .ч. 1-хлоркарбонил-3-метоксикарбонилимидазолидона (2} и 7,3 вес.ч. И, L, -/-тиенил(2)-глицина. Выход продукта 73%. Вычислено, %; С 44,0,: П 4,0; N 12,8 S9,8. Найдено, %: С 44,1; Н 4,0; N 12,0; S9,9. Полосы ИК-спектра при 3700-22 3280, 1775, 1740-1640, 1515 и 1015СМ (в Nu-jat ). Сигналы ЯМР при Т -0,9(1Н), 2,5-3,1(ЗН), 4.2(1Н), 6,15(4 и 6,20 ч. на млн. (ЗН). Пример 21. Матрий D-«(3-этилсульфонилимилазолидин-2-он-1-ил)карбониламино -бензилленициллина. 2,9 вес.ч. D - (3-этилсульфонилимидазолидин-2 он-1-ил)-карбониламино -фенилуксусной кислоты растворяют в 30 об.ч тетрагидрофурана, полученный раствор охлаж -30°С, а затем добавляют срадают до зу весь предварительно охлажденный до -30 С раствор 1,0 вес.ч. хлорида тетраме2тилхлорфэрмамидинияв 30 об,ч. дихлорметана. Прозрачный раствор образуется при температуре, равной от -25 до -20 С. Этот раствор выдерживают в течение 15 мин при -25 С. Затем весь раствор сразу вливают в поддерживаемую при. 0-5 С суспензию или раствор 2,3 вес.ч. 6-аминопенициллановой кислоты в 25 об.ч. 90%-ного водного тетрагидрофурана, рН которого добавлением 10%-ной водной соляной кислоты доводят до 2,5 и поддерживают его соответствующим добавлением 2 н. водного натрового щелока. Раствор охлаждают смесью из льда и воды, в результате чего температуру доводят до О С и поддерживают на этом уровне. Через час смесь разделяют несмотря то, что для поддержания значения рН 2,5 необходимо еще добавлять натровый щелок. Разделение происходит по примеру 11. Выход продукта 2,3 вес.ч. ИК-спектр данного пенициллина идентичен ИК-спектру пенициллина из примера 11. Формула изобретения Способ получения пенициллинов общей формулы 1 , A-Z-NH-CH-CO-NH-CH-CH X N. / СН. СН где А NHC-N-y-NN5C Ni a 5 R,-X-N-y-NT j-x -N г N-y-N ,-c- II Q. «X R.-)f-N-C-NR,-X-H I Й «1 I -M-y R-C-N-«-N 2тг8) N -с -где X - группа
I
-5 или - с Н С r I -армА -e QJ - группа & &Q 11 i -(С)-2ИАИ С CO - с I & I О & Qj - группа G 1 (С)-5ИАИ С 1 G -с - N-e I I fr & (с) I1 к & С (С) (С) -3t-j/ сI оiOMtNl Gfi €О где R - неразветвленный или разветвленный алкильный радикал с числом углеродных атомов до 5; G- водород или g, причем стрелка в двухвалентном промежуточном звене Ч показывает, что вызываемое двумя свободными валентностями этого промежуточного звена соединение двух атомов должно произойти не любым, а указанным стрелкой образом R - алкил с числом углеродных атеомов до 10, циклоалкил с числом углеродных атомов до 10, алкенил с числом углеродных атомов до 10 и циклоалкенил с числом углеродных атомов до 10, винил, аривинил, МОНО-, ди- и тригалоген-низший алкил, 2 7 №) - рил-чмизший алкил-, амино, алкоксил )с числом углеродных атомов до 8, аралкоксил ) с числом углеродных атомов до 8, циклоалкэксил ) с числом углеродных атомов до 7, арилок- сигруппа Только в том случае, если - SOg -). групX одновременно не означает g-O-V, . N-C-V JHI-CO-V, HjN-CO-v- Я-NH-CO-v-,, (К) N-CO-VOCCHJn1 5 S ;«..)„- -Hf -, 0 A / -./ y J N/ a/Njb/ где - двухвалентный оргш ический раикал с 1-3 атомами углерода; 4 , Rj И Т, каждый - водород, нит DO-, нитрил, (T), 2)N-CQ-, тг-co-N СО-, тг-со-0- T2-,R-o-H2.Nхлор, бром, йод, фтор или трифторметил, причем Ь имеет указанные значения; П. - целое число от О до 2 включител но; каждый - водород, алкил или алке нил, каждый с числом углеродных атомов до 8, винил, аллил, пропенил, циклоалкил и циклоалкенил, каждый с числом углерод ных атомов до 6, МОНО-, ди- и тригалоге низший алкил или арил, В - группа формулы где RT,S& и Rg - водород, галоген, T,,,,T;-S-, „итро, (.R)2.N-,-R-CO-NH-,HO,T -CO-0-, причем R имеет указанное значение, Z - группа -Ct:° или -С , С - ассиметричный атом углерода, или их солей, отличающийся тем, что 6-аминопенициллановую кислоту формулы II СН. Н N-CH-CH С- N //подвергают взаимодействию с функциональным производн лм карбоновой кислоты общей формулы 1И A-f -NH-CM-COQH В где А , 2 , В И Симеют указаные значения, в безводном Ии1И всдосодеижатцем пастве- ителе в присутствии основания с последуюим выделением целевого продукта в своодном виде или в виде соли. 2. Способ по п. 1, отличающийя тем, что реакцию проводят при значеии рН от 2 до 9.















Авторы
Даты
1976-07-25—Публикация
1972-10-12—Подача