(54) СПОСОБ ПОЛУЧЕНИЯ 4-АЦИЛ-1,3,4 ОКСАДИАЗОЛИНОВ


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 4-ацетил-5,5-диалкил1,3,4-оксадиазолинов | 1974 |
|
SU596582A1 |
| Способ получения диалкил-или диарил -/1-ацилокси-1-метил-2,2,2-трихлорэтил/фосфонатов | 1972 |
|
SU436823A1 |
| СПОСОБ ПОЛУЧЕНИЯ//ЯС-1,2^ЭПОКСИП! | 1971 |
|
SU320120A1 |
| Способ получения третичных аминокислот, или их сложных эфиров, или амидов,или тиоамидов,или нитрилов,или их солей | 1969 |
|
SU468426A3 |
| Способ получения производных оксадиазолона | 1972 |
|
SU437298A1 |
| Способ получения производных 11-аза-10-деоксо-10-дигидро-эритромицина @ | 1980 |
|
SU1093253A3 |
| Способ получения трифенилметильных производных S @ -глицеро-3-фосфохолина и S @ -глицеро-3-фосфоэтаноламина | 1985 |
|
SU1422999A3 |
| Способ получения 3-ацилоксициклогексен2-онов-1 | 1976 |
|
SU635090A1 |
| Способ получения гидразинопири-дАзиНОВ | 1975 |
|
SU799661A3 |
| Способ получения производных дигидро-ас-триазино (5,6- @ ) хинолина или его хлоргидрата | 1981 |
|
SU1014475A3 |

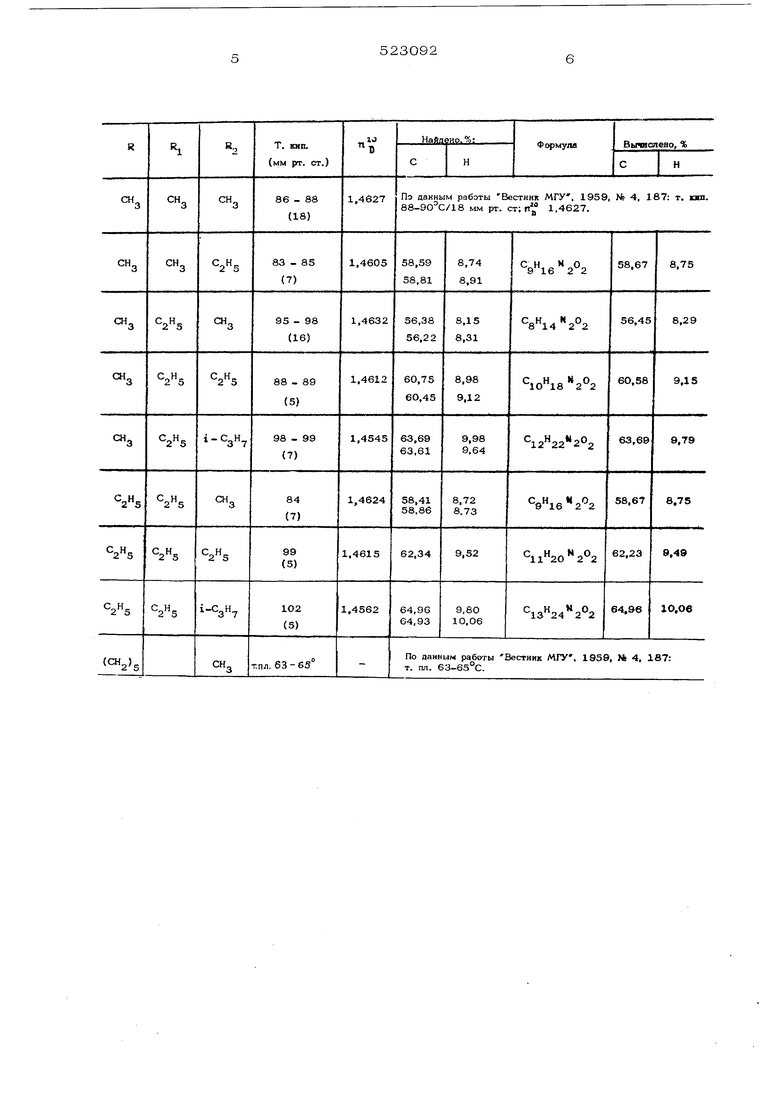
Изобретение относится к способу получения 2-апкипзамещенных 4-ацил-1,3,4-оксадиазолинов общей формулы нХ„ R одинаковые или разные и где R, R и означают апкил С Q которые могут найти применение как фармакологически активные вещества, гербициды, инсектициды или как исходные вещества для получения диа- цилгидразинов. Известен способ получения 4-ацетил-2-алкил(арил, гетероарил)-1,3,4-оксадиазолинов путем нагревания ацилгидразонов кетонов с избытком уксусного ангидрида при кипении в течение 0,5-1,5 час tilОднако известный способ не является уни версальным, а исходные вещества (ацилгид разоны) получают двухстадийным синтезом. Например, при получении 2-метилзамещен- ных оксадиазолинов на основе ацетона про- песс включает следующие стадии; получение ацетилгидразина, конденсация его с ацетоном, и ацилирование ацетилгидразона уксусным ангидридом. С целью упрощения процесса предлагают 3,3-диалкилдиазиридин общей формулы RS /INH R, Ж подвергать взаимодействию с ангидридом карбоновой кислоты ()О при температуре 160-165°С. 3,3-Диалкилдиазиридины получают в одну стадию из соответствующих кетонов, аммиака и хлорамина (или гидроксиламино-О-сульфоновой кислоты). Универсальность способа следует из того, что на основании одного и того же диазиридина ацилированием различными ангидридами получают одсадиазолины, содержащие в положениях 2 и 4 кольца различные алкильные группы. Пример. 2,5-диметил-5-этил-4- -ацетил-1,3,4-оксадиазолин. 0,03 г. моль (2, б г) 3-метил-З-этилдиазиридина охлаждают до О С и вначале медленно, по каплям, а затем быстрее, встряхивая смесь, прибавляют 0,10-.ОД2г..моль (10,2-12,2 г) уксусного ангидрида. Убирают охлаждение, при этом смесь слегка разогревается, а затем вьщерживают ее при 160-165 С в течение 40-45 мин. Удаляют в вакууме избыток ангидрида и образовавшуюся уксусную кислоту, остаток перегоняют, т. кип. 73-75 С/7ммрт. ст.; 1,4615. Выход 68%. Повторной перегонкой получают аналитически чистый продукт. П р и м е р 2. 5-Метил-2,5-ДИЭТИЛ-4-пропионип-1, 3, 4-оксаш1азолин. 0,03 г -моль (2,6 г) 3-м етил-3-этилдиазиридина охлаждают до О С и вначале медленно, по каплям, а затем быстрее, встряхивая смесь, прибавляют 0,10-0,12г-моль (13,0-1 5,6г) пропионового ангидрида. Уби рают охлаждение, при этом смесь слегка разогревается, а затем вьщерживают-ее при 160-16 5°С в течение 40-45 мин. Удаляют в вакууме избыток ангидрида и образовавшуюся пропионовую кислоту, остаток перегоняют, т. кип. 80-88 С/ 4 мм рт. ст.; П.0 1,4612. Выход 65%. Повторная дистилляция дает аналитически чистый продукт. Прим 9 р 3. 5-Метил-5-этил-2-изо- пропил-4-изобутирил-1,3,4-оксадиазолин. 0,03 г.моль (2,6 г) 3-метил-З-этилдиазиридина охлаждают до О С и вначале медленно, по каплям, а затем быстрее, встряхивая смесь, прибавляют 0,10-0,12 г-моль (15,8-18,9 г) ангидрида изомасляной кислоты. Убирают охлаждение, при этом смесь слегка разогревается, а затем вьщержива ют ее при 160-165 С в течение 40-45 мин. Удаляют в вакууме избыток ангидрида и образовавшуюся изомасляную кислоту, остаток перегоняют; т. кип. 94-99 С/ 7 мм рт. ст. 1,4540. Выход 607с. Повторная дистилляция дает аналитически чистый хродукт. Аналогично получают 2,5,5- триметил-4-ацетил-1,3,4-оксадиазолин из 3,3-диметилдиазиридина и уксусного ангидрида; 2-этил-5,5-диметил-4-пропионил-1,3,4-оксадиазо- ЛИН из 3,3-диметилдиазиридина и пропионо- вого ангидрида; 2-метил-5,5-диэтил-4-ацетия-1,3,4-оксадиазолин из 3,3-диэтилдиазиридинаи уксусного ангидрида, 2,5,5-триэтил-4-пропионил-1,3,4-оксадиазолин из 3, 3-диэтилдиазиридина и пропионового ангидрида; 2-изопропил-5,5-диэтил-4-изобутирил-1,3,4-оксадиазолин из 3,3-диэтилдиазиридина и ангидрида изомасляной кислоты; 2-метил-5,5-пентаметилен-4-ацетил-1,3,4оксадиазолин из 3,3-пентаметилендиазиридина и уксусного ангидрида. Константы полученных 2,5,5-триалкил-4-ацип-1,3,4-оксадиазолинов приведены в таблице. Строение полученных соединений подтверждено ИК-спектрами и спектрами ПМР. Формула изобретения Способ получения 4-ацш1-1,3,4-оксади золинов общей формулы I 5 где R, R и R - одинаковые или разные означают алкил С -Со. отличающийся тем, что, с цел 8 , 3,3-диалкипдиазиридин прощения процесса, бщей формулы II К RI NH подвергают взаимодействию с ангидридом карбоновой кислоты (i -СО) О при 16016В°С. Источники информации, принятые во внимание при экспертизе: 1. Р. С. Сагитуллин и др. Получение 2-метилзамещенных 4-ацетил-1,3,4-оксадиазолинов, Вестник МГУ, серия химическая, М. 1959. № 4, стр. 187.
Авторы
Даты
1976-07-30—Публикация
1975-02-21—Подача