5 R значения; вместе R и I,, jxiA 4j Д L 1 ti Juriv i}i-Jivi v j.v;; ri одновременно ознают метилендиоксигруппу, подвергают взаимодействию с водным раствором галоидводорода при 6О-150°С. Процесс предпочтительно проводить при 80-126°С. Для улучшения растворимости можно добавлять пригодный растворитель, например ледяную уксусную кислоту или ацетатгидрид Если в качестве средства .диметилирования берут соляную кислоту, то в некоторых слу чаях не бходим нагрев под давлением. Новые соединения проявляют улучшенные свойства по сравнению с их ближайшими ан логами, например - 1 - N-метил- N - ( З 4 -диметоксибензил)- Р-аминоэтил - теобр мин 2. Исходные соединения получают конденсацией 7-{ 3-галогенпропил)-теофиллина с за мещенными в ядре N -метил-JJ-фенилэтилам нами общей формулы CH,-NH-CH -CH или 7-(3-метиламинопропил)-теофиллина с замещенными в ядре Ь -фенилэтилгалогенидами общей формулы Нае - СН - СНв которых R , и I, имеют указанные значения. Пример 1. 7-ГМ-метил- Ы - ( |Ь -3-хлор-4-oкcифeнилэтил)-3-aминoпpoпил -тeo филлин. 56,1 г (0,13 моля) 7- М-метил-Н ( fi- 3-хл ор-4-метоксифенилэтил)-3-аминопропи -теофиллина и 12О мл водной бро мистоводородной кислоты (Б 1,5), что соответствует 96,4 г HBV , кипятят в течение 2 час с обратным холодильником, до бавляют 60 мл 48%-ной бромистоводородной кислоты и кипятят еще в течение 1 часа Реакционную смесь выливают в 1 л ледяной воды и точно нейтрализуют 40%-ным натровым щелоком. Вещество вьшадает и кристаллизуется при стоянии. Затем это ве щество растворяют в 2 н, соляной кислоте при этом выделяется гидрохлорид в )зиде белых кристаллов. После перекристаллизации из ацетона получают 25,2 г (41% от теоретического) гидрохлорида 7- М-метил-N -(, -3-хлор-4-оксифенилэтил)-3-аминопропил -теофиллина с т, пл, 114-116°С, Пример 2. 7- М-метил-Н-(Ь-3-окси-4-хлорфенилэтил) -3-аминэпропил -теофиллин. 4 10,7 г (0,03 моля) 7- Н-метил-М(р-З-метокси-4-хлорфе НИЛ этил)-3-аминопропил -теофиллина и 34,4 мл 48%-ной водной бромистоводородной кислоты обрабатывают аналогично примеру 1. Полученное вещество растворяют в ацетоне и добавляют раствор 3,5 г малеиновой кислоты в ацетоне. Выделившиеся кристаллы перекристаллизовывают из ацетона. Получают 43 г (32% от теоретического) малеината 7- М-метил-N - ( р - З-окси-4-хлорфенилэтил) -3-аминопропил -теофиллина с т, пл, 190-193°С, Пример 3, 7- Н-метил-М-( p-2-xлop-3-oкcифeнилэтил)-3-aминoпpoпил -теофиллин, 30,1 г (0,О72 моля) 7- N-метил-Ы-( pi - 2-хлор- 3-метоксифе НИЛ этил) - 3-ами нонропил -теофиллина и 97 мл 48%-ной водной бромистоводородной кислоты в течение 4 час кипятят с обратн1з1м холодильником и обрабатывают аналогично примеру 2. получают 8,8 г (24% от теоретического) малеината 7- N-метил-N-( |Ь-2-хлор-3-оксифеНИЛЭТИЛ )-3 -аминопропил -теофиллина, который после перекристаллизации из ацетона плавится при 195-19в°С, Пример 4, 7- М-метил-М-( Ь-3-фтop-4-oкcифeнилэтил)-3-aминoпpoпил -тeoфиллин, 60,3 г (0,137 моля) гидрохлорида 7- N-метил-М -(|:1-3-фтор-4-метоксифенилэтил)-3 аминопропил -теофиллина и 123 мл 48%-ной водной бромистоводородной кислото (I) 1,5), что соответствует 89 г НВг кипятят в течение 10 час в круглодонной колбе с обратным холодильником. Через 3 часа выделяется рассчитанное количество бромметана. Охлажденный бесцветш ш раствор смешивают с эквивалентным объемом дкэтилового эфира, в результате в виде кристаллов выделяется гидробромид 7- N-метил-М-( ( -3-фтор--4-оксифенилэтил)-3 аминопропил -теофиллина. После перекристаллизации из изопропанола получают 59,4 г (92%от теоретического) соли в виде б&лого кристаллического порощка с т, пл, 72,5 - 75°С, При дальпейшел4 нагревании расплав твердеет примерно при 145°С и затем вновь плавится при 225-227°С. 53,6 г (0,11 моля) упомянутого гидробромида растворяют в 1,3 л теплой воды и добавляют по каплям 114 мл 1 н, едкого натра под азотом, значение рН доводят до 7,0. Выделяют 43,5 г основания в виде белого кристаллического порошка с т,пл, 13О-132,5°С, которая не меняется после перекристаллизации из изопропанола, Раствор основания в метаноле с хлоридом железа (111) дает желтовато-красную окраску.
Если сухое основание растворяют в метаноле и пропускают хлористый водород до наступления слабокислой реакции, то выделяется гидрохлорид в виде белого кристаллического порошка. После перекристаллизации из смеси вода/этанол (1:5) т. пл. 234,5-237°С. Реакция с хлоридом железа
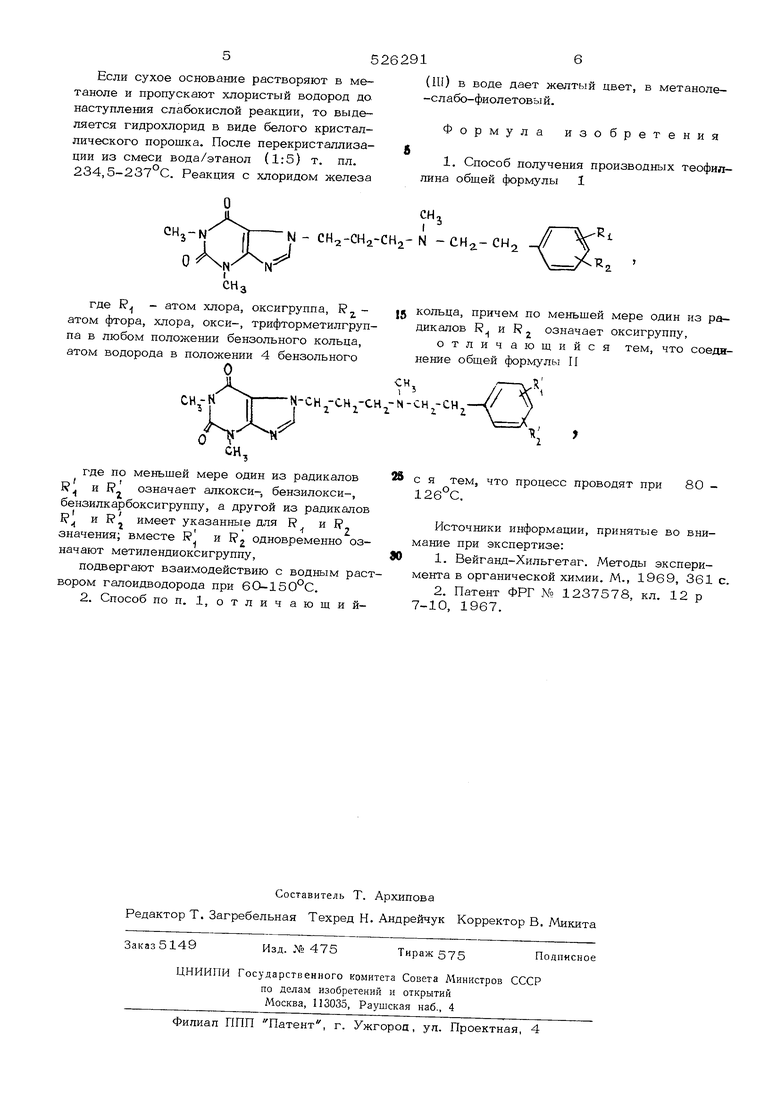
N - CH -CHa-CHj- N - СНз.- С где Р - атом хлора, оксигруцпа, К у. 15 атом фтора, хлора, окси-, трифторметилгруппа в любом положении бензольного кольца, атом водорода в положении 4 бензольного N-CH -CHj-CH -Nгде по меньшей мере один из радикалов
п означает алкокси-, бензилокси-.
R
бензилкарбоксигруппу, а другой из радикалов I. к к имеет указанные для R и I,
г-,Т-,
значения; вместе IV и к одновременно означают метилендиоксигруппу,
подвергают взаимодействию с водным расвором галоидводорода при 6О-150°С.
2. Способ по п. 1, о т л и ч а ю щ и й(ill) в воде дает желтый цвет, в метаноле-слабо-фиолетовый.
Формула изобретения
1. Способ получения производных теофиллина общей формулы 1
СИ. 1
2Ю
80 с Я тем, что процесс проводят при 126°С.
Источники информации, принятые во внимание при экспертизе:
1.Вейганд-Хильгетаг. Методы эксперимента в органической химии. М., 1969, 361 с.
2.Патент ФРГ № 1237578, кл. 12 р 7-10, 1967. кольца, причем по меньшей мере один из радикалов R и Rj означает оксигруппу, отличающийся тем, что соединение общей формулы П с„,-сн, 

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных теофиллина | 1974 |
|
SU507241A3 |
| Способ получения производных теофиллина | 1973 |
|
SU504490A3 |
| Способ получения производных теофиллина | 1974 |
|
SU507242A3 |
| Способ получения производных ксантина или их солей | 1977 |
|
SU668604A3 |
| Способ получения производных бензодиазепина или их солей | 1973 |
|
SU625607A3 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ГУАНИДИНА | 1973 |
|
SU382280A1 |
| Способ получения производных бензодиазепина | 1971 |
|
SU520917A3 |
| Способ получения производных 1-фенилалкил-4-окси-4-/3,4-метилендиоксифенил/пиперидина или их солей | 1974 |
|
SU531486A3 |
| Способ получения солей теофиллинизобутирата | 1971 |
|
SU447889A1 |
| Способ получения гидразин- -фенилпропионовой кислоты | 1972 |
|
SU539522A3 |


Авторы
Даты
1976-08-25—Публикация
1974-10-09—Подача