(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 8АЗАПУРИН-6-ОНА
1
Изобретение относится к способу получения производных 8- азопурин-б-она, обладающих ценными фармакологическими свойствами.
Способ получения основан на известных реакциях и позволяет получить новые производные азапуринона с важными терапевтическими свойствами.
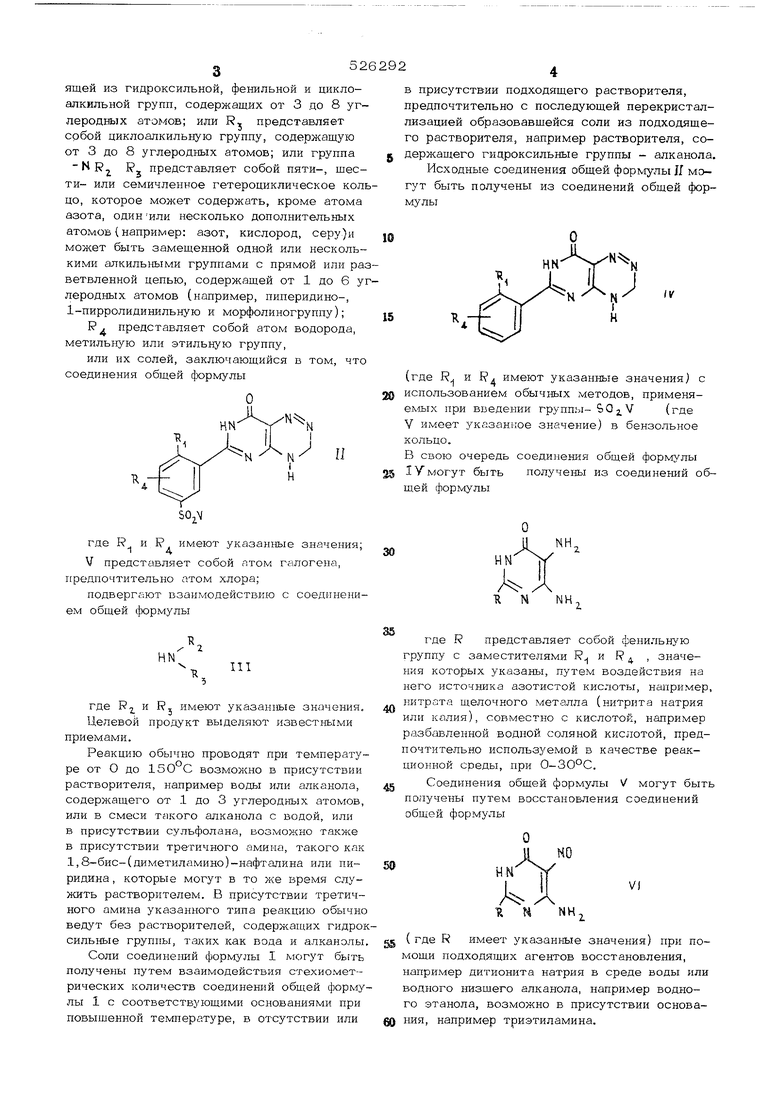
Предлагается способ получения производных 8-азапурин-6-она общей формулы
где R представляет собой гидроксильную группу, алкоксильную или алкилтиогруппу с прямой или разветвленной цепью, содержащую от 1 до 10, предпочтительно от 1 до 3 углеродных атомов;
R - атом водорода, алкильная, алкенильная или алкинильная группа, имеющая прямую или разветвленную цепь, причем каждая из групп содержит до 10 углеродных атомов и может иметь один или более заместителей, выбранных из группы, состоящей из гидроксильной группы, фенильной
и циклоалкильной групп , содержащих от 3 до 8 углеродных атомов, или R представляет собой циклоалкильную группу, содержащую от 3 до 8 углеродных атомов, или фенильную группу, которая может иметь
один или более заместителей, выбранных из группы, состоящей из алкильной и алкок сильной групп, содержащих от 1 до 6 углеродных атомов, атомов галогена (например, хлора) нитро- и трифторметильной групп;
5 атом водорода, алкильная , алкенильная или алкинильная группа, имеющая прямую или разветвленную цепь, причем каждая из этих групп содержит до 1О углеродных атомов и может иметь один или более
заместителей, выбранных из группы, состоящей из гидроксильной, фенильной и циклоалкильной групп, содержащих от 3 до 8 углеродных или R. представляет собой циклоалкильную группу, содержащую от 3 до 8 углерод1-1ых атомов; или группа
N К Ь, представляет собой пяти-, шести- или семичленное гетероциклическое кольцо, которое может содержать, кроме атома азота, одинИЛИ несколько дополнительных атомов {например: азот, кислород, серу)и может быть замещенной одной или несколькими алкильными группами с прямой или разветвленной цепью, содержащей от 1 до 6 углеродных атомов (например, пиперидино-, 1-пирролидинильную и морфолиногруппу);
Р представляет собой атом водорода, метильную или этильную группу,
или их солей, заключающийся в том, что соединения общей с юрмулы
О
HN
R
II
где R и I имеют указанные значения;
V представляет собой лтом галогена, предпочтительно атом хлора;
подвергают взаимодействию с соединением общей формулы
Б присутствии подходящего растворителя, предпочтительно с последующей перекристаллизацией образовавщейся соли из подходящего растворителя, например растворителя, содержащего гицроксильные группы - алканола. Исходные соединения общей формулы Я могут быть получены из соединений общей формулы
IV
(где R, и имеют указанные значения) с использованием обычных методов, применяемых при введении группы- (где V имеет указанное значение) в бензольное кольцо.
В свою очередь соединения общей формулы IV могут быть получены из соединений общей формулы
И N NH. где R2 и RJ имеют указанные значения. Целевой продукт выделяют известными приемами. Реакцию обычно проводят при температуре от О до 15О С возможно в присутствии растворителя, например воды или алканола, содержащего от 1 до 3 углеродных атомов, или в смеси такого алканола с водой, или в присутствии сульфолана, возможно также в присутствии третичного амина, такого как 1,8-бис-(диметиламино)-нафталина или пиридина , которые могут в то же время служить растворителем. В присутствии третичного амина указанного типа реакцию обычно ведут без растворителей, содержащих гидрок сипьные группы, так;их как вода и алканолы. Соли соединеьшй формулы I могут быть получены путем взаимодействия стехиомет-рических количеств соединений общей форму лы 1 с соответствующими основаниями при повыщенной температуре, в отсутствии или где R представляет собой фенильную группу с заместителями R и R , значения которых указаны, путем воздействия на него источника азотистой кислоты, например, нитрата щелочного металла (нитрита натрия или калия), совместно с кислотой, например разбавленной водной соляной кислотой, предпочтительно используемой в качестве реакционной среды, при О-ЗО-С. Соединения общей формулы V могут быть получены путем восстановления соединений общей формулы ( где R имеет указанные значения) при помощи подходящих агентов восстановления, например дитионита натрия в среде воды или водного низщего алканола, например водного этанола, возможно в присутствии основания, например триэтиламина. Соединения формулы могут быть получен путем взаимодействия соединений общей формулы (где R имеет указанные значения; X представляет собой анион неорганической кислоты, например соляной или сильной органической кислоты, например метансульфокислоты или толуол -парасульфокислоты; характеризует основность этой кислоты) с алкил-альфа-оксиминоцианоацетатом, например этил-альфа-оксиминоцианоацетатом, в присутствии низшего алкоголята щелочного металла-, в среде низщего алканола, например этилата натрия в этаноле, предпочтительно при температуре кипения реакционной смеси с обратным холодильником. Соединения, описываемые формулой VII, могут быть получены путем взаимодействи кислот, описываемых общей формулой , (в которой X и rt имеют указанные значения) с соединениями, описываемые общей формулой (в которой R имеет указанные значения), которые могут быть получены путем каталитического гидрирования соединений общей (ормулы (где R имеет указанные значения), предпоч тительно с использованием скелетного нике левого катализатора Ренея. Соединения (}юрмулы IX могут быть получены путем взаимодействия гидрохлорида гидроксиламина с соединениями общей формулыRCNX (где R имеет указанные значения) с использованием основного катализатора в под ходящем растворителе, например карбоната натрия в водном этаноле, гидрида натрия в этилцеллозольве или триэтиламина. Пример 1. 8-аза-2-(5- N,N -дим тилсульфамоил-2-пропоксифенил)-пурин-6-о 3,7 г 8-аза-2-(5-хлорсульфонил-2-пропоксифенил)-пурин-6-она растворяют при комнатной температуре в растворе диметил
амина в этаноле (75 мл, 33%-ный ) и раст-ед при 240-242°С; вор перемещивают в течение 90 мин, а затем его нагревают на паровой бане в течение 10 мин . Наиболее летучие компоненты удаляют р вакууме для получения масла, которое обрабатывают (5О мл) водой, содержащей несколько капель этанольного раствора диметиламина, фильтруют и фильтрат подкисляют рН - 1 при помощи концентрированной соляной кислоты. Белый кристаллический осадок перекристаллизовывают из водного этанола и сущат при температуре 140 С и давлении 10 мм рт.ст. Выход продукта 2,45 г; т.пл. 227-229°С, При проведении опыта аналогичным образом (с тем отличием,что продолжительность реакции была различной) заменяют этанольный раствор диметиламина соответствующими количествами следующих растворов:водный метиламин, 25%-ный; водный аммиак (уд.вес. 0,880); водный трет-бутиламин, 33%-ный (продолжительность реакции 24 часа); водный этилпмин, 35%-ный; водный 2-(метилс.мино)-этанол, ЗОто-ный; водный 1 -дезокси-1 - (метил е.мино) -глю- цитол, -ЗО о-ный, (продолжительность реакции 24 часа); водный пирролидин, 30%-ный; гексилбмин, 30%-ный, раствор в SO oном водном этаноле (продолжительность реакции 210 мин); водный N -метилбутиламин, 30%-ный (продолжительность реакции 24 часа); водный диэтиламин, 30%-ный (продолжительность реакции 24 часа); водный М -метилизопропиламин, 40%ный, (продолжительность реакции 24 часа); этанольный N -метилбензиламин, 12%ный (продолжительность реакции 24 часа); этанольный N -метилциклогексиламин,, 33%-ный (продолжительность реакции 24 часа); дипропиламин, 33%-ный, в 50%-ном водном этаноле (продолжительность реакции 24 часа). При этом получают 8-аза-2-(5- N -метилсульфамоил-2-пропоксифенил) -пурин-б-он, т.пл. 227-228°С (после удаления этанола и кристаллизации, проводимой путем растворения в горячем 2 н. водном аммиаке, с осаждением при помощи концентрированной соляной кислоты и сущки при температуре 140°С под давлением 10 мм рт. ст.); 8-аза-2-( 2-пропокси-5-сульфамоилфенил)-пурин-6-он, т.пл. 271-272°С (из уксусной кислоты); 8-аза-2-(5- N -трет-бутилсульфамоил-2-пропоксифенил)-пурин-6-он, он плавящийся 8-аза-2-( 5- N -этилсульфамоил-2-пропок сифенил)-пурин-6-он, плавящийся при 2402410С (из этанола); 8-аза-2-(5- N-2-оксиэтил- М-метилсуль фамоил-2-пропоксифенил) -пурин- 6-он, т. пл. 216-2170С (из этанола); N - 3-(8-аза-6-оксопурин-2-ил)-4 пропоксибензолсульфонил - 1-дезокси- 1-метиламиноглюцитол, т.пл. 183,5-185ОС (из воды); N (8-аза 6-оксопурин-2-ил)-4-пропоксибензолсульфонилЗ-1-амино-1-дезоксиглюцитол, т.пл. 205-207,5°С (из воды); N - 3-(8-аза-6-оксопурин-2-ил)-4-пропоксибензолсульфоршл -пирролидин, т.пл. 25О-251°С (из этанола); 8-аза-2-(5- N -гексилсульфамоил-2-пропоксифенил)-пурин-6-он, т.пл. 153-155°С (из метанола); сушка при температуре 100°С под давлением 10 мм рт.ст.; 8-аза-2-(5-Ы -бутил- N-метилсульфамоил-2-пропоксифенил)-пурин-6-он, т.пл. 178 1790С; 8-аза-2-( 5- N , N -диэтилсульфамоил-2-пропоксифенил)-пурин-6-он, т.пл. 228 (очищенный путем растворения в горячем 2 н. водном аммиаке и осаждения при помощи концентрированной соляной кислоты ); 8-аза-2-(5- N -изопропил- N -метилсульфамоил-2-пропоксифенил)-пурин-6-он, т.пл. 257-258 0 (из акрилонитрила); 8-аза-2-(5- М-бензил-М -метилсульфамоил-2-пропоксифеш1л)-пурин-6-он, т.пл. 132-1330О (из этанола); 8-аза-2-( 5- N -циклогексил- N -метилсул фамоил-2-пропоксифенил)-пурин-6-он, т.пл. 216-217°О; 8-аза-2-(5- N, N -дипропилсульфамоил-2 -пропоксифенил)-пурин-6-он, т. пл. НО 114°О (из водной уксусной кислоты; продукт содержит 1 молекулу кристаллизационной уксусной кислоты на молекулу). При проведении опытов аналогичным образом, но с заменой используемого в качестве исходного материала 8-аза-2-(5-хлОрсульфонил-2-пропоксифенил)-пурин-6-она соединением 8-аза-2-(5-хлорсульфонил-2-метоксифенил)-пурин-6-оном получают 8-аза-2-(5-N,N -диметилсульфамил-2-метоксипурин-6-он), плавящийся при 266-267°О. При проведении опытов аналогичным образом с использованием в качестве исходного материала 8-аза-2-(5-хлорсульфонил-2-метоксифенил)-пурин-6-она, но с заменой этанольного метиламина соответствующими количествами следующих растворов: водный изопропил амин, 33%-ный; водный трет -бутиламин, 33%-ный; водный N -метил-изопропиламин, 40%-ный, получены 8-аза-2(5- N -изопропилсульфамоил-2-метоксифенил)урин-6-он, т.пл. 274-275°С (из водной ксусной кислоты); 8-аза-2-( 5- М-трет-бухилсульфамоил-2метоксифенил)-пурин-6-он, т.пл. 233-235°С (из водной уксусной кислоты); 8-аза-2-(5- N-изoпpoпил-N -метилсульамоил-2-метоксифенил)-пурин-6-он, т. пл. 223-225°С (очищенный путем растворения в горячем 2 н. растворе аммиака и осаждения концентрированной соляной кислотой); 8-аза-2- (5-хлорсульфонил-2-пропоксифенил)-пурин-6-он, используемый в качестве исходного материала, получают следующим образом: 5,0 г 8-аза-2-(2-пропоксифенил)пурин-6-он постепенно растворяют в 35 мл перемешиваемой хлорсульфокислоты при . Смесь выдерживают при этой температуре в течение 48 час и затем медленно прибавляют к 150 г льда при поддержании температуры от О до 5°С. Осадок отфильтровывают, тщательно промывают охлажденной льдом водой и сушат в эксикаторе. Выход продукта 6,0 г. При проведении опытов аналогичным образом из 8-аза-2-(2-метоксифенил)-пурин-6-она получают 8-aзa-2-(5-xлopcyльфoнил-2-мeтoкcифeнил)-пурин-6-ол. Пример 2. 8-аза-2-(5-N-бензилсульфамоил-2-пропоксифенил)-пурин-6-он. 3,7 г 8-аза-2-(5-хлорсульфонил-2-пропоксифенил)-пурин-6-она прибавляют к 5 мл перемешиваемого раствора бензиламина в 50 мл безводного этанола при комнатной температуре. Омесь перемешивают в течение 2 час при комнатной температуре и: нагревают при температуре кипения с обратным холодильником в течение часа. Омесь охлаждают, и твердый продукт отфильтровывают, перекристаллизовывают из метанола с применением дрэвесного угля и сушат при мм рт.ст. Выход продукта 2,74 г, т. пл. 150-151°О. 45 Пример 3. N - 3-(8-аза-6-оксопурин-2-ил)-4-пропоксибензосульфонил -морфолин. Омесь из 5О мл морфолина и 3,7 г 8-аза-2-(5-хлорсульфонил-2-пропоксифенил)50 -пурин-6-она перемешивают и нагревают в течение 90 мин при температуре кипения смеси с обратным холодильником. Избыток морфолина после этого удаляют в вакууме, остаток растворяют в горячем 2 н, раствоSU ре аммиака, нерастворимый материал отфильтровывают и раствор после этого подкисляют до рН, равной 1, при помощи концентрированной соляной кислоты. Осадившийся твердый продукт перекристаллизовывают 60 из этанола и сушат при 14О°О/10 мм рт.ст.
Выход продукта 2,28 г, т,пл. 248 - 249°С.
При проведении опытов аналогичным образом, но с заменой морфолина, употреблявшегося в качестве исходного материала, соответствующим количеством пиперидина, полу ч ают N - 3- (8- аз а- 6-оксопу ри н- 2-ил) -4-пропоксибензолсульфонил -пиперидин с т.пл 270-271-С (после перекристаллизапии из водного этанола).
Пример 4. 8-аза-2-(5-N-метил- N -фенилсульфамоил-2-пропоксифенил)-пурин-б-он.
2,5 г 8-аза-2-(5-хлорсульфонил-2-пропоксифенил)-пурин-6-она медленно прибавляют к раствору 1,5 г чистого N -метил- анилина в 5О мл безводного пиридина при О С. После перемешивания при этой температуре в течение 2 час смесь перемешивают еш.е 24 часа при комнатной температуре. ОсадиБшийся твердый материал отфильтровывают и перемешивают с соляной кислотой (2н., 50 мл) в течение часа. Полученный белый твердый продукт после этого перекристаллизовывают из водной уксусной кислоты и сушат при 140°С/10 мм рт.ст.
Выход продукта 1,2 г, т.пл. 250-251°С.
При проведении опыта аналогичным образом, используя вместо N -метиланилина соответствующее количество анилина, получают 8-аза-2-(5- Н-феш1Лсульфамоил-2-пропоксифенил)-пурин-6-он, т.пл. 253-254°С (после перекристаллизации из водной уксусной кислоты).
Пример 5. 8-a3a-2-L5-N-(2-мeтoкcифeнил)-cyльфaмoил-2-пpoпoкcифeнил -пypин-6-oн.
3,7 г 8-аза-2-(5-хлорсульфонил-2-про- поксифенил)-пурин-6-она суспендируют в 50 мл безводного пиридина и после этого обрабатывают 5,0 г орто-анизидина. Полученную смесь перемешивают и нагревают при 60°С в течение 24 час. Полученную смесь выпаривают в вакууме досуха и остаток обрабатывают соляной кислотой (2 н., 100 мл). После охлаждения льдом из масла постепенно начинает образовываться твердый продукт. Его растворяют в разбавленном растворе аммиака и рН доводят до 8 при помощи разбавленной соляной кислоты. После фильтрования рН фильтрата доводят до 1 при помощи концентрированной соляной кислоты. Полученный твердый продукт вновь обрабатывают аммиаком, а затем концентрированной соляной кислотой.
Выход продукта 0,65 г, т.пл. 139-142 При проведении опытов аналогичным образом, но с заменой орто-анизидина соответствующими количествами мета-, пара-анизидина и 3-трифторметиланилина получают:
8-аза-2- 5- N -( 3-метоксифенил)-сульфамоил-2-пропоксифенил -пурин-6-он, т. пл. 137-139°С, 8-аза-2- 5- N -(4-метоксифенил) -сульфамоил- 2-пропоксифенил -пурин-6-, -он, т.пл. 150-1520С и 8-a3a-2- 5-N-(3-трифторметилфенил)-сульфамоил-2-пропоксифенил -пурин-6-он, т.пл. 15О-152 - С, соответственно.
Пример 6. 8-аза-2-(5-N - N-дигексилсульфамоил- 2-пропоксифенил) -пурин-6-он.
3,7 г 8-аза-2-(5-хлорсульфонил-2-пропоксифенил)-пурин-6-она медленно прибавляют при перемешивании к раствору 30 мл дигексиламина в 30 мл этанола. Смесь перемешивают в течение 24 час при комнатной температуре и после этого этанол удаляют в вакууме. Образовавшееся масло после этого разбавляют петролейным эфиром (т.кип. 4О-60 С, 250 мл), осадившиеся твердые вещества отфильтровывают и промывают дополнительным количеством петролейного эфира. Эти твердые вещества растворяют в водном растворе гидроокиси натрия (2н.) и раствор экстрагируют петролейным эфиром. Водный слой после этого подкисляют до рН 1, при помощи концентрированной соляной кислоты и полученную суспензию встряхивают с хлороформом (100 мл). Твердые вещества отфильтровывают, органический слой отделяют, промывают водой и сушат над сульфатом натрия. После удаления хлороформа получают масло, которое затем переходит в твердое состояние, и подвергают перекристаллизации из воднпго- этанола. Выход продукта 0,9 г, т. пл. 126,5-128,5°С.
Пример 7. 8-aзa-2-(4-мeтил-5-N-мeтилcyльфaмoил-2-пpoпoкcифeнил)-пypин-6-oн.
7,7 г 8-аза-2-5-(хлорсз льфонил-4-метил-2-пропоксифенил)-пурин-6-она медленно прибавляют к перемещиваемому раствору метиламина в этаноле (18О мл, 33%-ный), затем смесь перемешивают в течение 210 мин при комнатной температуре и нагревают на паровой бане Б течение 1О мин. Раствор выпаривают досуха, остаток суспендируют в воде и прибавляют водный раствор метиламина (40%-ный) до образования прозрачного раствора. После этого раствор обрабатывают древесным углем, фильтруют, охлаждают льдом и подкисляют до рН 1 при помощи концентрированной соляной кислоты. Образовавшийся светло-желтый продукт отфильтровывают, промывают водой и перекристаллизовывают из изопропанола. Выход 6,78г. 60 т.пл. 254-257°С (разложение). При проведении опытов аналогичным образом, но с заменой этанольного раствора метиламина следующими растворами: этанольным раствором диметиламина (25%-ный;; водным раствором аммиака (уд. в.0,880) и водным раствором трет-бутиламина (33%ный), получают: 8-аза-2-(4-метил-5- N, N-диметилсульфамоил-2-пропоксифенил) -пурин-6-он, т.пл. 256-2570С; 8- чза-2- (4-метил- 2-пропокси- 5-сульфамоилфенил)-пурин-6-он, т.пл. 299-ЗОО°С (разложение); 8-аза-2-(5- N -трет-бутилсульфамоил-4-метил- 2-пропоксифенил) -пурин- 6-он, т. пл. 233-235°С. Используемый в качестве исходного материала 8-аза-2-(5-хлорсульфонил-4-метил-2-пропоксифенил)-пурин-6-он получают следующим образом: 28,5 г 8-аза-2-(4-ме тил-2-пропоксифенил)-пурин-6-она растворяют при перемешивании в хлорсульфокислоте (150 мл) при и выдерживают при этой температуре в герметизированном сосу де в течение 40 час. Затем эту смесь осто рожно прибавляют к смеси льда с водой (5ОО мл) при внешнем охлаждении с тем, чтобы температура была не выше З-С. После перемешивания в течение Ю мин продук отфильтровывают, промывают водой и сушат в вакууме над пятиокисью фосфора. Выход продукта 32 г. 8-аза-2-(4-Метил-2-пропоксифенил)-пурин-6-он (т.пл. 213-215°С) получают из 4-метилсалицил амида. 4-Метилсалициламид с т.пл. 184-186°С получают из метилового эфира 4-метилсалидиловой кислоты. Пример 8. 8-аза-2-(5-Н-этил-N -изопропилсульфамоил- 2-пропоксифенил) -пурин-6-он. Смесь, состоящую из 1,85 г 8-аза-2- (5-хлорсульфоНИЛ-2-пропоксифенил)-пурин-6-она, 0,87 г Vi-этил-изопропил-амина и 1,О7 г 1,8-бис-(диметиламино)-нафталина в безводном сульфолане (15 мл) перемешивают и нагревают в течение ночи при 60°С. После этого смесь охлаждают и прибавляют к 100 мл 25%-ной соляной кислоты. Осадившиеся твердые продукты отфильт ровывают, промывают водой и перемешиваю с водным раствором карбоната натрия (1 н 10О мл) в течение 1О мин. После отфильт ровывания фильтрат подкисляют концентриро ванной соляной кислотой, а осадок.тшательно промывают сначала кипящей водой, а затем холодной. Твердый продукт растворяют в 2 н. водном растворе гидроокиси натрия и раствор промывают петролейным эфиром. Водный слой подкисляют соляной кислотой, осадок экстрагируют этилацетатом, экстракт промывают водой, сушат и выпаривают. Затем остаток растворяют в водном растворе аммиака, осаждают путем обработки соляной кислотой, перекристаллизовывают из водной уксусной кислоты. Выход продукта 0,17 г, т. пл. 154-157°С. При проведении опытов аналогичным образом, используя вместо N-этилизопропиламина W -втор-бутилметиламин, получают 8-аза-2-(5- N -втор-бутил- М у етилсульфамоил-2-пропоксифенил)-пурин-6-он; т. пл. 224°С (из изопропанола). Пример 9. 8-аза-2-(5-N-изoпpoпилcyльфaмoил-2-пpoпoкcифeнил)-пypин6-oн. 3,7 г 8-аза-2-(5-хлорсульфонил-2-пропоксифенил)-пурин-6-он прибавляют при охлаждении и перемешивании к 50 мл 30%ного изопропиламина. Смесь перемешивают в течение 3 час при комнатной температуре и выпаривают при пониженном давлении. Остаток суспендируют в воде (5О мл), прибавляют изопропиламин (5 мл), и смесь нагревают на паровой бане до получения раствора. Раствор подкисляют концентрированной соляной кислотой, и осадившийся твердый продукт отфильтровывают, промывают водой, сушат и перекристаллизовывают из водной уксусной кислоты; т.пл. 272274°С (разложение). Выход 2,0г. Пример 10. 8-аза-2- 5-М-(2,6-диметилфенил)-сульфамоил-2-пропоксифенил -пурин-6-он. 2,5 г 2,6-диметиланилина прибавляют к перемешиваемой суспензии 1,85 г 8-аза-2- - ( 5-хлорсульфонил-2-пропоксифенил)-пурин-6-она в 4О мл безводного пиридина. Смесь перемешивают и нагревают при температуре кипения с обратным холодильником в течение 20 час. После этого растворитель удаляют в вакууме, остаток обрабатывают соляной кислотой (2 н., 100 мл) и нагревают при перемешивании на паровой бане в течение 5 мин. После охлаждения выделившаяся смола постепенно превращается в твердый продукт, который кристаллизуют с древесным углем из изопропанола. Выход продукта 1,04 г; т.пл. 240 2420С. Пример 11. 8-аза-2- 5-N-(4-xлopфeнил)-cyльфaмoил-2-пpoпoкcифeнилЗ-пypин-6-oн. Смесь, состоящую из 1,85 г 8-аза-2- (5-хлорсульфонил-2-пропоксифенил)-пурин-6-она, 1,28 г 4-хлоранилина и 1,07 г 1,8-бис-(диметиламино)-нафталина в безводном сульфолане (10 мл) перемешивают и нагревают при 11О-115°С в течение 2О час.





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 8-азапуринона-6 | 1971 |
|
SU439981A1 |
| Способ получения -(аминофенил)алифатических карбоновых кислот | 1970 |
|
SU442594A1 |
| Способ получения производных 2-окси-3-аминопропана или их -окисей или солей | 1974 |
|
SU659089A3 |
| Способ получения производных диазепина | 1973 |
|
SU520918A3 |
| Способ получения производных бензодиазепина | 1971 |
|
SU520917A3 |
| ПИРАЗОЛОПИРИМИДИНОНОВЫЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ | 1991 |
|
RU2114114C1 |
| Способ получения производных -фенилжирной кислоты | 1971 |
|
SU530635A3 |
| Способ получения 4-фениловых эфиров 3-амино-5 сульфамоилбензойных кислот | 1973 |
|
SU523635A3 |
| ПИРАЗОЛОПИРИМИДИНОНЫ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ИНГИБИРОВАНИЯ ФОСФОДИЭСТЕРАЗЫ ЦИКЛИЧЕСКОГО ГУАНОЗИН-3',5'-МОНОФОСФАТА | 1992 |
|
RU2114113C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПИРАЗОЛОПИРИМИДИНОВЫХ СОЕДИНЕНИЙ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ | 1991 |
|
RU2047617C1 |


Авторы
Даты
1976-08-25—Публикация
1974-06-11—Подача