Таблица 1
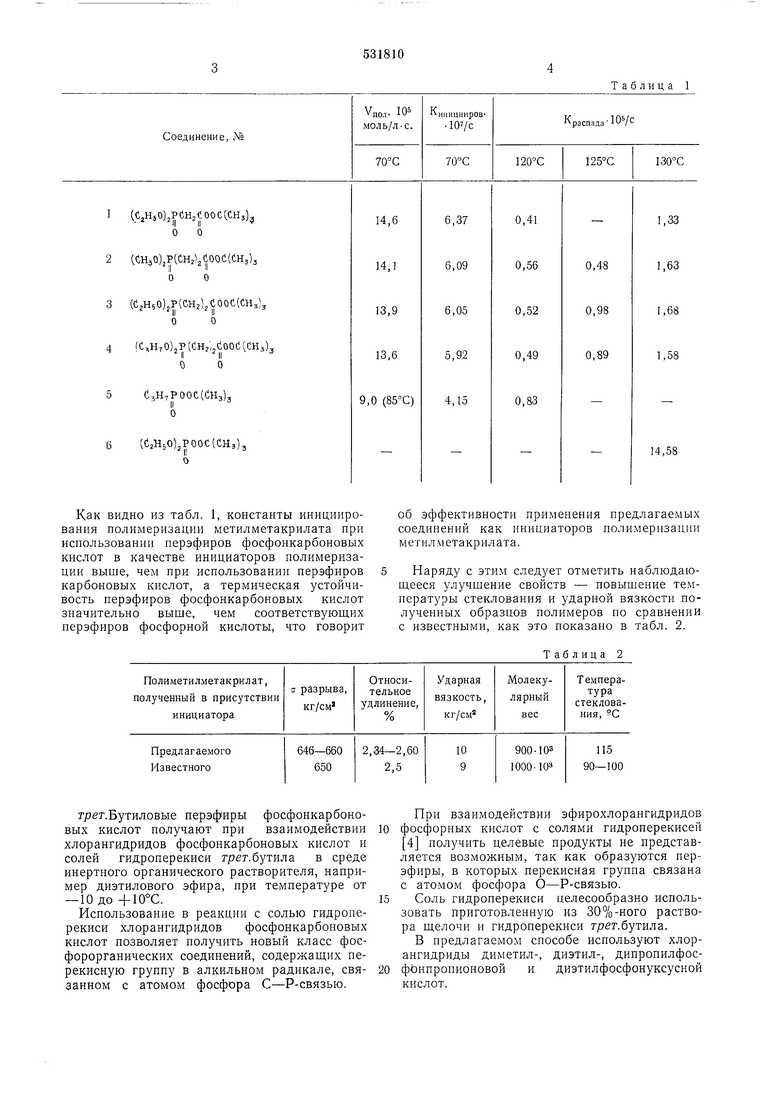



Как видно из табл. 1, константы инициирования полимеризации метилметакрилата при использовании перэфиров фосфонкарбоновых кислот в качестве инициаторов полимеризации выше, чем при использовании перэфиров карбоновых кислот, а термическая устойчивость перэфиров фосфонкарбоновых кислот значительно выше, чем соответствуюш,их перэфиров фосфорной кислоты, что говорит
грет.Бутиловые перэфиры фосфонкарбоновых кислот получают при взаимодействии хлорангидридов фосфонкарбоновых кислот и солей гидроперекиси грет.бутила в среде инертного органического растворителя, например диэтилового эфира, при температуре от - 10 до .
Использование в реакции с солью гидроперекиси хлорангидридов фосфонкарбоновых кислот позволяет получить новый класс фосфорорганических соединений, содержащих перекисную группу в алкнльном радикале, связанном с атомом фосфора С-Р-связью.
об эффективности применения предлагаемых соединений как инициаторов полимеризации метилметакрилата.
Наряду с этим следует отметить наблюдаюш.ееся улучшение свойств - повышение температуры стеклования и ударной вязкости полученных образцов полимеров по сравнении с известными, как это показано в табл. 2.
Таблица 2
При взаимодействии эфирохлорангидридов фосфорных кислот с солями гидроперекисей 4 получить целевые продукты не представляется возможным, так как образуются перэфиры, в которых перекисная группа связана с атомом фосфора О-Р-связью. Соль гидроперекиси целесообразно использовать приготовленную из 30%-ного раствора ш,елочи и гидроперекиси т/зет.бутила.
В предлагаемом способе используют хлорангидриды диметил-, ДИЭТИЛ-, дипропилфосфЪнпропионовой и диэтилфосфонуксусной кислот.
Для улучшения протекания процесса взаимодействия исходных веществ его ведут в инертном органическом растворителе, например в диэтиловом эфире.
Пример 1. Получение трег. бутилового перэфира р-диэтилфосфонпропионовой кислоты.
К 12 мл 30%-ного водного раствора едкого кали приливают по каплям 5,4 г (0,06 моля) гидроперекиси грет.бутила при 0-|-5°С при интенсивном перемешивании. Затем добавляют 50 мл диэтилового эфира и при температуре О-5°С прибавляют по каплям 14 г хлорангидрида р-диэтилфосфонпропионовой кислоты (0,06 моля). После прибавления хлорангидрида реакционную массу перемешивают еще 15 мин, затем медленно поднимают температуру до . Реакционную массу промывают раствором бикарбоната натрия и водой до нейтральной реакции. Эфирный слой сушат над безводным сульфатом магния. Растворитель удаляют в вакууме и иерэфир хроматографируют в среде эфир : этиловый спирт 20 : 0,5 на силикагеле.
Rf 0,49. Полученная нерекись - малоподвижная бесцветная жидкость, 1,4328; df 1,0807; мол. вес. вычисл. 282; мол. вес. найд. 275; MRn 67,7; найдено 67,9.
Найдено, %: С 46,86; Н 8,01; Р 10,76; . 5,69.
СпН2зОбР.
Вычислено, %: С 46,83; Н 8,15; Р 10,85;
Оакт. 5,67.
Пример 2. Получение грег.бутилового перэфира р-диметилфосфонпропионовой кислоты.
К 24 мл 30%-ного водного раствора едкого кали приливают по каплям 10,8 г гидроперекиси грет.бутила (0,12 моля) ири О-5°С,при перемешивании. Затем добавляют 50 мл диэтилового эфира и при этой же температуре приливают осторожно 11,6 г (0,12 моля) хлорангидрида р-диметилфосфонпропионовой кислоты. Реакционную смесь промывают раствором бикарбоната натрия и водой до нейтральной реакции, эфирный слой сушат над безводным сульфатом магния. Растворитель удаляют в вакууме. Перекись хроматографпруют в среде эфир : этиловый сиирт (20 : 0,5) на силикагеле. Rf 0,47.
Полученный перэфир - малоподвижная бесцветная жидкость.
Выход 50%. 1,4371; 1,1277; мол. вес. вычпсл. 254; мол. вес. найд. 249,7 MRo 58,5;
Пайдено 59,0.
Пайдено, %: С 42,81; П 7,29; Р 12,31; Оакт. 6,28.
СдНшОбОР.
Вычислено, %: С 42,52; П 7,48; Р 12,20; Оант. 6,29.
П Р и м ер 3. Получение трет.бутилового перэфира диэтилфосфонуксусной кислоты.
К 24 мл 30%-ного водного раствора едкого кали прикапывают 10,8 г (0,12 моля) гидроперекиси грег.бутила прп температуре О-5°С и перемешивании. Добавляют 50 мл диэтплового эфпра П при этой температуре прил1шают по каплям 11,6 г (0,12 моля) хлорангид5 рнда диэтилфосфонуксусной кислоты. Полученный раствор перекиси в эфире промывают раствором бикарбоната натрия и водой до нейтральной реакции. Эфирный слой сушат над безводным сульфатом магния.
0 Растворнтель отгоняют в вакууме. Перэфир хроматографируют в среде эфир : этиловый сиирт 20 : 0,5 на силикагеле Rj 0,39.
Полученный продукт - малоподвижная бесцветная жидкость.
5 Выход 60%. 4° 1,4311; d 1,1786; мол. вес. вычисл. 268; Мол. вес. найд. 264; MRn 58,81; Найдено 58,94;
Найдено, %; С 44,77; Н 8,21; Р 11,72; Оакт 6,01.
0 CioHgiOeP.
Вычислено, %: С 44,53; Н 8,35; Р 11,56;
Оакт. 5,97.
Аналогично получают грег.бутиловый перэфир р-дипропплфосфонпропионовой кнсло5 ты. Выход 71%; 14358; d 1,0638; мол. вес. вычисл. 310. Мол. вес. иайд. 308; MRn 76,9; найд. 77,1.
Для определения инициирующих свойств указанных веществ проводят полимеризацию метплметакрплата в запаянных ампулах, предварительно продутых аргоном п вакуумпрованных при мм рт. ст. Скорость полпмеризацпп измеряют по усадке мономера с HOMOHibFO катетометра. В табл. 1 приведены константы инициирования (Km,) и константы раснада (Красп) при различиых темнературах для различных предлагаемых 1-4 и известных 5 и 6 соединений.
Формула изобретения
№о),р;сн,)„соос(снз)з , о о
где R алкил Ci-Сз., п 1 или 2, проявляющие ин1щиирующне свойства при полимеризации JмeтI лмeтaкpплaтa. 2. Способ получения соединеннй по п. 1, отличающийся тем, что взаимодействию подвергают хлорангидриды диалкилфосфонкарбоновых кислот и соли гидроиерекиси трег.бутила в среде инертного органического растворителя, например диэтилового эфира, при температуре от -10 до +10°С.
Источники информации, принятые во внимание при экспертизе:

Авторы
Даты
1976-10-15—Публикация
1974-06-27—Подача