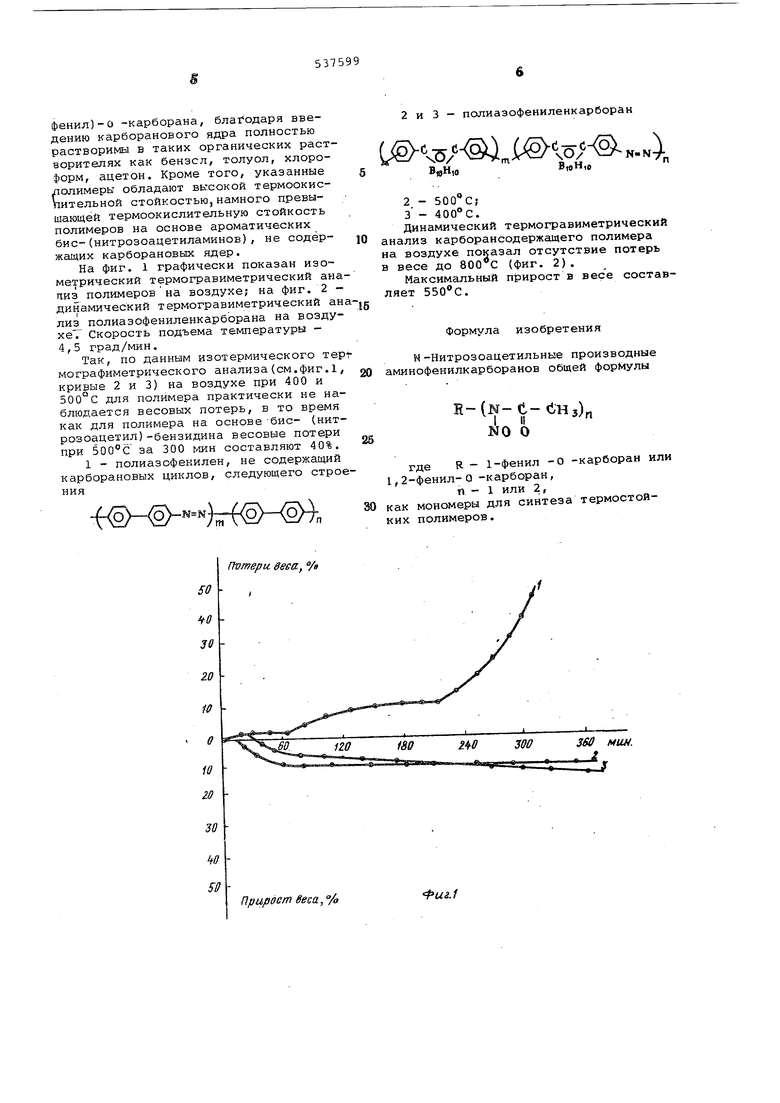
Вследствие нестабильности N -нитроз оацетильных производных аминофенил карборанов при комнатных температурах невозможно идентифицировать зти соединения методами элементного анаииза и ИК-спектроскопии. Поэтому иден тификацию N -нитрозоацетильных производных аминофенилкарборанов проводили по вьщелению азота при . Во вс случаях количество выделившегося азота соответствовало теоретическому соцержс нию азота в Ы -нитроэоацехнльных производных аминофенилкарборанов Для лучшего понимания данного кзоб ретения. приводятся следующие примеры получения 1 С N -нитрозоацетиламинофенил) -карборана и 1,2- бис--(Н -ни розоацетиламинофенил)- о -карборана, Пример 1, В 300 мл смеси ледяной уксусной кислоты и уксусного ан гидрида () при вносят 6 г (0,02 моль) I- (N ацетиламлнофенил) - о -карборана и перегдешивают до полного его растворения. Затем при nepeiv шивании барботируют через раствор оки азота со скоростью 20-30 мл/мкн в течение 6 ч« После этого раствор выливают при перемешивании в 2 л воды со льдом, Выпавашй осадок отфильтровывают, промывают на фильтре холодной водой и высушивают под вакуумом, при охлаждении от О до -10 С .. Получают 5,6 г (75%) 1-(М-нитрозРацетиламинофекил)- О -карборана, Выделилось из О,-30 г при 50С з бе золе 21,3 мл азота,- что составляет 99,5% от теории., П р и м е р 2. В 300 мл смеси уксусной кислоты и уксусного ангидрида (312 по объему) при вносят б г (0,02 моль) 1(N -ацеткламинофани.л} -О -карборана и перемешивают до полного его растворения Затем постепенно прибавляют к раствору 6г (0,05 мол нитрозилсерной кислоты и продолжают перемешивать еще 2 ч при 4°С, После. этого раствор выливают при перемегливании в 2 л воды со льдом. Выпавший желтый осадок отфильтровывают, промывают колодной водой м высушивают под вакуумом при охлаждении от О до --10° С Получают 6,3 г (85%) 1(N -нитрозоацетиламинофенил) - О --карборана.. При м ер Зо В 20О мл смеси уксусной кислоты и уксусного ангидрида (Isl по объему) при 4°С вносят 5 г (0,017 моль) 1-(N -ацетиламинофенил) -О -кардорана и перемешиваЕот до пол ного его растворения Затем постепенно прибавляют к раствору 1,3 г (0,02 моль) хлористого нитрозила ., растворенного в 5 мл уксусного ангидрида и продолжают перемешивание н течение 2 ч, После этого раствор выливают в 2 л воды со льдом, .ий желтый осадок отфильтровывают, npONibiвают холодной водой и высушив.ают под вакуумом при охлаждении (от О до ) Получают 4,9 г (80%) 1-(N -нитрозоацетиламинофенил)-о -карборана, П р и м е р 4. При действии 10 г (0,1 моль) уксусного ангидрида на |.0 г (0,03 моль) 1,2-бис-(аминофенил)-о карборана в 180 мл метилового спирта при 30-40 С получают 11,8 г (96%) (М -ацетиламинофенил)-| -карборана. Найдено, %s С 52,84; Н 6,25; В 26,12; Ы 6,23, Вычислено, %s С 52,63; Н 6,39; B 26, 38 N б,80. Аналогично примеру 1 из 4 г(Of0.l2 моль) 1,2-бис- ( W-ацетиламинофенил)0 -карборана получают 3.-12 г (70%) 1, (Н -нитрозоацетила-Минофенил)-0 -карборана. Выде-ли.пось из 0,23 г при 50°С в бэнзоле 22 fl мл азота (н.у,), что составляет .00% от теорр1и. Примерз, Аналогично примеру 2 из 4 г (0,012 моль) 1,-2-бис( 4 -ацети.ламинофенил) - о -карборана, полученного как указано в примере 4,- и 6 г (0,05 моль) нитрозилсерной кислоты получают 3,.,6 г 1,2-бис (N -нитрозоацетилaJvшнoфeнил) -о -карборана Примере Аналогично примеру 3 из 4 г (0,012 моль) 1,2-бис-(М -ацети.ламинофенил) О -карборана, получен™ ного как указано в примере 4, и 2,0 г (0,03 моль) хлористого нитрозила, растворенного в 7,5 мл и уксусного ангидрида , п ол уч ают 3 J 7 г (80%) 1, 2-бис-(f-4 -нитрозоа.цетиламинофенил) - О карборана„ . Н Нитрозоадетильные пpoизвo :; ныe аминофенклкарборанов представляют собой соединения, в которых ароматическое кольцо связано с карборановым ядром Такие соединения могут быть использованы в качестве мономеров для синтеза карборансодержащих термостойких по.лимеров, в качестве вулканизующих агентов для эластомеров, содержащих двойные связи, в качестве сомономеров для введения карборановых ядер в макромолекулы полимеров, получаемых ПС радикальному механизму, в качестве инициаторов радикальной полимеризации, а также для других целей. Полимеры общей формулы i{o) ( олучае1 Гс1е путем взаимодействия проуктов распада ароматических бис--(нитэозоацетиламино) , обладают ограниченой рэ.створимостью, не превышающей 16% в бензоле и невысокой термостойостью. Полимеры общей формулыр получаеые ггутем Е;зэимодействия продуктов аспада бис-(М -нитрозоацетиламинофенил)-О -карборана, блат одаря введению карборанового ядра полностью растворимы в таких органических растворителях как бензол, толуол, хлороформ, ацетон. Кроме того, указанные лолимерк обладают высокой термоокиспительной стойкостью,намного превышающей термоокислительную стойкость полимеров на основе ароматических бис-(нитрозоацетиламинов), не содёржащих карборановых ядер. На фиг. 1 графически показан изометрический термогравиметрический ана пиз полимеровна воздухе; на фиг. 2 - динамический термогравиметрический ан ЛИЗ полиазофениленкарборана на воздухе. Скорость подъема температуры - 4,5 град/мин. Так, по данным изотермического тер мографиметрического анализа(см.фиг.1, кривые 2 и 3) на воздухе при 400 и 500 С для полимера практически не наблюдается весовых потерь, в то время как для полимера на основе -бис- (нитрозоацетил)-бензидина весовые потери при 500°С за 300 шн составляют 40%. 1 - полиазофенилен, не содержащий карборановых циклов, следующего строе ния
nvmeptt веса, %
Прирост веса, %
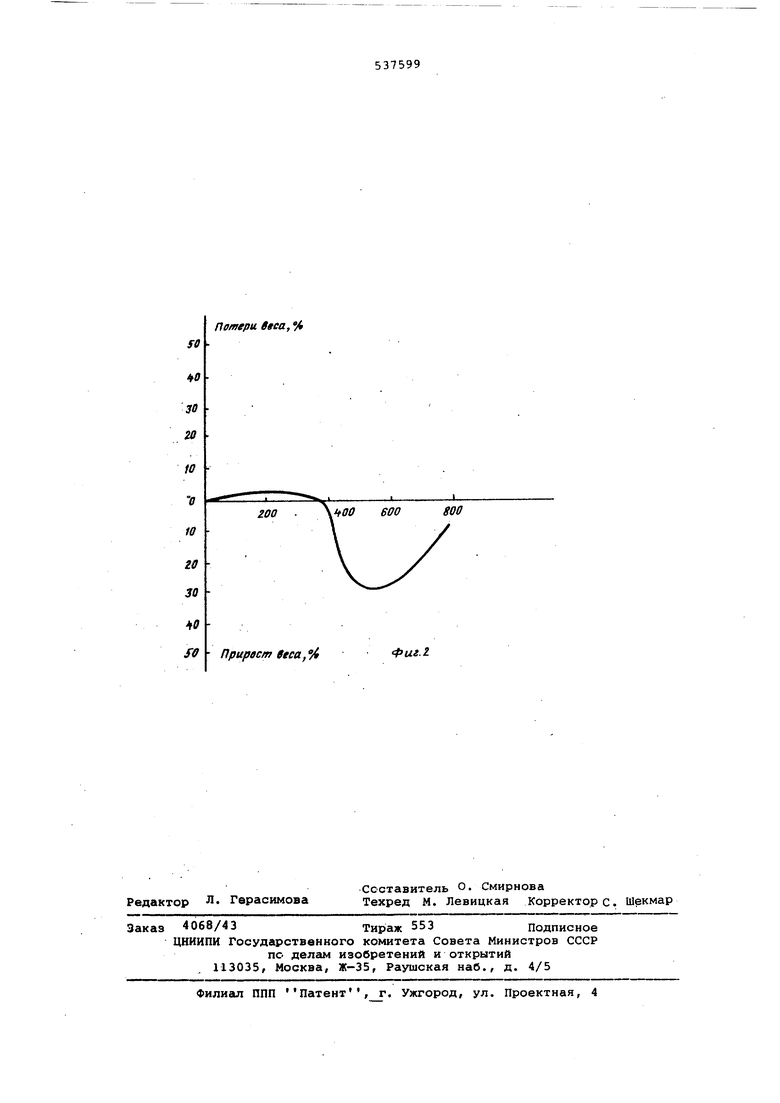
Pus.1 2 и 3 - полиазофениленкарборан .м), . П 2 - З - 400° С. Динамический термогравиметрический лиз карборансодержащего полимера воздухе показал отсутствие потерь есе до (фиг. 2). Максимальный прирост в весе составт . Формула изобретения N-Нитрозоацетильные производные нофенилкарборанов общей формулы R(N-C(iH3)n N0 О где R - 1-фенил -О -карборан или -фенил-а -карборан, п - 1 или 2, мономеры для синтеза термостойполимеров.
Потери веса, %
Прирост веса, 4
Фиг. I

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения карборансодержащих ацетофенов | 1975 |
|
SU526622A1 |
| Карборансодержащие имиды фенолфталеина для синтеза полимеров и способ их получения | 1975 |
|
SU533597A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЗОТСОДЕРЖАЩИХ ЦИКЛОЦЕПНЫХ ПОЛИМЕРОВ | 1974 |
|
SU401160A1 |
| Способ получения карборансодержащих полиамидов | 1976 |
|
SU539907A1 |
| Способ получения карбонилпропионовой кислоты или ее замещенных | 1978 |
|
SU740782A1 |
| Способ получения полифениленов | 1977 |
|
SU663697A1 |
| Способ получения карборансодержащих нитрилов | 1973 |
|
SU476271A1 |
| Карборансодержащие алифатические нитрилы как промежуточный продукт в синтезе карборанилпропионовой кислоты | 1978 |
|
SU732267A1 |
| Способ получения карборансодержащих полиамидов | 1976 |
|
SU619492A1 |
| Способ получения полибензоксазолов | 1973 |
|
SU447928A1 |



Авторы
Даты
1977-10-05—Публикация
1975-04-09—Подача