(54) СПОСОБ ПОЛУЧЕНИЯ УРЕТАНОВ оксимегилен, димегиленсульфон или осгаго диме тиленке гона, jR может представлять собой алкил, цик лоалкил, алкилен, циклоалкилен или аралкил который может содержать в цепи атом кислорода, азота или серы, сульфоксидную, сул фоновую, аминную, амидную, карбонильную или циклокарбоксильную эфирную группы. Кро ме того, R может быть замещен на алкил, арил, алкоксил или арилоксил не менее чем с 10 атомами углерода, Чаще всего из спиртов применяют метиловый, этиловый, н- и втор-пропиловый, низо- и трет-бутиловый, амиловый, гексило- вый, лауриловйй, цетиловый, бензиловый, хлорбенэиловый, метоксибензиловый спирты, этилекн-, диэтилен-, пропилен- и дипропи/tенгликоль, глидерол, триметилолпропан, гексантриол, пентаэритритол, а также сложные эфиры полиолов, у которых по крайней мере одна гидроксильная группа остается неэтерифицированной, Этерифицированная группа в таких эфироспиртах обычно содержит до 10 атомов углерода и представляет собой предпочтительно алкил, циклоалкил или apajt кил, который может быть замещен, на гало ид. Фенолы могут содержать в бензоидных кольцах заместители, например алкил или алкоксил с 1-10 атомами углерода и галоид. Из используемых моно- и полиатомных фенолов могут быть названы фенол, хлори алкилфенолы, катехин, резорцин, гидрохинон, 4,4-дигидроксидифенилметан, нафтолы, хлор-, метил-, эти., бутил- и октилнафтолы, антранолы, , метил-, этил-, бути№ и октилантранолы, фенантролы, хлор-, мети№-, эти№-, бутил и октилфенантролы, пирогаллол, флороглюцин и простые эфиры поли- гидроксифенолов, при условии, что по Kpai ней мере одна гидроксильная группа являет ся неэтерифицированной, Этерифицирующаяся группа в таких эфирах обычно содержит до 10 атомов углерода и представляет собой предпочтительно алкил, циклоалкил или apaj кил, который может быть замещен, например на галоид. Примером азотсодержащих соединений могут служить соединения, содержащие по край ней мере одну нециклическую группу, в которой атом азота непосредственно соединен с одним атомом углерода и через двойную связь с атомом кислорода или другим атомом азота. Такие сое-динейий включают органические нитро-, нитрозо-, азо- и азокс№соединения, содержащие до 24 атомов углерода, предпочтительно нитроароматические и третичные нитроалифатические соединения. В качестве нитросоединений используют мононитросоединения, такие, как нитробев зол, алкил- и алкоксйнитробензолы, в которых атжил содержит 1-1О атомов углерода,, арил- и арилоксинитробенаолы, в которых арил представляет собой незамещенные или замещенные на хлор фенил, толил, ксилил, нафтил, хлорнитробензолыг динитросоединения, такие, как о-, м- и п-динитробензолы, алкил- и алкоксидинитробензолы, хлординитробензолы, тринитросоединения, такие, как тринитробензол, алкил-, алкокс№-, арил- и арилокситринитробензолы, хлортринитробензолы, моно- и полинитропроизводные нафталина, дифенила, дифенилметана, антрацена и фенантрена. Замещенные или незамещенные алифа.тические нитросоединения, такие, как мононитропроизводные метана,этана, пропана, бутана, циклопентана, циклогексана, циклобутана, октадекана, 2,2 диметилнитробутан, 3-ме- тилнитробутан, З-нитропропен-1, фенилнитрометан, п бром-, п-нитро и п-метоксифе- нилнитрометан, динитропроизводные этана, пропана, бутанае гексана, декана, циклогек- сана, метилциклогексана, ди-(нитроцикло- гексил)-мета -, также могут быть испольгзованы. Однако при использовании первичных, вторичных и циклоалифатических соединений выход уретанов снижается. Из ароматических нитросоединений лучше всего брать нитробензол, нитротолуол, динитробе№зол, динитротолуол, тринитробензол, 4,4- -динитродифенилметан, п-нигроанизол, п- и о-нитроэтоксибензол, 2,4-динитроанизол, 2,4-динитроэтоксибензол, 3,5-динитробенгзилацетат, 1-хлор 2,4-диметокс№-5-нитробензол, 1,4-диметокси-2-нитробензол, п-нитрофенилнитрометан и третичные алифатические нитросоединения, такие, как 2-метил-2-нитропропан и 1-метил-1-нитроциклогексан. Наиболее предпочтительно применение 2,4-, 2,5- и 2,6-динитротолуолов, м- и п-динитробензолов и 4,4-динитродифенилметана. Из нитросоединений можно назвать монои динитрозопроизводные бензола и толуола, нитрозобутан, нитрозоциклогексан и дини1 розометилциклогексан. В качестве азосоединений могут быть спользованы соединения общей формулы , где R, и R, одинакоые или различные незамещенные или замеенные алкилы или арилы, например азобенол, нитрозобензол, хлоразобензол, алкил- или рилзамещанные азобензолы. Из азоксисоединений общей формулы (0)K как укаано выше, наиболее предпочтительны азок- сибен ол, нитро- и хлоразоксибенаол, алкил или арилзамещенные азоксибензолы. Для получения уреганов можно исноль зевать смеси нитро-, нитрозо-, азо- или азоксисоединений со смесью гидроксилсодер жащих соединений, а также соединения, содержашие обе функциональные группы, т.е. гидроксинитро-, гидроксинитрозо-, гидрокси- азо- и гидроксиазоксисоединения, такие, как 2-гидроксинтроэтан, 2.пидроксинитрозоэтан, нитробензолы, нитрозофенолы, нит- ро- и нитрозонафтолы, гидроксиазо- и гидроксиазоксибензолыОднако самый высокий выход уретанов наблюдается при использовании нитросоединений. В качестве катализатора можно прим&нять металлический селен, особенно в виде порошка, и его производные, например двуокись и трехокись селена, смеси окислов селена, хлорокись селена, дисел.енид титана дисульфид селена, селениты натрия и цинка, селениды цинка и вольфрама, сульфид селена, селеновую кислоту, димети№-, диэтил-, дифенилселенид, диэтилдиселенид, карбони; селенид, диэтилполиселенид, дибутилполиселенид; элементарную серу и. ее производные например сероводород, сероокись углерода, сероуглерод сульфиды натрия и калия, двухлористую серу, полисульфиды, меркаптаны, тиоэфиры, содержащие до 20 атомов угл&рода, или их смеси. Катализатор можно использовать самостоятельно или наносить его на инертный носитель, такой, как окись алюминия, двуокись кремния, уголь, сульфат бария, карбо нат кальция, асбесты, бентонит, инфузорная земля, фуллерова земля, органические ионообменные смолы. В качестве основания обычно применяют органические основания, например триэтил- амин, пиридин, хинолин, N , N -диметил анилин, диэтиламин, трег-бутиламин, 1,4-ди азобицикло-(2,2,2)-октан, N, N , N , N,
-тетраметилэтилендиамин, гетраметилендиамин, этилендиамин, поливинилпиридин, и соли металлов карбоновых, сульфоновых и фосфорных кислот, например ацетаты лития, натрия, калия, кальция, палладия и рутения, п-толуолсульфонаты, метилсульфонаты, кислые фосфаты, бораты лития, формиаты натрия и лития, триацетат сурьмы. Перечисленные соли могут быть непосредственно введены в реакционную смесь или получены из соответствующих реагентов в ходе опыта.
Реакцию можно проводить и без использования основания в присутствии только воды. Однако целесообразнее использовать основание в сочетании с водой.
ход реакции.
Количество окиси углерода обычно составляет 3-50, предпочтительно 8-15 моль, на нециклическую группу, в которой атом азота азотсодержащего соединения непосредственно соединен с одним атомом углерода и через двойную связь с атомом кислорода или другим атомом азота. Окись углерода можно подавать в реактор непрерывно или периодически. При непрерывном введении окиси углерода и рециркуляции непрореагировавшей окиси углерода расход последней значительно снижается.
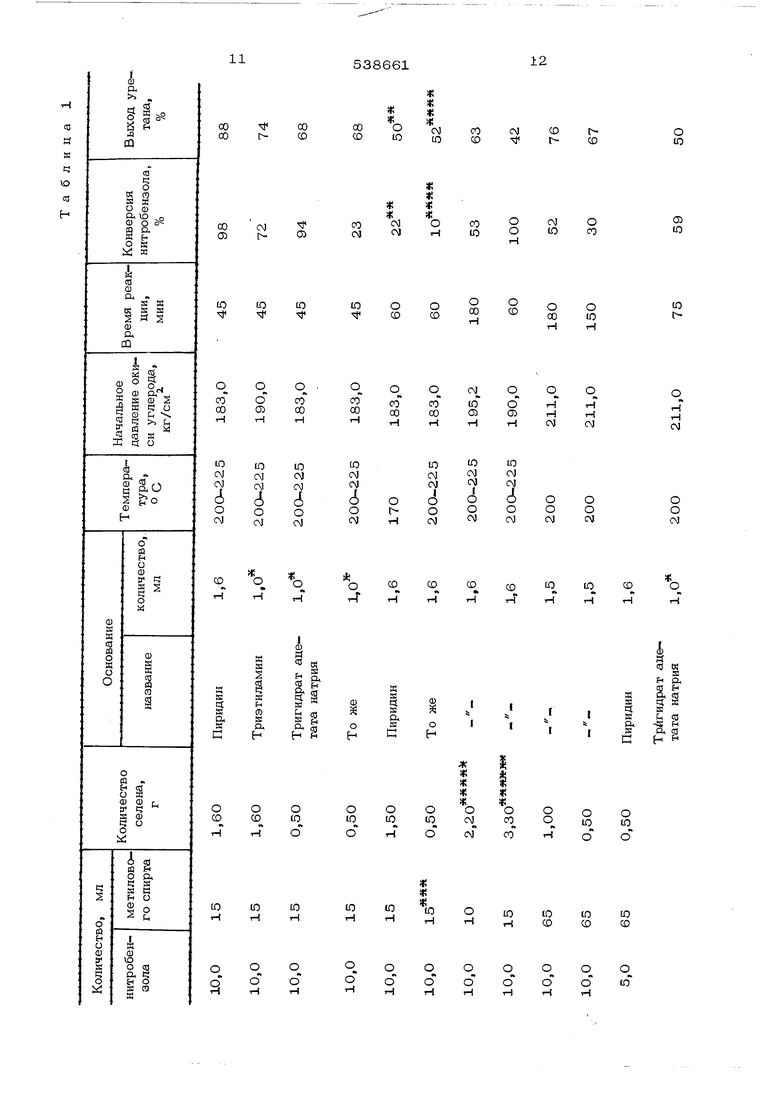
Температура реакции 100-2ОО С, давление окиси углерода 1О-1ОО ата. При более Процесс можно проводить в присутствии растворителя, такого, как бензол, толуол, ксилол, ацето- и бензонитрил; N , N - -диметилформамид и N , N -диметилацетамид; диметилсульфоксид; 1,1,2-трихлор-1,2,2-трифторэтан; моно-, ди и трихлорбен- зол; тетрагидрофуран (ТГФ), 1,4-диоксан, 1,2-диме токсиэ та н. При повышенных температуре и давлении можно осуществлять реакцию в среде инертного разбавителя, например алифатического или ароматического углеводорода, такого, как н-пентан, толуол, простые и сложные эфиры, кетоны. Молярное соотношение менщу катализатором и азотсодержашим органическим соединением составляет 1:1О - 1:1000. При определении молярного соотношения исходят из содержания элементарного селена или серы и активных аэотсодеришщих групп, например ни грогрупи. Молярное соотношение между азотсодержащим соединением и основанием равно 50:1 - 1:10, а между водой и катализатором 0,5:1 - 1000:1, предпочтительно 1; 1 - 200:1, При температуре реакции больше можно использовать только воду без основания. При более низких температурах применение основания в сочетании с минимальными количествами воды для достижения высокого выхода целевых продуктов необходимо. Вода, необходимая для проведения реакции, может выделиться при получеНИИ соли, используемой в качестве основания, из соответствующих кислоты и гидрата окиси металла, В ходе реакции наряду с уретанами может образоваться некоторое количество побочных продуктов, в основном аминов, особенно при использовании серного катализатора и/или большего количества воды. Порядок смещения реагентов зависит от конструктивных особенностей применяемого оборудования и не влияет существенно на высокой температуре возможно разложение исходных или образующихся веществ, Процесс получения уретанов, протекающий в маСсе, можно осуществлять полунепрерывным или непрерЫБН-Ым способом Для непрерывного способа особенно подходящими являются катализаторы ионообменного типа, Время реакции зависит от природы реагирующих веществ, температуры, давления, ти па катализатора и типа используемого оборудования. Обычно оно составляет менее 180 мин, например 10-75 мин. Целевые продукты выделяют известными методами. Полученные уретаны содержат одну или несколько уретановых групп и по своей природе могут быть мономерными или полимерными. Из уретанов, содержащих не более трех уретановых групп на молекулу, можно получить соответствующие изоцианаты, используя термическую и каталитическую обработку. Линейные полиуретаны, используемые в пооизводстве волокон или эластомеров, мо- (Г гуг быть получены непосредственно из диолов, динитросоединеник и окиси углерода или из гидроксинитросоединений и окиси углерода, тогда как сщитые полиуретаны, применяемые в качестве гибких или твердых ,, ПЛаСТИЧНЫХ материалов, могут быть получены из смесей ди- или полинитросоединени диолов или полиолов и окиси углерода. Во всех примерах конверсию и выход целевых продуктов определяют методом газовой и жидкостной хроматографии, Примеры 1-11, Нитробензол, ме тиловый спирт, селен и основание загружаю во вращающийся автоклав емкостью 110 мл выдерживают необходимое время при опреде- ленных температуре и давлении окиси углерода и выделяют образующийся уретан. Результаты опытов приведены в табл, 1, Пример 12, 5 мл нитробензола. 30 мл метилового спирта, 0,5 г селена,45 35 мл ТГФ и 1 или 2 г тригидрата ацетата натрия выдерживают при начальном да&лении окиси углерода 56,2 кг/см и темпе- ратуре 200 С во вращающемся автоклаве емкостью 110 мл. Через 10 мин конверсия50 нитробензола достигает 64 или 70%, а выход уретана 74 или 63% соответственно, При проведении реакции при 170°С через 6О мин конверсия нитробензола составляет 72 или 100%, а выход целевого про-55 дукта 7О или 74% соответственно, Пример 13, Из 5 мл нитробен- зола, ЗО мл метилового спирта, 35 мл ТГФ, О,ОО8 моль моногидрата ацетата лития и 0,5 г селена аналогично примеру 12 (на-60 5 1 чальное давление окиси углерода 5 6,2 кг/см , температура 170 С) через 10 мин получав юг целевой продукт с выходом 68%, Конверсия нитробензола 94%, При проведении реакции при 170 или в течение 60 мин или при 13О°С в течение 140 мин конверсия нитробензола составляет 100, 87 или 71%, а выход уреf 3 85 или 71% соответственно, Пример 14, Как в примере 13, но при использовании в качестве катализатора 0,1 г дисульфида титана и проведении реакции при 150°С через 60 мин получают «елевой продукт с вьрсодом 88%. Конверсия нитробензола 86%. В отсутствие моногидрата ацетата лития нитробензол не вступает в реакцию. Пример ы , О,29 г гидроокиси лития, 0,72 г уксусной кислоты, нитробензол, метиловый спирт, 15 мл диоксана и катализатор помещают в автоклав емкостью 110 мл и выдерживают при определенных температуре и начальном давлении - „ окиси углерода. Результаты опытов приве- j tдены в табл. 2 Пример 20, 10 мл нитробензола, 65 мл метилового спирта, 2, 1 или и 0.5 г сеоы, 1,6 мл пиридина и 1 г тригид„ «no; c r nvжaют R янтокляв рата ацетата натрия загружают в автоклав емкостью 300 мл и вьщерживают при начальном давлении окиси углерода 183 кг/см и температуре 200 С в течение 45 мин. Конверсия нитробензола 94, 83 или 46%, выход уретана 33. 38 или 32% соответстПример 21, В автоклав емкостью ЗОО мл загружают Ю мл нитробензола. 0 метилового спирта, 35 мл 1,4-ди- океана, 0,5 г металлического селена щ раэличные основания, выдерживают 30 мин при температуре 20О Си начальном давлении окиси углерода 183 кг/см и выделяют целевой продукт. При использовании в качестве основания 1 г тригидраха ацетата натрия; 1 г ацетата натрия (расплавленного); 1 г ацетата натрия (расплавленного) в присутствий 0,2 г воды; ацетата натрия, пснлученного из 0,48 г гидроокиси натрия и 0,72 г уксусной кислоты в реакционной смеси; 1 г безводного ацетата калия и 1 г безводного ацетата калия в присутствии 0,2 г воды конверсия нитробензола составляет 100, 8, 100, 91, 50 и 100% соот ветственно, В присутствии 0,2 г воды конверсия нитробензот достигает 64%, а в отсутствие воды и основания только 9%, Пример 22, 0,29 г гидроокиси лития, 0,72 г уксусной кислоты, 0,50 г селена, 1О,7 г нигробенаола или 19,8 г ааоксибензола, ЗО мл метилового и 35 мл диоксана загружают а автоклав емкостью 300 мл и вьщерживают 30 мин при температуре 200 С и начальном давлении окиси углерода 183 кг/см , Конверсия азотсодержащего соединения достигает 100 или 86%, а выход уретана 7О или 69% соответственно. Примеры 23-27. 10,9 г 2,4-динитротолуола, этиловый спирт, гидроокись калия, уксусную кислоту, основание и порошкообразный металлический селен загружают в автоклав емкостью 300 мл и подают в него окись углерода до давления 56,2 кг/см и вьщерживают при определе ной температуре. Во всех опытах, результаты которых св дены в табл. 3, конверсия 2,4-динитротолу ола составляет 10О%, Пример 28. В полупромышленну установку, включающую реактор, снабженны мешалкой, подают жидкую смесь, содержаШую (в вес.%): 1О промышленного динитротолуола (80% 2,4-динитротолуола и 20% 2,6-динитротолуола), 87 промьш1ленного этанола (денатурированный этанол, содержащий 2% бензола), 1 уксусной кислоты, 1 гидроокиси калия и 1 двуокиси селена, вместе со стехиометрическим избытком окиси угле рода. Оптимальные условия реакции: температура 177°С, время контакта ЗО мин, давление 71 кг/см. В этих условиях конверсия динитротолуола 100%, выход диуре танов 90-95%. При температуре 152°С и времени контакта 6О, 30 и 15 мин конверсия составляет 100, 90 и 76% соответственно. При проведении процесса при температуре ниже 177 и времени контакта 30 мин выход диуретанов уменьшается с одновременным увеличением выхода моноуретанов. При проведении реарщии при температуре выше 177°С и времени контакта больше 30 мин обычно снижается выход диуретанов. В оптимальных условиях реакция идет быстро даже при низкой концентрации катализатора, например конверсия достигает 90% при концентрации селенового катализатора 0,07 вес.%.
15
538661
16
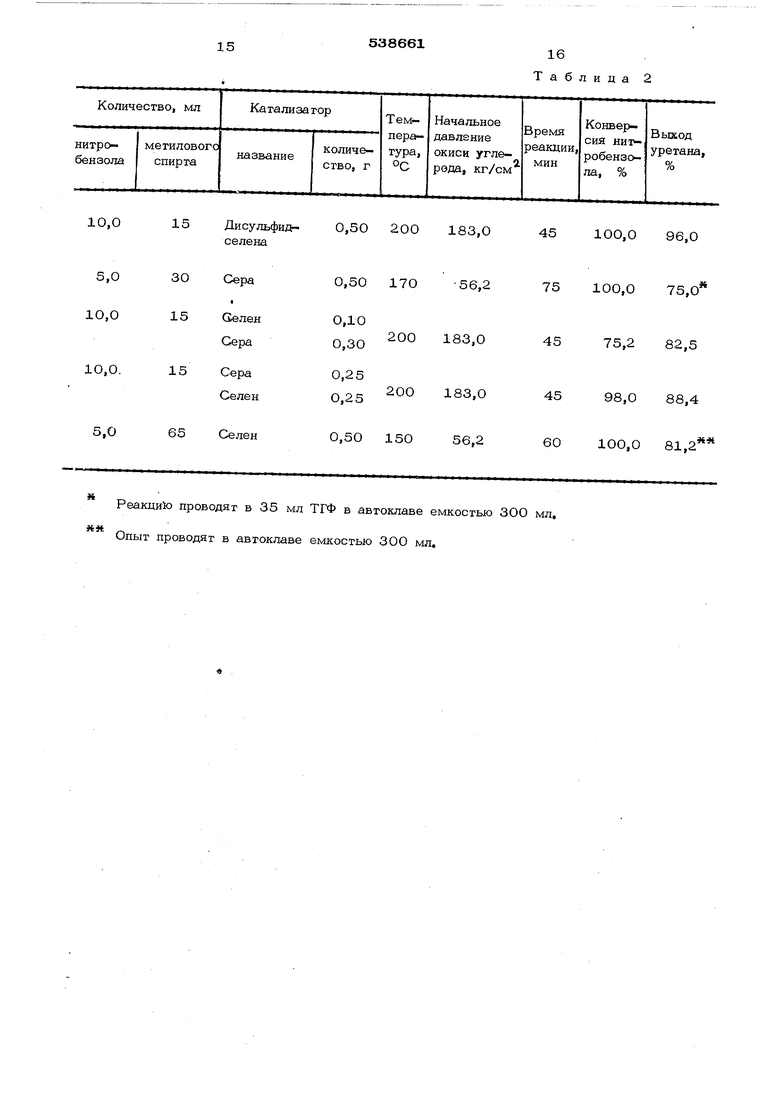
Таблица 2







| название | год | авторы | номер документа |
|---|---|---|---|
| Способ регенерации селеномочевины из уретановых смесей | 1981 |
|
SU1009507A1 |
| Катализатор для синтеза карбаматов и способ его приготовления | 1986 |
|
SU1431827A1 |
| Способ получения сложных эфиров циннолинкарбоновых кислот | 1973 |
|
SU493969A3 |
| СПОСОБ ПОЛУЧЕНИЯ СПИРТОВОГО РАСТВОРА КОБАЛЬТКАРБОНИЛЬНОГО КАТАЛИЗАТОРА | 1995 |
|
RU2077948C1 |
| Способ получения окиси этилена | 1979 |
|
SU1060110A3 |
| Способ получения -алкилароматических аминов | 1978 |
|
SU781200A1 |
| Катализатор для синтеза метил- @ -фенилкарбамата | 1982 |
|
SU1131531A1 |
| Способ получения производных 2,4-диаминопиримидин-3-оксида | 1975 |
|
SU584770A3 |
| СПОСОБ ПОЛУЧЕНИЯ АЛЬДЕГИДОВ И/ИЛИ СПИРТОВ | 1972 |
|
SU342335A1 |
| СПОСОБ СИНТЕЗА МЕТАЛЛ-УГЛЕРОДНОГО КАТАЛИЗАТОРА И ПРОЦЕСС ВОССТАНОВЛЕНИЯ НИТРОСОЕДИНЕНИЙ | 2013 |
|
RU2581166C2 |

Реакций проводят в 35 мл ТГФ в авгоклаве емкостью 300 мл.
Кй
Опыт проводят в автоклаве емкостью 300 мл.
1920
Формула иаобрегенияселен, серу, соединения селена, соединения
ВИИ катализатора с последующим выделени-3, Способ по пп, 1и2, отлича юем целевого продукта известными приемами,щ и и с я тем, что процесс ведут при моотличающийся тем, что, с целью юлярном соотношении между катализатором
повышения выхода и чистоты целевого про-и азотсодержащим органическим соединенидукта, в качестве катализатора используютем 1:1О - 1: 1000,
538661
серы или их смеси и процесс ведуг в при
Авторы
Даты
1976-12-05—Публикация
1973-08-29—Подача