1
Изобретение относится к химии фосфорорганических соединений, а именно к усовершенствованному способу получения алкил-М-имиHO-N - алкоксиалкилметилфосфоиатов общей формулы
OR .
«Г
3t
0-R -C-OR
О II fin
где R - Ci-С4-алкил,
R - низший алкилен нормального или изостроения.
Эти соединения могут быть использованы как. полупродукты фосфорорганического синтеза.
Известен способ получения фосфорилированных иминов взаимодействием фосфинистой кислоты с .нитрилами при нагревании до 100°С в запаянной ампуле в присутствии в качестве катализатора алкоголята натрия.
Наиболее близким к описываемому изобретению по технической сушности и достигаемому результату является способ получения алкил-М-имино-N - алкоксиалкилметилфосфонатов, который заключается в том, что смешанные алкиловые, цианалкиловые эфиры алкилфосфоновых кислот подвергают взаимодействию со спиртами и хлористым водородом при температуре 5-10°С и соотношен 1И реагентов 1:1; 3-4 с последующей обработкой хлористоводородной соли фосфорилированного иминоэфира триэтиламином в среде диэтилового эфира. Выход целевого продукта 66-85% в расчете на фосфорилированный нитрил.
К недостаткам этого способа следует отнести двухстадийность получения исходного смешанного алкилового, цианалкилового эфира алкилфосфоновой кислоты из дихлорангидрид,а фосфоновой кислоты и соответствующих спиртов в присутствии триэтиламина, а также
сравнительно низкий выход целевого продукта, большой расход реагентов (триэтиламина, диэтилового эфира), что вызвано многостадийностью процесса.
Целью изобретения является упрощение
процесса и увеличение выхода целевого продукта.
Поставленная цель дост1 гается описываемым способом получения алкил-М-имино-Х-алкоксиалкилметилфосфонатов, который заключается в том, что хлорангидрид цианалкилового эфира метилфосфоновой кислоты подвергают взаимодействию с низшим алифатических спиртом и хлористым водородом при мольном соотношении реагентов 1:2:1,5 соответственно, при температуре (-10) - (+10)°С, с
последующей обработкой образующейся хлористоводородной соли иминоэфира органическим основанием в среде инертного органического растворителя.
Предлагаемый сноеоб достаточно прост в осуществлении. Применение в качестве исходных веществ хлорангидридов цианалкиловых эфиров алкилфосфоновых кислот позволяет в одной стадии совместить образование алкоксигруппы у атома фосфора и промежуточного гидрохлорида фосфорилированного имидата, использовать в процессе реакционный хлористый водород, образующийся при замещенцн хлора у атома фосфора иа алкоксигруппу, а сократить в 2-2,5 раза расход вводимого хлористого водорода (сырья), который необходим, по-существу, только для создания его избытка в реакционной массе с целью ускорения процесса.
Предлагаемый способ позволяет повысить выход целевых продуктов. Так, в известном способе выход фосфорилированных имидатов составляет 66-85% в расчете па алкиловые, цианалкиловые эфиры алкилфосфоновых кислот или 56-72% в расчете ла хлорангидриды цианалкиловых эфнров алкилфосфоновых кислот. Выход целевых продуктов в предлагаемом способе составляет 72-88% в расчете на хлорангидрид циапалкилового эфира метилфосфоновой кислоты.
Пример 1. Синтез этил-а-{иминоэтоксиметил) -изопропилметилфосфоната.
В реактор, содержащий 5,06 г (0,1 г моль) этилового спирта, медленно приливают при интенсивном перемешивании 10 г (0,055 г-моль) хлор ангидрид а сс-цианизопропилметилфосфоната при температуре не ниже . Паблюдается высокий экзотермический эффект. Температуру реакции (-7°С) поддерживают с помощью охлаждающей бани. После добавления всего количества хлорангкдрида сс-цианизопроиилметилфосфоиата в реакционную смесь подают по барботеру 3,03 г (0,083 г-моль) осушенпого хлористого водорода при температуре- 5-0°С в течение 1 час.
Выдерживают реакционную смесь 2 час при 0°С, затем избыточный хлористый водород удаляют вакуумированием до теоретического количества, осуществляя контроль пер}10дическим взвешиванием.
Выход гидрохлорида фосфорилироваилого иминоэфира, нредставляющего собой бесцветную, вязкую жидкость (п : 1,4562), близок к теоретическому.
К полученной соли фосфорилированного иминоэфира приливают 20 мл безводного диоксана и при температуре 10°С приливают 6,07 г (0,06 г-моль) триэтиламина, растворенного в 10 мл диоксаиа. Образовавшийся осадок солянокислого триэтиламина отфильтровывают, из фильтра под вакуумом водоструйного насоса отгоняют растворитель и избыток триэтиламина, а остаток подвергают перегонке при ,8-I мм рт. ст. Выход фосфорплированного иминоэфира составляет 9 3 г (72 %).
Результат опыта и характеристика полученного соединения представлены в таблице (соединение 1).
Пример 2. Синтез этил-р- (иминоэтоксиметил)-этилметилфосфоната.
В реактор, содержащий 9,2 г (0,2 г-моль) этилового спирта, при температуре -5°С медленио при перемещивании приливают 15,15 г (0,1 г-моль) хлораигидрида р-циаиэтилметилфосфоната. Паблюдается большой экзотермический эффект, температуру реакции поддерживают с помощью охлаждающей бани (лед+ -j-соль). После подачи всего количества хлорангидрида р-циапэтилметилфоефоната по барботеру пропускают 5,46 г (0,15 г-моль) осушенного хлористого водорода при температуре 0°С в течение 1,5 час. Реакционную смесь выдерживают 2 час и затем удаляют избыточный хлористый водород до теоретического количества, контроль осуществляют взвешиванием.
К образовавшейся соли иминоэфира в 30 мл диоксапа медленно приливают 10,1 г (0,1 гмоль) триэтиламипа в 10 мл диоксапа при температуре 10°С.
Образовавшийся осадок солянокислого триэтиламина отфильтровывают (выход 96%), из
фильтрата отгоняют растворитель, а остаток
подвергают нерегонке при Я -0,95 мм рт. ст.
Выход иминоэфира - 87%.
Результаты опытов и характеристика полученных соединений представлены в таблице.
Строение сиптезироваппых соединений подтверждено элементным анализом, ИК-спектрами, молекулярной рефракцией, а также химическими превращениями.
Пример 3. Синтез этил-а-(иминоэтоксиметил)-изопронилметилфосфоната в среде бензола.
В четырехгорловый реактор, снабженный
мешйлкой, термометром, обратным холодильником и капельной вораикой, загружают 3,03 г (0,066 г-моль) абсолютного этилового спирта и при интенсивном перемешивании медленно приливают 6,0 г (0,033 г-моль) хлорапгидрида
сс-цианизопропилметилфосфоната при те.мпературе - 8°С. Наблюдается значительный экзотер1мический эффект. После добавления всего количества хлорангидрида а-цианизопропнлметялфосфопата в реакционную смесь по
трубке пропускают 1,8 г (0,049 г-моль) сухого хлористого водорода при температуре 0°С в течение 35 мин. Выдерживают реакционную смесь 2 час при температуре О-5С, избыточный хлористый водород удаляют вакуумированием.
К полученной соли фосфорилировапного иминоэфира, представляющей собой бесцветную, вязкую жидкость (Лд 1,4560), приливают 15 мл сухого бензола, и при температуре около 10°С медленно дозируют раствор, соАлкил-Ы-имино-Ы-алкоксиалкилалкилфосфонаты
О
в-р-о-11 С ек
-т

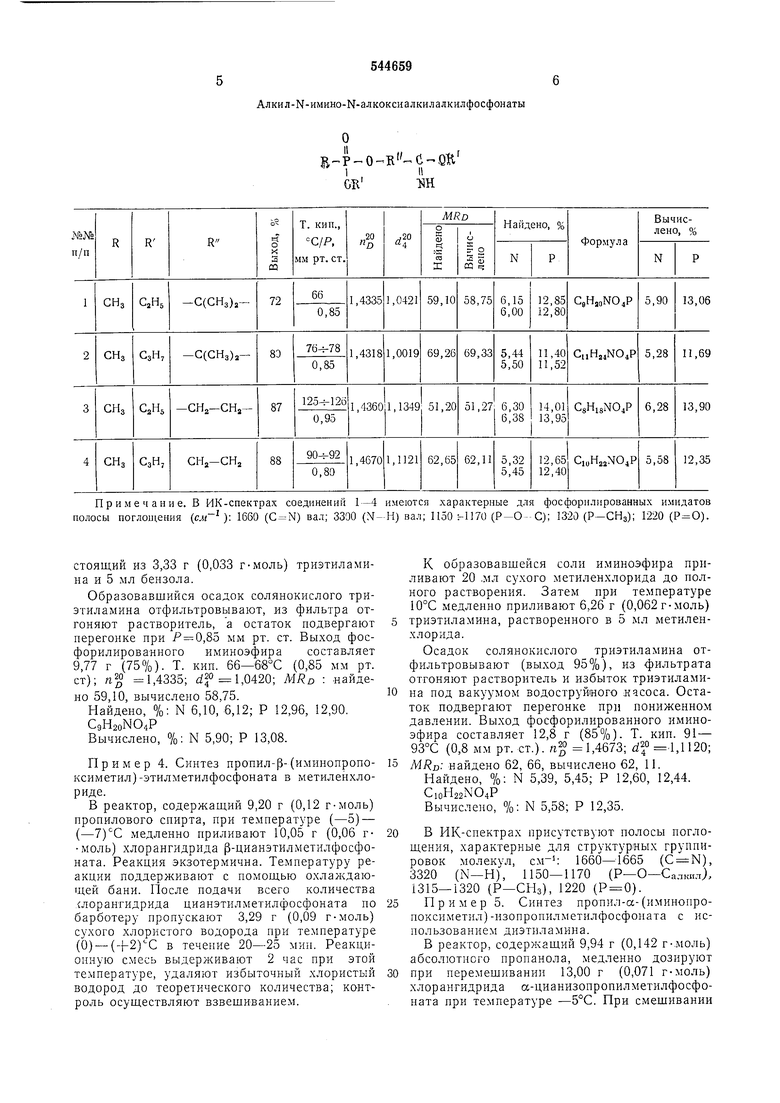


Примечание. В ИК-спектрах соединений 1-4 имеются характерные для фосфорилированных имндатов полосы поглощения (см ); 1660 (C N) вал; 3300 (N-Н) вал; 1150 н1170 (Р-О- С); 1320 (Р-CHj); 1220 ().
СТОЯЩИЙ из 3,33 г (0,033 г-моль) триэтиламина и 5 мл бензола.
Образовавшийся осадок солянокислого триэтиламина отфильтровывают, из фильтра отгоняют растворитель, а остаток подвергают перегонке при Р 0,85 мм рт. ст. Выход фосфорилированного иминоэфира составляет 9,77 г (75%). Т. кип. 66-68°С (0,85 мм рт. ст); 1,4335; df 1,0420; MRo : -найдено 59,10, вычислено 58,75.
Найдено, %: N 6,10, 6,12; Р 12,96, 12,90.
C9H2oN04P
Вычислено, %; N 5,90; Р 13,08.
Пример 4. Синтез пронил-р-(иминопропоксиметил)-этилметилфосфоната в метиленхлориде.
В реактор, содержащий 9,20 г (0,12 г-моль) пропилового спирта, при температуре (-5) - (-7)С медленно приливают 10,05 г (0,06 гмоль) хлорангидрида р-цианэтилметилфосфоната. Реакция экзотермична. Температуру реакции поддерживают с помощью охлаждающей бани. После подачи всего количества {лорангидрида дианэтилметилфосфоната по барботеру пропускают 3,29 г (0,09 г-моль) сухого хлористого водорода при температуре (0) -(+2)С в течение 20-25 мип. Реакционную смесь выдерживают 2 час при этой температуре, удаляют избыточный хлористый водород до теоретического количества; контроль осуществляют взвешиванием.
К образовавшейся соли иминоэфира приливают 20 ,мл сухого метиленхлорида до полного растворения. Затем при температуре 10°С медленно приливают 6,26 г (0,062 г-моль) триэтиламииа, растворенного в 5 мл метиленхлорида.
Осадок солянокислого триэтиламина отфильтровывают (выход 95%), из фильтрата отгоняют растворитель и избыток триэтиламина под вакуумом водоструйного насоса. Остаток подвергают перегонке при пониженном давлении. Выход фосфорилированного иминоэфира составляет 12,8 г (85%). Т. кип. 91- 93°С (0,8 мм рт. ст.). ng 1,4673; ,1120; MRo- найдено 62, 66, вычислено 62, 11.
Найдено, %; N 5,39, 5,45; Р 12,60, 12,44.
CioH22N04P
Вычислено, %: N 5,58; Р 12,35.
В ИК-снектрах присутствуют полосы поглощения, характерные для структурных группировок молекул, см-: 1660-1665 (C N), 3320 (N-нУ, 1150-1170 (Р-О-Салкил), 1315-1320 (Р-СНз), 1220 (Р 0).
Н Р и м е Р 5. Синтез пропил-а-(иминопропоксиметил)-изопропилметилфосфоната с использованием диэтиламина.
В реактор, содержащий 9,94 г (0,142 г-.моль) абсолютного пропанола, медленно дозируют
при перемешивании 13,00 г (0,071 г-моль) хлорангидрида а-цианизопропилметилфосфоната при температуре -5°С. При смешивании реагентов наблюдается значительный экзотермический эффект, температуру реакции (-5°С) ноддерживают с помощью охлаждающей бани (лед+соль). После добавления всего количества хлорангидрида а-циапизопропилметилфосфоната по барботеру в реакциоииую смесь подают 3,65 г (0,1 г-моль) осущенного хлористого водорода при температуре 0°С в течение 30 мин. Затем выдерживают реакционную смесь 3 час для завершения реакции при /нулевой температуре. Избыточный хлористый водород удаляют вакуумированием до теоретического количества галоидоводорода, осуществляют контроль периодическим взвешиванием. Выход гидрохлорида фосфорилированного иминоэфира, представляющего собой очень вязкую, бесцветную жидкость, близок к теоретическому. Образовавщийся гидрохлорид иминоэфира растворяют в 25 мл сухого диоксаиа и ири температуре около ilO°C приливают при интенсивном иеремещивании реакционной смеси 5,33 г (0,073 г-моль) осушенного диэтиламина, растворенного в 15 мл сухого диоксана. Осадок солянокислого диэтиламина отфильтровывают и промывают на фильтре Шотта 20 мл диоксана. Из фильтрата под вакуумом водоструйного насоса отгоняют растворитель и избыток диэтилами«а. Остаток подвергают вакуумной перегонке при ,8-1,0 мм рт. ст. Выход фосфорилпрованного иминоэфира 5,42 г (82%). Т. кип. 80-82°С (0,9 ммрт.ст.). п 1,4320; df 1,0016; MRo: найдено 69,25, вычислено 69,33. Формула изобретения Способ получения алкил-Ы-имино-Ы-алкоксиалкил.метилфосфонатов общей формулы 0-R -C-OR II где R - Ci-С4 алкил; R - низщий алкилен нормального иЛи изостроения; взаимодействием нроизводного цианалкилового эфира метилфосфоновой кислоты с низшим алифатическим спиртом при охлаждении с последующей последовательной обработкой реакционной смеси хлористым водородом и органическим основанием в среде инертного органического растворителя, отличающийся тем, что, с целью упрощения процесса и увеличения выхода целевого продукта, в качестве производного цианалкилового эфира метилфосфоновой кислоты используют хлорангидрид и процесс ведут при температуре (-10) - (+10)°С с использованием 2 моль спирта и 1,5 моль хлористого водорода на 1 моль хлорангидрида цианалкилового эфира метилфосфоновой кислоты. Источники информации, принятые во внимание при экспертизе: 1. Авт. св. № 321126, кл. С 07f 9/50, 1972. 2. Авт. св. Afc 507041, кл. С 07 9/40, 1973 (прототип).
Авторы
Даты
1977-01-30—Публикация
1975-04-28—Подача