1
Предлагаются новые химические соединения, а именно сульфоланилизотиоцианаты общей формулы
И
Чо,
где R - Н, СН«;
R- NCS или CHg-NCS.
Сульфоланилизотиоцианаты общей формулы I являются биологически активными соединениями.,Они могут быть использованы как фунгициды в медицине, сельском хозяйстве к промыЕлленности.
Указанные соединения и их свойства в литературе не описаны.
Известны эфиры 6-изотиоцианатов капроновой кислоты общей формулы
RCOO(CH2)5NCS П
где R - натрий, алкил Cjj-Cg водород, которые также обладают фунгицидными свойствами,
Однако введение в йзотиоцианаты оульфолана приводит к появлению у соединений общей формулы Т фун ицидной активности, они активнее подавляют рост мицелия, чем соединения общей формулыХТ.
Целью -изобретения является синтез сульфоланилизотиоцианатов, которые могут быть использованы в качестве фунгицидных средстй.
Изотиоцианатк. сульфолана общей
л формулы Т получают разложением соответствующих солей сульфоланилдитиокарбаминовых кислот хлорокисью фосфора .
Соли сульфоланилдитиокарбаминовойкислоты получают взаимодействием амн5 носульфоланов с сероуглеродом в присутствии третичных аминов, например триэтиламина. Прибавляют сероуглерод к смеси сульфоланиламина и третичного амина в органическом растворителе,
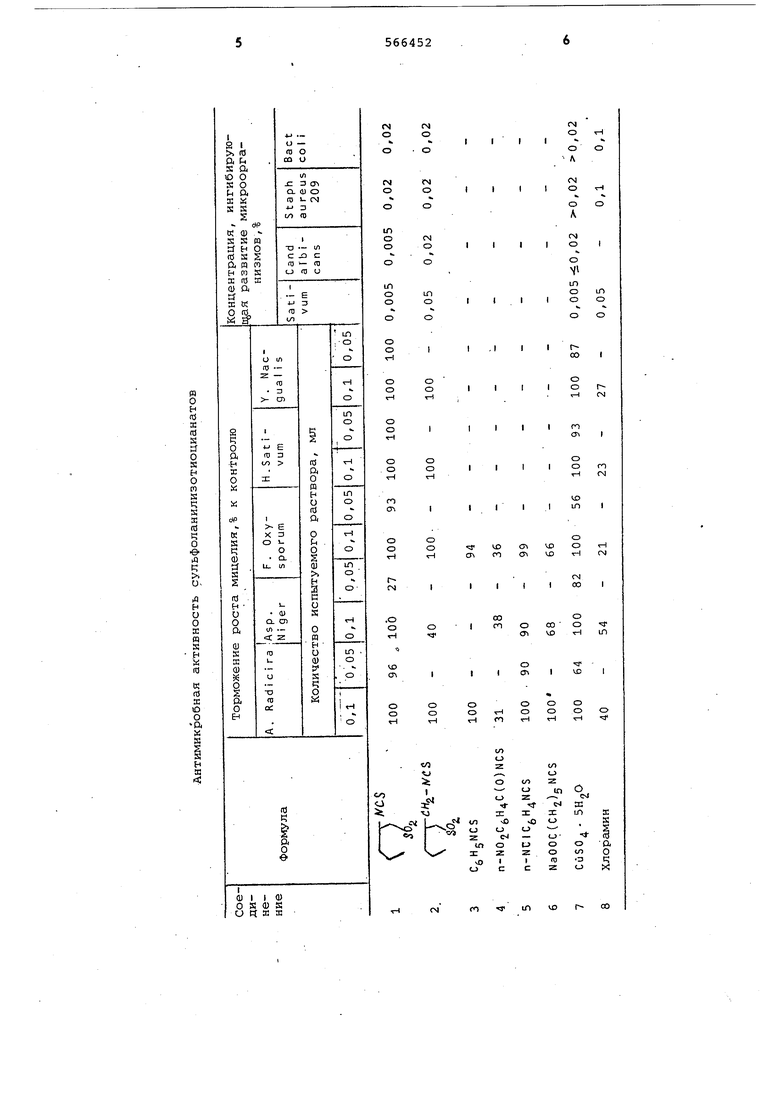
0 например в серном эфире, бензоле, хлористом метилене, и в образующуюся суспензию соли дитиокарбаминовой кислоты вводят хлорОкись фосфора в абсолютном органическом растворителе, например серном эфире, при минус 10 - минус . Промывают водным раствором бикарбоната натрия для удаления побочных продуктов. Изотиоцианат выделяют и очищают перегонкой после осушки органического раствора ,Н№ сернокислым натрием. Выход 60Сульфо 1анилизотиоцианаты MOKHQ также получить разложением солей ди тиокарбамвновой кислоты при помощи фосгена или эфиров хлоругольной кис лоты или реакцией тиофосгена с суль фолаииламинами. Пример 1. Сульфоланил-3-изотиоцианат (соединение 1). К смеси 40,55 г (0,3 моль) 3-ами носульфолана, 126 мл (0,9 моль) три этиламина и 150 мл хлористого метил на, охлажденной до минус , прикапывают 18 мл (0,3 моль) сероуг-. лерода и оставляпот на 8 ч при комнатной температу эе. К образовавшемуся раствору при минус 10 - минус 5°С прибавляют 28 мл (0,3 моль) хлорокиси фосфора в 30 мл хлористог метилена. Реакционную смесь вьвдержи вают 8 ч при комнатной температуре Выпавший осадок отделяют. Фильтрат несколько .раз промывают раствором бикарбоната натрия, затем водой до нейтральной среды. Органический сло сушат сульфатом натрия. Растворител упаривают в вакууме. Оставшееся мас ло перегоняют, выход 31 г (58%). Сульфоланил-3-изотиоцианат пред ставляет собой кристаллическое веще ства, т.пл. 85-8б°С, т.кип. 160170°С. В ИК-спектре имеются характерист ческие полосы поглощения при 1145 и 1300 см (502 - группа) и.20902120 см широкая двугорбая полоса (NCS - группа) . Найдено,%: С 33,5; Н 4,2;N 6,8; S 36,2; NCS 32,5. C5Hj 402Sa Вычислено,%: С 33,8; Н 4,0; N 7,9; S 35,1; KCS 32,7. Пример 2. Сульфоланил-3-(метиленизотиоцианат) (соединение 2). Вещество получают аналогично сул фоланил-3-изотиоцианату из 24,32 г (0,164 моль) 3-(аминометилен) сульфолана, выход 21,27 г (68%), т.пл. 65-67°С, т.кип. 140-145 0/ /1, мм рт.ст.. В ИК-спектре имеются характеристические полосы поглощения при 1125 и 1300 см. (SO2 - группа) и 20702160 см широкая, двугорбая полоса (NCS-rpynna). Найдено,%: С 37,8; Н 5,0;N 7,2; S 33,3; NCS 30,12. CjHjNOjS . Вычислено,%: С 37,6; Н 4,7; i N 7,5; S 33,5; NCS 30,36. Фунгицидную и бактерицидную активность сульфоланилизотиоцианатов изучали в лабораторных условиях Института органической химии АН Украинской ССР по общепринятым методикам. Результаты приведены в таблице. Из данных, приведенных в таблице, видно, что сульфоланилизотиоцианаты активнее подавляют рост мицелия, чем эталоны (соединения 3-8). Наиболее токсичным для мицелия является сульфоланил-3-изотиоцианат (соединение 1). Фунгитоксичность для спор определяли методом торможения прорастания конидий гриба Н. Sativum в водной среде. Из таблицы видно, что сульфоланилизотиоцианаты активнее эталона-хлорамина (соединение 8) и не уступают эталону - сернокислой меди (соединение 7) . Сульфоланилизотиоцианаты обладают выраженным антикандидозным действием, превс,,;ходящим активность сернокислой меди, фунгициднай концентрация совпадает с фунгистатической. Сульфоланил-3-метиленизотиоцианат .(соединение 2) обладает выраженным бактериостатическим действием, ингибируя развитие бактерий в концентрации 0,02%, превосходя активность -эталона - хлорамина (концентрация О ,%).
pq
О
н (б ad а
S
а о
S
в о
т S
гй Ч О
ел
ил и и о к п к
к (в ас о о
D.
н
а: -а:
(N
о гН
IIII «
о о
л
м
11110
о о
л
CN
IIIIоI
о
N1
1Л
от
I I I I о о
г
00
оо
оI I I I о гvt. N
п
о I о п
т-1 см
ю
I1Л
о о
G4 vn о СП П СГ 4D гЧ CN
IIIIСОI
00о
о I го о со о
ЧО гН 1Л
о-а-
IIОЛIVDI
ооо о о
оо н о о о о
vHvH го гН гЧ iH 7. Формула изобретения Сульфоланилизотиоцианатыо(щеи формулы В 1.д 5664526 где Н, CHj; R- NCS, GHgiJICS; проявляющие фунгицидную и бактери. цидную активность. .

| название | год | авторы | номер документа |
|---|---|---|---|
| Производные аллиотиоцианатов,проявляющиефуНгицидНую АКТиВНОСТь и СпОСОб иХпОлучЕНия | 1974 |
|
SU522605A1 |
| N-/1-метил-2-фенилтиовинил/уретаны и мочевины, обладающие фунгицидной активностью | 1979 |
|
SU750986A1 |
| Фосфорсодержащие производные мочевины и тиомочевины для борьбы с грибными заболеваниями растений | 1974 |
|
SU525398A1 |
| Способ получения ксантонов или их солей | 1975 |
|
SU593665A3 |
| Хлористые 2-( @ -алкилтио)-этиловые эфиры @ -аммонийфенола, проявляющие свойства регуляторов роста растений, фунгицидов и нематоцидов | 1980 |
|
SU959391A1 |
| Способ получения оптически активных производных оксазафосфорина | 1979 |
|
SU867314A3 |
| Замещенные ди-или тривиниловые эфиры фосфорной и тиофосфорной кислот,обладающие инсектофунгицидной активностью | 1976 |
|
SU630861A1 |
| Способ получения производных хиназолина или их формацевтически приемлемых кислотно-аддитивных солей | 1990 |
|
SU1838309A3 |
| 3-ГИДРОКСИ-2-ТИОКСО-4(3Н)-ХИНАЗОЛИНОН, ОБЛАДАЮЩИЙ ФУНГИЦИДНЫМИ И РОСТОРЕГУЛИРУЮЩИМИ СВОЙСТВАМИ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 2004 |
|
RU2275362C2 |
| 2-Алкилтио-5-(1,2,4-триазол-1-илметил)-1,3,4-оксадиазолы, способ их получения и фунгицидные композиции на их основе | 2022 |
|
RU2794339C1 |


Авторы
Даты
1981-04-23—Публикация
1975-08-06—Подача