3,13 г (0,01 моля децнлового эфира N-малеилглицина, 5 мл водного раствора, содержащего 0,013 моля бисульфита натрия и 5 мл этанола греют на кипящей водяной бане с отгонкой спирта). Через 2 ч реакционную смесь охлаждают, при этом она превращается в вязкую парафинообразную массу, которую обрабатывают ацетоном до превращения ее в белый порошок.
Полученная Na-соль iN-сульфосукцината децилового эфира глицина при нагревании выше 250°С темнеет и при 280°С разлагается. Выход 3,81 г (87%).
Найдено, %: N 3,22; S 7,89. CieHaaNOeSNa.
Вычислено, %: N 3,35; S 7,67.
Пример 2. Динатриевая соль N-сульфосукцината гексилового эфира ip-фенил-ааланина.
5,20 г (0,015 моля) гексилового эфира Nмалеата :р-фенил-а-аланина в 5 мл этанола смешивают с 1,89 г (0,015 моля) NagSOa в 8 мл воды и греют при 80°С до получения гомогенного раствора. Затем отгоняют спирт, продукт высаживают ацетоном. Получают 6,43 г (90,8%) динатриевой соли N-сульфосукцината гексилового эфира р-фенил-ааланина в виде белого порошка, разлагающегося при нагревании выше 250°С.
Найдено, %: N 2,70; S 6,96.
CigHsgNOsSNaa.
Вычислено, %: N 2,95; S 6,76.
Пример 3. Калиевая соль N-сульфосукцината миристилового эфира а-аминомасляной кислоты.
3,97 г (0,01 моля) миристилового эфира Nмалеата а-аминомасляной кислоты в 5 мл этанола и 5 мл водного раствора, содержащего 0,012 моля бисульфата калия греют на водяной бане с отгонкой спирта в течение 2 ч. Охлажденную парафинообразную массу растворяют в минимальном количестве воды и добавляют спирт до помутнения раствора. После охлаждения в холодильнике выпавший осадок фильтруют и промывают ацетоном. Получают 3,81 г (72,8%) калиевой соли :Nсульфосукцината миристилового эфира ааминомасляной кислоты в виде пушистого белого порошка, разлагающегося при нагревании выше 250°С.
Найдено, %: N 2,9056; S 6,29.
C22H4oO8NSK.
Вычислено, %:iN2,71; S 6,19. Пример 4. Диаммонийная соль N-сульфосукцината гексилового эфира лейцина. 3,13 г (0,01 моля) гексилового эфира Nмалеиллейцина и 10 мл 15%-иого водного раствора сульфита аммония греют при 60°С до образования прозрачного раствора, после чего температуру повышают до 80°С и выдерживают в течение 30 мин. Охлажденную реакционную массу обрабатывают ацетоном до получения плотного аморфного осадка, который высушивают в вакуум-эксикаторе. Получают 3,52 г (81,5%) диаммонийной соли N10 сульфосукципата гексилового эфира лейцина, разлагающегося при нагревании до 200°С.
Найдено, %: N 9,95; S 7,55.
CieHssNsOsS.
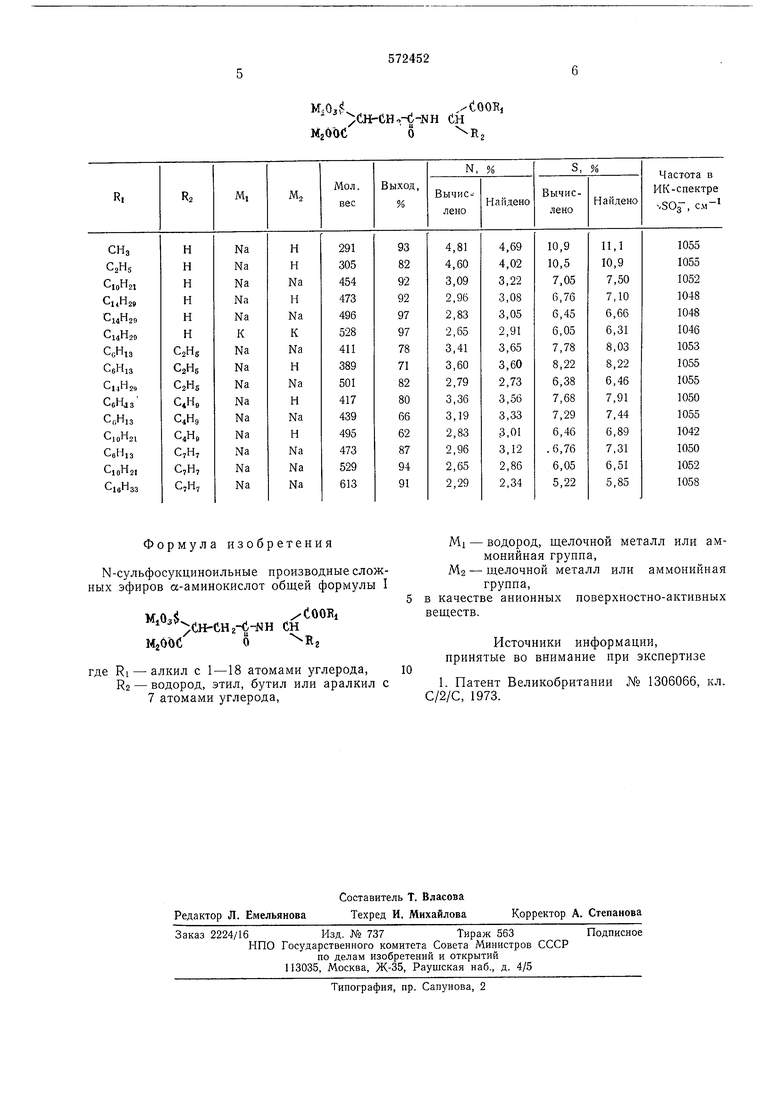
Вычислено, %: N 9,80; S 7,46. 15 Аналогично полученные N-сульфосукционоильные производные сложных эфиров а-аминокислот формулы I приведены в таблице.
Новые соединения общей формулы I проявляют хорошую поверхностную активность; особенно это касается соединений формулы I, где .
Полученные продукты хорошо растворяются в воде, при встряхивании их водные растворы дают обильную пену. Интересной особенностью обладают соли синтезированных соединений с , а именно - способностью растворяться в неполярных органических растворителях, таких как алифатические
0 углеводороды, бензол, диоксан, диэтил, эфир. Они растворяются также и в полярных органических растворителях, например в низшем алифатическом спирте, диметилформамиде, ацетоне.
5 Синтезированные продукты обладают ярко выраженной солюбилизирующей способностью. Так, в 10%-ном водном растворе Naсоли N-сульфосукцината децилглицина можно получить 3%-ные растворы левомицетина
0 или синтомицина. Для сравнения: использующийся солюбилизатор твин-80 позволяет в 10%-ном его водном растворе получать 0,8- 0,9%-ные растворы синтомицина. Новые соединения проявляют также высокую эмульгирующую способность. Так, эмульсия касторового масла в воде с добавкой 1 % новых ПАВ стабильна в течение 18 месяцев (в условиях ускоренного старения). Для сравнения: широко применяющийся в фарма0 Ции эмульгатор № 1 (анионное ПАВ, представляющее собой сульфатированные кашалотовые жиры) в аналогичных условиях дает эмульсию, стабильную лишь 12 месяцев. Таким образом, полученная группа веществ
может найти применение как анионные поверхностно-активные вещества.
.
MjOoc
/Сн-сн,-с/-ын
о

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения S @ -/-3-(3-ацетил-4-4-)3-трет -бутил-амино-2-гидроксипропокси/-фенил @ -1,1-диэтилмочевины | 1985 |
|
SU1333235A3 |
| СПОСОБ ПОЛУЧЕНИЯ ФЛУОРАНТИЛ-4-УКСУСНОЙ КИСЛОТЫ | 1969 |
|
SU245072A1 |
| СПОСОБ ПОЛУЧЕНИЯ-)-а-АМИНО-п- | 1971 |
|
SU309520A1 |
| Способ получения производных 1-/3-(3,4,5-триметоксифенокси)-2-пропил/-4-арилпиперазина | 1978 |
|
SU893133A3 |
| 4-(3-Арил-5-фенил-2-пиразолинил-1)фталевые кислоты, или их метиловые эфиры, или ангидриды, или соли в качестве фотостабильных органических люминофоров сине-зеленого свечения | 1984 |
|
SU1173705A1 |
| Комплексные соединения кобальта /п/ с 1,10-фенантролином и анионами @ -аминокислот, обратимо присоединяющие молекулярный кислород и способ их получения | 1979 |
|
SU883051A1 |
| ФОСФОРИЛИРОВАННЫЕ СЕРИНЫ | 1989 |
|
RU2057133C1 |
| Анион-радикальная соль 2-метил-7,7, - 8,8-тетрацианохинодиметана в качестве добавки к проводящим органическим материалам | 1989 |
|
SU1696428A1 |
| Способ получения азотсодержащих полициклических соединений или их солей, или рацематов, или оптических антиподов | 1975 |
|
SU554816A3 |
| N-фенацетил-N-этилдитиокарбаминовая кислота в качестве промежуточного продукта для синтеза тиазолиевых солей и способ получения тиазолиевых солей | 1990 |
|
SU1796619A1 |

Формула изобретения N-сульфосукциноильные производные сложных эфиров а-аминокислот общей формулы I W о xtOOKi СН-СНг-e-NH СН М200СоНа где RI - алкил с 1 -18 атомами углерода, ю R2 - водород, этил, бутил или аралкил с 7 атомами углерода, 5 MI - водород, щелочной металл или аммонийная группа, Mg - щелочной металл или аммонийная групиа, в качестве анионных поверхностно-активных веществ. Источники информации, принятые во внимание при экспертизе 1. Патент Великобритании № 1306066, кл. С/2/С, 1973.
Авторы
Даты
1977-09-15—Публикация
1976-01-22—Подача