АЗ замещенная или незамеи ниая araiipa тическая алкиленовая цепь, проявляю1 пшохолеристеномическую активность 2, Однако ciiiiiea новых представителей замещенных пол гцилических соеданенш, проявляющих физиологическую активность, является важным направлением определенных исследовательных работ.
На основе извесгаого метода получе}шя эфиров кислот иди aNfflHO согласно изобретегшю получены новые замещенные бензо (a,d) циклогептет общей формулы Г
О
где X - водород, алкил Ci -€4, галоген, тиоалкил Gi-C4, трифторметил,
RI и R2 - одинаковые или различные и представляют собой водород или алкил Ci-C,
Вз - алкоксил Ci-C4, 2,2 - диметил - 1,3 «диоксолан - 4 - ил - метилоксигруппа или группа NR4Rs; е
R4 и RS - одинаковые или различные и представляют собой водород, алкил Ci-Сд, фенил или совместно с атомом азота R4 и Rj представляют собой пяти - или шестнчеленный гетерощ1кл, который в некоторых случаях может содержать допол1штельпо кислород, серу или азот, а также алкильньш С)-€4 радикал, или их соли, которые обладают определенной физиологической активностью. Осуществлеьше способа ведут взаимодействием хлорангидрида общей формулы
О
где X, RI, R2 имеют указанные значения, с соединением общей формулы RjH, где Ra имеет казанные значения, в среде органического инертного растворителя, например метиленхлорида, при 0,30° С, причем, когда используют соединение, где Вз - алкоксил или 2,2 - диметил - 1,3 - диоксолан 4 - ил - метилоксигруппа, то продесс ведут в присутствии акдептора хлористого водорода, например, пиридина.
В случае, когда используют в качестве реагента замещенный амин, то его для улавливания выделяющегося хлористого водорода берут в избытке.
Пример 1.К раствору 10 г 5 - оксо - 10,11 дишдродибензо (a,d) щгклогептенил - 2 - 2 пропионилхлорида в 3 00 см метиленхлорида добавляют в течение 30 NmH при 0°С 250 см хлорметиленового 2,6 н. раствора метиламина. Реакционную смесь вьщаривают, добавляют 100 см дистиллированной воды и 300 см бензола. Органический слой декантируют, высушивают на безводном сульфате натрия и выпаривают при 60° С и умеренном давле1ши (20 мм рт.ст.). Полученный продукт перекристаллизовьшают в 100 им окиси изопропила. В результате получают 5,8 г 5 - оксо -10,11 - дигидродибензо (a,d) диклогепте1шл - 2 - 2
N метилпропионамида, плавящегося при 140°С (выход 5 9%).
Вычислено,%; С 77,79; Н 6,53; О 10,91; N 4,77.
Найдено,%: С 78,3; Н 6,6; О 10,9; N 4,7.
Пример 2. Аналогично примеру 1, но из 10 г хлорида 5 - оксо - 10,11 - дигидродибензо (a,d) Щ1клогептенил - 2 - 2 - пропио1шла - 4,5 г диметиламина, получают в виде масла 10 г 5 - оксо - 10,И
-дигидродибензо (a,d) циклогептенил - 21 - 2 - N N Диметилпропионамида (выход 99%).
,55 (окись крем1шя, хлороформ-этилацетат 80-20 по объему)
Вычислено,%: С 78,14; Н 6,89; О 10,41 N4,56. Найдено,%: С 78,2; Н 6,7; О 10,7; N 4,8. Пример 3. Аналогично примеру 1, но из 8 г хлорида 5 - оксо - 10,11 - дигидродибензо/ (a,d) пиклогептенил - 2 - 2 - пропиоьшла и с 7,5 г анилина после перекристалггизащ1и в 100см изопропанола получают 6,7 г 5 - оксо - 10,11 дигидродибензо (a,d) щ клогептенил - 2 - 2 - N фенилпропионамида, плавящегося при 149°С. Пример 4. Аналогично примеру 1, но из 8 г
хлорида 5 - оксо - 10,11 - дигидродибензо (a,d) циклогептенил - 2 - 2 -пропионила и 8,2 г метилпиперазина, получают в виде масла 10 г - оксо -10,11 - дигидродибензо (a,d) циклогептенил - 2 - 2 -пропионил j - 4 - метил - 1 - пиперазина.
Это масло растворяют в 100 см анестизирующего эфира, добавляют 8,5 см эфирного раствора хлористого водорода (3,1 н.). Кристаллизующийся продукт отделяют путем фильтрации и перекристаллизации в 10 см ацетона. В результате получают 4,3 г хлорида - оксо - 10,11 - дигидродибензо (a,d) - диклогептенил - 2) - 2 - прогШонил
- 4 - метил - 1 - пиперазина, плавящегося при 216° С (выход 40%).
Вычислено,%: С 69,25; .Н 6,82; О 8,02; N 7,02.
Ншщено,%: С 68,8; Н 6,6; О 8,6; N 6,95. Пример 5. Аналогично примеру 1, но из 1 г хлорида 5 - оксо - 10,11 - дигидродибензо (a,d) циклогептенил 2 - 2 - пропионила и с 2 г аминоэтанола получают 11 г 5 - оксо - 10,11 Дигидродибеизо (ad) циклогептенил - 2 - 2 - N - -оксизтилпропионамида, . плавящегося при И 8° С (выход 57%).
Вычислено,%: С 74,28; Н 6,55; О 14,84; N 4,33. Найдено,%: С 74,4; Н 6,4; О 15,0; N 4,4.
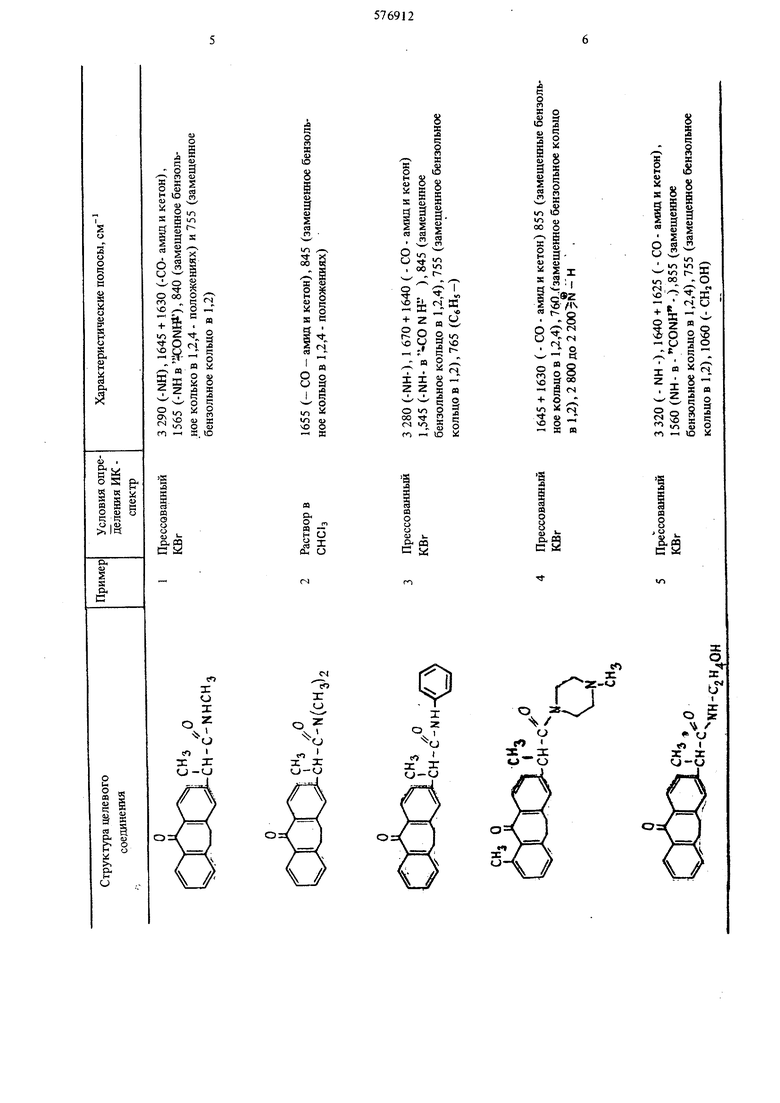
В таблице приведень показатели ИК-спектров соединений, полученных в указанных примерах.
а


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных дибензо /а, /циклогептена или их солей | 1975 |
|
SU564804A3 |
| Способ получения -трициклических производных азетидина или их оптических изомеров или их солей | 1976 |
|
SU715020A3 |
| Способ получения производных нафтиридина или их стереоизомеров или их солей | 1977 |
|
SU655314A3 |
| Способ получения 2-( -хлоралкокси) -2-оксо-1,4,2-диоксафосфоринанов | 1979 |
|
SU777040A1 |
| Способ получения производных 4-оксихинолинкарбоновой кислоты | 1986 |
|
SU1584749A3 |
| Способ получения трициклических соединений или их солей | 1975 |
|
SU591146A3 |
| Способ получения производных 2-амино-1,2,3,4-тетрагидронафталина или их солей | 1977 |
|
SU927110A3 |
| СПОСОБ ПОЛУЧЕНИЯ НЕНАСЫЩЕННЫХ АМИНОВ | 1971 |
|
SU420171A3 |
| Способ получения производных изоиндолина или их солей | 1971 |
|
SU528869A3 |
| Способ получения производных анилина | 1975 |
|
SU688123A3 |

a,
о„
SО
иI
(о
n
8
K
&{
Формула изобретения
8
или их солей, отличающийся тем, что соответствующее соединение формулы РзН, где РЗ имеет указанные значения, подвергают взаимодействию с хлорангидридом формулы
С-СОТ, где X - водород, алкил Ci-C4, галоген, тиоалкил GI -€4, трифторметил; RI и Rj - одинаковые или различные и представляют собой водород или алкил С) Сц; RS - алкоксил С, -С, 2,2 - диметил - 1,3 диоксолан - 4 - ил - метилоксигруппа или группа NR4Rs;R4 и RS - одинаковые или различные и представляют собой водород, алкил , фенил или совместно с атомом азота 84 и RS представляют собой пяти- или шестичленный гетероцикл, который в некоторых случаях может содержать дополнительно кислород, серу или азот, а также алкильный С,-С4 радикал, где X, RI , RJ имеют указанные значения, в среде органического инертного растворителя при О-30°С, причем когда RS представляет собой алкоксильный радикал или 2,2 - диметил - 1,3 даоксолан - 4 - ил - метилоксигруппу, то процесс проводят в присутствии акцептора хлористого водорода с последующим выделением целевого продукта в свободном виде или в виде соли, когда Вз - групда - NR4R5. Источники информации, принятые во внимание при экспертизе: 1.Патент США № 3647860, кл. 260-475, 1972. 2.Патент США №3641110, кл. С 07 С 69/76, 1972. 3.К. Бюлер и Д. Пирсон Органические синтезы 0.288, 1973.
Авторы
Даты
1977-10-15—Публикация
1975-06-05—Подача