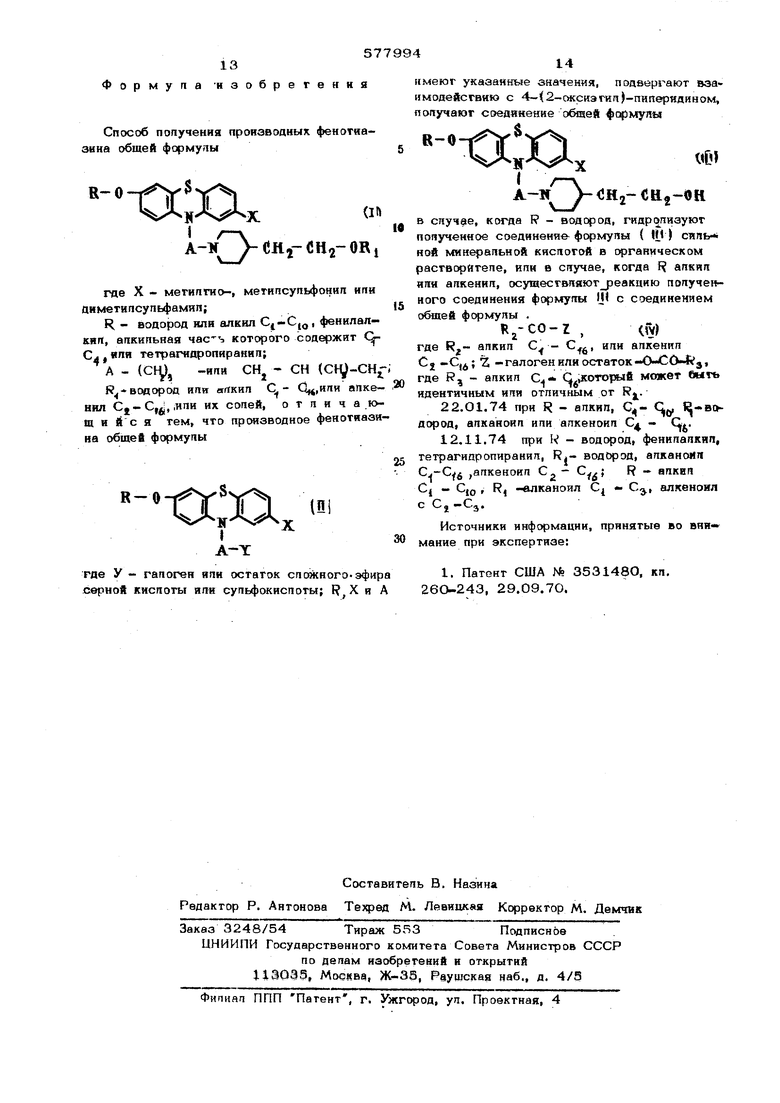
Изобретение относится к синтезу новых производных фенотиазнна, обпадахяцих фарма кологической активностью, которые могут найти применение в медицине. Известны способы получения N - аамешен ных фенотиазинов взаимодействием|М-гапоип апкиппроизвоцных фенотиазина с соогветству шнми аминосоединениями, в частности, с производными пиперидина |l Цепью изобретения явпяется получение новых производных фенотиазина, обпадакьших фармакологической активностью. Для постижения этой цепи получают производные фенотиазина обшей формуль L II П J А- СНз где X - метиптио-, метилсупьфонил- или виметилсульфамип; R - водород или алкил С - С фенилалкил, алкильная часть которого содержит С., или тетрагидропиранил; А - -(Сфд - или - CHj - СН(СН )R - или алкил Q ипи алкеил и,- , или их соли. Способ заключается в том, что производые фенотиазина обшей формулы Л Л . Л-Y где 1, X и А имеют указанное значение; У - галоген или остаток сложного эфира серной или сульфокислоты, подвергают вз имодействию с 4- (2-оксиэтил)- пиперидином, получают соединение общей формулы 8-«-i l h. & . . 1Г A-l/ -CHj-CHg-OH огда R - водород, полученное соединение ормулы ( 1П ) гидролизуют сильной минеальной кислотой в органическом растворитепе, ипи,в случае, когда R апкил ипи апкенип, осуществляют реакййю)полученного соепинений формулы 1 с соединением общей формулы, . Т -СО-7(IV) С или алкеннл С - С -С,Л -галоген или остаток - О - CO-R гае RJ- алкип, который может быть идеЙ1 иуным или отличным от R. Реакцию соединения формулы И с 4-{2оксиэтил)-пиперидином проводят в диметилформамиде в присутствии бикарбоната натрия пои температуре от до температуры ки пения реакционной смеси. Гидролиз соединений формулы Шдо соединаннй формулы 1( когда водород, ведут в присутствии сильной минеральной кислоты в органическом растворителе. Предпочтительно, испольэук}т соединение общей формулы Ш, где R - изопропил, бензил или тетрагидропиранил. Реакцию Ведут в хлороформе в присутствии серной кислоты и при температу ре до 10°С;. Получение соединений формулы I, в случае, когда R. - алкенил или алкил ведут взаимодействием соединения формулы с соединением формулы tV . В случае, когдаZгалоген, и в частности, хлор, целесообразно процесс проводить в инертном органическом растворителе (например в бензоле, толуоле или хлороформе), при температуре кипения 9ТОГО растворителя и в присутствии основного акцептора или без него. Когда Z - алк .нилоксилили алкенилЬксил, реакцию ведут в присутствии инертного органического растворителя, например хлороформа, или без него, при температуре от 5О G до темпер йтуры кипения реакционной смеси. П р и м е PI . Смееь 44,4 г 2-мётокс -в-диметилсупьфамйл-1й-(3.«яо5Н1ропйл)-фекотиазина, 13,7 г 4 окси:этилпипериш на .- ое- п .. ..:- лс-л -/,- и 35,8 г бикарбоната натрия в 450 см диметилформамида нагревают до 7 ч и перемешивают Раствор охлаждают, выпаривают досуха при аониже нном давлении (15 мм рт. ст.) при нагревании до 65 С. Сырой продукт навлекают 6ОО см дистилякрованной воды, за тем экстрагируют 450см хлористого метилена. Объединенные органические кстракты промывают водой, затем йодкисляют путем добавления раствора 115,2 г метансульфоновой |киспоты в 6ОО см воды. Этот кислый раствор экстра гируют в 6ОО см хлористого метилена, подщелачивают добавлением 15%-ного раствора едкого натра, экстрагируют 5ОО см хцдриегагр мв.ткпвщ. Органический экстракт «рвмьивют вОО емаиетиппираванкэй аады, высушивают над безводным сульфатом рия. Растворитель выпаривают при пониженHOiA давлении ( 15 мм рт. ст.) при . Получают 39, .7 г сырого 2-мегокси-в-диметипсульфамил-1О- -3 - (4 - оксиэтилпиперидино) - пропилJ - фенотиазина, в виде желтого аморфного порошка. Продукт чистят хроматографйчески на колонке, содержащей 400 г силикагеля (высота 500 мм, диаметр 45 мм). Раствор 39,4 г сырого основания, полученного выше, в ЗОО см хлористого метилена; элк ируют 4 л хлористого метилена, 2 л этилацетата, 2 л смеси этилацетат - ацетон (8О:20), 1 смеси этилаЦегатацетон (50: 50), 3 л ацетона. Ацетоновый элюат, содержащий очйщенное основание, концентрируют досуха при 15 мм рт. ст. Получают 27,6 г очищенного оснрвания в виде вязкого маслообразного вещества. 14,9 г полученного основания растворяют в 50 см кип5пцего этанола, добавляют кипящий раствор 2,6 г щавелевой кислоты в 15 см этанола, охлаждают, добавляют 25 см изолропанола. Выдерживают 4 ч при температуре 54 С, затем отфильтровывают полученные кристаллы, промывают в ЗО см охлыжденного до 5 С этанола, затем в 75 см охлажденного до 5 С изопропанола. Сушат при О,О5 мм рт. ст. 16 ч при 55 С. Получают 15,5 г оксалата 2-метокси-6-диметилсульфамил-Ю-13-(4-оксиэтиллиперидино)-пропил -фенотиазина с т. пл. 174-.. 62,6 г 2-метокси-6-диметилсульфамил-1О-(3-хлорпропил)-фенотиааина (с т. пл. 1Й4-126 С) палуЦаЮг взаимодействием 147 г 1-брок1-3 Хпорпропана t 84,4 г 2-метркси-6-диметилсуПьфаМйЛфвнотиазина в прксутствйн 25,8 г поташ, диспергированного в 300 сМ. мётилэтилкетона. 79,6 г 2-метокси-6-диметилсульфамилфенотиазина с т. пл. 196 - получают метилированием 74,5 г диметилсульфата, 168 г 2-окси-б-диметилсульфамилфенотиа зина в присутствии ЗО,8 г едкого натра, суспендированного в 182О см метилэтилкетона. 207,6 г 2-окси-6-диметилсульфамилфенотиазина с т. пл. 2О8-21О с получают восстановлением 250 г в-диметилсульфамил-фенотиазинона - 2 19О г гидросульфита натрия в смеси 1350 см метилэтилкетона и 450 см дистиллированной воды. 32О г 6-диметилсульфамилфенотиазинона - 2 q т. пп. 244 -245°С получают окислением 57О г 3 - диметилсупыЬамилфенотиазина раствором 1382 г хлорного жепеаа в 8000 ем аиетилпированной вэаы, П р и м а р 2. Смесь 9,2 г 2-метокои-6-метилтио-1О-(3-хлорпролип)-фенотказина, 3,2 г 4-оксиэтиппипериаина и 8,4 г бикарбонате натрия в 90 см диметилформамида греют при 120 С, при перемешивании в ч. Растворитель выпаривают при 0,1 мм рт. ci при во С. Остаток извлекают 80 см хлороформа и ВО см. дистиллированной воды подкисляют и переосаждают как указано в примере 1. Получают 7,9 г 2-метокси-6-мв- тилтио-10- 3-( 4-оксиэт илпиперидино)« ропилЗ фенотиазина в неочищенном сыром виде в форме аморфного порошка бежевого двета. Этот псфошок извлекают 15 см кипящего ацетонитрипа. Охлаждают 7 ч при температур 2О С, кристаллы отделяют фильтрованием, промывают 1О см йцетонитрипа и вО циэтилового эфира, высушивают при 45 С при пониАенно1у1 давлении (О,О5 мм рт. ст.) 17 ч. Получают 7,37 г 2 метокси-6-метиптио-lO- 3-(4-оксиэтилпиперидино)-пропипЗ фёвотиазина, с т. пл. 101-103 С. 10,1 г 2- летокси-6-метилтио-10- (3 -хлорпроаип)-фенотиазина получают вааимо- действием 47,5 г 1-бром-3-хпорпропана и 22,0 г 2-метокси-6-метилтиофенотиазина 2О,1 г 2-метокси-6-метилтиофенотиа:зина с т. пл. 152-154 с получают метилированием 37,8 г 2-оксй-в-метилтиофенотиазима.22,2 г диметипсупьфата в присутствии ЗО,1 г карбоната натрия в ацетоне. 37,8 г 2-окси-6-метиптиофенотиазина с т. пл. получают взаимодействием 45,0 г цинковой соли 2-амино-4 метилтиофена с 64,О г 2-хпоргидрохинона с т. пл. в присутствии 17,8 г едкого натра в тсже кислорода. Полученный, фенотиазинон; восстанавливают iti si-it) 81,0 г гидросульфита натрия. Пример 3. ;13,7г 2-метокси-&-метилсульфонил-1р-(3-хлорпропил)-фенотиа зина, 4,7 г 4-оксиэтиппиперидина и 12,0 г бикарбоната натрия в 125 см диметилформаМИДа греют при перемешивании 7 ч при 125 Затем по методике описанной в примере 1, получают 13,8 г сырого основания. Раствор полученного сырого основания в 150 см хлористого метилена очищают хроматографически на колонке, содержащей 13О г силика геля (высота : 45О мм, диамвтр:27 мм) элюируя ЗОО см хлористого метилена, ЗОО см смеси хлористый метилен-этилйцетат (5О;5О), 900 смэтилацетата, ЗООсм смеси этилацетат - ацетон (50:50), 9ООсм ацетона. Объединяют фракции, соответствующие элюированию чистым этилацетатом и смесьюэтипацетата-ацетон, и выпариваютраст ворители пои пониженном давлении (15мм. рт.с Получают 9,65 г очищенного основания в виде оранжево-желтого масла. Основание растворяют в 185 см безводного эфира. Выдерживают 24 ч при комнатной температуре, и 7 ч при 5 С, кристаппы отделяют фильтрованием, промывают 200 см эфира и высушивают при 45 С при пониженном давлении (О,О1 мм рт. от), 18 ч. Получают 8,0 г 2-метоксн-6-мвтилсульфонил-10-Т 3-( 4-оксиэтилпипериди-но)-Пропил -фенотиазина, с т..пл. 117°1.18 С. 15,0 г 2-.метокси-6-метипсульфонип-1О-3-хпорпропйл)-фенстиазйна с т. пл. 122 -124°С получают действием ЗО,4 г 1-бром-З-хлорпропана на 15,9 г 3-метипсульфонил-7-метоксифеноти93ина в присутствии 5,6 г 85%-ного измельченного поташа, растворенкого в 75 см метилэтилкетона. 16,06 г ; 2-метокси- 6- 4втилсульфонилфенотиазина с т. пл. 2 04-2О6 С получают вростановлением 47 г 2-метокси-в-метипсупьфонип-9 оксофеногназина с 28 г цинковой пылк в 175 см диметилформамица, 73 см уксусной киспотк и 73 смдистиплирован° 48, г 2-метокси-6-мвтилсупьфонип-9 .-оксофенотиазина с т. пл. получают окислением55,0г 2-.метокси-6-метилтио-. , -1-ацетилфенотиазина с т. пл. J-V J-JLVO ( в. 95 см 95%-ного этанола ,842 см перекиси водорода. Полученный сырой 2-метокси- -6-метилсульфонип-9-оксо-Ю-ацетилфено тиазин с т. пл. 160 С омыляют спиртовым раствором 11,2 г поташа в 2ОО см этанола. 29,6 г 2-метокси-6-метиптио-1О-оцетилфенотйазина ст. пл. 1О6-ЮЗ С полу- чают ацетипированим 26,2 г 2-метокси-бметилтиофенотиазнна с т. пл. 152-154с уксусным ангидридом. П р и м е р 4. Смесь 27,8 г 2-изопронокси-6-диметилсульфамил-1О-(3-хлорпропип)-фенотиазина, 8,2 г 4-оксиаэтилпиперидина, 21,1 г бикарбоната натрия в 265 см диметилформамида нагревают при 130°С 7 ч. Реакционную среду обрабатывают (как описано в примере 1). Получают 15 г очищенного основания. Лиофилизацией водного-раствора его хлоргидрата получают 11,6 г хлоргидрага 2-изопропокси- димегипсупьфамил-1О- 3-(4-оксиатилаиперидино) -пропил - фенотиазина с т. пл. 14О С. 160 г сырого 2-изопропокси-6-диметнпсульфамн№.10и(з- клорпропил) -фенотиазина получают взаимодействием 80,8 г 1-бром-3-хлорпропака с 52,0 г 2-изопропокси-6-диметипсупьфамнпфенотиазина с т. пл. . 42,8 г 2-изопропокси-©-димегипсупьфам фвнотиааина получают взаимодействием 33,8 2-иодпропана с 40,0 г 2 окси-6-димвтиг1. супьфамипфеыогиазнна, полученного как ука- аано в примере 1. П р и м е р 5. Смесь 2О г 2-изопропок си-6 метипсу пьфонид-1О 13-«л орпропил) -фенотиазина, 6,4 г 4 жси9типп11перидина и 16,5 г бикарбоната натрия в 170 смцкметипформамида нагревают при 15О°С 7 ч ЗО KfHH, п емешивают. Реакционную среду обрабатывают, как описано в примере 1. Получают 9,0 г 2-иаопропокси-б-мет ипсульфонил-10- 3-(4-оксиэтилпипери дино)пропип1 фенотиазина, с т. пп. . 128 г сырого 2-изопропокси-в-метил- супьфония-10-(3-хлорпропип )-фенотиазина получают взаимодействием 100 г 1-бром-Зг-хлориропана с 1 ОС г 2- изопропокСн- 6-ме типсульфонинфенотиаакнаст. пп. 179-180 С, 21,7 г 2-изопропакСи в-метйпсульфонил фенотиазина получают взаимодействием 17,0 2-иодпроиана с 19,0 г 2-окси 6-метипсульфонилфенотиазина с т. пл. 218-219 С, 126 г 2-окси-6-метилсуп ьфонипфенотиа зина получают восстановлением 175 г б-метипсупьфонилфенотиазинаг-2, растворенного в 155О см метипэгилкетона, с помощью 152,5 г гидросульфита натрия в 525 СМ дистиллированной воды. 130 г 6-метилсульфонилфенотиазина-2 с т. пл. 275°-28О°С получают окислением SOO г 3-метилсупьфонклфенотиазина с по, мощью 2,25 питров эояного раствора хлорного железа ( cl/ si,45). Примере. Смесь 24,3 г 2-гептилокси-6-диметипсульфамип-10-(3-хпорпропнл)-фенотиаэина, 7,1 г 4-оксиэтилпиперидина и 16,1 г бикарбоната натрия в.18О C диметилформамида нагревают До 130°8 ч., перемешивают. Охлаждают, выпаривают досу при пониженном давлении (15 мм рт. ст.) Промывают ЗОО см дистиллированной воды, экстрагируют 56О см хлористым метипеном. Объединённые органические экстракты подкисляют добавлением раствора 57,6 см метансульфоновой кислоты в 250 см воды. Органическую фазу промывают ЗОО см водного в%-ного раствора едкого натра. затем дистиллированной водой и высушиваю над сульфатом натрия. Раствори те ль выпаривают при 15 ммрт, ст. при 4U С. Получают 21,1 г сырого (2-ге П ти л окси-6-ди ме ти лсу льфа ми 71-1О - (4-оксиэтилпиперидино)-пропилн} енотиазина в виде вязкого масла коричневого цвета. Раствор 21 г этого основания э ЗОО см бензола очищают хроматографически на колонке со 150 гсиликагеля|(высота 450м диаметр 30 мм), эпюируя l,ti л бензола, 1 л смеси бензол-хлороформ (50:50), 3 я хлороформа, 2 л смеси хлороформ-этиладетат {5О:501, 1 л смеси хлороформ-этил адетат (33:6б), 3 л этилаавгата, 1л апвтова, 3 л этанола.. Объединяют элюаты, соответствующие люированию чистым этипацетатом и и концентрируют их при 15 мм рт. ст., высушивают полученный остаток при 2О 0,1 мм рт. ст. в течение 16 ч. Получают 9,6 г очищенного основания. Растворяют 9,2 г полученного основания в 150 см O.lN соляной КИСЛОТЬ при 30 С, ЛИОФ.ШИЗУ-, ют раствор при О,О1 мм рт. ст. и сушат 18ч при 5р°С и при 0,О5 мм рт. ст. Получают S,2 г хлоргидрата 2-гептилоксн-6-диметилсульфами л- 1О- 3- {4 -оксиэтилпиперндино) -пропил -фенотиазина с т. пл, около . 24,4 г 2-гептилокси-6-диметилсульфамил-1О {3 хлорпропил)-фенотиазина в виде вязкого масла получают взаимодействием. 31,3 г .1-бром-З-хлорпропанас 23,3 г 2нгептилокси-6-диметилсульфамнлфенотиа- зина в присутствии 5,6 г поташа, диспергированного в 70О см метилэтилкетона. 23,4 г 2-гептилокси-6-диметилсульфамил-фенотиазина с т.пл. 16О°-162 С получают взаимодействием 8,4 г 1-иод-гептана на 76,8 г 2-окси-6-диметнлсульфамш1фено- тиазина в присутствии 41,4 г поташа, диспергированного в 600 см метилэтилкетоны-. П р и м е р 7. Смесь 48,9 г 2-бензилокси-6-диметипсульфамил-10- (3-хлорпропил)-феноГйазина, 12,9 г 4-оксиэтилпипе ридина и 33,6 бикарбоната натрия в 400 см диметилформамяда нагревают до 13О-С 8 ч, перемешивают, охлаждают, раствэр выпаривают досуха при пониженном давлении {15 мм рт. ст), нагревая до 65с. Сырой продукт извлекают 150 см дистиплированной воды, экстрагируют 2ОО см хлористого метилена. Объединенные органические экстракты промывают 4ОО см воды. Органический экстракт высушивают над безводным сульфатом натрия. Растворитель выпаривают при 15 мм рт, ст, при 4О С, Получают 58,3 г сырого 2-бензилокси-6-диметипсульфамил-1О 3-(4-окснэтилпиперидино)-пропид -фенотиазина. Полученный сырой продукт очищают хроматографически на колонка, содержащей 20О г снликагеля (высота 62Омм, диаметр 27 мм), элюируя 6ОО см бензола, 70О см смеси бензол-хлористый метилен -(50:50), 2ОО см хлористого метилена, 600 смэтилацетат, 5ОО см смеси этипацетат-ацетон (5О:5б), 1200 смацетона, Элюаты, соответствующие трем послед- ним растворителям элюирования, объединяют, концентрируют при о, 1 мм высушивают ст. при . Попученвый остаток выртдерживают при этом давпенин и при эоой температуре в течение 2О часов. Попучают 28,4 г очищенного аморфного основания. Растворяют 12,0 г этого основания в 30 см безвадного хлороформа, аатем до6ав пяют 5,7 СМ 3,5 N сопянокиспого эфира. Растворители выпаривают при 15 мм рт. с и сушат при 0,01 мм рт. ст. при 18 ч. Попученный аморфный хпоргидрат л& Опекают 350 см дистиппированной воды, раствор обесцвечивают дс авпением 3 г активированного угпя, фильтруют, фипьтрат лисфипйзуют и высушивают при 0,05 мм рт.с л ч гч . гч. . хч ...п. при45С 18ч. Получают О. 5гхлоргидрата 2-бензилоксв-6-диметилсульфамил-10 3-(4-оксиэтилпиперидино )-лропил }фенотиазина с т. Ш1. 140°С. . 89,О г 2-бензйлокси-6-диметилсульфамил-Ю- (3-хлс пропил)-фенотиазина с т. ПЛ; 124°-126°С получают взаимодействие 92 г 1-бром 3-хлорпропана с 69,0 г 2«бензилокси-6- иметилсульфамилфенотиа-зина в присутствии 16,4 г поташа, диспергированного в23О см метилэтилкетона, 69,О г 2-бензипокси-6-диметилсульфамилфенотиазина с т. пл. 192-194 С получают взаимодействием 106,0 г хлористо го бензила с 200 г 2-окси-6-диметилсул1г фамилфенотиазина. П р и м е р 8. Нагревают при температуре около в течение 8 часов и при перемешивании смесь 16,0 г 2-тетрагидропиранилокси-6-диметилсульфамил-10-ГЗ-хлорпропил)-фенотиазина, 4,3 г 4-оксиэ илпиперидина, 11,О г бикарбоната натр и 135 см диметипформамида, нагревают до 130 С 8 ч, перемешивают, упаривают досу ха при пониженном давлении (15 мм рт. ст нагревают до 65 С, остаток промывают 15О см дистиллированной водой и 15О см хлороформа. Декантированную органическую фазу промывают 20О см воды, высушиваю затем очищают хроматографически на копон ке, содержащей 22О г силикагеля (высота 560 мм, диаметр 27 MI), элюируя 3 л хлороформа, 2 П этилацетата 2 л aueToka, 2 л метанола. Элюаты, соответствующие эпюированию этилацетатом и метанолом, объединяюти Концентрируют при пониженном давлении. высушивания при 0,О1 мм рт. ст. После 35 С, получают 9,6 г очищенного при аморфного основания. Растворяют 9,5 г основания в 25 см кипящего ацетонитрила. Охлаждают 4 при +2 С, кристаллы отделяют фильтрованием и промывают 1О см ацетонитрила пр температуре 5 С, затем 50 см диизопропипового эфира. Высушивают при пониженном авлении (0,05 мм рт. ст.) 18 ч при 5О С, получают 7,0 г 2-теграгидропиранипокси-6диметилсульфамип-10- 3-(4 -оксиэтилпипв. идино)-пропил -фенотиааина, с т. пп. при 29L-131 C. 15,7 г 2-тетрагидррпиранипокси-6-диметипсупьфамил-1О-( 3 -хлорпропил) ч|)енотиазина с т. пл. 150 152С получают йзаимодействием 102 г дигидропирана на 17,2 г 2-окси-6-дим9Тилсульфамил-10(З-хлорпропил)-фенотийзина в присутствии 0,1 см 8 н раствора HCJJ в этаноле. П р и м е р 9. Смесь 11,4 г 2-метокси-6-диметилсульфамил-1О- ГЗ-{4-оксиэтил . .. Q d пиперидино)-пропил1 -фенотиазина с 3,8 г гептаноипхлорида в 150 см толуола нагревают 6 ч, перемешивают, охлаждают, добавляют 75 см этилацетата, подщелачивают так, чтобы.температура не поднималась выше 5°С, добавляют раствор 2,3 г безводного карбоната натрия в 75 смдистиллированной воды.ПослеДекантации, водный слой, экстрагируют 100 ,см этилацетата. Органические экстракты объединяют, затем промывают 240 см дистиллированной воды. Органический экстракт высушивают над |сульфатом натрия и растворитель выпаривают. Получают 14,4 г 2-метокси-6--ДИметилсульфамил-10- З- (4 нгептаноилоксиэтилпипери-; дино)-пропилЗ -фенотиазина в неочищенном виде. К кипящему раствору 14,2 г полученного сырого основания в 25 см этанола добавляют нагретый раствор 2,0 г щавелевой .кислоты в 15 см этанола. Перемешивают, затем добавляют 2О смизрпропанола, охлаждают 4 ч при 5 °С ; образовавшиеся кристаллы отделяют фильтрованием, промывают 20 см этанола, затем ВО сми опропанола, высушивают при 55 ° С при О,О5 мм рт. ст. 18 ч. Попучают 9,85 г оксалата 2-метокси-6-диметилсульфамил-10- З- (4-гептанонлоксиэтнлпиперидино)-пропилJ фенотиазина с т. пп. 138-140 С. П р и м е р 10. Как описано в прим ре 9, исходя из 13,6. г 2-мeтoкcи-6-димeтилcyльфaмип-lO- З- 4-оксиэтилпиперидино)-пропил} фенотиазина, 6,1 г хлорангиврида ундецен - 1О-овой кислоты и 175 см . толуола, получают 17,1 г сырого 2-метокси-6-диметилсульфамил-1О- | S-(ундецен-1О-оил) -4-.-оксиэтилпиперидино1- пропил|фенотиазина. Растворяют 17,0 г основания в 25 см кипящего этилацетата, добавляют 2,3 г щавелевой кислоты в ЗО см кипящего |втипаце7ата, охлаждают, кристаллы отделяют фильтрованием, промывают 1О см этипацетата, затем высушивают при 4 5 С при 0,05 MM.pt. ст. 18Ч. Получают г оксалата 2-метокси в-димвтипсупьфамкп-1О-| 3-ундецен--1О-оип)- - этилпипврндинос пропигг)-фенотиазнна, с т. пл. 1222l24°C.П -р и м е р 11. Как описано в примере 5 9, на 10,0 л 2-метокси-6-метнптио-1О 3-l4-OKCHsTiuinHnepHnHHo)- ponHn -фенотиаайг на и 3,8 г гептаноипхпорида в 15О ск топуопа, получают 11,3 г оксапата 2-мегокси-6 -метиптио 1О 3- (4-гептаноипоксиэтип- 0 :рипвридино -«ропвп} фенотиазина, с тГпл. . , Пример 12. Как описано в примере 9, ив 10, 7 г 2-мегокси-в-метипсуп онн11«-1О З-{4-рксиэтилпиперидино)-пррпил i тиазитга г гептаноипхпорида в 150 смтолуопа, получают 11,6 г оксапата 2-метЪкси-0-метипсупьфОнип-10-,3- {4-гептаноип. оксиэтиптпиперидино)-пропип J фенотиазина, с т. пи. 13О-132 С. П р и м-е р 13. Смесь 11,5 г 2-бензоил. окси-6-диметилсупьфамил-1а-.|3-(4-окси9тилпиперидино)пропипД - фенотиазина с 22,6 Г уксусного ангидрида и 56,5 г безводного пиридина, нагревают ЗО мин от25 8О до 85 С, перемешивают, охпаждают и раствор выливают в 450 с.мпедяной дистиилирсванной воды, экстрагируют 400 хлороформа. Объединенные органические акстракты промывают BjjenoM 400 см с о ля-30 нойкислотыпрн С,за текГпромывают400см дистиппироаанной воды,-310смводного 1О%-ного раствора бикарбоната натрия и окончательно 6ОО см истилпйрованной воды Вбюушивают над безводнымсупьфатом нат- 35 , растворитель упаривают при 15 ммрг. ст. и температуре ниже .|Продукт сушат 18 ч при при 0,О1 мм рт. ст. Получают 10,0 г основания, которое иавлекают 100 см хлороформа, затем очи- 40 щают хроматографически на колонке, содержащей 140 г силикагеля (высота 5ОО мм, диаметр 20 мм элюируют 6ОО см хпороформа, этипацетата, -ЗОО см ацегона, 300 см метанола. Элюат, соотвегствук 15 щий элюированию этилацетатом, выпаривают при 15 мм рт. ст. при 20 С. Получают 8,2г амфорного продукта, который кристаллизуется при перемешивании в 8О см диизопропилевого эфира. После декантации растворите- «О ля добавляют 80 см диизопропипового эфира, выдерживают 3 ч при температуре 2 С, кристаллы отделяют фильтрованием, промывают 150 см диизопропилового эфира и сушат при 45 С 8 ч при О,05 мм рт, ст. Попучают 5,9 г 2-бензилокси-6-диметилсульфамил-10- 3-(4-ааетоксиэтилпиперидино)-п;ропил 3.-фенотиазина с т. пл. 94-96 С Пример 14. Смесь 17,35 г 2-метoкcи-6-димeтилcyльфaмил-lQ-| 3-(4-oкcи 128тлпипериднно)-пропилЗ-фенотиааина с 32,3 г уксусного ангиорида и 80 см беэводного пиридина нагревают 1 ч пря 8O,G, перемешивают, охлаждаюг, реакционную смесь выпивают в 150 см дистиппированнойводы,раствсчзупаряваютприО.бммрт.ст Попученный сухой остаток экстрагяруюг 40О см диизопропипового эфира, сушат при.О,О1 мм рт.ст. при 5О С 18 час. Получают 21,2 г вязкого месгеообраэного продукта, добавляют 20О см днстиппированной воды и 150 см хлороформа; смесь перемешивают при 5 С со 12О см насыщенно го раствора бикарбоната натрия. Декантиру- , ют и хпороформошлй спой промывают j 12Осм дистиппированной воды. Высушенный хлороформный раствор чистят хроматографичёски на колонке, содержащей 160 г сипикагеля (высота 58О мм; диаметр 28 мм), эпюируя 3 л хлороформа, 3 п этилацетата. Элюат,соответствующий элюированию этипацетатом, выпаривают при 15 мм рт. ст. при 45 С 1н полученный продукт высушивают при 0,01 мм рт. ст. при 20 С в течение 1В ч. Получают 16,3 г маслянистого основания оранжевого цвети. 1 г основания растворяют в 5О см этанола и добавляют раствор 2,7 водной щавелевой кислоты в 15 см этано а. Охлаждают при температуре 2°С 6, ч, |Кристаллы фильтруют и промывают 80 см этанола, затем сушат при пониженном дав-, лении {0,О1 мм рт. ст) при 50 С 18 ч. Получают 15,6 г оксалата 2-метокси-6диметипсупьфамил-1О-3- (4-ацетокси-этилпиперидино)-пропил-февотиазина с т. пл. 148-15О С. Пример 15. К смеси 10,9 2-изо„ропокси-б-диметилсульфамил-Ю. 3-(4-оксиэтилпиперидино) Цпропип енотиазина дО смбезводного хлороформа, добавляк)т за 30 сек 1О9 г концентрированной серной кислоты, охлаждают до 5°С. пёре., смесь выливают на 15О г иэмельченного льда, рН раствора доводят до 7,5.добавлением раствора едкого нат ( ai;33) охлаждают, экстрагируют 35О 6мхлороформа. Хлороформный раствор высушивают над 5 г безводного сульфата натрия, растворитель выпаривают при пониженном давлении и высушивают.Получают 5,1 г аморфного продукта, который растворяют в 35 см кипящего ацетонитрила, охлаждают, кристаллы отделяют фильтрованием, промывают 5 см ацетонитрила и высушивают при 50 ° С при 0,О5 мм рт. ст. 20. ч. Получают 3,9 г 2-окси-6-диметилсульфамил-1О 3-(4-oкcиэтилпипepидинo),пропил -фенотиазина с т. пл. 163-165 С. Формула -нзобрегения Способ получения производных фенотиазина общей формулы СНт OR I где X - мегипгио-, метипсупьфонип ипи днметипсульфамип; R - водород или алкил ,о, фенилалкип, апкипьная которого содержит С Сд, тетрагиаропираннл; .. ,, , 1, А - {СЬу, -или СН - СН (СН,-СН R водород или япкил ц- 0,или апкеНИЛ С5-С,,,ипи их солей, отпича. и и с я тем, что производное фенотиази на общей формулы где У - галоген ипи остаток слюнного.эфир серной кислоты или сульфокислоты; и нмеюг указанные значения, подвергают взаимодейсгвию с 4-(2-сжсиэгип)-пйперядином, огеучаюг соединение общей R-e-| Y 4j4,fA. А A-1/ V JH2-Cttg-OH в случае, когда R - водород, гидропизуюг попученное соединение формулы { 1И ) сипь ной минеральной кяслогой в сч ганическом растворителе, или в случае, когда f алкип или алкеннл, осутиесгвляют реакцию полученного соединения формулы И с соединением общей фс эмулы . R -CO-Z ,OV) рде апкип С - С, или алкенил - 1- - - С,-С.; Z-галоген или остаток-O-CCMVj, Д 1 „ Я,.который может вы«. идентичным или отличным от К. 22.O1.74 при R - апкип, Ц i -водород, алкаиоил или апкеноил С - Ц. 12.11.74 при R - , фенилапкип, тетрагипропиранил, R.- водород, алканоия С.-Су ,апкеноил С - R - алкип Cj - С,о , R, -влканоил С - С, алкеноил с Са -Cj, Источники информации, принятые во внимание при экспертизе: 1. Патент США № 3531480, кп, 26О-243, 29.09.7О.







Авторы
Даты
1977-10-25—Публикация
1975-01-21—Подача