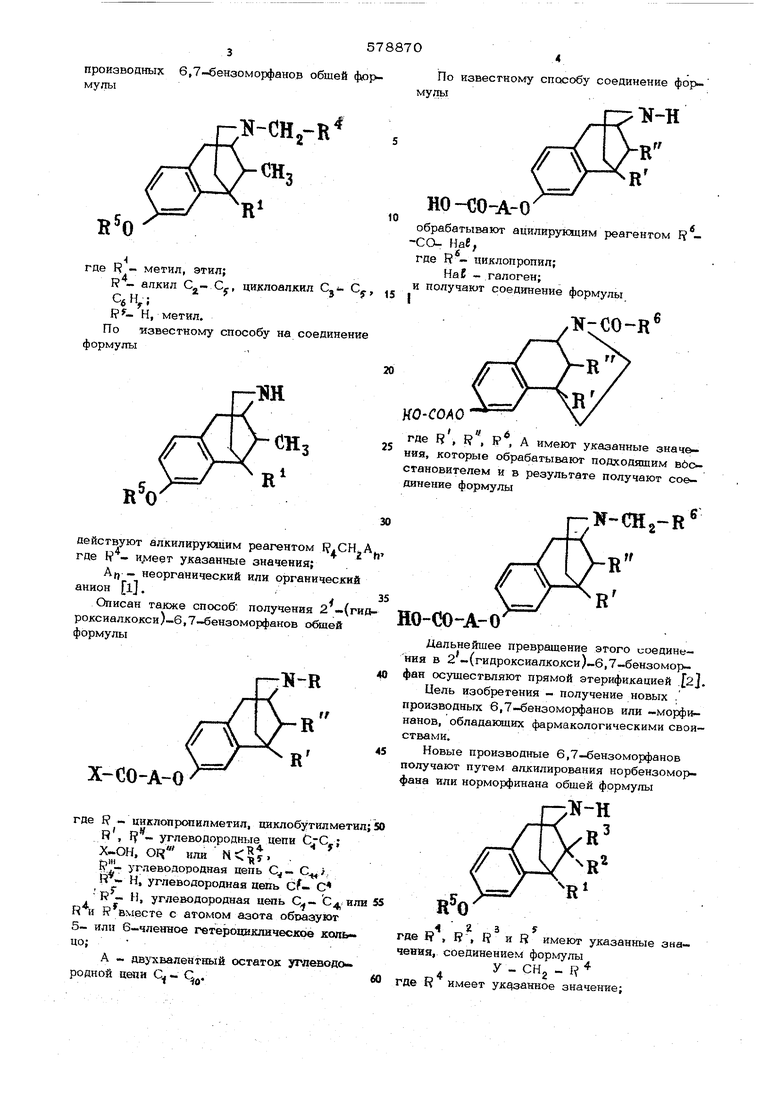
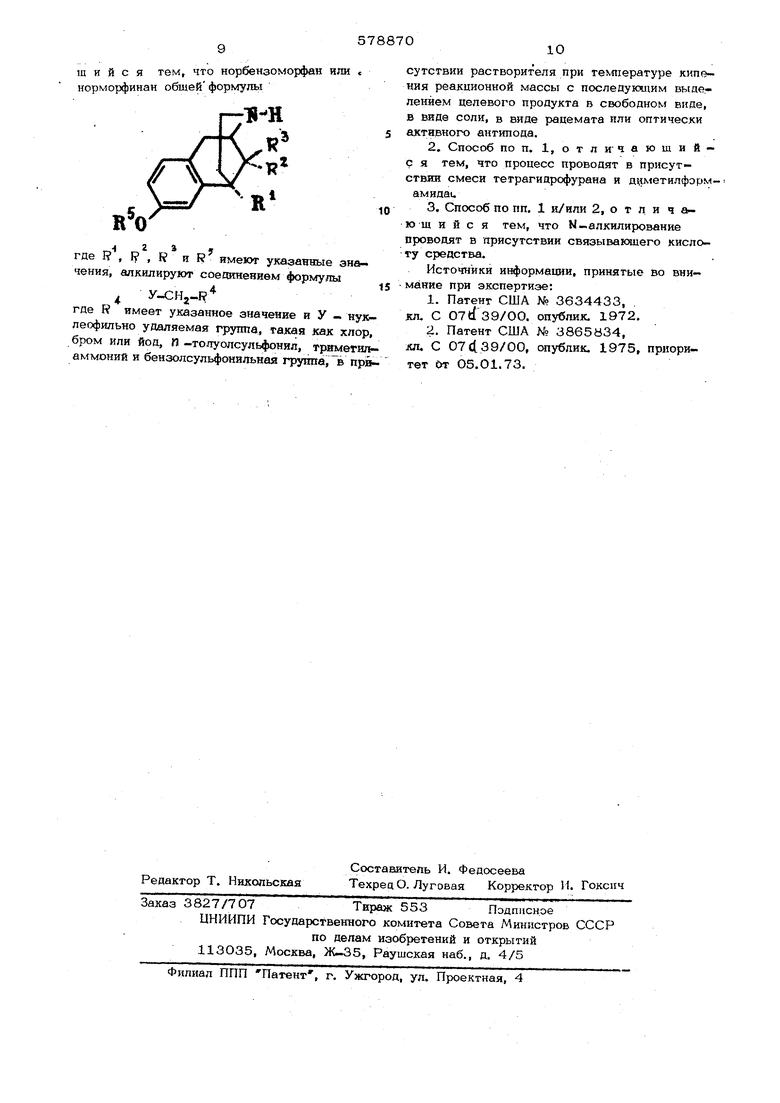
производных 6,7-йензоморфанов обшей ф01 .IJ-OHj-R где R - метил, этил; г ivicMUJii ain.4if алкил С - Су, циклоалкил С,- Су, Г U . СбН,5 J - Н, метил. По известному способу на соединение формулы г-ж действуют алкилирующим реагентом RlCH где R - указанные значения; Afj - неорганический или органический анион ij. Описан также способ получения 2 (ги роксиалкокси)-6,7-бензоморфанов формулы Х-СО-А-0 где 1 - циклопропилметил, циклобутилмети R, углеводородные цепи Х-ОН, OR или . . 1.- углеводородная цепь С С, R - Н, углеводородная цепь cf- С R - Н, углеводородная цепь С и Ни f вместе с атомом азота образуют 5- или 6-членное гетероциклическое копь- цо; А -. дв тсвалентный остаток углеводо родной цепи С - С. По известному способу соединение ИО-СО-А-0 обрабатывают ацилирукщим реагентом f - СО- Нав; где R - циклопропил; НаС - галоген; получают соединение формулы О-СОАО где R , I , Р , А имеют указанные значеия, которые обрабатывают подходящим вбсгановителем и в результате получают соеинение формулы К-СНв Н О-СО-А-0 Дальнейшее превращение этого соедини- ния в 2 -(гидроксиалкокси)-6,7-бензоморфан осуществляют прямой этерификацией .t2j. Цель изобретения - получение новых . производных 6,7-бензоморфанов или -морфи- нанов, обладаклцих фармакологическими свойствами. Новые производные 6,7-бензоморфанов получают путем алкилирования норбензоморфана или норморфинана общей формулы ;lf-H 1 г 3 f где I , I , 1 и R имеют указанные значения, соединением формулы y-CHg-if где f имеет указанное значение; У нуклеофильно удаляемая группа, такая как хлор, бром или- йод, П -толуолсупьфонил, .тримегиламмоний и бензолсульфонильная группа. Применяют эквимолярное количество или избыток алкилирующего средства и процесс проводят преимущественно в присутствии связывающего кислоту средства, например карбоната натрия или калия, гидрокарбоната натрия, триметиламина. Работают в инертных растворителях или в смеси растворителей (тетрагидрофуран и диметилформамид). Температуру реакции поддерживают в пределах точки кипения раст ворителя или смеси растворителей. Предлагаемые соединения являются осно- ваниями и могут быть переведены обычным способом в соли минеральных или органи- ческих кислот (соляная, метансульфоновая, щавелевая) . Способ позволяет получать как рацематы так и оптические активные антиподы, предпочтительно L (-)-формы предлагаемых соединений. Пример 1. 5,9-ci-диметил-2-(2-МО токсиметилфурил-(з)-метил-2 -окси-6,7- -бензоморфанметансульфонат. 1,63 г (7,5 ммоль) 5,9-еС-Диметил-2-окси-6,7-бензоморфана с 1 г гидрокарбоната натрия и 1,31 г (8,25 ммоль) 3-хлорметил-2-метоксиметилфурана в 10 мл абсолютного диметилформамида и 15 мл абсолютного-тетрагидрофурана в течение 4 ч, размешивая, кипятят с обратным холодильником. Затем в ротационном выпарителе под вакуумом упаривают и остаток экстрагируют 35 мл хлороформа и 35 мл воды путем встряхивания. После отделения хлороформо- вой фазы водный раствор экстрагируют еще 2 раза, каждый раз 15 мл хлороформа пу- тем встряхивания. Соединенные хлороформовые растворы промывают 30 мл воды, сушат сульфатом натрия и упаривают в вакууме. Остаток от упаривания состоит из сырого продукта превраихения, который с по- мо1лью метансульфоновой кислоты переводят в соответствующий метансульфонат. Для это го растворяют остаток основания примерно в 10 мл метанола, раствор подкисляют 0,72 г (7,5 ммоль) метансульфоновой кислоты. После добавления к раствору абсолютного простого эфира до начинающегося noMy нения кристаллизуется указанное соединение. Для окончания кристаллизации раствор останшяют стоять в холодильном щкафу в течение ночи. Затем отсасывают и промывают примерно 5 мл смеси метанол-эфир (l:2), затем 1О мл простого эфира. Крис- таллизат сушат сначала на воздухе, затем при температуре 8О С. Выход 2,9 г (88,5% от теории); т. пл. 220-225 С. После перекристаллизации из смеси метанола эфира т. пл. 224-225 С. П р н м е р 2. Гндрохлорид 5,9-cd-Диметия-2-(2-метоксиметил-фурил-(з)-метил)- . -2-метокси-6,7-бензоморфана. 2,68 г (0,01 моль) гидрохлорида 5,9- ot-диметил-2 -метокси-6,7-бензоморфана подвергают взаимодействию с 1,75 г (0,011 моль) З-хлорметил-2-метоксиметилфурана и 2,1 г гидрокарбоната натрия в 15 мл диметилформамида и 25 мл тетра- гидрофурана при размешивании и кипячении в течение 4 ч с обратным холодильником. Реакционную смесь аналогично примеру 1 разделяют.и продукт реакции кристаллизуют в виде гидрохлорида. Для этого остаток от упаривания экстрактов хлорс форма растворяют Б небольшом количестве абсолютного этанола (примерно 10-15 мл), раствор подкисляют 4 мл 2,5н. этанольной соля- ной кислоты и к нему добавляют абсолютный простой эфир до начинающегося помутнения. Раствор с выпадакяцими кристаллами оставляют отстаиваться в течение ночи в холодильном шкафу. Затем отсасывают, промывают сначала смесью этанола с простым эфиром (l:2) и затем простым эфиром. После высушивания на и затем в сушильном шкафу при 80 С получают ука- занное соединение с выходом 2,5 г (бв% от теории); т. пл. 140-142 С. После перекристаллизации из смеси этанола и простого эфира т. пл. повышается до 142-144°С. П р и м е р 3. 5,9-оС-аиэтил-2-окси-2-(2-метоксиметнл-фурил-(з)-мeтил)- -6,7-бензокюрфанметансульфонат. Из 1,83 г (7,5 ммоль) 5,9-оС-Диэтил- -2 -окси-6,7-бензоморфана аналогично примеру 1, путем взаимодействия с 1,32 г 2-метоксиметил-3-хлорметилфурана получают указанное соединение с выходом 2,8 г (80% от теории); т. пл. 172-174 С . После перекристаллизации из 90%-ного из смеси этанола и простого эфира т. пл. 173-175 С. П р и м е р 4. 2-Окси-2-(2-метоксиметилфурил-(З)-метил)-5-метил-6,7-бен- зоморфанметансульфонат. Из 1,52 г 2 -окси-5-метил-6,7-бе изо- морфана аналогично примеру 1 путем взаимодействия с 1,32 г 2-метоксиметил-3- -хлорметилфурана получают указанное соединение с выходом 1,8 г (57% от теории); т. пл. 160-163 С (она не изменяется после перекристаллизации из смеси этанола и простого эфира. П р и м е р 5. 2 Окси-2-(2-метоксиметил-фурил-(з)-метил)-5-Н -пропил-6,7-. -бензоморфанметансульфонат. Из 1,73 г ( 7,5 ммоль) 2 оксй-5- - Н-пропил-6,7-ббнзоморфана аналогично пр меру 1 путем взаимодействия с 1,32 г 2-м«гокск.етип-3-хлорметилфурана получают указанное соединение. Выход составляет 2,8 г (82,5% от теории); т. пл. 187-190 После перекристаллизации из смеси этанола и П1ХЮТОГО эфира т. пл. 189-191 С. П р и м е р 6. 5,9-о1-диметил-2(2-. -метоксиметк лфу рил-(з)-метил )2 -окси- -6,7-бензоморфанметансульфонат. 1,63 г (7,5 ммоль) 5,9-сС-Диметил-2 -окси-6,7-бензоморфана, 1,5 г карбоната калия и 1,5 г З-бромметил-2-метоксиметияфурана в 10 мл циметилформамида и 15 мл тетрагидрофурана нагревают с обрат ным холодильником при размешивании в течение 3 ч. После переработки аналогичто примеру 1 получают 2,35 г мегансульфона- та с т. пл. 223-224°С., П р и м е р 7. 5,9-сС-диметил-2 -окси -2-(2-метоксиметилфурил-(з)-метил)-6,7- -бензоморфанметансульфонаг. В смеси из 10 мл диметилформамида и 15 мл тетрагидрофурана кипятят в течение 1 ч с обратным холодильником 1,3 г З-хлорметил-2-метоксиметилфурана и 1 г триметиламина. В раствор добавляют 1,83 (7,5 моль) 5,9- ; -диметил-2-окси-6,7-бензоморфана и смесь нагревают с обрат- ным холодильником в течение 2 ч, В результате переработки аналогично пр меру 1 получают 2,79 г метансульфоната с т. пл. 174-.175°С. П р и м е р 8. 2 -ркси-2-(2-метокс15. метил-фурил-(з)-метил)-5-метил-6, зоморфанметансульфонат. В смеси из 10 мл диметилацетамида и 1О мл тетрагидрофурана с. обратным холодильником кипятят в течение 1 ч 1,75 г 3-оксиметил-2-метокСиметилфурана эквимолярное количество хлорида П - толу олсульфокислоты. После охлаждения добавля ют 1,8 г 2 -окси-5-метил-в,7-бензоморфана и раствор кипятят с обратным холодильником в течение 3 ч. В результате пер работки аналогично примеру 1 соединение получают с выходом 74% от теории; т. пл. 160-161°С. П р и м е р 9. Метансульфонат; 5,9-о(- диметил-2 -окси-2-(2-метоксимегил- .фурил-(З)-метил)-6,7-бензоморфана. К смеси из 10 мл диметилформамида и 15 мл тетрагидрофурана добавляют 1,О г 3-йодметил-2-мегоксиметилфурана, 1 г гидрокарбоиата натрия и 1,83 г (7,5 ммоль 5,.)- ct-диметил- 2-окси-6,7-бензоморфана и нагревают в течение 2 ч с обрат- iibiM холодильником. Переработку проводят сишлогично ujniMepy 1. Получают 85 г метансульфоната ст. пл. 174-175°С. П р и м е р 10. Метансульфонат 2-окси- -2-( 2-метоксиметилфурил-( 3 )-метил)-5- -метил-6,7-бензоморфана, 1,75 г З-оксиметил-2-метоксиметилфурана и эквимолярное количество хлорангидрида бензолсульфоновой кислоты нагревают в течение- 2 ч с обратным холодильником в смеси из 10 мл диметилацетамида и 10 мл тетрагидрофурана. После охраждения добавляют 1,8 г 2-окси-5-метил-6,7- -бензоморфана и раствор кипятят в течение 3 ч с обратным холодильником. Переработку проводят аналогично примеру 1. Получают указанное соединение с выходом 87% от теории; т, пл. 160-161 С. Формула изобретения 1. Способ получения N -(метоксиметилфурилметил)-6,7-бензоморфанов или -морфинанов общей формулы -. i tгде F и R - одинаковые или различные и означают атом водорода или алкил Cj; Н - атом водорода или метильная группа (бензоморфаны) J или R и I вместе 1,4-бу- тиленовая цепь, R атом водорода (-морфи- наны ); R - метоксиметилфурильный радикал форНзСО - СНпч и ил1 н,со-ш FJ- атом водорода, метильная или ацетиль,- ая группа, или их солей, отличаюш я и с я тем, что норбензоморфан или , норморфинан обшей формулы где Г , I , R и F имеют указанные значения, алкилируют соединением формулы А y-CHj-ff где R имеет указанное значение и У - нуклеофильно удаляемая группа, такая как хлор, бром или йод, П -толуолсуяьфонил, триметиламмоний и бензолсульфонильная гру1та,Пв присутствии растворителя при тектературе кипения реакционной массы с последующим выделением целевого продукта в свободном виде, в виде соли, в виде рацемата или оптически активного антипода. 2.Способ по п. 1, о т л и ч а JO ш и и с я тем, что процесс проводят в присутствии смеси тетрагидрофурана и щ метилформ3.Способ по пп. 1 и/или 2, о т л и ч аю щ и и с я тем, что Ы-алкилирование проводят в присутствии связывающего кислоту средства. Источники информации, принятые во внимание при экспертизе: 1.Патент США № 3634433, . кл. С 07tf 39/ОО. опублик. 1972. 2.Патент США № 3865834, JOI. С 07439/00, опублик. 1975, приоритет От 05.О1.73.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 2-(ФУРИЛМЕТИЛ)-6,7- БЕНЗОМОРФАНОВ | 1972 |
|
SU421187A3 |
| Способ получения 2-(фурилметил)-6,7бензоморфанов | 1972 |
|
SU479290A3 |
| Способ получения (метоксиметилфурилметил)6,7-бензоморфанов или морфинанов | 1973 |
|
SU511005A3 |
| Способ получения 2-тетрагидрофурил-6,7-бензоморфанов или их солей | 1975 |
|
SU588916A3 |
| Способ получения 2-(фурил-метил)6,7-бензоморфанов | 1972 |
|
SU467519A3 |
| Способ получения 2-(фурилметил)6,7-бензоморфанов | 1973 |
|
SU493066A3 |
| Способ получения 5,9 -дизамещенных 2-тетрагидрофурфурил-6,7-бензоморфанов или их солей | 1976 |
|
SU587859A3 |
| Способ получения -(гетероарил-метил) бензоморфанов или = морфинанов | 1974 |
|
SU543347A3 |
| Способ получения 5,9- -дизамещенных-2-тетрагидрофурфурил-6,7бензоморфанов или их солей | 1976 |
|
SU587858A3 |
| СПОСОБ ПОЛУЧЕНИЯ 2-{ФУРИЛМЕТИЛ)- 6,7-БЕНЗОМОРФАНОВ | 1972 |
|
SU440836A1 |


Авторы
Даты
1977-10-30—Публикация
1974-10-25—Подача