где Rt -С апкип;
Кл - атом водорода, метильная, метоксильная или метилтиогруппа, метилсульфиниль ная или метилсульфо тпьная группа;
Rj и Rg каждый - С.-С -циклоалкил; С -С;г-циклоалкилметил; Сз-С -метилциклоалкйп; &5 С7-ЦИклоалкенил; Cg-Cjt -алкил; тишил или группе
-(CHaVXQ(
Т1ричем, когда R4 - атом водорода, по меньшей мере один из Rj и Rj представляет собой группу, отличную от фенольной;
X - анион, имеющий заряд от 1 до 3;
У и Z каждый - атом водорода, галоид, нитрогруппа, цианогруппа, С -С -алкил, С1-С4-алкоксил или группа
fi Q или 1;
№- 1; 2 или 3, которые обладают биологической активностью и могут найти применение в сельском хозяйстве.
Известен способ получения производных пиразолина взаимодействием d , ;в-ненасыщеного кетона с производным гидразина l j.
Предлагается способ получения соединений общей формулы I, основанный на известной в органической химии реакции, заключающийся в том, что Ы , ;6-ненасыщенныи кетон общей формулы
R5-C-C CH
П о R .
где R,, R и Rj имеют вышеуказанные значения, подвергают взаимодействию с солью 1,2-диалкипгидразина общей формулы
Jll-TSIH-ЪГН-Вг-Ш: Ш
где Rt и Rg имеют вышеуказанные значения, в присутствии протонного растворителя при 50-15О°С.
В качестве анионов применяют галогениды, такие, как хлорид, бромид или йопид. 3 ацетат,сульфат, оксигруппу, бисульфат, метил сульфат, бензопсупьфонат, апкокси .()бевзрлсульфоиат, алкип-(С7-С)-бенэопсупь- фонат, предпочтительно топуопсупьфонат, такой как п-толуолсупьфонат, нитрат, фосфат, карбонат, бикарбонат, алкан-(С{-С,|)-супьфо нат, перхлорат, 9 е е Bf, Зэ, О-С-С-В м 58 1 е о Kg о-с сн-о-// j . R - атом водорода или метил; Щ - атом хлора или метип; Ry,- галоид, метил, галоидметил или дигалоидметил. Пример 1, Йодид 1,2-диметйл-3,5. -дифенил-2 -пиразолиния.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения эфиров тиолфосфорной кислоты | 1973 |
|
SU583762A3 |
| Гербицидная композиция | 1978 |
|
SU759046A3 |
| Способ получения производныхоксадиазолина | 1973 |
|
SU509232A3 |
| Способ получения -карбамилзамещенных -пиразолинов | 1973 |
|
SU479295A3 |
| Способ получения замещенных феноксиалифатических кислот или их производных | 1970 |
|
SU508175A3 |
| Способ получения бис-триазинобензи-мидазолов | 1974 |
|
SU509238A3 |
| Способ получения пиридобензодиазипимонов или их солей | 1976 |
|
SU587864A3 |
| Способ получения производных 1,4-диазепина или их солей | 1975 |
|
SU583758A3 |
| Способ получения пиридазинаминов, или их фармацевтически приемлемых солей присоединения кислот, или их стереохимических изомеров, или их таутомеров | 1985 |
|
SU1384198A3 |
| Способ получения стильбеновых соединений | 1974 |
|
SU633479A3 |

. 148-149
з з -С;
7 137-139
сн„ сн„ н
СНд CH.J Н , 3 з zy 4 сн, снз -CVcH, н са/з з
сн.
сНд сНд н сго 161-166
н
СНз СНз
X CHj
56,Об 4,74
(зазл.)
51,48 4,61
{разл.)
: 165-167
51,О7 4,,61 3 J
51,89 4,41
55,88 5,59
-J- 163-166 (разп.) 5,74 146-149 175-176 56,46 5,88 53,О1 5,38 94-96
Раствор дигиаройодида симм-диметилгидразина в абсолютном этаноле дигиаройодид симм-диметипгиаразина готовят из дигидрохпорида симмигиметипгиаразина (13,3 г. ОД мопь) в этаноле путем нагревания при температуре кипения с обратным холодильником с избытком йодистого капия (33,2 г, 0,2 мопь) в течение 3 час прибат ляют к суспензии халькона (15,6 г) в абсолютном этаноле. Реакционную смесь нагревают при температуре кипения с обратным холодильником при постоянном перемешивании и выдерживает в таких условиях 18 час. После охлаждения реакционной массы до комнатной
7Д5
7Д4 32,36
9,78 5ДО 55,50 4,66 7,62
7,59
6,76 29,7О 29,99
6,83 32,09 6,76 6,89
6,38 2Э,44
18,96
7,57
6,76
температуры растворитель выпаривают, а полученную смесь перемешивают с водным раствором йодистого калия. Образовавшееся вещество отфильтровывают и сушат. Получают 5,95 г (21%) целевого продукта, т. пп. 175-176°С.
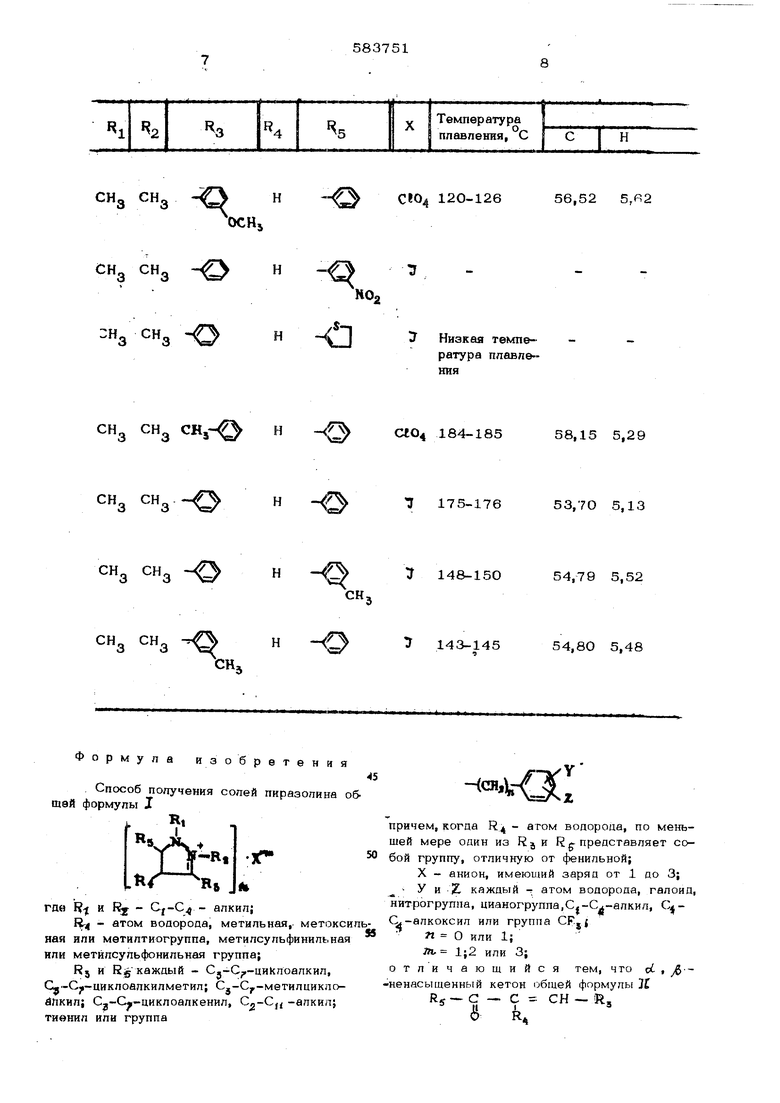
Пример 2. Аналогично примеру 1, используя соответствующие - bt ,.-ненась ц1енные кетоны и соль симм-диалкилгидразина или :соответствуюшую соль 1,2-аиалкил-3,5дизамешенного пиразопия, получают сопи пи-, разолина общей 4 ормупы I, показатели кото-; рых приведешь в таблице
55,10 5,40 7Д4
51,52 4,58 7,07 32,03
9,64 5Д7
51,52 4,68 7,О7 32,03
51,52 4,68 7,О7 32,ОЗ
56,16 5,71 6,90 56Д6 5,71 6,90 52,76 5,58 6,47 31,24
18,42
53,ОО 4,71 7,28
- 56,16 5,71 6,9О
н
CHg СНз
з
н СНд СНд СНз- н Н Сг04
Н 175-176
CHg СНз СНз з Н
н 143-145
СНз Формула изобретени Способ получения солей пиразолина общей формулы J .Д где 1 и 1 - С|-С - алкил; - атом водорода, метильная,- метокс ная или метилтиогруппа, метилсульфинильна или метйпсупьфонильная группа; Rj и Р каждый - Сд-С -циКпоалкил, С--С -циклоалкилметил; С -С -метилциклоdfiKHn; Cj-C -циклоалкенил, -алкип; тиенил или группа
tr Низкая температура плавпе-ния
53,70 5,13
54,80 5,48 184-18558,15 5,29 148-15054,79 5,52 -{сн4причем, когда R - атом водороца, по меньшей мере один из Rj и R представляет собой группу, отличную от фенильной; X - анион, имеющий заряд от 1 до 3; У и каждый - атом водорода, галоид, нитрогруппа, цианогруппа,С,-С -алкил, С Сх-алкоксил ипи группа CF.jj « О или 1; Ль 1;2 или 3; отличающийся тем, что ti , ненасыщенный кетон общей формулы ЗС R - С - С СИ - R,
9
9,35- 56,76 5,56 7,36
7,22
7,84
7,42
7,00
7,05
583751
10 Продолжение таблицы.
9,31
58,21 5,46 7,99
53{98 5,07 7,41
55,11 5,40 7,14
55,11 5,40 7,14
Авторы
Даты
1977-12-05—Публикация
1975-07-01—Подача