(54) СПОСОБ -ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 4Н-БЕНЗО 4 ,5 ЦИКЛОГЕПТЛ l , 2- ) ТИОФЕНА ИЛИ ИХ СОЛЕЙ
1
Изобретение относится к способу получения не описанных в .литературе производных 4Н-бензо 4,5 циклогепта l , 2-в тиофена общей формулы
где атом водорода, атом хлор или низший алкил,
низший алкил; RJ- низший алкил;
А и В оба обозначают aTcw водорода или совместно образуют связь,
или их солей.
Соединения формулы 1 и их соли обладают интересными фармакодинамическими свойствами имогут найти применение в медицине.Предлагаемый способ основан на известной реакции дегидратации карбинолов с использованием известных дегидратирующих средств, таких как HCf , ii РОх , метансульфокислота и др.
Использование в известной реакции соединений формулы 1 позволяет получить новые соединения форму.пы 1 .
Предлагаемый способ получения,заключающийся в том, что соединения формулы . А .17,
гдеТ,-Кз , А В имеют указанные выше значения, подвергают дегидратации известным способом с последующим выделением целевого продукта в виде основания или соли.
В соединениях формулы Я - преимущественно атом водорода. Во всех случаях заместители Т расположены в положении 6 или 7 кольца. Если R, - низший алкил, то этот радикал преимущественно содержит 1-3 атома углерода и представляет собой, в частности,метил. Обозначаемые символом Rg иизшие алкилиые остатки содержат преимущественно 1-4 атома углерода и представляют собой метил. -Радикал - содержит от 1 до 4 атомов углерода и представляет собой метил. А и В - атомы водорода и К-.- низший алкил, -предпочтительно метил.
Согласно изобретению отщепление воды от соединении формулы и проводят известным для аналогичных карбинолов образом, например, воздействием на соединения J подходящих средств,способных отщеплять воду, в некоторых случаях при добавлении инертного растворителя, например низшего спирта. В качестве способного отщеплять воду средства могут быть использованы минеральные или сильные органические кислоты, например спиртовый раствор хлористого водорода, смесь концентрированной соляной кислоты и ледяной уксусной кислоты, трифторуксусная, бензосульфокислота, или ангидриды кислот, или галогенангидриды кислот, например ангидрид уксусной кислоты,или хлористый тионил.
Соответствующие соединения формулы 1 выделяют из реакционной смеси и очищают с помощью известных способов . Свободные основания обычным способом переводят в их соли с кислотами
Пример. 4-(9, Ю-Дигидро-Ю-метил-4Н-бензо 4 , 5} циклогепта l, 2-t) тиофен-4-илиден-1-метилпиперидин,
Раствор, содержащий 17,0 г 9,10-дигидро-1О-метил-4-(1-метил-4-пиперидил) -4Н-бензо , 5 циклогепта. l, 2- j тиофен-4-ола в 350 мл 7 и. раствора хлористого водорода в изопропиловом спирте, нагревают в- течение 4 час при температуре кипения реакционной смеси затем реакционную смесь упаривают до получения сухого остатка, полученный остаток растворяют в 150 мл воды, раствор доводят до щелочной реакции посредством прибавления концентрированного раствора едкого натрия и экстрагируют хлористым метиленом. Экстракт промывают водок, сушат над углекислым калием, затем обесцвечивают животным углем и упаривают. Полученное в виде маслообразного остатка соединение перводят в среде этилового спирта в солянокислую соль (температура плавления солянокислой соли соединения 210°С (разложение из смеси ацетона и этилового спирта).
Исходное соединение может быть получено следующим образом.
Л. К суспензии 4,5 г порошкообразi:oro метилата натрия в 100 мл безводного диметилфорМамида прибавляют по каплям при 20-30с в атмосфере азота раствор, содержащий 10,0 г 2-ацетил-тиофена и 21,0 г диэтил-о-цианбензилфосфог1ата в 70 мл безводного диметилфО1 мамида, реакционную смесь перемешивают в течение 2 час при 40 С и 2 час при 100°С. Затем реакционную.смесь охлаждают до комнатной температуры и разбавляют 600 мл ледяной воды. Продукт с реакции конденсации зкстрагируют зфиром, экстракт промывают водой до нейтральной реакции промывных вод, раствор сушат над углекислым калием и упаривают. Полученный после упаривания ос таток хроматографируют при применении 110 г силикагеля смесью, состоящей из бензола и петролеяного эфира (1 : 4). Ввделенный в виде основной фракции 2- 2-(2 тиенил)-1-пропенил -бензонитрил; 1,6460, т. кип. 165-175с (0,15 0,7 мм рт.ст.) применяют без дополнительной очистки.
Б. Раствор, содержащий 14,0 г продукта в 400 мл этилового спирта, гидрируют В присутствии 4,0 г 5%-ного палладия на окиси алюминия в течение 24 час при 100°С и давлении 20 ати.После фильтрования через диатомовую землю раствор упаривают до получения сухого остатка. Полученный в виде маслообразного остатка (2-тиенил)-пропил -бензонитрил используют для дальнейших превращений без особой очистки.
В. К смеси, содержащей 24,0 г едкого калия в 60 мл монометилового эфира диэтиленгликоля, медленно прибавляют 12,0 г полученного выше продукта при 100°С.
Реакционную смесь перемешивают в течение 6 час при 160°С, затем охлаждают примерно до 70°С, реакционную смесь выливают в 30.0. мл горячей воды. После охла адения полученный раствор промывают толуолом, подкисляют концентрированной соляной кислотой и затем
экстрагируют диэтиловым эфиром. Эфирный экстракт промывают водой, сушат над сернокислым магнием и затем упаривают. Полученную в качестве остатка 2- 2-(2-тиенил)-пропил -бензойную кис, лоту перекристаллизовывают из гексана; т.пл. 66-68°С.
Г, Смесь 10,0 г этой кислоты и 100 г полифосфорной кислоты Нагревают 45 мин до 130°С.
Реакционную смесь охлаждают до 90°С и выливают в 500 мл воды. Полученный раствор экстрагируют хлористым метиленом, органический раствор промывают раствором углекислого натрия и водой, сушат над сернокислым натрием и затем
упаривают. Полученный после упаривания остаток перегоняют в высоком вакууме, причем 9,10-Дигидро-10-метил-4Н-бензо , 5 циклогепта l, 2- bJ тиофен-4-он перегонялся при 160-165 С (0,1 мм рт.ст)
0 т. пл. 67-68с (из эфира).
Д.4,8 гактивированного йодом магния заливают 60 мл безводного тетрагидрофурана и затем прибавляют несколько капель бромистого этилена. Затем прибавляют по каплям раствор 25,0 г 4-хлор-1-метилпиперилина в 160 мл беэводногЭ тетрагидрофурана, причем прибавление производят таким образом, чтобы в течение всего времени прибавления происходило кипение растворителя, и непосредственно после этого перемешивани продолжают в течение 2 час при темпера туре кипения реакционной смеси. Затем реакционную смесь охлаждают до и при указанной температуре добавляют по каплям раствор, содержащий 20,0 г 9,10-дигидро-10-метил-4Н-бензо 4,циклогепта l, 2-Ь тиофен-4-она в 100мл безводного тетрагидрофурана. После дальнейшего перег ешивания в течение 1,5 час при комнатной температуре и в течение 30 мин при температуре кипения реакционную смесь охлаждают, выливают в 300 мл 20%-ного раствора хлористого аммония и затем отделяют органическую фазу. Водный раствор экстрагируют хлористым метиленом, объединенные органические растворы промывают водой, сушат над сернокислым натрием и упаривают. Полученный в виде остатка после упаривания 9,10-дигидро-10-метил-4-(1-метил-4-пиперидил)-4н-бензо 4,5J циклогептаfl ,2-1 тиофен-4-ол дважды перекристаллизовывают из изопропиловог спирта; т.пл. 177-178 С. Пример. ,10-Дигидро-10-метил-4Н-бензо 4 ,5 циклогепта l, 2-b} тиофен-4-илиден -1-метилпиперидин. Работают так же, как в примере 1, приме няя вместо 7 и. соляной кислоты (изопропанол): а)5 н. бромистоводородную кислоту (спирт, или б)5 н. серную кислоту / спирт, или в) 10%-ную фосфорную кислоту / спир или. г)90%-ную метансульфоновую кислот спирт, или д)150 г ацетангидрида, или е)150 г пиперидина и 8 г тионилхлорида, получают после обработки реакционной смеси гидрохлорид получаемог соединения; т.пл. 210°С. (с р .вложени П р и м е р 2. 4-(10-этил-9,10-дигидро-4н-бензо 4 , 5 циклогепта l, 2- tJ тиофен-4-илиден -1-метилпиперидин. Раствор 15,0 г 10-ЭТИЛ-9,10-этилдигидро-4-(1-метил-4-пиперидил)-4Н-беизо 4 ,5 циклогепта l, 2-1 J тиофен-4-ола в 450 мл 3,5 н. раствора хлористого водорода в изопропиловом спир те нагревают в течение 4 час при темп ратуре кипения реакционной смеси и по лученное после обработки реакционной смеси целевое соединение переводят в гидрофумарат; т.пл. 220-221 С (из сме си метилового и этилового спирта). Исходный материал а) (2-тиенил)-1-бутенил1бензо нитрил, очистка неочищенного продукта посредством дистилляции; т.кип 150-АБЗ С (0,2 мм рт.ст) ; б)2- 2- ( 2-тие1 ил) -бутил бензонитрил, очищен посредством дистилляции; т. кип. 128-132 C (0,1 №-1 рт. ст) ; в)2-С2-(2-тиенил)-бутил бензойная кислота, подвергают дальнейшей переработке без дополнительной очистки; г)10-ЭТИЛ-9,10-дигидро-4И-б.ензо 4 , 5 циклогепта l, 2- Ь 1 тиофен-4-он , очищен с помощью дистилляции; т, кип. 185-190 С°(0,1-0,15); д)10-ЭТИЛ-9,10-ДИГИДРО-4-(2-метил-4-пиперидил)-4Н-бензо 4,5 циклогепта 1,2- тиофен-4-ол, получен из 2,4г магния, 12,5 г 4-хлор-метилпиперидина и 10 г 10-ЭТИЛ-9,10-дигидро-4Н-бензо , 5 циклогепта l , 2-1э тиофен-4-она в 150 мл тетрагидрофурана; т.пл.145- 148°С (из изопропилового спирта). Примерз. 4-|.10-Метил-4Н-бензо 4 , 5J циклогепта l, 2- } тиофен-4-илиденУ-1-метилпиперидин. Целевое соединение получают по примеру 1 из 1,0 г 10-метил-4-(1-метил-4-пиперидил) -4Н-бензо 4 , 5J циклогепта l,2-b тиофен-4-ола в 40 мл 3,5 н. раствора хлористого водорода в изопропиловом спирте. Температура плавления солянокислой соли ниже 295°С. Исходные соединения получают следующим образом. Д. Смесь 20,0 г 9,10-дигидро-10-метил-4Н-бензо 4 , 5 циклогепта l, 2- b тиофен-4-она, 15,6 г -бромсукцинимида и 0,5 г перекиси дибензоила медленно нагревают в 150 мл безводного четыреххлористого углерода до 70с, причем происходит экзотермическая реакция, и непосредственно после этого нагревание продолжают в течение 2 час при температуре кипения реакционной смеси. После охлаждения отфильтровывают выделившийся в осадок сукцинимид, фильтрат упаривают до сухого состояния и полученный остаток нагревают в 130мл триэтиламина в течение 2 час до температуры кипения. Затем растворитель упаривают, остаток растворяют в хлористом метилене и воде, органическую фазу отделяют и промывают 2 н. раствором соляной кислоты и затем водой. После отгонки растворителя полученный остаток перегоняют в глубоком вакууме, причем 10-метил-4Н-бензо 4 , 5 циклогепта 1,2-}з тиофен-4-ОН перегонялся при температуре 205-210°С (0,1 мм рт.ст.); т. пл. 75-76°С (из диэтилового эфира). Б. 10-Метил-4-(1-метил-4-пипе1 идил) -4Н-бензо 4 ,5 циклогепта l ,2-Ь тиофен-4-ол, полученный из 1,2 г магния, 6,8 г 4-хлор-1-метилпиперидина и 5,4 г 10-мвтил-Н4Н-бензо 4,5 циклогепта 1,2- тиофен-4-она в 50 мл безволного тетрагидрофурана, подвергают дальнейшей переработке в неочищенном виде. По аналогии с примером 1 отшеплением воды от соответствующих производных 10-алкил-4-(1-алкил-4-пиперидиЛ)-4Н-бенэо 4 , 5| циклогепта l ,2- тиофен-4-олов также получают следуюиие производные 10-алкил-4-(1-алкил-4-Г1Ипериаилиден) -4Н-бензо 4 , 5 циклогепта j , 2-fj) тиофена, результаты приведены в таблице.
Формула изобретения
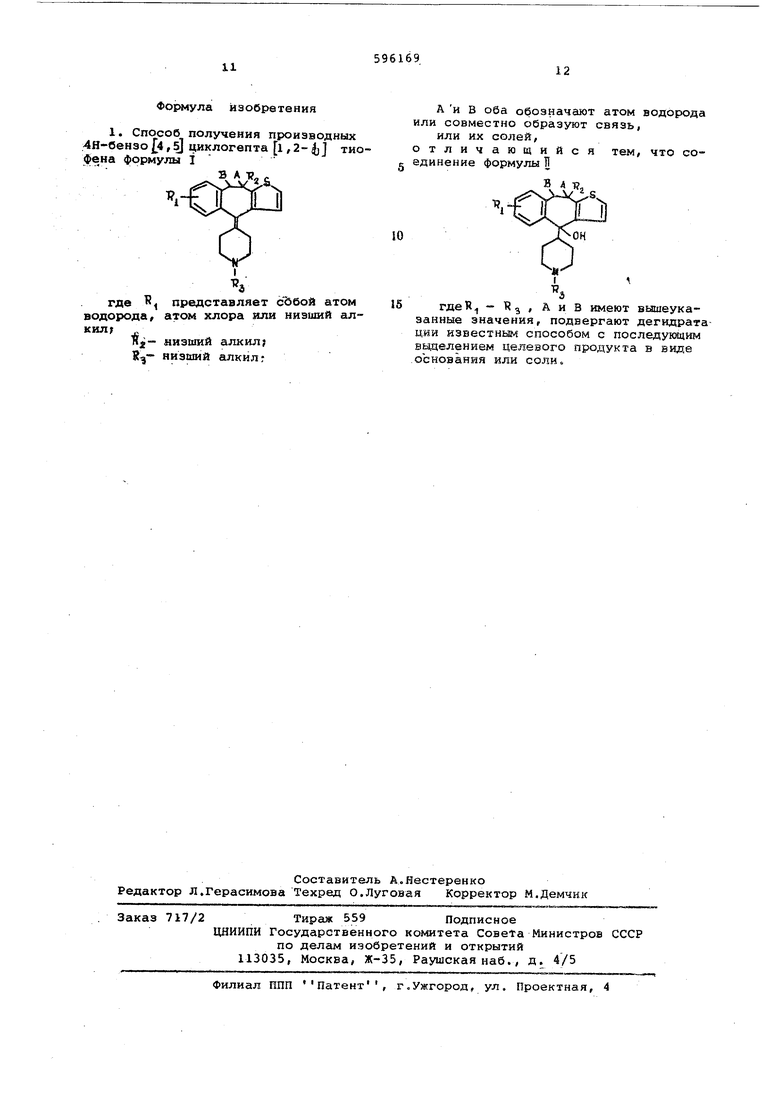
1. Способ получения проиэводных 4Н-бензо 4,5 циклогепта lf2-|jj тиофена формулы 1
где представляет сЬбой атом водорода, атом хлора иля низший алкил;
iSjj- низший алкил; R:,- низший алкил г
А и В оба обозначают атом водорода или совместно образуют связь,
или их солей, отличающийся
тем, что соединение формулы Б
В А
гдеН - 3 А и В имеют вышеуказанные значения, подвергают дегидрата
ции известным способом с последующим ввделением целевого продукта в виде .основания или соли






Авторы
Даты
1978-02-28—Публикация
1975-03-31—Подача