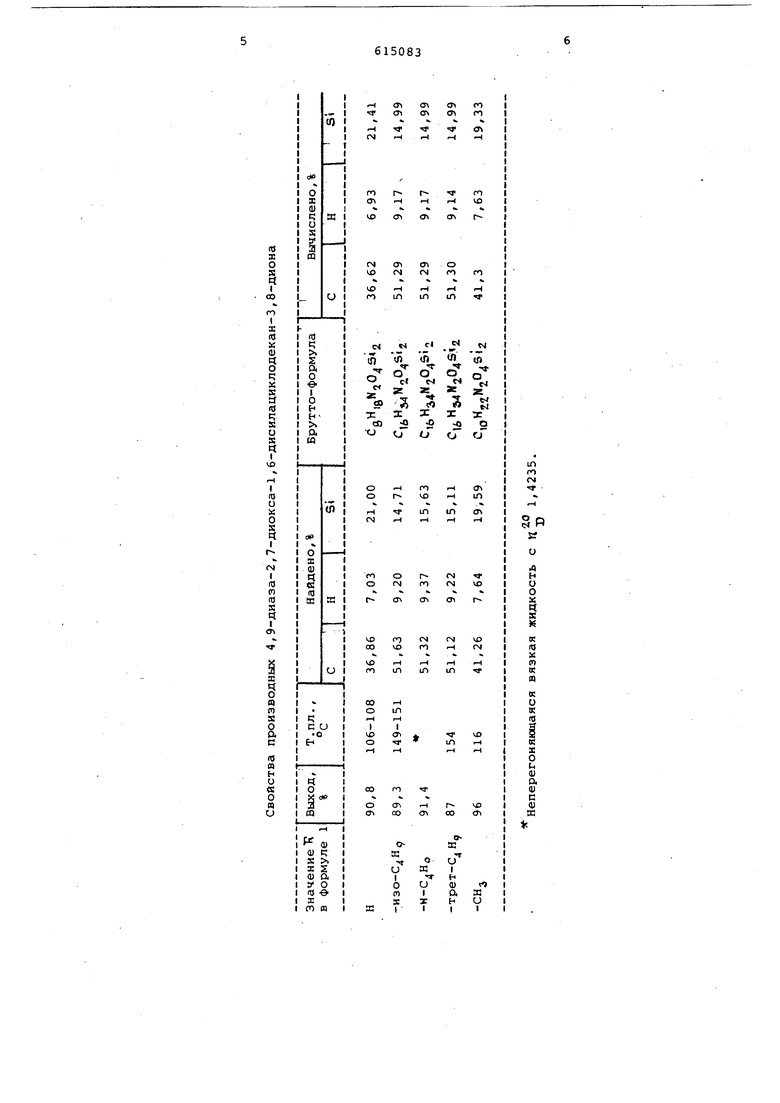
лалкоксидиметилсиланов с гексаметилдисилазаном при температуре кипения последнего. Наиболее близким к описываемому способу является способ получения соединений формулы I, заключающийся в том, что силилированный eJ-аминосилан, а именно W -(триметилсилил)-М-(алкил)амииометилалкоксидиалкилсилан подвергают взаимодействию с двуокисью углерода при 20- . 2. К недостаткам указанного способа следует отнести предварительную силильную защиту карбаминосилана, кото рая сопряжена с необходимостью утилизации NH СЕ и аммиака. Целью изобретения является упроще ние процесса. Указанная цель достигается за сче того, что kXi -аминосилан общей формулы 1 н N-«iH - i -ОСНз , / Н 5 К - водород, алкил с Сд-Сд аллил подвергают взаимодействию с тримети силиловым эфиром диэтилкарбаминовой кислоты. Отличит льньм признаком предложенного способа является осуществление взаимодействия (Х, -аминосилана общей формулы . N-(iH2 $i-ОЙНз , гл/ Iгде К - водород, алкил с , аллил, с триметилсилиловым эфиром диэтилкарбаминовой кислоты. Реакция протекает одинаково успешho как в среде органических растворителей, так и без них. Пример. В колбу загружают 10.2г (0,07 моля) аллиламинометилметоксидиметилсилана, 13,4 г (0,07 моля) уретана Et2NC(0)OSi(Me)3 и 13,4 г абсолютного изооктана. Через 10 ч выпавший осадок отфильтровываю7 и выделяют 11,3 г (93,3%) 1,1,6,6.-тетраметил-4,9-диаллил-4, 9-диаза-2,7- диокса-1,6-дисилациклодекан-З,8-диона с т.пл. 127-130с. Пример 2. В колбу загружают 14.3г (0,1 моля) аллиламинометилметоксидиметилсилана и 18,9 г (0,1моля) уретанае12КС(0)051(МеУа и через 8 ч выделяют 31,6 г (94,а%) 1,1,6,6-тетраметил-4,9-диаллил-4,9-диаза-2,7-диоксана-1,6-дисилациклодекан-з , 8-диона с т.пл. 127-129С. Свойства других соединений, полученных в аналогичных условиях, приве-. Г,ены в таблице. .7615 Формула изобретения Способ получения производных 4,9-диаза-2,7-Диокса-1,6-дисилациклодекан-3,8-диона общей формулы OC(0)N(IlJ СКг (СНз), ЦС/Нз) J ,/ СНгК(В)С(0)0 где В - водород,алкил Cvj-C ,аллил,на основе ей -аминосилана, от л и ч а ющ и и с я тем, что, с целью упрощения процесса,с4.-аминосилан общей формулы 3 СИ 7 , - 3 где R имеет указанные значения подвергают взаимодействию с триметилсилиловым эфиром диэтилкарбоновой кислоты. Источники информации, .принятые во внимание при экспертизе: 1. Миронов В.О. и др.. Реакции раеширения цикла производных 2,5-дисилапиперазина, ЖОХ, 1973, № 3, с.. .2573. 2. Авторское сврщетельство СССР 499266, кл. С 07 J 7/18, 1975.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 4,9-диаза2,7-диокса-1,6-дисилациклодекан-3,8-дионов | 1974 |
|
SU499266A1 |
| Способ получения органосилилметилкарбаминоилхлоридов | 1974 |
|
SU527436A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2,2,7,7-ТЕТРАМЕТИЛ-4,9-БИС(ДИМЕТИЛАМИНО)-ТЕТРАГИДРО-1,6,4,9,2,7-ДИОКСАДИАЗ АДИСИЛЕЦИН-5,10(2H,7H)-ДИОНА | 2002 |
|
RU2215744C1 |
| Способ получения 0-силилуретанов | 1976 |
|
SU737402A1 |
| Способ получения дифенилмочевины | 1976 |
|
SU583126A1 |
| Способ получения диметилдихлорстаннана | 1977 |
|
SU721444A1 |
| Способ получения о-силилуретанов | 1976 |
|
SU745904A1 |
| Композиция на основе синтетического полимера | 1972 |
|
SU455547A3 |
| Способ получения силиловых эфиров карбазиновых кислот | 1974 |
|
SU570613A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ угТ-ДИЛАКТОНОВ ДИКАРБОНОВЫХ КИСЛОТ | 1971 |
|
SU317652A1 |


Авторы
Даты
1978-07-15—Публикация
1976-04-12—Подача