(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2-НИТРОИНДАН 1,3-ДИОНА ИЛИ ИХ СОЛЕЙ









| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ 3-ОКСО-19-НОР-А4-СТЕРОИДОВ | 1974 |
|
SU439089A3 |
| 1,3-Диалкил-1,3-диазапирен-2,8-дионы-, обладающие люминесцентными свойствами | 1975 |
|
SU550387A1 |
| Способ получения спирогидантоиновых соединений или их солей | 1977 |
|
SU741795A3 |
| Способ получения спиробензоциклануксусных кислот | 1973 |
|
SU491233A3 |
| СПОСОБ ПОЛУЧЕНИЯ3,4,4'- | 1969 |
|
SU239346A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2-ОКСИЦИННАЛ10ИЛЦИКЛОПЕНТАНДИОНА-1,3 | 1971 |
|
SU436485A3 |
| ВИ&ЛИО'^ГК^ | 1973 |
|
SU372815A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ДИФЕНИЛАМИНА, СОДЕРЖАЩИХ ЭЛЕКТРОНОАКЦЕПТОРНЫЕ ЗАМЕСТИТЕЛИ | 1969 |
|
SU233679A1 |
| Способ получения 4-окси-3-нитрокарбостирилов | 1974 |
|
SU578869A3 |
| Способ получения производных пиразола или их солей или эфиров органических кислот | 1976 |
|
SU649315A1 |

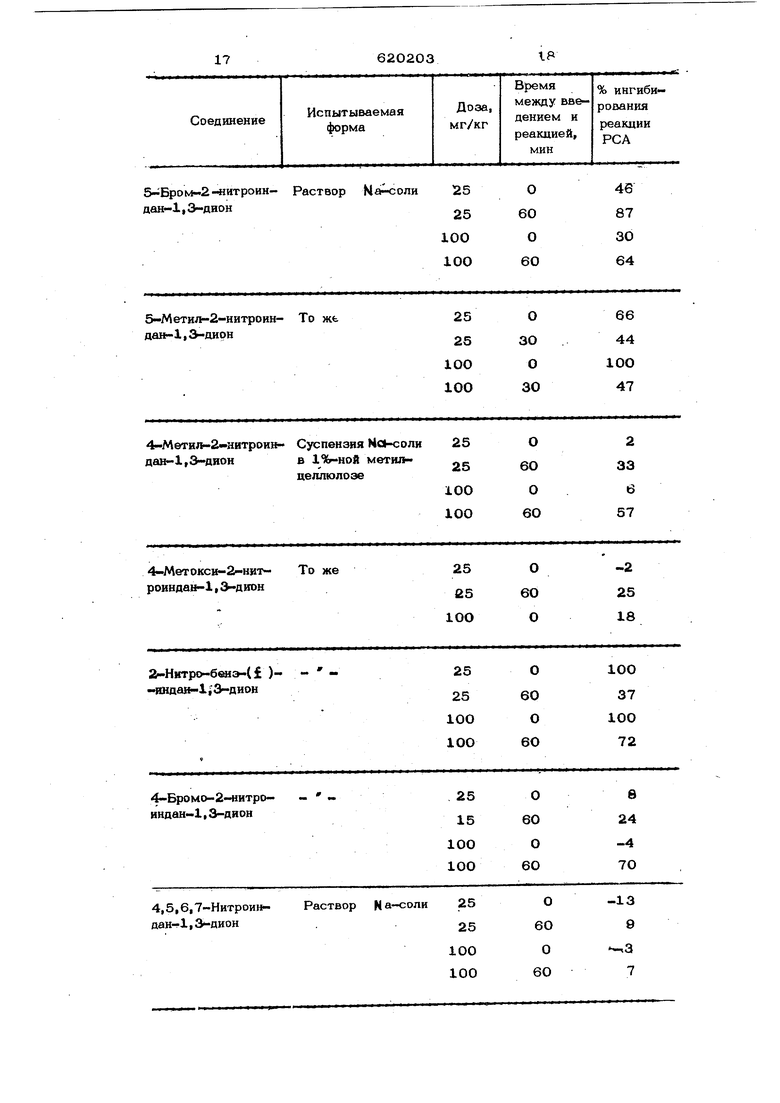
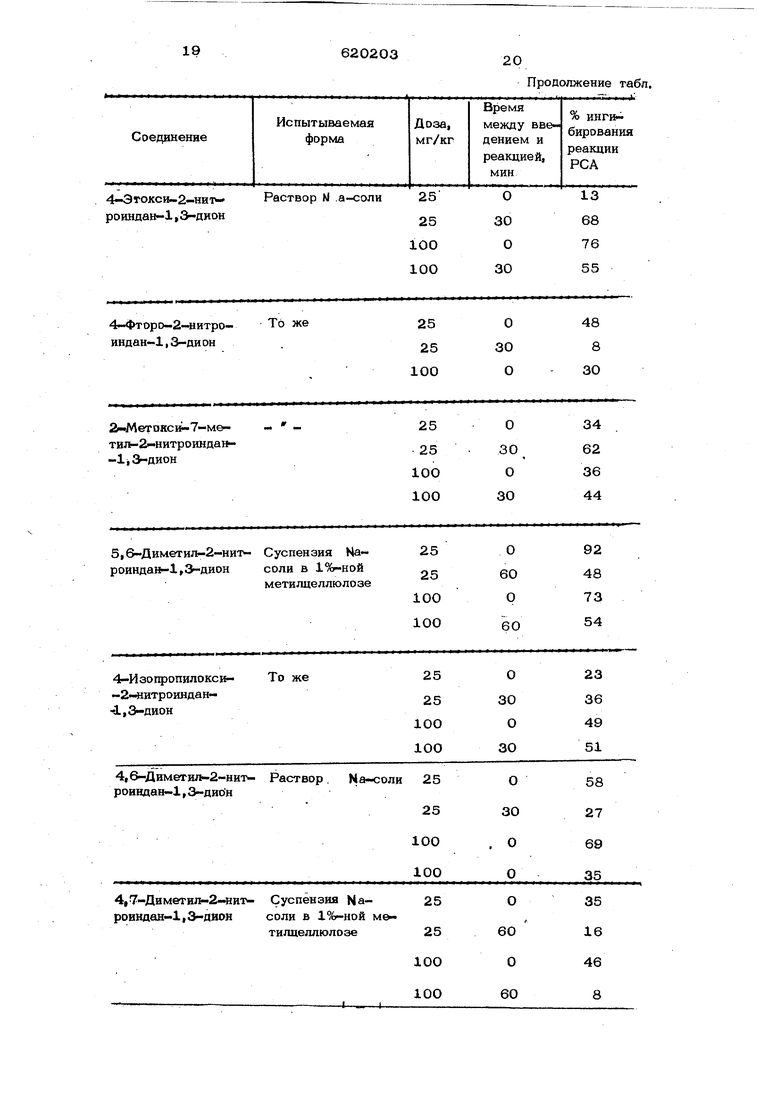
Изобретение относится к способу полу ченйя новых производных 2-нитроиндан-1 3-диона и их солей, которые могут найти щзименеиие в качестве физиологически активных соединений. Известеи способ получения производных 2 иитроиндан-1,3-диона нитрованием производаых индан-1,3«диона дымящей кислотой при температуре ииже 25°С, предпочтительно 5-10°С, в среде безводиого афира у.. Однако, не известно, что полученные производные могут обладать физиолошчес- КИМ действием, в частности служить анти шлергическими препаратами. Целью изобретения является разработка способа получения новых гфонзводных 2-нитройндан-1,3-диона, обладающих анти- аллергическим действием. Способ получения производных 2-нитроИндан-1,3-диона общей формулы где I - К представлшот собой каждый атом водорода или алкил С.-С-, алкоксигруппу Ц-С-, фенид-, пиридилрадикал или атом галогена} или смежные группы R и1,Р, иI илиRJ и1 ; могут представ лять собой тримегилен- или твтраметиленовую группу, или, если указанные группы находятся в «положении 1,4, означают бута-1,3-диеииловую группу, причем, если Р - водород, хлор, бром, метил, Р ® означаег водород или если Rjj - метоксигруппа, . бром, хлор, йод, то RJ Нэ я&ляется водородом, или их солей, заключается в том, что производное индан -1,Э-диона общей фор мулы где R - R имеаот указанные значения, подвергают взаимодействию с дымящей азотной кислотой в среде растворитеяя с последующим выделением целевого проду та в свободном виде или в виде соли. Новые соединения обладают выраженной антиаллергической активностью, в бол шинстве случаев превосходящей активность явунатриевой соли кромогликолевой кисло- ГЫ (см, таблиду), обладающей также указакной активностью. . Пример. а) 4-Метилиндан-1,дион. К 5О%г-ной суспензии гидрида натрия (8,2 г, 0,17 моля) в минеральном масле добавляют раствор диэтилнй метилфталата (28 г, 0,119 моля) в этиладетате (4Ом и смесь кипятят с обратным холодильником с периодическим перемешиванием на даровой бане 4 час. После охлаждения ф1Шьтруют светло-желтую натриевую соль Я промывают небольшим количеством колодного этилацетата. К высушенной соли ( 27,2 г) быстро добавляют горячий (8О°С) раствор хлористоводородной кислоты ( 48 мо ля) в воде (48О мл) и продукт выдерживают при до прекращения декарбексилирования (7 мин), охлаждают до б С и бледно-желтое твердое вещество от фильтровывают и промывают водой. Перекристаллизация из бензола дает бледно-желтое кристаллическое вещество с т. Ш1. 125-12в°С. Найдено, %:С 75,38} Н 5,О4. Вычислено, %: С 74,99} Н 5,03. б) 4-Мети; -2 нитроиндан-1,3-дион. К перемешиваемой суспензии 4-метил-1,3 индандиона (1,02 г, 0,ОО6 моля) в безводном эфире (5 мл) при 10 С.добавляют дымящую азотную кислоту( 2,0 мл). Через 10 мин из полученного темного раствора оседает светло-желтое твердое вещество. Его отфильтровывают и промы- вают 5 Н. хлористоводородной кислотой. Перекристзллизадней из смеси вода-хлористоводиродная кислота получают продук с т. пл. 108-10е®С, Найдено, %:С 5вДб}Н 3,74} N16,32 O. Вычислено,%: С S6,O} Н 3,76} N 6,54 Выход 75%. Пример 2. а)5-Метилиндан-1,3-дион. Получают в условиях примера 1а из ДИ9ТИЛ-4-метилфталата, т. пл. (бензол) 114-11бс. Найдено, %: С 75,04; Н 5,19. . Вычислено, %: С 74,99i Н 5,ОЗ. . б)5-Метил-2-нитроиндан-1,3-дион, Нитрованием &-метилиндан-1,3-диона в условиях примера 16 получают продукт нитрования с т. пл. 115-117°С (вода, хлористоводородная кислота). Найдено, %:С 58,43} Н 3,39} N6,86. Вычислено,%: С 58|54}Н 3,44} N 6,83} Выход 36%. П р и м е р 3. а) 4-Метоксииндан-1,3-дион. Диметил-3-метоксифталат (13,8 г, ,062 моля) в этил цетате (20 мл) доавляют к 5О%-ной дисперсии гидрида натия (4,1 г, 0,085 моля МаН) и смесь ипятят с обратным холодильником 4 час а водяюй бане. После охлаждения красое масло обрабатывают водой, твердое елтое вещество отфильтровывают и тщаельно промывают холодной водой. Натривую соль (16,8 г) декарбоксилируют 5н. лористоводородной кислотой (23 мл) при 0°С, т. пл. (бензол) 145-147°С. , %: С 62,22} Н 4,63. Вычислено, %:G 68,18} Н 4,58. б) 4-.Метокси-2-нитроиндан-1,дион. Нитрованием 4 метоксииндан-1,3-дина в УСЛОВИЯХ примера 1б получают соеинение с т.пл. 132-134С вода, хлориЬоводородная кислота).. Найдено, %: С 54,39}Н 3,22} N 6,42. - C-LoH N Од. Вычислено,%: С 54,31} Н 3,19} N 6,33. Выход 79%. П р и м е р 4. а) 4-Этоксииндан-1,Э-дио н. Диметил-3-этоксифталат (т. пл. 58°С) ревращают в 4«этоксииндан-1,дион в словиях примера 1а. Найдено, %: С 69,48} Н 5,34. Вычислено, %: С 69,46} Н 5,30. б) 4-Этокси-2-нитроиндан-1,3-дион. Прямое нитрование 4-этоксииндан-1,3 йона дымящей азотной кислотой в услових примера 16 дает нитропроизводное с . пл. 95-96 С (вода, хлористоводородая кислота). Найдено,-%:С 48,83}Н 4,61| N 4,97. Вычислено,%: С 48,71{Н 4,83 Ы5,17 Выход 46%. Пример а) Бенэ-С )-индан-1,3-дион. Получают по методике, аналогичной ме тодике примера 1а, т, пл, 136°С (из бен зола) . Найдено,%: С 73,80j Н 4,15. Вычислено, %: С 72,89 j Н 4,71. б) 2-Нитробенэ-( f )- ндан-1,дион. Китровании бенэ-( )-индан-1,3-диона дымящей азотной кислотой в эфире при 10 С дает указанное соединение с т.пл. 163-164°С. Найдено,%: С 64,89; Н 3,06; Ы 5,03 Вычислено,%:С64,74;Н2,93; N 5,81 Выход 41%. П р и м е р 6. а) 3-Метокс№-6-метилфталилуксусная кислота. З-Метокси-6-метилфталевый ангидрид (21,29 г, 0,11 моля) обрабатывают свежепрокаленным ацетатом калия (16,7 и уксусным ангидридом (35 мл). Полученную смесь нагревают. 1 час при 1ОО С и з§тем еще 4 час при 150-155 С..После охлаждения добавляют воду (100 мл), темный осадок отфильтровывают и промыв ют водой и метанолом до получения бесцветного фильтрата. Твердое вещество экс трагируют 5%-ным водным бикарбонатом натрия (5ОО мл) и отфильтрованный экстракт подкисляют. Бледно-желтый осадок фталилуксусной кислоты выделяют с ко- личественным выходом, т. пл. (диоксан), 260-262 С. 61,13; Н 4,40. Найдено, Вычислено, %: С 61,54; Н 4,ЗО; б) 4-МетЬкси-7-метилиндан-1,3-дион, Мети лат натрия (из 10,8 г натрия) в 10О мл метанола добавляют при сильном встряхивании к раствору 3 метокси-6-м& тилфталилуксусной кислоты (10,8 г, 0,О46 моля) в метаноле (250 мл) и сме оставляют стоять при комнатной температуре в течение 2 час. Получившийся оранжевый гель нагревают 5 час при 10О°С; охлаждают и ,затем отфильтровывают. При добавлении горячей (80 С) 5 Н. хлористоводородной кислоты происходит самопроизвольное декарбоксилирование и образуется оранжево-желтое твердое вeщectBD. После отфильтровывания и перекристаллизации (бензол) получают ин- андион с т. пл. 172°С в виде темно-желого твердого вещества. Найдено, %: С 69,50; Н 5,34. . Вычислено, %: С 69,46; Н 5,30. в) 4-Метокси-7-метил-2-нитроивдан1,3-дион. Обработка 4-метокси-7-метилиндан-1,Э-диона дымящей азотной кислотой, как в примере 16, дает нитропроизводное в виде желтого твердого вещества с т.пл, (вода, хлористоводородная кислота) 143 146С. Найдено, %: С 56,61;Н 3,93; N5,80. Вычислено,%:;С56,18;Н 3,86; N5,96. Выход 79%. Пример 7. а) 5- Бро минда Н-1,3-дион. Раствор .4-бромофталевого ангидрида (4,15 г, 0,018 моля) в уксусном ангидриде (10 г), содержащем триэтиламин (4 г)., обрабатывают при комнатной температуре этилацетоуксусным эфиром (2,38 г, 0,02 моля). После 24 час перемещивания добавляют дробленый лед (2О г) и концентрированную соляную кислоту (10 мл) и осадок твердого красного вещества от- фильтровывают. Его декарбоксилируют добавлением к твердому веществу горячего (7О-80 с) раствора соляной кислоты (150 мл) в воде (750 мл) с образованием 5-бромоиндан-1,3-диона в виде краст. пл. 152-153 с (аценых пластинок, тон). Найдено, %: С 48,04; Н 2,17; Bh 35,63. .о Вычислено, %: С 48,05; Н 2,24; Bf 35,52. б) 5-Бромо-2-нитроиндан-1,3-дион. Нитрованием, как описано в примере 16, превращают 5-броминдан-1,3-дион в его нитропроизводное с т. пл. 127-129°С (вода, соляная кислота). Найдено, %: С 4О,03; Н 1,55; N 5,11; Bh 29,32. Вычислено, %: С 40,О1; Н 1,49; N5,l8;Bh 29,38. Выход 83%. Пример 8. а) 4-Бромоиндан-1,3-дион. Используя методику примера 7а и зам нив ацетоуксусный эфир трет-бутилаце- тоуксусным эфиром, получают из анги рида 4-бромоиндан-1,3-дион, т. разл, i20°Q, б) 4-Бромо-2-нитроиндан-1,3-дион. Получают в условиях примера 76, т.п 127-128с (вода, соляная кислота). Найдено, %: С 40,16; Н l,6Oi N5,36;B| 28,65. Выдислено, %: С 40,01 Н 1,49} N5,18iBJ 29,48. Выход 51%. П р и м е р 9, а) 4-Фтороиндан-1,3-дион. Пользуясь методикой примера 8а, из 4 фторофталевого ангидрида получают 4 -фтороиндан-1,3-дион, т. ил. 117-118 (бензол). Найдено, %: С 65,87} Н 3,15. Вычислено, %: -С 65,86} Н 3,О. б) 4-Фторо-2-нитроиндан-1,дион. Это соединение получают нитрованием 4-фгоройндан-1,3 диона при Ю С, т. пл 124°С (вода, соляная кислота). Найдено, %:С 47,75;Н 2,68i N6, 2° Вычислено,%:С 47,59|Н2,66; N 6, Выход 84%. Пример 10. а)4,5,6,7-Тетрахлориндан-1,3-дион Тетрахлорфталевый аншдрид превращ JOT в индандион и по методу, описанном в примере 8а, продукт разлагают прв на гревании. Найдено, %: С 39,01j Н 0,75 се 50,15. Вычислено, %: С 38,07} Н 0,71} се 49,60. б)2-Нитро-4,5,6,7-тетрахлориндан«1,3-дион.. 2-HHTDOпронаводное получено нитрова нием 4,5,6,7 тетрахлориндаи-1,3-диона -при 1О°С, т. пл. 184-185°С, Найдено, %:С 27,89}Н 1,40} N3,41 СдНСС 0 Вычислено, %: С 28,22; Н 1,84} N3,66. Выход 83%. П р и м е р 11. а) Диметил-3,6-дигидро-4,&-диметил фгалат. 2,3-Диметилбугадиен (39 г, 0,366 моля) и диметилацетилендикарбоксилат (47,69 г, 0,366 мола) нагревают в а&токлаве при 140°С 4 час. После охлаждения добавляют эфир и раствор фильтруют. После испарения фильтрата получают указанное соединение, перекристаллизовывают из метанола, т. пл. 71-72°С (петролейный эфир,40-60°С). Найдено, %: С 64,41} Н 7,16 Вычислено, %: С 64,27} Н 7,19, б)Диметил-4,5-диметилфталат. Это соединение добавляет к палладию (10%) на древесном угле (2,5 г) и смесь аэрируют при 22О-225°С 3 час. После охлаждения добавляют эфир и смесь отфильтровывают. Испарением и отгонкой получают диметил-4|5-диметилфталат, т. пл. 53-54 С (метанол, петролейный эфир, 40-60 с). . Найдено, %; С 64,87} Н 6,36; Вычислено, %: С 64,85} Н 6,35, в)5,6-Диметилиндан-1|3-дион. Диметил -4,5-диметш1фталат (14,6 г, 0,666 моля) в этилацетате (20 мл) добавлжот к 50%-нрй дисперсии гвдрида нат рия (4,63 г, О,96 моля МаН) и смесь кипятят 4 час с обратным холодильником на паровой бане. После охлаждения желтое твердое вещество отфильтровывают небольшим количеством холодного зтиладетата. Обработка горячим раствором (80 С) концентрированнойсоляной кислоты ( 2О мл) в воде (200 мл) в течение 7 мин дала указанное соединение, т. пл. 159 С (бензол) . . Найдено, %: С 75,77} Н 5,79. Вычислено, %: С 75,84} Н 5,79. г)5,6-Диметил-2-нитроиндан-1,3-дион. 5,6--Диметилинда№-1|3-дион (0,52 г, 0,ООЗ моля), суспендированный в безводном эфире (5 мл), перемешивают приЮ С и по каплям добавляют дымящую азотную кислоту (1,0 мл). После окончания доба Ленин смесь перемешивают при комнатной температуре 1 час и осевшее желтое твердое вещество отфильтровывают, т. пл. lllllЗ°C (вода, соляная кислота). Найдено,%:С 60,11; Н 4,10; N 6,14. CllH9 04 Вычислено,%: С 50,28}Н 4,14} N 6,39. Выход 0,17%. Пример 12. а) 4-Изопроггилоксииндан-1,3-дион. Димети№-3-изопропилокскфталат (41,93 0,166 моля) в атилацетате (55 мл) ос- торожно добавляют к дисперсии гидрида натрия {11,0 г, 0,228 моля) в минеральном масле и смесь нагревают с обратным холодильником 4 час на парово .бане. Выделившееся после охлаждения твердое желтое вещество отфильтровывают и промывают небольшим количеством этиладетата. Декарбоксилируют добавлением этого твердого вешества к 1 н. соляной кислоте при 80°С в течение 10-15 мин. После охлаждения и фильтрования пере кристаллизация (бензол, петролейный эфир 40-60°С) дает продукт, т. пл.. бЭ-ТО С, Найдено, %: С 70,88i Н 5,93. Вычислено, %: С 70,S8; Н 5,92. б) 4-И зопропилокси-2-нитроиндан-1,34-Изопропилоксииндан-1,3-дион{ 6,16г 0,003 моля), суспендированный в сухом эфире (3 мл), обрабатывают дымящей азотной кислотой (1,0 мл), добавляемой по каплям при перемешивании. Полученный темный раствор обрабаты вают 5 н. соляной кислотой и упаривают до получения желтого кристаллического продукта, т. пл. 8O-8l C (вода, соляная кислота). Найдено,%: С 57,94; Н 4,43; N5,46. Вычислено,%:С57,83;Н4,45; N5,62 Выход 59%. Пример 13. а)4,6-Диметилиндан-1,3-дион. Диметил-3,5-диметилфталат (15,1 г О,О68 моля) в этилацетате (22 мл) обрабатывают 50%-ной дисперсией гидрида натрия (4,8О г, О,10 моля МаН) в минеральном масле и смесь нагревают с об ратным холодильником 4 час при 100°С. После фильтрования полученную желтую натриевую соль ибрабатывают 7 мин при 70-80°С соляной кислотой (11,0 мл) в воде (11О мл), продукт отфильтровывают и перекристаллизовывают, т, пл, 137-138°С Найдено, %: С 75,73; Н 5,67. Вычислено, %: С 75,84; Н 5,79. б)4,6-Диметил-2-нитроиндан-1,3-дион. 4,6-ДиМетилиндан-1,3-дион (0,52 г, 0,003 моля) суспендированный в безвод ном эфире 5 мл), нитруют, как описано в примере 12, и получают продукт с т.пл 111-112°С. Найдено, %: С 6О,12; Н 4,16; Ы0,14 CI, Вычислено, %: С 60,28; Н 4,14; N 6,39. Выход 73%. Пример 14. а)Бенэ-(е)-индан-1,3-дион. К 50%-ной дисперсии гидрида натрия (4,55 г) в минеральном масле добавляют раствор диэтилнафталин-1,2-дикарбоксилата (18,5 г) в атилацетате (22 мл) и смесь нагревают с обратным холодильником 3,5 час на паровой бане. После охлаждения осевшее желтое твердое вещество отфильтровывают, Декарбоксилируют соляной кислотой (35 мл) с водой ( ЗбОмл) при 7 о с в течение 7 мин, получают бенз-(е)-индан-1,3-дион, т. пл. 178°С (бензол, разложение). Найдено, %: С 79,21; Н 4,22. Вычислено, %: С 79,58; Н 4,11. б)2-Нитробенэ-(е)-индан-1,3-днон. Нитрование бенэ-(е)-индан-1,3-диона, как описано в примере 12, двет 2-нитропронзводное в виде оранжевого кристаллического вещества, т. пл. 143,5-135,5°С (вода, соляная кислота). Найдено, %:С 64,74; Н 2,91; N 5,59. Вычислено,%:С 64,74;Н 2,93; N 5,81. Выход 29%. Пример 15. а)3,6-Диметилфталилуксусная кислота. 3,6-Диметилфталевый ангидрид (т. пл. 144-145°С, 15,3 г, 0,087 моля) обрабатывают прокаленным ааетатом калия (13,3 г) и уксусным ангидридом (27 мл) и нагревают при 1ОО°С в течение 1 час. Затем смесь нагревают до 15О-155°С и поддерживает при этой температуре 4 час. После охлаждения добавляют воду(8Омл) и коричневое твердое вещество отфильтровывают и промывают водой и холодным метанолом. После экстр)агирования остатка 5%-ным бикарбонатом натрия и подкис- ления экстракта соединение получают в виде желтого твердого вещества с т. пл. 264-265°С. Найдено, %: С 66,04; Н 4,69. , . Вычислено, %: С 66,05; Н 4,62. б)4,7-Диметилиндан-1,3-дион. Метилат натрия (800 мл раствора 8,05 г натрия в метаноле) добавляют при сильном перемешивании к раствору 3,6-диметилфталилуксусной кислоты (7,5 г) в метаноле (200мл) и гель выдерживают 2 час. Затем красную суспензию нагревают 5 час с обратным холодильником на паровой бане, охлаждают и отфильтровыва ют, рекарбоксилируют добавлением к твер ному веществу горяней (8О°С) . соля ной кислоты (120 мл). После охлаждения иняандион отфильтровывают, высушивают, перекристаллизовывают и получают продук с т. пл. 187-188°С (бензол). Найдено, %: С. 75,48; Н 5,88. Вычислено, %: С 75,84j Н 5,79. в) 4,7-Диметил-2--нитроиндан-1,3-дио 4,7-Диметилиндан 1,3-дион (0,52 г, 0,003 моля) в сухом эфире (5 мл) нитру ют дымящей азотной кислотой (1,0 мл), как описано в примере 12, и получают 4,7-диметил-2-нитроиндан-1,3-дион, т.пл 108-110 С (вола, соляная кислота). Найдено, %: С 60,07;Н 4,20j N6,29. Вычислено,%:С 60,28;Н 4,14| N 6,39 Выход 73%. Пример16. а)Димети/ь-З-этилфталат. Диметилацетилендикарбоксилат (26,0 г Of 183 моля) добавляют к раствору 1,3- -гексадиена (15,0 г, 0,183 моля) в сухом бензоле (100 мл) и смесь перемешивают в автоклаве при 65°С 24 час. После выпаривания и отгонки получают дигидроароматический аддукт в виде бесцветного масла, т. кип. 80-100°С (О,3 мм рт.ст). Аэрация его при 22О-225°С в присутствии 109о-ного палладинизированного угля в течение 3 час дает соединение в виде бесцветного масла, т. кип. 126°С (1,2 мм рт. ст.). Найдено, %: С 64,46; Н 6,46. Вычислено, %: С 64,85; Н 6,35. б)4-Этилиндан-1,3-дион. Раствор диметил-3-этилфталата (7,38 0,033 моля) в этилацетато (10 мл) добавляют к 50%-ной дисперсии гидрида нат рия (2,32 г) в минеральном масле исмес нагреваЕот 4 час с обратным холодильником на паровой бане. После охлаждения желтую натриевую соль отфильтровывают, хорошо промывают сухим эфиром и вьюушивают. Обработка горячей (8О С) соля- иой кислотой с водой (1ОО мл) в течедает дИон, т; пл. 148 С (бе ние 10 мин зол). С 76,65} Н 5,45. Найдено, Вычислено, %: С 75,85; Н 5,80. в) 4-Этил-2-нитроиндан-1,3-дион. Суспензию 4-этилиндан-1,3-диона. {О,52 г, О,ООЗ моля) в сухом эфире (5 мл) обрабатывают по каплям при10°С дымящейся азотной кислотой (1,0 мл) и через 40 мин осевщ 1й продукт отфильтровывают при комнатной температуре, т. пл. GO-iOO C (вода, соляная кислота). Найдено, %:С 59,88;Н 4,18; N6,34. СцНдМО Вычислено,%:С 60,28;Н4,14; N6,39. Выход 10%. Прим ер 17. а) 4-Метокси-6-метилиндан-1,3-дион. Диметил-3-метокси-5-метилфталат (14,8 г, 0,062 моля) в этилацетате (20 мл) добавляют к 5О%-ной суспензии гидрида натрия (4,1 г, 0,085 Моля) в минеральном масле и смесь нагревают с обратным холодильником 4 час при 100°С. Добавление эфира, этилацетата к пол 1енному охлажденному маслу дает желтре твердое вещество, которое отфильтровь;1ают. Обработка его 5 н. соляной кислотой (30 мл) в течение при 70 с дает 172-17 3°С желаемый продукт, (бензол). Найдено, %: С 69,45; Н 5,43. Вычислено, %: С 69,46; Н 5,30. б) 4-Метокси-6-метил-2-нитроиндан-1,3-дион. Суспензию 4-мeтoкcи-6-мeтилиндaн-l,3-диoнa в сухом эфире нитруют, как в примере 16а, и получают 2-нитропроизводное с т. пл. 156-157°С (вода, кислота). Найдено, %: С 56,00;Н 3,86; N5,90. Вычислено,; С 5 6,16; на, 8 6; N 5,96. Выход 79%. Пример 18. а)б-Этил-4-Метоксииндан-1,3-дион. Конденсацией 5-этил-3-метоксифталата (т. пл. 89 с), как описано в примере 166, получают с т. пл. 112-113С (бепзол, петролейный эфир, 4О-6Ос). Найдено, С 70,60; Н 5,97. Вычислено, %: С 70,57; Н 5,92. б)6-Этил-4-мeтoкc -2-нитpoиндaн-l,3-диoн. Нитрованием суспензии 6-этил-4-метоксииидан-1,3-диона в сухом эфире, как описано в примере 16в, получают 2-нитропроизводное с т. гш. 116 С (вода, соляная кислота). Найдено, %;С 57,85;Н 4,47; N 5,77. Bbi4HcneHO,%:C57,83iH4,45i N 5,62 Выход 59%. Пример 19. а) 5-Фенилиндан-1,3-дион. Димети№-4-фенипфталат (т. кип. 17О0 С в этилацетате) циклизируют в ин- дандион, как описано в примере 166, получают продукт с т. пл. (бензол, петролейный , 4О-60с). Найдено, %: С 80,96} Н 4,70. Вычислено, %: 81,07; Н 4,54. б) 2-41итро-5-фенилиндан 1,3-аион. Нитрование 5-фенилиндан-1, Района ды мгацей азотной кислотой, как описано в примере 16в, дает 2-нитро-5-фенилиндан -1,3-дион с т. пл. И9°С (вода, соляна кислота). Найдено, %:С 65,54;Н 3,39; N 4,9 C gHgNO - 0,5Н20 Вычислено,%:С 65,21jH 3,65; N 5,0 Выход 82%. При мер 20. а) 4-Изобутилоксииндан-1,3-дион. Раствор диметил- изобутилоксифталата (26,6 г, О,1 моля), т. кип. 140 144°с (ОД мм рт. ст.) в этилацетате (34 мл) обрабатывают 5О%-ной дисперси ей гидрида натрия (6,64 г, 0,137 моля) в минеральном масле и коричневый раство нагревают 4 час с обратным холодильником на паровой бане. Светло-коричневое твердое вещество отделяют фильтрованием и очищают растиранием с этанолом (3:1) декарбоксилирование 5н. соляной кислотой (45 мл) при 70°С в течение 10 мин дает требуемый продукт с т. пл. 65°С (бен зол, петролейный эфир Ю-бО С). Найдено, %: С 71,63; Н 6,52. Вычислено, %: С 71,54; Н 6,47. б) 4-Изобутилокси-2-нитроиндан-1,3-дион. 4-И зобутилокси-2- итроиндан-1,3-дион (0,654 г, 0,003 моля), суспендированный в сухом эфире (5 мл), обрабатывают по каплям дымящей азотной кислото (1,О моль) при 10°С и прозрачный темно-красный раствор перемешивают при ко натной температуре 1 час. Выпаривание в присутствий 5н. соляной кислоты дает 2нитропроизводное в виде желтого твердого вещества с т. пл. 75-77°С (вода, соляная кислота). Найдено, %:С 58,92;Н 5,00; N 5,48. Вычислено,%:С 59,,98; N5,32. Выход 77%. Пример 21. а)4-н-Бутилоксииндан-1,3-дион. Это соединение получают конденсацией диметял-З-н-бутилоксифгалата (т. пл. 48°С) с этилацетатом, как описано в примере 166, продукт имеет т. пл. 66°С( бензол, петролейный эфир, 4О-60°С). Найдено, %: С 71,41; Н 6,54. Вычислено, %: С 71,54; Н 6,47. б)4-н-Бутилокс№-2-нитроиндан-1,3-дион. Нитрованием 4-н-бутнлоксииндан-1,3-диона, как описано в (фнмере 206, получают 2-ннтропроизводное с т. пл. (вода, соляная кислота). Найдено, %:С 59, 5,13; N5,13. Вычислено,%:С 59,31}Н4,98; N5,32. Выход 84%. Пример 22. а)4-н-Проп1шоксииндан-1,3-дион. Конденсация диметил- н-пропилоксифгалата с этилацетатом, как описано в примере 2Оа, дает 4-н-пpoпилoкcииндaнl,3-диoн с т. пл. 94-95с (бензол). Найдено, %: С 7О,69}Н 6,05. Вычислено, %: С 7О,58; Н 5,92. б)2-Нитро-4-Н-пропилоксииндан-1,3- дион. Нитрование 4-н-пропилоксииндан-1,3диона, как описано в примере 16а, дает 2-нитропроизводное с т. пл. 114-115°С (вода, хлористоводородная кислота). Найдено, %:С 57,57; Н 4,43; N5,48. Вычислено,%: С 57,83;Н 4,45j N 5,62. Пример 23. а)4-Фенилиндан-1,3-дион. Диметил-3-фенилфталат(5,0г, 0,055 моля) в атилацетате (20 мл) добавляют к дисперсии гидрида натрия (3,6 г) в минеральном масле и смесь нагревают с обратным холодильником 4 час на паровой бане. После отделения светло-желтого твердого вещества и последующего декарб- оксилирования горячим () раствором соляной кислоты (25 мл) с водой (250 мл) получают желаемый продукт с т. пл. 125128°С (бензол). Найдено, %: С 8О,94; Н 4,69. Вычислено, %: С 81,07; Н 4,54. б)2-Нитрсь-4-фенилиндан-1,3-дион. Нитрование 4-фенилиндан-1,3-аиона, как описано в примере 16в, дает 2-нитропроиэ- 15 62 (вода, соляная кис водное с т. пл. лота). Найдено, %:С 67,04{Н 3,37j N 5,24. Выход 75%. Пример 24. а)4,5-Циклогексаноиндан-1,3-дион. Конденсацией диметилтетралин-5,6 дикарбоксвлата ( г, 0,О465 моля) с этилацетатом (15 мл), как описано в при мере 16, получают 4,5-циклогексаноиндан -1, в виде желтого кристаллическо го соединения с т.пл. 97-99°С (бензол). Найдено, %: С 77,80; Н 5,74. Вычислено, %: С 77,98; Н 6,04. б)4,5 ииклогексано 2-«итроиидан-1, . К перемешиваемой суспензии 4,5-цик- логексаиояндаи 1,Э дкона (1,0 г, О,ОО5 м ля)вбезводномэфире(8,)при-2О%дэ-.| бллляот дымящую азотную кислоту(1,0 мл) по КАПЛЯМ. После перемешивания лри О 5 С а течение 1 час и затем еще 1 ча комиатной температуре добавляют 2О мл волы, «фмр удаляют в вакууме и рлсглор фильтруют. После добавления конвеитрировакиой соляиой кислоты к прозра ному мьтрвту П1Ж охлаждении получают укаэшиое соединение с т. пл. 108 (вода, соляная кислота). Найдено, %:С 63,67jH 4,48; N 5,43. Вычислено, %: С 63,67; Н 4,52; N5,71. Выход 13%. Пример а)4,5-ииклопеитаиоиндан-1,3-дион. Конденсация дмметилиидан-4,5-анкарбоксилата (12,42 г, 0,053 моля) с тил етатом, как в примере 1б, дает дион в иде желтого твердого Вещества, т. пл. 15&-162 С (бензол, петролейный афир, 4СХ-вО°С). Найпеио, %: С 77,55; Н . Вычислено, %: С 77,4О; Н 5,4i. б)4,5-Ш1Клопентано-2-нитроиндан-1,Э янои, К перемешиваемой суспенжи 4,5-цик-. лопентано- нндан«1,3-днона (0,95 г, 0,ОО5 моля) в сухом эфире (8,0 мл) ; при О-5 С добавляют дым5Ш1ую азотную 16 ислоту (1,0 мл) и смесь перемешивают ри этой температуре 45 мин. Затем перемешивание продолжают еще час при комнатной температуре, доба&яют 20 МП воды и после испарения эфиа и фильтрования получают прозрачный елтый фильтрат. После добавления к не у равного объема концентрированной соляной кислоты получают 2-нитропроизаодое в виде желтого кристаллического вещества, т. пл, 128-130°С (вода, соляная кислота), Найдено, %: С 59,96;Н 3,96; М 5,89. .0 ,5Н2 Н 4,20; ; С 60,80; Вычислено, % N 5,83. Выход 30%. Пример а)5-Метокси-6-метилиндан-1,3-дион, Раствор диметил-4-метокси-5-метилфталата (14,21 г, 0,О6 моля), т, пл. в6-6в°С в этилацетате (20 мл) добавляют к 5О%г-иой дисперсии гидрида натрия (3,95 г, 0,О82 моля NaH) в минеральном масле и смесь нагревают с обратным холодильником 4 час. Выделившуюся оранжево-коричневую натриевую соль растворяют в смеси этанола и эфира (1:1), фильтруют и высушивают в вакууме. Добавление высушенного твердого вещества к горячей (80°С) 5 Н. хлористоводородной кислоте (15 мл) и последующее перемешивание в течение 7 мин при 7О°С дает указанное соединение в виде твердого вешества.т.пл. 215-216°С (бензол). Найдено, %; С 69,11; Н 5,50. Вычислено, %: С 69,46; Н 5,30. б)5-MeTOKCH-e-MeTHJVi2-HHTpOHHAaH-1,дион. Нитрование 4-метокси-6-метилиндан- -1,3-диона, как указано в примере 16, дает 2-нитропроизводное первоначально в виде желтого твердого вещества, делается оранжевым при обезвоживании, т. пл. 110°С. Найдено, 56,59;Н 3,83; N 6,03. Вычислено,%,С 56,17;Н 3,88; К5,96. Выход 6%. В таблице приведены результаты испытания предлагаемых соединений.
Продолжение табл.
2-Нитробенэ-( е)«индан-
4-Этил-2-нитр1 То же ивдан 1,
Раствор Ка- 25О
соли
2530
Суспензия М а- 25-Q соли в 1%-«ой
метилцеллюлозе 256О
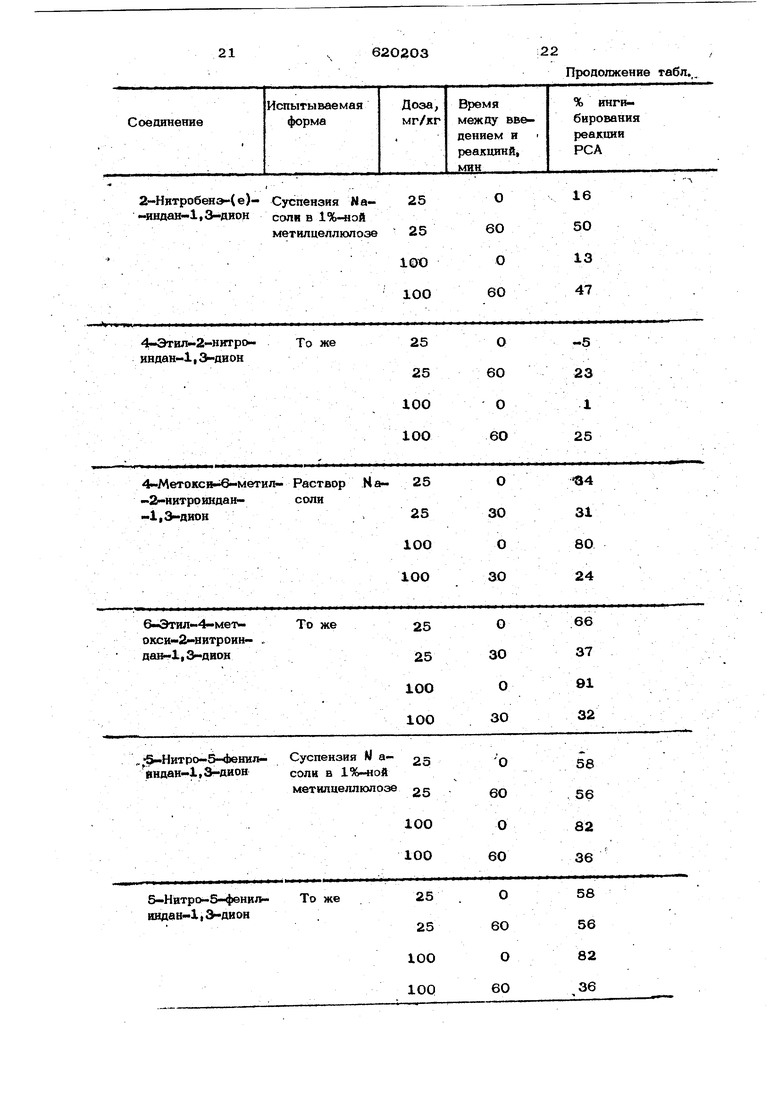
Продолжение табл.
16 50 13 47
О 60
О 60
О
-5 60
23
О 60
1
25
84 31
100О 80 24
1ООЗО
58 56
100О 82 36
10060
Продолжение габл.
Формула изобретения
Способ получения производных 2-нитро- ИНДан-1,3-диона общей формулы
О
Ж
где R - 1 представляют собой каждый атом водQpoдa или алкил .., алкоксигруппу , фенил-, пиридилрадикал или атом галогена; или смежные группы . и Р,, Н, и Rj или и Н могут представлять собой триметилен- или тетраметиленовую группу или, если указанные группы находятся в положении 1,4, означают бута-1,3-диениловую группу, причем, если I - водород, хлор, бром, метил, Б не означает водород - метоксигруппа, бром, хлор, йод, то R не являет ся водородом,
или их солей, отличающийся тем, что производное индан-1,3-диона общей формулы
HI О
н
10
где R - R имеют указанные значения, подвергают взаимодействию с дымящей азотной кислотой в -феде растворителя с последующим выделением целевого продукта в свободном виде или в виде соли. Источники информации, принятые во внимание при экспертизе:
l.Q.Cema.V.(.Loitv.PS1l.Zinat. Alcad.Vestis (K110W. Ser.) 3, 328, 1968.
Авторы
Даты
1978-08-15—Публикация
1973-06-08—Подача