Изобретение относится к способу получения .19-нор-А - стероидов, обладающих биологической активностью.
Известны способы получения 3-01Ксо-19-НорА -стероидов восстановлением ароматического кольца А стероидов по Берчу.
Ооноваиный на известной реакции предлагаемый способ получения З-оксо-19-iHOip-A стероидов общей формулы
R, R
где М - остаток кольца D стероида; Ri-пизший первичный Ci-С5-алкил; R, Нз и lR - водород или нивШий алкил, заключается в том, что 10-(3-заме1ценный )-дес-А-стероид общей формулы
Й1 М
Яг
гЧлЛЕь
R
где RI-R4 и М имеют приведенные выше значения; Rs - остаток O.Re, где Re - моноциклический низший аралкил, водород, ацил или ради1кал общей формулы
-С-Еа
R9
10
в которой RT, Rs и Rg - низший алкил, нагревают с кислотой или, если Re - водород, то только нагревают или обрабатьгвают кислотой, образующееся в результате циклизации соединение общей формулы
20
25
где RI-R и М - как указано выше, гидрируют в присутствии благородного металла в качестве катализатора и основания до образования соединения общей
где Ri-Rt и М имеют указанные выше значения, это соединение о-брабатывают амиеОМ общей формулы RNHs, где R - оксигруппа, низшая алкоксигруппа или радикал обшей формулы
./
-N.
Y
в которой X и Y - низший ал.кил, или солью, полученное соединение общей мулы
В,
В,
J
но Ш, N
Е R
где RI-iR4, R и М - как выше указано, избирательно Окисляют до соединения общей формулы
где RI-R4, R и М имеют указанные выше значения, образующееся соединение обрабатывают водным раствором .кислоты в среде инертного смешивающегося с водой органического растворителя и выделяют целевой продукт известными приемами.
В исходных, промежуточных и целевых продуктах М означает половину частной формулы
где Z-карбонил или группа общей формулы
™
в которой - водород или низший ацил; R -тадород или низший алифатичаский гидрокарбюнил; т- 1 или 2.
Циклизацию обычно проводят при нагреваНИИ в прИСут1сгвии м-инеральной (серная, солЯ|Ная) или оргаиичеокой (бе|Н30л-, п-толуолсулыфоновая) кислоты, в среде углеводорода,
на прИ|Мер бензола или толуола.
Гидрирование осуществляют преимущественно .в прИСутствии палладия на угле и основания в инерт1ном растворителе, например бензоле или толуоле, .при комнатной температуре и атмосферном давлении. В качестве основания на стадии гидрироваНИН применяют низший триалкиламин, например триэтиламин.
Обработку амино.м .проводят в инертнОМ органическом растворителе, например пиридине, дИМея-ялфОрмамиде (ДМФА), тетрагидрофуране (ТГФ), диоксане или изопропаноле, предпочтительно при комнатной те-мпературе. Амины формулы RNHj применяют преимущественно в виде соли с неорганической, например серной или галоидводородной, или
органической, наери-мер уксуаной, прапионовой или щавеле1вой, кислотой. Чаще всего исполызуют амины, в которых R представляет собой низшую алко1ксигрутпу, особенно мет1оксигруп1пу. Реакцию проводят нреимущественно в присутствии основания, нанример пириди1на, или тр.иэтиламина.
В качестве окислителя можно иопользовать хромовую Кислоту, углекислое серебро или проводить окисление по методу Опивнауэра.
Окисление хромовой «ислотой проводят в среде низшего М,Ы-диалкилалканоиламида, например ДМФА, при О-25°С.
Циклизацию в целевые соединения осуществляют предпочтительно в среде низшего
спирта, ТГФ или диоксана в присутствии водной органической или минеральной кислоты, юреимущественно серной, галоидводородной, Низшей алкановой, арилкарбоновой или арилсульфоновой кислоты.
Цример 1. Бензольный раствор 14,1 г (±)-6-(3-грет - бутоксибутил) - За,р-.этил-4, б,8,9,9а,9&-ге1ксагидро - 1Н - 6eiH3 - е -индвн3,7 - 2Н, ЗаН - диона обрабатывают 0,6 г п-толуолсульфокислоты и нагревают 4,5 час
с обратным холодильником. После охлаждения и обычной обработки в атмосфере азота при 4°С и в темноте получают (±)-2-вдетил6а,р-этил-2, 3,4, 6,8,9, 9а,9&, 10, М - декагидроци1Клапента-(5,6) - нафто - 2,1-6 - пиран7- 6аН -он, т. пл. 109-II6°C (дважды из гетесана).
Для синтеза исходного вещества 71,5 г 5ХЛор-2-1пентанона растворяют в 260 мл эфира и в течение 50 мин нри -40°С добавляют к
суапензии 12 г литийалюминийгидрида, переме щивают 0,6 час при -30°С, добавляют П5 мл насыщенного водноло раствора сульфата натрия, фильтруют, промывают осадок эфиром, удаляют эфир в BaiKyyMe и выделяют
5-хлор-2-1пе1Нтанол, 2Э8 г которого растворяют в 500 мл метиленхлорида, добавляют 24 мл ковцентрированйой серной кислоты с 500 мл метиленхлорида, вводят 1 л жидкого изобутилена и .выдерживают 20 час при комнатной температуре. Органическую фазу прОМЫ1вают рассоло м и водным раствором бикарбоната натрия, высушивают «ад сульфатом мапния, удаляют растворитель в ва.кууме и получают 5-хлор-:2-грег-бутоксипента«.
10 г металличеакаго маш«я активируют кристаллом йода, наливают на наго 20 мл сухого ТГФ, добавляют 5 капель дибромэтана, перемешивают 15 мин с обратным холо-дильником и добавляют 5-Х1Лор-12-г/ ег-бутокси1пентан в две стадии. К реакционной омеси добавляют 20 мл эфира, сощержаш.его растворенйый хлор (63,5 r/Q50 мл), и после, того, «ак реакщия «ачнется (16 мин-24 час), добавляют в течение 1 час оставшиеся 230 мл раствора, нагревают 1 час с обратным холодилыником, оклаждают и ф-ильтруют.
Получеияый реактив Гриньяра добавляют К pacTiBOpy 30 г свежеперепнанйого глутарового альдегида в 400 мл ТГФ при -05°С, перемешивают 15 мин при -25°С и 1 час при 0°С, добавляют 050 мл 20%-iHoro водного раствора хлорида аммония, юодкисляют 1 в. соляной кислотой до рН 4, экстрагируют эфиром и получают 91 г 6-(4-г/5ег-бутокси)-2-тетра1ГИДрО(пиранола в виде масла.
Полученный 1продукт перемешивают с 650 МЛ 20%-,ного раствора сулыфата натрия, по дкисляадт ледяной уксусной кислотой до рН 6,6, добавляют 20%-1ную соляную кислоту до рН 7,5, перемешивают 1 час при 40°С, экстрагируют эфиром, подщелачивают водный слой 20%-ньш едким натром и экстрагируют эфиром. После вьшаривания эфира в вакууме выделяют чистый 6-(4-т/7ет-бутокси)-2-тетрагидропиранол.
Раствор 4,6 г 4-(4-трет-бутокси)2 - тетрагидропиранола в 200 мл ТГФ в течение 20 мин при 0°С добавляют к раствору 300 мл ви1нилма1пнийхлорида в ТГФ, перемешивают 1 час при комнатной температуре, добавляют 200 мл эфира и 100 мл 20%-ного водного раствора хлорида аМмония, экстрагируют эфиром и получают 3,7-диокси-11-г/7ег-бутоксидодец-Ьен в виде воскообразного твердого вещества.
41,3 г 3,7-дио«си-11-г;оет-буток1сидодец-1-ена растворяют в бензоле, добавляют к суспензии 320 г активированной д.вуо«И|СИ магния в 1600 мл бензола, содержанцето 120 мл диэтиламина, перемешивают 20 час лри кОМнатной температуре и фильт1руют, удаляют растворитель Б вакууме, остаюшееся светло-коричневое масло растворяют в эфире и экст|рагируют 1 н. соляной кислотой. К экстракту добавляют едкий натр, экстрагируют эфиром, упаривают и получают 2- (2-диэтиламиноэтил) -6- (4-третбутоксипентил)-2-тетрагидропиранол.
К нагреваемому с обратным холодильником раствору 2-этиЛ|Цикло1пента№-1,3-диона в 4ilO мл ксилола, содержащего 220 мл уксусной
кислоты, добавляют 42;2 г 2-(2-диэтила1Миноэтил) - 6 - (4 - гре7-бутоксипентил)-2-тетрагидрапиранола, нагревают 1 час с обратным холодильником, ОХлаждают до комнатной температуры, промывают водой до исчезновения уксусной кислоты в промьквных водах, упаривают в вакууме и получают 3- (4-третбутоксипентил) - 6а, р-этил-2,3,5,6,6а, 8 - гексагидроциклапента - -бвнзопкран - 7 в виде светло-красного масла, которое хроматографируют на 1,2 кг нейтральной окиси алюминия (1П ст. акт.) и выделяют 38,8 г чистого вещества. Раствор 8,6 г 3-(4-грег-буто1КСИ1пентил) 6а, р - этил-2,3,6,6,6а, 8 - гаксагидро-циклояента - f - бенЗ01пиран-7- 1Н -она в 80 мл эфира при -10°С даба1вляют к 4 г литийалюминийгидрида в 200 м-л эфира, перемешивают 1 час при комнатной температуре, добавляют
20 мл насыщенного раств10ра сульфата натрия, отфильтровывают осадок, промывают его 160 мл эфира, удаляют растворитель в вакууме и получают 3-(4-грег-бутокси1пентил)6а, р - этил-2,3,5,6,6а,в-гексагидродиклопента - f 1 -беН13опиран-7- 1Н -ол, т. пл. 71 - 74°С (гакса-н).
6,3 г 3-(4-трет - бутоисипентил) - ба.р-этил2,3, 6,6, 6а,8-гексагидроциклопента - бензопиран-7- 1Н -ола растворяют в 100 мл
толуола, содержащего 1,5 г катализатора (палладий на угле), гидрируют при атмосферном давлении и комнатной температуре до прекращения поглощения водорода (1,05 моль), фильтруют, упаривают фильтрат в вакууме и выделяют маслообразный 6а, 9а-транс-3-(4-трег-бутоксипентил) - 6а, р этил - 2,3,5,6,6а, 8,9,9а - октагидроциклопента- Л 1 -бензопиран-7- 1Н -ол, чистота которого подтверждается данными тонкослойной
хроматографии на силикагеле.
36,9 г 6а, 9а-транс-3-(4-грег-бутоксипентил)6а, Р-ЭТИЛ - 2, 3, 6,6,6а, 8,9,9а - октагидроциклoпeнтa- f 1 -бензопиран-7- 1Н - ола растворяют в 700 мл ацетона, обрабатывают 200 мл
3 н. серной кислоты, выдерживают два дня при комнатной температуре, разбавляют рассолом, экстрагируют эфиром, упаривают в вакууме и получают смесь 6а, 9а-транс-3-(4трет - бутоксипентил) - 6а, р - этилпергидроциклопента - / - бензопиран-4а, 7-диола
и За, 7а-транс-4-(3-трет - бутокси - 3 - оксиоктил) - 7а, р - этилпергидроиндан-1,5-диона.
4,65 г полученной смеси растворяют в
200 мл ацетона, обрабатывают 10 мл раствора хромовой кислоты по Джонсу, перемешивают 30 мин при комнатной температуре, разбавляют рассолом, экстрагируют эфиром, удаляют растворитель в вакууме и получают За, 7а-транс - 4 - (7-трет - бутокси - 3 - оксооктил) - 7а, р - этилпергидроиндан-1,5-дион в виде масла, которое дает одно пятно при тонкослойной хроматографии.
25,4 г За, 7а - транс - 4 - (7-трет-бутокси-Зоксооктил) - 7а, р - этилпергидроиндан - 1,5диона растворяют в 70 мл трег-бутилового
спирта, добавляют 250 мл трег-бутилового спирта и 1 г порошка едкого натра, перемешивают 1 час в атмосфере азота при 55°С, охлаждают, обрабатывают рассолом, экстрагируют эфиром, удаляют растворитель в вакууме, хроматографируют на окиси алюминия (III ст. акт.), элюируя 15%- и 25%-ными растворами эфира в петролейном эфире, и получают прозрачный маслообразный 10-(3грег-бутоксибутил) - 18 - метил - 19 - нордес-А-андрост - 9 - ен - 5, 17 - диоп, или 6-(3трет - бутоксибутил) - За, Р-ЭТИЛ - 4,5,8,9,9а, 9& - гексагидро - ЬН - бенз - -инден-3,,ЗаН - дион. После перегонки получают бесцветный маслообразный продукт, т. кип. 180°С/0,05 мм.
Пример 2. 33,3 г (±)-2-метил-6а, р этил - 2,3,4,6,8,9,9а, 9&, 10, 11 - декагидроциклопента - 5,6 - нафто - 2, 1-6 - пиран7- 6аН -она в 300 мл толуола обрабатывают 5 г катализатора (палладий на угле) и 2,5 мл триэтиламина и гидрируют при комнатной температуре и атмосферном давлении до прекращения поглощения водорода (2,8 л, в течение ночи). Твердые вещества отфильтровывают, растворитель удаляют в вакууме и выделяют (±)-2-метил - 6а, р - этил - 2,3,4, 4&, 5,6, 8,9,9а, 9&, 10, 11 - додекагидроциклопента - 5,6 - нафто - 2,1-6 - пиран - 7 в виде масла, представляющего собой смесь изомеров по Сг (1 : 1), т. пл. 111 - 115°С (дважды из гексана). После повторной перекристаллизации из гексана получают продукт, обогащенный одним из изомеров, т. ил. 118-122°С.
Пример 3. 600 мл жидкого аммиака в течение 45 мин насыщают сухим ацетиленом (пропущен через ловущку при -72°С), вносят 3 г металлического калия при непрерывном пропускании ацетилена, перемещивают 30 мин, в течение 20 мин обрабатывают 8 г (±) - 2 - метил - 6а, р - этил - 2,3,4,46,5,6, 8, 9, 9а, 96, 10, 11 - додекагидроциклопента ,6 - нафто - 2,1-6 - пиран-7- 6аН -она, т. пл. 118-122°С, растворенного в 120 мл сухого ТГФ, перемещивают 2 час, добавляют 400 мл эфира и отгоняют половину аммиака. К реакционной смеси добавляют 20 г твердого хлорида аммония и через 15 мин 180 мл воды, подачу ацетилена прекращают, полученный продукт обрабатывают эфиром и после перекристаллизации из гексана выделяют (±) - 2 - метил - 6а, этил - 7а-этинил 2,3,4,46, 5,6, 6а, 7, 8, 9, 9а, 96, 10, 11 - тетрадекагидроциклопента - 5,6 - нафто - 2,1-6 пиран - 7 - ол, т. пл. 138-143°С.
.Вычислено, %: С 80,21; П 9,62.
С21НзоО2.
Найдено, %: С 80,19; Н 9,48.
ИК-спектр, CM-I: 3600 (-ОН); 3300 (Н-С С-); 1675 (О-С С).
Для синтеза исходного вещества, который можно проводить, как в примерах 1 и 2, 6-(3-грет - бутоксибутил) - За, р - этил-4, 5, 8, 9,9 9а,96-гексагидро-1Н-бенз - е - инден 3,7 - 2Н, 3fliH - дион растворяют и 50 мл этанола, добавляют 0,3 мл триэтиламина и 100 мг катализатора (5%-ный палладий на угле), гидрируют при комнатной температуре 5 и атмосферном давлении до прекращения поглощения водорода, фильтруют, упаривают в вакууме и получают 10-(3-т/7ег-бутоксибутил) - 18 - метил - 19 - нор - дес - А-андростан - 15,17 - дион, дающий одно пятно при
10 тонкослойной хроматографии.
500 мг 10-(3-грег-бутаксибутил) - 18 - метил - 19 - нор - дес - А - андростан-15, 17 диона растворяют в 25 мл бензола, содержащего следы п-толуолсульфокислоты, нагревают 2,5 час с обратным холодильником, промывают органическую фазу водным раствором бикарбоната натрия до отсутствия кислоты в промывных водах, удаляют растворитель в вакууме, перекристаллизовывают оста0 ток из гексана и получают (±)-2-метил-6а,,рэтил - 2, 3, 4, 46, 5, 6, 8, 9, 9а, 96, 10, 11 - додекагидроциклопента - 5,6 - нафто- 2,1-6 пиран-7- 6аН -он, т. пл. 111 - 115°С. Пример 4. 1,5 г (±)-2-метил-6а, р-этил.5 7а - этинил-2, 3, 4, 46, 5, 6, 6а, 7, 8, 9, 9а, 96, 10,11 - тетрадекагидроциклопента - 5,6 нафто - 2,1-6 - пиран-7-ола растворяют в 5 мл пиридина, содержащего 0,25 мл воды, обрабатывают 1 г метоксиамина в виде хлор0 гидрата, выдерживают 20 час при комнатной температуре (одно пятно при тонкослойной хроматографии), обрабатывают рассолом, экстрагируют дихлорметаном, промывают экстракт водой, высушивают в вакууме и по5 лучают (±)-6-(3-оксибутил) - За, р-этил-Заэтинил - 3-окси - 7 - метоксииминопергидро ЗН -бенз- е - индан в виде твердого вещества, т. пл. 163-165°С (изопропиловый эфир). Вычислено, %: С 73,09; Н 9,76; N 3,87.
0 С22НзйМОз.
Найдено, %: С 73,23; Н 9,81; N 3,81. Пример 5. 1 г (±)-6-(3-оксибутил)-За, Рэтил-Зсс - этинил - 3 - окси - 7 - метоксииминопергидро - ЗН -бенз- е -индана в 10 мл
5 ДМФА при 5°С обрабатывают раствором 1 г трехокиси хрома в 10 мл ДМФА, к которому добавлен раствор 5 мл концентрированной серной кислоты в 3 мл ДМФА, нагревают до комнатной температуры, перемешивают
0 1 час, добавляют дихлорметан и водный раствор бикарбоната натрия, промывают органическую фазу рассолом, 10 мл 2%-ного водного раствора бисульфита натрия, высушивают над сульфатом магния, упаривают досуха
5 в вакууме и получают (±)-6-(3-оксобутил)За, р - этил - 7 - метоксиимино-За-этинил-3оксипергидро - ЗН - бенз - б -индан в виде стекловидного вещества. Пример 6. 430 мг (±)-6-(3-оксобутил)0 За, р-этил.-7-метоксиимино-За - этинил - 3 -оксипергидро - ЗН -бенз - е -индана в 15 мл метанола обрабатывают 7,5 мл 4 н. соляной кислоты, нагревают 2 час с обратным холодильником, обрабатывают дихлорметаном и
выделяют беловатое твердое вещество, которое хроматографируют на силикагеле (0,2- 0,5 меш), элюируя 5%-, 10%- и 20%-ными растворами этилацетата в бензоле. При тонкослойной хроматографии вещество дает одно пятно; т. пл. 185-195°С. После перекристаллизации из смеси гексана с ацетоном (вместе с веществом, выделенным из маточных растворов) получают (±)-13р-этил-17аэтннил-17-окси-гон-4-ен-3-он.
Пример 7. 1 г (±:)-а-метил-6а, р-этил7а - этинил-2, 3, 4, 46, 5, 6, 6а, 7, 8, 9, 9а, 9Ь, 10, 11-тетрадекагидроЦИклопента - 5,6 -нафто - 2,1-Ь)-пиран - 7 - ола в 5 мл пиридина, содержащего 0,1 мл воды и 0,5 г Ы,Ы-диметилгидразина, выдерживают 24 час при комнатной температуре, обрабатывают дихлорметаном и получают (±)-6-(3-оксибутил)-За,рэтил-За - этинил - Зр - оксипергидро- ЗН бенз- е -индан-7-он-Ы,Ы-диметилгидразон.
Пример 8. Аналогично примеру 5 (±)-6-(3-оксибутил) - За, р-этил-Зсс - этинилЗр - оксипергидро - ЗН - бенз - е -индан-7он-|М,Ы-диметилгидразон переводят в (±)-13рэтил-17а - этинил-17-окси - гон - 4 - ен - 3 - он, используя в качестве промежуточного продукта (±)-6-6(3-оксобутил)-За,р-этил - За - этинил-3-оксипергидро- ЗН -бенз - е - индан-7OH-N,N - диметилгидразон и (±)-6-(3-оксобутил)-3а, р-этил-За - этинил - 3 - оксипергидро ЗН -бенз- е -индан-7-он.
Пример 9. 10 г (±)-6-(3-грет - бутоксибутил)-3а, р - метил - 4, 5, 8, 9, 9а, 96-гексагидро- 1Н -бенз- е -инден-3,7- 2Н, ЗаН -дион растворяют в 300 мл бензола, содержащего 500 мг п-толуолсульфокислоты, нагревают 3,5 час с обратным холодильником, охлаждают, промывают водным раствором бикарбоната натрия, удаляют растворитель в вакууме и получают (±)-2-метил-6а, р-метил - 2,3,4, 6,8,9,9а, 96, 10, 11 - декагидроциклопента ,6 - нафто - 2,1-6 - пиран-7- 6аН -он в виде масла.
ИК-спектр, 1735 (циклопентанон), 1645 (диеноловый эфир).
УФ-спектр, ммк: А,макс 249 (е 17500).
Для получения исходного вещества 28 г (dz) - 2 - (2-диэтил-аминоэтил) - 6 - (-третбутоксипентил) - тетрагидрофуран-2-ол растворяют в 140 мл ксилола, добавляют 13,7 г 2-метилци.клопентан - 1,3 - диона, 280 мл ксилола и 140 мл уксусной кислоты, нагревают 45 мин с обратным холодильником, охлаждают, промывают водой и водным раствором бикарбоната натрия, высушивают над сульфатом натрия, упаривают, хроматографируют на 870 г нейтральной окиси алюминия (III ст. акт.) и получают (±)-3-(4-трегбутоксипентил)-6а,:р-метил - 1, 2,3,5,6,6а-гексагидроциклопента - f 1 - бензопиран - в виде масла.
Вычислено, %: С 76,27; Н 9,89.
Найдено, %: С 76,47; Н 10,03.
УФ-спектр, ммк: Амако 253 (е 17700).
23,1 г (±)-3-(4-грет-бутоксипентил)-6а, рметил-1,2,3,5,6,6а - гексагидроциклопента 1 - бензопиран-7- 8Н - она растворяют в 464 мл ТГФ при -10°С, добавляют к суспензии 4,6 г литийалюминийгидрида в 232 мл ТГФ, перемешивают 45 мин при 0°С, обрабатывают водой, фильтруют, упаривают и получают (±)-3-(4-грег-бутоксипентил) 6а,р-метил-1,2,3,5,6,6а, 6а, 7,8 - октагидроциклопента - f 1 - бензопиран - 7р-ол, т. пл. 97-101°С (гексан).
.Вычислено, %: С 75,78; Н 10,41. Найдено, %: С 76,01; Н 10,28. УФ-спектр, ммк: Хмакс 252 (е 18700). Раствор 22,5 г (+)-3-(4-гре7-бутоксипентил) - 6а, р-метил - 1, 2,3,б,ба, 7, 8-октагидроциклопента - f 1 - бензопиран - 7р-ола в 450 мл толуола гидрируют в присутствии 3,4 г катализатора (5%-ный палладий на угле) при комнатной температуре и атмосферном давлении до поглощения 1 моль водорода, фильтруют, упаривают в вакууме и получают (±)-3-(4-трег - бутоксипентил) - 6а, Рметил - 1,2, 3,5,6,6а, 7, 8,9,9а - декагидроциклопента - f 1 - бензопиран-7р-ол в виде светло-желтого масла, которое после хроматографирования на нейтральной окиси алюминия (III ст. акт.) сильно поглощает УФлучи.
Вычислено, %: С 75,38; Н 10,93. Найдено, %: С 75,15; Н 10,93.
ИК-спектр (хлороформ), см-: 3625 (ОН), 1680 (енольный эфир).
22,1 г (±)-3-(4-трег-бутоксипентил) - 6а, Рметил-1, 2, 3, 5, 6, ба, 7, 8, 9, 9а-декагидроциклопента - f 1 - бензопиран - 7р-ола в
220 мл ацетона обрабатывают ПО мл 1н. серной кислоты, выдерживают 3 час при комнатной температуре, большую часть ацетона удаляют в вакууме при 35°С, экстрагируют эфиром, упаривают и выделяют (±:)-3-(4грет-бутоксипентил) - 6а, р - метилпергидроциклопента - f 1 - бензопиран-4а, 7р-диол в виде стекловидного продукта. После хроматографирования на нейтральной окиси алюминия (III ст. акт.) получают вещество, в
ИК-спектре которого обнаружены полосы поглощения при 3625 (ОН) и 1200 см- (О-.м-бутил) и не обнаружены полосы поглощения, характерные для енольного эфира. Охлажденный до 15°С раствор 17,4 г (±)3-(4-грег-бутоксипентил)-6а, р - метилпергидроциклопента - f 1 - бензопиран - 4а,7рдиола в 700 мл ацетона в течение 20 мин обрабатывают раствором 12,7 трехокиси хрома в 63,5 мл серной кислоты, перемешивают
2 час при комнатной температуре, экстрагируют бензолом и получают (±)-гранс-4-(3оксо-7-трет - бутоксиоктил) - 7а, р-метилпергидроиндан - 1,5 - дион в виде масла. После молекулярной перегонки при 195-
205°€/0,01 мм в ИК-спектре продукта обнаружены полосы поглощения при 1735 (циклопентанон); 1708 (циклогексанон или алкилкетон) и 1200 см- (О-ж-бутил). Вычислено, %: С 72,49; Н 9,95.
Найдено, %: С 72,21; Н 10,00. Раствор 13,8 г {1Ь)-транс-4-(3-оксо-7-третбутоксиоктил) - 7а, (3 - метилпергидроиидан1,5 - диона в 38 мл грет-бутилового спирта в атмосфере азота добавляют в раствору 544 мг едкого натра в 136 мл г оег-бутилового спирта, перемешивают 1 час при 55°С, обрабатывают 1 мл уксусной кислоты, затем бензолом, удаляют бензол в вакууме и получают (±)-6(3-г/7ег-бутоксибутил) - За, р-метил-4, 5, 8, 9, 9а,9Ь . гексагидро - 1Н - бенз- е -и:нден3,7 - 2Н, ЗаН - дион в виде светло-желтого масла, которое показывает сильное поглощение при Лмакс 247 ммк (е 13000). ИК-спектр, CM-I: 1730 (циклопентанон), 1660 и 1600 (циклогексанон). Пример 10. 8г (±) - 2 - метил - 6а,§метил-2,3,4, 6, 8, 9, 9а, 9Ь, 10, 11-декагидроциклопента - 5,6 -нафто - 2, пиран - 7 .растворяют в 200 мл толуола, содержащего 1,5 мл триэтиламина и 1,5 г катализатора (5%-ный палладий на активированном угле), гидрируют .при комнатной температуре и атмосферном давлении до поглощения 1 моль водорода, фильтруют, упаривают в вакууме и получают (±)-2-метил-6а, §-метил - 2, 3, 4, 4Ь, 5, 6, 8, 9, 9а, 9Ь, 10, 11-додекагидроциклопента - 5,6 - нафто- 2,1- пиран-7- 6йН -он в виде масла, которое очищают на нейтральной окиси алюминия (III ст. акт.). Вычислено, %: С 78,98; Н 9,42. Найдено, %: С 78,79; Н 9,55. ИК-спектр, CM-I: 1740 (циклопентанон); 1680 (енольный эфир). Пример И. 747 мг (±)-2-метил-6а, р-метил-2, 3, 4, 4Ь, 5, 6, 8, 9, 9а, 96, 10, П-додекагидроциклопента - 5,6 - нафто - 2,1-6)пиран-7- 6а Н -она смесь изомеров по С (1:1) в 4 мл пиридина обрабатывают 0,1 мл воды и 500 мг хлоргидрата метоксиамина, выдерживают 48 час при комнатной температуре, разбавляют дихлорметаном, экстрагируют рассолом, упаривают экстракт в вакууме и выделяют 954 мг (±)-6-(3-01Кс.ибутил) - За, р-метил-3,7 - диметоксииминопергидро - ЗН - бенз - ej-индана, который хроматографируют на ,50 г силикагеля (0,2- 0,5 меш), элюируя 10%- и 20%-ным растворами этилацетата в бензоле. Исходное вещество синтезируют, как в примерах 9 и 10, или же 1,5 г (±)-6-(3-грегбутоксибутил) - За, р - метил - 1, 5, 8, 9, 9а, 9Ь - гексагидро- 1Н -бенз - е - инден-3,, ЗаН - диона растворяют в 25 мл этанола, содержащего 0,15 мл триэтиламина и 200 мг катализатора (5%-ный палладий на активированном угле), .гидрируют при комнатной температуре и атмосферном давлении до прекращений поглощения водорода, фильтруют, упаривают фильтрат в вакууме и получают рацемат 6-(3-7рет-бутоксибутил)-3а, рметилнергидробенз - е -инден - 3,7-диопа в виде масла, ИК-спектр которого содержит полосы поглощения при 1735, 1705 и 1200 Этот продукт растворяют в 25 мл бензола. содержащего 100 мг «-толуолсульфокислоты, нагревают 4 час с обратным холодильником, охлаждают, промывают рассолом, упаривают в вакууме, фильтруют остаток через колонку, заполненную нейтральной окисью алюминия (III ст. акт.), и получают (±)-2-метил6-а,|р-метил - 2, 3, 4, 4Ь, 5, 6, 8, 9, 9а, 96, 10, 11 - додекагидроциклопента - 5,6 - нафто ,1-6) - пиран - 7 - . Пример 12. 640мг (±)-6-(3-оксибутил)За,р - метил-3,7 - диметоксииминопергидро ЗН -бенз- - индапа в 30 мл ксилола обрабатывают 3 г углекислого серебра, нанесенного на целит, нагревают 1 час с обратным холодильником в атмосфере азота, фильтруют, промывают бензолом, удаляют растворитель в вакууме и получают маслообразный продукт, после кристаллизации которого из гексана выделяют чистый (±)-6-(3оксобут.ил)-3а, ,р - метил-3,7 - диметоксииминопергидро - ЗН - бенз - е - индан, т. пл. ПО-111°С. Вычислено, %: С 68,93; Н 9,26; N 8,04. СгаНзгМзОд. Найдено, %: С 69,09; Н 9,24; N 8,14. Пример 13. 107 мг (±)-6-(3-оксобутил)За, р-метил - 3,7 - диметоксииминопергидро ЗН -бенз- е -индана в 5 мл метанола обрабатывают 1 мл 6 Н. соляной кислоты, нагревают 2,5 час с обратным холодильником, охлаждают, обрабатывают дихлорметаном и насыщ1ен.ным водным раствором бикарбоната, удаляют растворитель в вакууме и после кристаллизации из смеси ацетона с гексаном получают (±:)-19-нор-андрост-4-ен-3,17-дион. Пример 14. 3 г 2-метил-6а,,р-метил-2, 3, 4,46, 5, 6, 8, 9, 9а, 96, 10, 11 - додекагидроциклопента - 5,6 - нафто - 2,1-6 - пиран - в 20 мл эфира при 10°С добавляют к суспензии 600 мл литийалюминийгидрида в 25 мл эфира, перемешивают 1 час при комнатной температуре, добавляют воду, отфильтровывают твердые вещества, удаляют растворитель и получают (±)-2-метил-6а,р-метил-2, 3,4,46,5,6,6а,7,8,9,9а,9&, 10 11 - тетрадекагидроциклопента- 5, 6 -нафто- 2, 1-6 - пиран7р-ол в виде стекловидного вещества, ИКспектр которого содержит полосы поглощения при 3600 (ОН) и 1680 см-1 (енольный эфир). Пример 15. 837мг (±)-2-метил-6а, р-метил-2, 3, 4, 46, 5, 6, 6а, 7, 8, 9, 9а, 96, 10, 11-тетрадекагидроциклопента - 5,6 -нафто- 2,1-6 пиран-7р-ола смесь изомеров по Са (1:1) растворяют в 5 мл пиридина, содержащего 500 мг хлоргидрата метоксиамина и 0,2 мл воды, выдерживают 48 час при комнатной.температуре (тонкослойная хроматография не показывает никаких изменений через 24 час), обрабатывают дихлорметаном и рассолом, упаривают в вакууме, маслообразный остаток хроматографируют па 60 г силикагеля (0, 0,5 мещ), элюируя 30-75%-ными растворами этилацетата в бензоле, и выделяют (±)-6-(3оксибутил)-За,р-метил-Зр - окси - 7 - метокСииминопергидро- ЗН -бенз - е - индан в виде стекловидного вещества.
Пример 16. 417мг (±)-6-(3-оксибутил)За,р-метил-3р - окси-7-метоксииминопергидро ЗН -бенз- е - индана в 5 мл ДМФА обрабатывают смесью 500 мг трехокиси хрома, 0,25 мл серной кислоты и 5,5 мл ДМФА, выдерживают 2 час при комнатной температуре, разбавляют водой, насыщенным раствором бикарбоната натрия, экстрагируют дихлорметаном, выделяют дикетон в виде масла, растворяют его в 15 мл метанола, содержащего 7,5 мл 4 н. соляной кислоты, нагревают 2 час с обратным холодильником, разбавляют рассолом, экстрагируют дихлорметаном и выделяют (±)-19-нор-андрост-4-ен-3,17 - дион в виде масла, которое при хроматографировании на силикагеле (0,2-0,5 меш) дает одно пятно. При элюировании 10%- и 20%-ным растворами выделяют выщество с т. пл. 145-155°С.
После перекристаллизации из смеси дихлорметан-изопропиловый эфир т. пл. 155-157°С.
Пример 17. 980 мг (±)-2-метил-6а, р метил - 2, 3, 4, 46, 5, 6, 8, 9, 9а, 9Ь, 10, И - додекагидроциклопента - 5,6 - нафто - 2,1-& пиран-7- 6аН -она в 5 мл пиридина, содержащего 0,1 мл воды и 550 мг хлоргидрата гидроксиламина, выдерживают 24 час при комнатной температуре, экстрагируют дихлорметаном и выделяют диоксим (±)-6-(3-оксибутил) - За, - метилпергидро- ЗН -бенз - е индан-3,7-диона в виде масла.
Пример 18. 700 мг диоксима (±)-6-(3оксибутил) - За,р - метилпергидро - ЗН бенз- е -индан-3,7-диона растворяют в бензоле, содержащем 4 мл метилэтилкетона и 700 мг изопропоксида алюминия, нагревают 24 час с обратным холодильником, обрабатывают водным раствором едкого натра, экстрагируют метиленхлоридом и выделяют диоксим (±)б-(З-оксобутил) - За, р-метилпергидро - ЗН бенз- е -индан-3, 7-диона.
Пример 19. (±) - 2 - Метил - 6а, р-этил2, 3, 4, 46, 5, 6, 8, 9, 9а, 9Ь, 10, 11-додекагидроциклопента - 5,6 - нафто - 2,1-& -пиран-7 6аН -он, как в примерах 2 и 11 - 13, превращают в 13 р-этил-гон-4-ен-3,17-дион с использованием в качестве промежуточных продуктов (±)-6-(3-оксибутил)-За, Р - этил - 3,7-диметоксииминопергидро - ЗН -бенз - е -индана и (±) - 6 - (3 - оксобутил) - За, Р-ЭТИЛ 3,7 - диметоксииминопергидро - ЗН - бенз е -индана.
Предмет изобретения
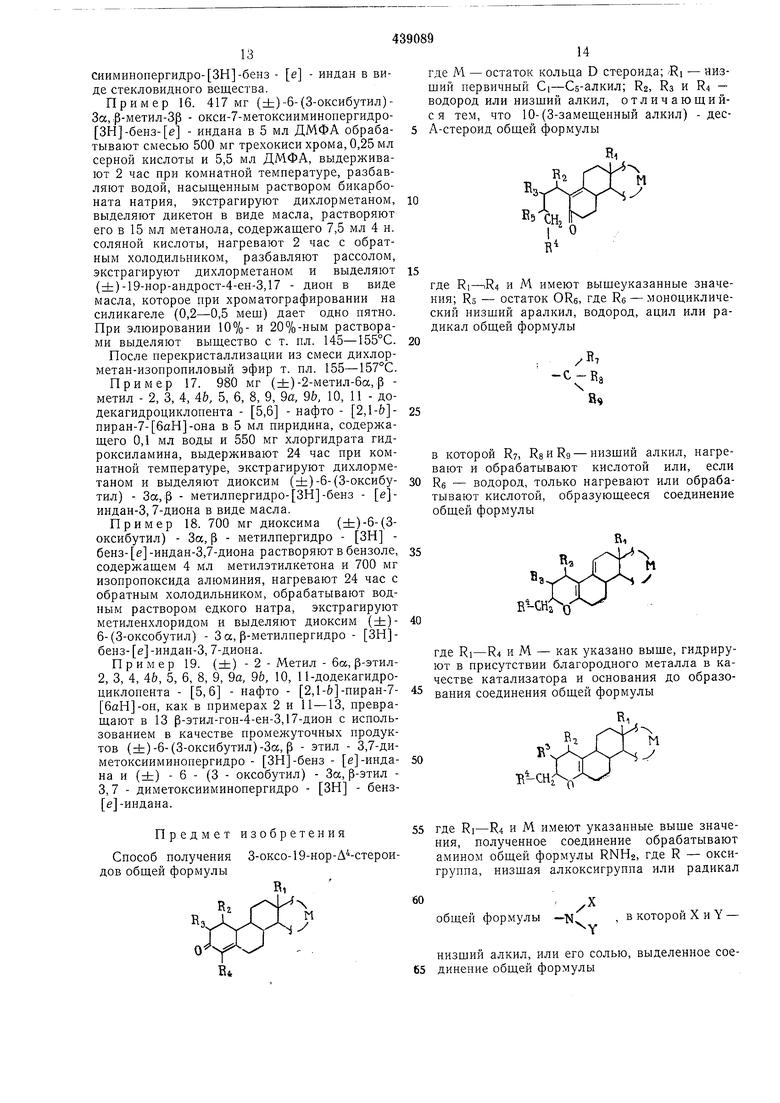
Способ получения 3-оксо-19-нор-Д4-стероидов общей формулы
RI
Нг
Л
м у
rYr
Bt
где М - остаток кольца D стероида; -Ri - низший первичный Ci-Сб-алкил; Ra, Кз и R4 - водород или низший алкил, отличающийся тем, что 10-(3-замещенный алкил) - десА-стероид общей формулы
10
где RI-(R4 и М имеют вышеуказанные значения; RS - остаток ORe, где Re - моноциклический низший аралкил, водород, ацил или радикал общей формулы
/Й7
-С-ЕЗ в
25
в которой Ry, R8иR9 - низший алкил, нагревают и обрабатывают кислотой или, если Rg - водород, только нагревают или обрабатывают кислотой, образующееся соединение общей формулы
35
40
где RI-R4 и М - как указано выше, гидрируют в присутствии благородного металла в качестве катализатора и основания до образо вания соединения общей формулы
50
,
55 где RI-R4 и М имеют указанные выше значения, полученное соединение обрабатывают амином общей формулы RNH2, где R - оксигруппа, низшая алкоксигруппа или радикал
60
X
/
общей формулы , в которой X и Y -
низший алкил, или его солью, выделенное сое65 динение общей формулы rVVN N где Ri-R4, R и M имеют вышеуказанные значения, селективно окисляют до соединения обш.ей формулы 10 где Ri-Нч, R и M - как указано выше, это соединенне обрабатывают водным раствором кислоты в среде инертного смешивающегося с водой органического растворителя и выделяют целевой продукт известными приемами.








Даты
1974-08-05—Публикация