котором разложение первичной или вторичной апкипароматвческой гидроперекиси общей формулы I в присутствии киспого катагтазатора ведут в растворителе апкипсупьфоне, содержащем 3-6 метипенов групп, причем одна ипи несколько этих групп могут быть замещены Cj- пом, ИЛИ карбонате С„ С. апкипенгпико пя. В качестве супьфонов применшот триме« тиленсульфон, ©С -метилтриметиленсульфон,-й(,- метиптетраметипенсупьфон, тетраметипенсуяьфон (супьфопан), пентаме-. тиленсульфон, ( мeтилпeнтaмeтилeнcyльфcl гексаметиг1енсупьфон,с(,«К.-ДИметиптетраметиленсульфои, предпочтительны в качеств растворителя супьфолан игги карбонаты этиленгпикопя ипи пропипенгпиколя. Указанные полярные растворители позволяют проводить разложение гидроперекисей общей формулы I в присутствии каталитических количеств соединений киспого характера с селективностью по фенопьным продуктам, по крайней мере, равной, а в основном большей, чем селез тивность, получаемая в известных методах, причем время реакции, необходимое для получения высоких степеней конверсии гидроперекисей, заметно уменьшается и составляет порядка нескольких минут. В.качестве алкипароматических гидро перекисей берут: бензип-, С -ксигга 1-, 1 -ксилил-, Я-этиггбензип-, Г} изопропип- бензип-, 2,4 диметипбензип-, 3,5--диметйлбензил-, 2,4,6-триметилбензйп-, П метоксибензип-, 1-фенипэтип, 1 {г1 метйпфенип)-этип-, 1(о этипфенил)-этип, 1-{| -этип фения)-этил-, 1--(2,4 диметипфенип}-этип-, 1.(3,5-диметипфенип)-эти 1-0 -хлорфенип}-этип, 1-(fj-метоксифенил)-этип-, 1-(Л- нитрофенил)-этип-, 1-фенип-)1)-пропил, 1 фенип «бутил-, 1-фенЕЛ-2,2 диметил-й-пропип-, циклогексипфенилметигс-, дифенипметип-, (б-меТ1у1фенил)-фенилметип-, (й-метилфении)-фенй пметй ге, ({у-хпорфени п)-фени пмети п, {h ,-мeтoscифeни л) -фени лмети п-, 1,2«яифе нипатип или оС тетрапшпгйщзоперекись. Предложенный способ разложения налболее пригоден дпя бензип-, -ксйпмл, 1 фенилэтил- или 1,2-диф0яилэтйпгййроперекйси. Применяемь @ первичные и вторичньге гидроперекиси подучают обычным способом, состоящим в пропусканви газа, содержащего кисдород, в яекатапйтйческих усповидх в жидкой фазе через соответствующий углеводород при заданной темпер туре; полученные гидроперекиси очищаю звестным методом, таким как перевод в натриевую соль и обработка уг-лекислым Ьазом.. Способ осуществляют следующим образом Гидроперекись вводят в смесь, состоящую из соединения кислого характера i и полярного растворитегш, предварительно выдержанную при температуре от 2 О С до температуры кипения смеси, предпочтительно при 50-110 С. Гидроперекись вводят в виде раствора в выбранном полярном растворителе. Можно использовать сырую гидропере кись, полученную частичным окнсзле шем углеводорода, после удаления большей гшсти непрореагировавшего углеводорода, например отгонкой. Используемьй в качестве катализатора кислотный агент может быть минеральной ипи органической протонной кислотой, например хлорной, азотной, серной, алкан- сульфокислотой, например метансульфо-. кислотой, арилсупьфокислотой, например бензолсульфокиспотой и | -тог1уолсу|1ьфо кислотой. Кислоту используют предпочтигепьно в чистом виде ипи в виде концентрированного водного раствора. Кроме того, в качестве кислых катализаторов используют безводное хлорное железо, треххпористый бор, окись кремния, диатомит, катализаторы Фридепя-Крафтса, такие как хлористый алюминий и хлористый цинк. Количество чистого кнспого реагента, применяемого для проведения разложения гидроперекисей формулы I, изменяется от О,1 до 1О вес.% по отношению к превращаемой гидроперекиси. После введения гидроперекиси реакцию продолжают при заданной температуре в течение времени, необходимого для получения наиболее высокой степени превращё ния гидроперекиси с минимальным проте канием реакций распада. Затем реакционную массу нейтрализуют щелочью. В случае применения протонной кислоты, она попкостью растворяется в реакционной смеси, вследствие чего рэакционная масса полностью гомогенна и для обеспечения контакта реагентов требуется только умеренное перемешивание. При этом на стадии . нейтрализации избыток необходимого щелоч ного агента очень невепик и соответственно невысоко количество образующихся солей нейтрализации, частично растворимых в реакционной смеси, что позволяет изба-г виться от дополнительной стадии разделе- ния. Из полученного раствора любым подходящим способом выделяют фенольные и сарбонипыйге продукты, например фракционной перегонкой. Можно работать при тех аавпени$1х и-температурах, при которых образующееся карбонипьное соединение удаляется по мере его образования.
Пример. В стеклянную копбу, снабженную центральным перемешиванием, 5 обратным хоподитЕзником, капельной воронкой, термометром и внешним обогревом, вводят 12,5 г супьфопана, содержащего 0,О5 г i. серной кислоты 98 вес.%), нагревают до 100 С, затем быстро добав- пяют 1,82 г бензипгидроперекйси, содержащей 85% шстой гидроперекиси. Далее смесь продолжают перемешивать при заданной температуре в течение определенного времени до полного разложения гидропереки- си. Затем нагревание прекрапхают и
нейтрализуют избыток кислоты теоретически необходимым количеством нормального метанольного раствора едкого натра
Баланс реакции, т. е. выход фенола и бензальдегида по отношению к чистой превращаемой гидроперекиси, определяют методом газовой хроматографии (ГХ). При аналогичных ycnoBHiix проводят опыт с использованием метилциклогексана (12,5 г) вместо сульфолана.
В опытах берут 0,0125 моль чистой бензилгидроперекиси, 0,0005 моль чистой серной кислоты при молярном отношении серной кислоты к гидроперекиси О,О4 и процентном (по весу) отношении серной кислоты к гидроперекиси 3,16%. Результаты приведены в табл. 1.
Таблица 1.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения фенолов и карбонильных соединений | 1974 |
|
SU555840A3 |
| СПОСОБ ПОЛУЧЕНИЯ КРЕЗОЛА И БЕНЗОЛДИКАРБОНОВЫХКИСЛОТ | 1971 |
|
SU294336A1 |
| ПОЛУЧЕНИЕ СОЕДИНЕНИЙ ОКСИРАНА | 2001 |
|
RU2282625C2 |
| Способ получения фенола и циклогексанона | 1976 |
|
SU586157A1 |
| Способ получения фенола и ацетона | 1977 |
|
SU687062A1 |
| Способ получения этилфенола | 1975 |
|
SU584756A3 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОПЕРЕКИСЕЙ МОНО- ИЛИ ДИИЗОПРОПИЛБЕНЗОЛА | 1968 |
|
SU209460A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОПЕРОКСИДА КУМОЛА | 1994 |
|
RU2131414C1 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОПЕРЕКИСИ КУМОЛА И/ИЛИ ГИДРОПЕРЕКИСИ ВТОРБУТИЛБЕНЗОЛА | 2002 |
|
RU2222527C1 |
| Способ получения гидроперекисей алкилароматических углеводородов | 1975 |
|
SU567723A1 |

Продолжительность, мин
Выход,%: ,
фенола
бензальдегида Пример 2 В стеклянную колбу аналогичную примеру 1 и обогреваемую снаружи, вводят 12,5 г сульфолана содержащего 0,О5 г (98 вес.%) серной кислоты, нагревают до , затем быс ро добавляют 2,77 г п-ксилилгидропере киси, содержащей 62,5 вес.% чистой ги роперекиси. Далее смесь перемешивают при данной температуре в течение опре.деленного времени до полного разложени гидроперекиси. Затем работают по мето ке примера 1. Выходы п-крезола и п толуилового альдегида по отношению к чистой превращаемой гидроперекиси опре деляют методом ГХ. Получены следующи результаты: 12,5ООО Сульфолан, г fl-Кси ли лги дроперекись 0,0125 чистая, мопь Серная кислота чидтая, О,ООО5 моль Молярное отнощение серной кислоты к гидро0,04ОО перекиси Процентное (по весу) отношение серной кисло2,8300 ты гидроперекиси,% Продолжительность, мин 7,ООО Содержание перекисного 16,8ООО кислорода,%
70
18,3 30,0 Выход,%: П-крезола51,ОООО П -топуипового альдегида17,4000 П р и м е р ы 3 и 4. В стеклянную колбу, аналогичную примеру 1 и обогреваемую снаружи, вводят 25,4 г супьфолана, содержащего 0,1 г (98 вес.%) серной кислоты, нагревают до 1ОО С, затем быстро добавляют 3,57 г 1-фениг этилгидроперекиси, содержащей 96,7% чистой гидроперекиси. Далее смесь продолжают перемешивать при заданной температуре в течение определенного времени до полного разложения гидроперекиси. Затем работают по методике примера 1. При аналогичных условиях проводят опыт с 25 г карбоната этиленгликоля в качестве растворителя. Для сравнения прово.оят аналогичные опыты с использованием неполярных растворителей, например этилбензола (17,4 г), или основных, например диоксана (2О,6г) и ацетонитрила (15,66 г). Баланс реакции, т. е. выходы фенола и образовавшихся карбонильных продуктов по отношению к чистой превращаемой гидроперекиси, получают методом ГХ. Во всех опытах берут 0,025 мопь 1-фенилэтипгидроперекиси, Р,ОО1 моль чистой серной кислоты при молярном отношении серной кислоты к гидроперекиси 0,О4 и процентном (по вебу) отношении
Взяты для сравнения
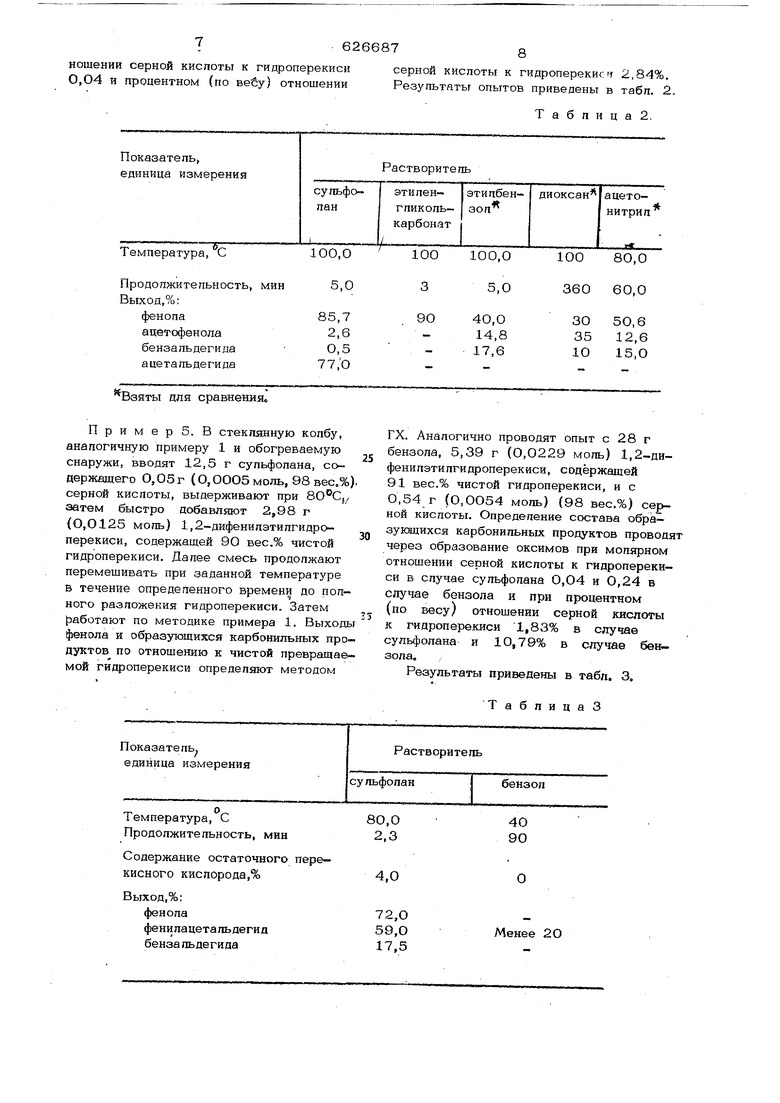
Пример 5. В стеклянную колбу, аналогичную примеру 1 и обогреваемую снаружи, вводят 12,5 г сульфолана, содержащего О,05г (О,ООО5моль, 98вес,%) серной кислоты, выдерживают при ,/ затем быстро добавляют 2,98 г (О,О125 моль) 1,2-дифенилэтилгидроперекиси, содержащей 90 вес.% чистой гидроперекиси. Далее смесь продолжают перемешивать при заданной температуре в течение опредепенного времени до полного разложения гидроперекиси. Затем работают по методике примера 1. Выходы фенола и образующихся карбонильных продуктов по отношению к чистой превращаемой гидроперекиси определяют методом
Содержание остаточного
кисного киспорода,%
Выход,%:
фенола
фенилацетальдегид
бензальдегида
серной кислоты к гидроперекисf 2,84%. Результаты опытов приведены в табл. 2.
Т а б л и ц а 2.
ГХ. Аналогично проводят опыт с 28 г бензола, 5,39 г (0,0229 моль) 1,2-дифенилэти лги дроперек иси, с одёржащей 91 вес.% чистой гидроперекиси, и с О,54 г (О,ОО54 моль) (98 вес.%) серной кислоты. Определение состава обра- зукнцихся карбонильных продуктов провод через образование оксимов при мол$фном отношении серной кислоты к гидроперекиси в случае супьфопана 0,04 и 0,24 в случае бензола и при процентном (по весу) отношении серной кислоты к гидроперекиси 1,83% в случае сульфолана и 1О,79% в случав бензола.
Результаты приведены в табл. 3.
Таблица 3
О
Менее 2 О Формупа изобретени Способ попучения фенолов и карбонипьиых соединений разпожением первичных и вторичных агасипароматическнх гидроперекисей общей формулы СНООН ПRII) где R - водород, С - С -алкип, галоген, нитро- ипи С|,- агосоксигруппа} R - водороп, С,- , циклоалкип арил, арапкип ипи R вместе с орто-С- С апкипом R образует двухвалентный радикал - алкилен; П 1-3, в присутствии кислого катапизатора при повьпиенной температуре в среде инертного органического растворителя и выделением целевых продуктов, отличаю,62 щ и и с я тем, что, с целью упрощения технологии процесса, в качестве растворителя используют алкиленсупьфон, содержащий 3-6 метиленовых групп, причем одна или несколько этих групп могут быть замещены С алкилом, или кар бонат Cjj-алкипенгликопя. 2. Способ по п. 1, о т л и ч а ющ и и с я тем, что в качестве растворителя используют сушзфолан ипи карбонат этиленгликопя, или карбонат пропипенгпикоИсточники информации, принятые во внимание при экспертизе: 1.Кружалов Б. Д. Совместное получение фенола и ацетона. М., 1963. 2.Патент США N1)2874147, кп. 26057, 1959.
Авторы
Даты
1978-09-30—Публикация
1974-07-26—Подача