л; о; кт
; ;Г1оннер; нужно полуил растворовf содержа;баль,- со более: удобно ;- еталла вместе и отде ба.ль г от малн .
;;ко;: ;::;; ;;ра;-п: аник нейтрально -/. лек;.:г обь-ч ю плет с выделениС:лсг:ы 1-,сжел КОзниккуть необхоГ:- лос;; B.iRHKJi ;ге:1Очи для поддероП :: .-jfjcy С:М(:;М уровне. ХинО i к-;:(; сную т,:ислоту |-4ожно также полнос/ью или част1- чно в соли inGJKi Kj-o металла, хотя :;iocov i-n car удобен для непре:) О прс рзволотва .
(-j/cci; нь-чеокого раотво;;: ;:р11;.0 1гсгь любой подвижt.cKMH ра:сс}зоритель или
с: ; орые не смешиваются с .L.cjMcoiv; рИ являются .. с . к воде, к ме О(С:;инечипх и к хинолин -
iC; кислоте, например али
I арок лтические углеводоc::-4J04 .ie углеводороды,
:1 CF;H;I разделения водной уэ:- желательно при:1ор1-1тсль с п;ютнг:стью, :я СУ- полного слоя, Разде-П1.Г er-;;;i;TC:n при максималь-, i .;,-1стей ;;;идкС;оти . лпчуусс ;:е .пг,ностыо раотр;.с-чсрителе, но полнос-i/ vcH то луч::1€; приме;р1 е. г ч KOTOpiJX плотчe1 c:i -) раст)ЭОрите;1Я такочс1:ччп:: нанкый твердый
;). :сееть ИЗ ПОВерХ ;л;; рч с гвоэител ь - вода, р-лсуворителей являч;: частчорители, например гччуус у 41чг-о.иородь S Е ча Ч ч KJF) ч ч ч л е ч i4-Hi X л о р э О а к
ЧЧ)ччч, ч-;стзоди1ь путем :-одчс 43 часччора и раство- ччи;;;; :: коной кислоты 1 - срсчзч ческом rujyjTBOpH:ччч8ечс ;:В;-юшен температуу: 1м:-1Рт гЮй ; при Г1ере -.1е1ли iyiyroM способе взмучивания i44 vofo тобы увеличить 1 раядеаа вода-раствориоолэ : чаат образование комччле--еч.зс Затем перемейшоагуают - дают разделиться я:5 - слою растворителя. б-учь :)егч-1О,цическим или .. Во ачез; случаях раотво-с сучонять от с одержимолере:п псЕторкым кополь( I
ао органического раство 1рают таким, чтобы оно зало объему экстрагируеморастворЕ;, концентрации еталла ч установке для осу;-:,ествдения процесса. Отношение оргаг ический растворитель-вода обычно 5;1-1:5. Нет необходимости во всех случаях применять такое количество растворителя, чтобы происходило полное растворение образующегося комплекса, так как избыточный в растворе комплекс обычно остается в виде с:,спензии полностью в органическом растворителе и не мешает переработке и разделению слоев растворителя и воды
При желании можно применять смеси хинолин-2-карбоновых кислот и других соединений, например длинноцепочных алифатических спиртов, например каприлового спирта, изодеканола, тридецилового спирта или 2-этилгексанола, которые помогают образованию и экстрагированию комплексного соединения, в количестве 0,510% по весу органического растворителя .
Иногда желательно добавлять поверхностно-активные вещества, например продукты конденсации окиси этилена и алкилфенолов , для оР легчения разделения водной и органической фаз путем умень1-1ения эмульгирования.
Желательно применять растворы растворителей, содержащие более 2% хинолин-2-карбоновой кислоты.
Металл можно выделять из растворителя после стадии извлечения любым обычным способом, например экстрагированием в водную фазу при более кислой среде, в которой комплекс разлагается.
Если в растворителе имеется комплекс более чем одного металла, то разделение металлов можно в некоторых случаях вести экстрагированием отдельными водными растворами с повышающейся кислотностью для последовательного раздельного разложения комплексов. По другой методике комплекс в растворителе можно прямо гидрировать и получать металл. При такой обработке регенерируется лиганд и выделенный растворитель, содержащий хинолин-2-карбоновую кислоту, можно снова использовать в процессе, особенно при непрерывной работе.
Предлагаемый состав особенно применим к водным растворам, полученным от обработки минеральных руд, металлолома и других металлсодержащих остатков водны.ми кислотами, например серной, соляной, фтористоводородной или азотной, или к металлсодержащим сбросным жидкостям от электролиза или химических процессов Он пригоден для выде1 ения металлов из растворов, содержащих не менее 0,5 г/л и особенно для обработки растворов, содержащих более 2 г/л
MGT аЛЛ а.
Хинолин-2-карбоновые к ислоты, применя eiVCJe при- осуществлении этого способа, являются .човыми ьешес1ва.ми.
Хинолин-2-карбонопые кислотк мочено получать из сложных эфиров, лучше из низших алкильных эфиров хинолин-2-карбоновых кислот формулы Г, где К -гидроксильная грхппа, путем превращения гидроксилькой группы в нужный атом галоида или произвольно замещенную алкоксильную, алкеноксильную, циклоалкокси, арилоксильную или аралкилоксильную группу известными методами для 4-оксихинолинов и гидролизом эфирной группы, например 1иелочью для получения кислоты.
Хинолин-2-карбоновь;е кислоты форьгулы 1, где хлор или бром, можно получать из алкильных эфиров хиь:олин-2-карбоновых кислот формуль.
1 , где R это гидроксил, путем нагревания с хлорокисью фосфора или пятихлористым фосфором, или бромокисью фосфора , соответственно ;; гидролизом
эфирной группы.
20
Хинолин-2-карбомовые кислоты формулы Г, где R - произвольно замещенные алко1 сил bHhJC , алкеноксильные , - циклоалкилокси.чьные, арилоксил ьные или аралкилокси-группы, можно получать из алкильных эфиров хинолин-2-карбоновых .пот формулы I , где хлор или бром, Плгем нагревания с производным ; елочного металла со) I
ответственно произвольно замешенного сгтирта или фВнола с последующим гплролизом эф:иг:м-ой группк. ИлгреваН1-:о удобно вести в таком растворителе, как ксилол. Этот метод особенно при получении хинолин-2-карбоиовкх кислот, где - а.)илоксигруппа.
,1 Хинолин-2-карбоновые кислоты формулы Г, где R - произвольно заме:;;ениь;е алкокси, алкенокси, циклоалкокси или ара.чкокси-группы, можно получать из алкильных эфиров хи 1олин-2-карбоновых кислот формулы Г, где R- гидрокскл ьна я группа, путем iiaг, гревания с соответствующим алкил, а;1кенил, цкклса-пкил или аралкилхлоридом или бромидом в присутствии основания, ь:ап1-)имер карбоната калия, и гидролизом эфирной группы. Нагре, вание удобно вести в таком растворителе, как .
Алкильные эфиры хинолин-2-карбоновой кислоты форму-пъ; Г, где R ,5 это окси-группа, применяемые как исходные вещества в указанных процессах, можно получать, например, известньчзми методами из ариламинов форхулг, II и алкмла, напри.мер этилокс а.1:оац;- ЛЬ11::1Х эСИров формулы III , нагрявсГ:П1ем, например, в кипящем толуоле с образогзанием.- этилфени.пиминоrj cyKUHHaia, который циклиз ют в 4-оксихннолин-2-карбоновую кислоту н греванием ггр-н 240-250Ct , Vv СО , Пример л. Около 180 вес.ч, 6 н серной кислоты по каплям добавляют в течение 10-15 мин к хорошо перемеыиваемой смеси 209 вес.ч. этил натрийоксалацетата, 500 ., воды и 870 вес,ч. толуола при Of , Полученную слегка кислую смесь (рН - 3 перемешивают при этой темг1ерату1)е в течение 45 мин, Толуольный слой удаляют, водный слой и выпавший сул фат натрия промывают толуолом (2 порциями по 65 вес.ч.), соединенный толуольный слой и промывки отьмвают затем от кислоты аодой, сушат сульфатом магнии и фильтруют. К толуольному раствору этилоксалацетата добавлямт 117,, вес. ч, ;( -толуидина и смесь кипятят с С)брс Тной перегонкой в течение 60 мин. за это время выделяется 18 Бес.ч,, аоды которые удаляют в аппарате Диб аСтарка. После ослаждения оранжевый толуольный раствор промывают 2 н„ соляной кислотой (3 порции по 100 вес.ч для удаления непрореагмровав шего rt -толуидина, затем до отсутствия кислоты сушат над сульфатом магния. Из этого раствора пос ле отгонки толуола в вакууг-ле гюлучают 258,2 вес „ч . этил-(П -толнлими -сукцината в виде оранжевого масла, которое смеилизают со 11С вес. ч. тер мекса (эвтектическая смесь дисренила и окиси дифенила) к затем по каплям. э течение 60--90 мин лобаьляют к 1920 вес,ч. хорошо перемешиваемого термекса при 240-250. После ЕЫ,делени я этанола (37 в ее. ч.) и оттонки его в ректификапионной колонне; тем ной реакционной смеси дают охладить ся, затем ее выдеркиважт при комнат ной температуре 2-3 дня. Выделившие ся коричневые кристаллы (. 45,2 вес. фильтрованием, промывают . 300 вес. ч. петролейного эфира IT„ки 60-80 С) и сушат на воздухе. Псусле очистки перекристалл;-1Эацией лз ацетона получают 115,2 вес, ч. этил--4 ок ил - X и н о л и н - 2 - к ар 5 о к с и л а та в виде небольших светло-ксфичневых игл с т . пл . 214- 2 16 С После упаривания ацетонового магочного раствора получают 13,9 вес.ч, мпнее чистого продукта с т . пл . 207-208с. Хорошо перемешиваемую смесь 34;5 вес . ч . этил-4-окси-6-метилхиноллН--2-карбокс;г-:лата,- 21 вес. ч. безводного карбоната калия, 46,-5 в«;С,ч, 4-додецилбензилхлорпда {полученного из замещсчногс сильно разветвленног додецилбензола, клороульфоновой кис-лоты; метанола и П -формальдегида) и 615 вес,ч. безводного ацетона нагревают с обратной перегонкой в течение 68 ч. Охлажденную коричневую реакционную смесь фильтруют для удаления неорганических солей и непрореагировавшего этил-4-окси 6-метилхинолин-2 карбоксилата (3,7 вес.ч.), ацетон отгоняют ti вакууме. Раствор остаточного коричневого масла в эфире (285 вес. ч.) промывают последовательно 1 н. раствором едкого натра (2 порции по 50 аее.ч.) и водой (2 порции по 50 вес ,ч.) , затем сушат над, сульфатОМ магния и отгоняют растворитель. Остается 69,2 вес.ч. этил-6 метил-4-(4 -додецилбензилокси)-хинолиН-2-карбоксилата в виде вязкого ко-ричневого масла, которое растворяют в 120 вес.ч . этанола и кипятят с обратной перегонкой 2,5 ч с раствором 6 вес.ч. едкого натра 3 25 вес.ч, воды. После охлаждения реакционной смеси до натриевую соль 6-метил-4-(4 - додецилбензилокси) -хинолин-2-харбоновой кислоты, выделившуюсяв виде бесцветных грану/ (53 ,,4 вес. ч.) . собирают фильтрованием, прогллвают 25 вес. ч. этанола и сушат 34,2 вес„ч. натриевой соли 6-метил-4-(4 -додецилбензилокси) -хинолин-2-карбоновой кислоты суспендируют в 750 вес.ч. хлороформа, содержащего 50 вес.ч. ледяной уксусной кислоты. После интенсивного встряхивания смеск 3 течение 10 мин добавляют 200 Bec.-i, воды, переме1:-1ивание ведут в течение еще 5 мин и отделяют нижний хлорофоркенный слой,. Этот органический слой повторно азбалтывают с 10%-ной водной уксусной кислотой (5 порций по 50 вес.ч.), затем с зодой (порции по 100 вес. ч.) до удаления кислоты и сушат над сульфатом магния. ; лороформ удаляют из фильтрованного раствора в вакууме, остави ийся вязкий остаток нагревают при лм рт.ст, в течение 4 ч для удаления всего растворителя. При охлаждении нязкое масло затвердевает. Получают 30,8 вес.ч. 6-метил-4- ( 4 -.г;одецилбе:нэилокси ) -)синолин-2-карбоновой кислоты з виде бледно-желтогс твердого осадка- с т.пл. 95-9б-с (размягчение при -- 70с) . Найдено,% г С 78,7; Н 8, 1 ; N 2,6 ., В 1числено, % С ,1: Н 8,5; Пример 2. По методике примера 1, применяя Г -бутиланилин вместо П -толуидина, получают этил-4-окси- 6 -н-бутилхинолин-2-к арбомовую кислоту с т . пл. 165 С и 6-н-бутил-4-(4 -додецилбснэи1;окси) -хинолин-2-карбоновую кислоту Б виде очень вязкой светло-коричневой смолы-. Пример 3. Перемешивают сме этил-4-окси-б-н-бутилхинолин-2-карбоксилата, полученного аналогично примеру 2, и 213 вес,ч. хлорокиси фосфора. По окончании экзотермическ реакции темно-окрашенную смесь оста ляют на 1 ч при комнатной температу ре, затем охлаждают до О С,разбавляют 75 вес.ч. этанола для усиления подвижности и потом по каплям добав ляют к 500 вес.ч. льда 1500 вес.ч. воды. Водную смесь нейтрализуют до рН 7-8 добавлением карбоната натрия при этом выпадает 133,2 вес.ч. свет ло-коричневого кристаллического оса ка, который собирают фильтрованием и сушат. Это вещество очищают кристаллизацией из 380 вес.ч. ацетона (с обработкой углем), получают 100,8 г этил-4-хлор-6-н-бутилхиноли -2-карбоксилата, который выделяют в виде светло-серых игл с т.пл. SBSB, . Дополнительные 27,5 вес.ч. менее чистого продукта с т.пл . 54,5 получают при разбавлении ацето новой маточной жидкости водой. 4-Хлор-6-н-бутилхинолин-2-карбоновую кислоту получают обычным способом из этилового эфира (43,7 вес. гидролизом при кипячении с 20%-ным раствором едкого натра и подкислением. Она выделяется в виде бесцвет ных игл (28,7 вес.ч.) из водного 5,5, М 4,5 Найдено,: C,4H|4NO.CP Вычислено,%: С 63, Н 5,35; 5,3; се 13,45 . Хорошо перемешиваемую смесь 55 вес.ч. 4-нонилфенола (смешанные изо меры, полученные алкилированием фенола тримерами пропилена) , 870 вес. ксилола и раствор 20 вес.ч. едкого натра в 25 вес.ч. воды кипятят с об ратной перегонкой в течение 4,5 ч и обезвоживают с помощью аппарата Дина-Старка. Затем добавляют 72,9 вес.ч. этил-4-хлор-6-Н-бутилхинОЛИн -2-карбоксилата и безводную смесь кипятят с обратной перегонкой в теч ние 40 ч. Ксилол отгоняют паром и водную маточную жидкость декантирую (в горячем состоянии) с оставшейся светло-коричневой резиноподобной массой, которую затем промывают 1200 вес.ч. воды и суспендируют в 1500 вес.ч. хлороформа. В суспензию натриевых солей добавляют 100 вес.ч ледяной уксусной кислоты и пере мешивают в течение 60 мин, затем обрабатывают 200 вес. ч. воды. Водный слой удаляют, оставшийся хлорформен ный раствор промывают 10%-ной водной уксусной кислотой (4 порции по 200 в ее.ч.) и водой (порциями по 200 вес. ч.) до отмывки всей кислоты После сушки над сульфатом магния хлороформ отгоняют в вакууме и полу 710 чают 120,1 вес.ч. прозрачного красного масла, которое растворяют в 500 вес.ч. этанола, затем нагревают с обратной перегонкой 30-60 мин с раствором 12,5 вес.ч. едкого натра в 25 вес.ч. воды и 20 вес.ч. этанола. После охлаждения реакционной смеси и перемеггивания ее в течение ночи при комнатной температуре фильтрованием собирают 95,1 вес.ч. натриевой соли 6-н-бутил-4-(4 -нонилфенокси)-хинолин-2-карбоновой кислоты, которую выделяют в виде светло-корич 1евых гранул, их промывают 85%-ным этанолом (100 вес.ч.) и сушат в вакууме . 95,1 вес.ч. натриевой соли 6-н-бутил-4-(4-нонилфенокси)-хинолин-2-карбоновой кислоты суспендируют в 750 вее.ч. хлороформа, содержащего 35 вес.ч. ледяной уксусной кислоты. После встряхивания смеси в течение 10 мин добавляют 200 вес.ч. воды, перемешивают eiie 5 ми и отделяют нижний хлороформеиный слой. Органический слой снова взбалтывают с 10,ной водной уксусной кислотой (Ь порций по 50 в ее . ч.) , затем с водой (порции по 100 в ее. ч.) до вы ывaния всей кислоты и сушат над сульфатом магния. Хлороформ отгоняют от фильтров анно1О раствора в вакууме, остается 91,6 вес. ч. fi-н-бутил-4-(4 -нонилфенокси) -хинолин-2-карбоновой кислоты - прозрачного красного масла, строение которого доказано спектральН 1м анализом. Пример 4. По мсзтодике примера 3, применяя 2-трет-бутил-4-метилфенол вместо 4 -нонилфснола, получают 6-Н-бутил-4 -(2-трот-бутил-4-метилфенокси) -хинолин-2-карбоновую кислоту в виде красной вязкой смолы. Пример 5. По методике примера 3, применяя 2-трет-бутил-5-метилфенол вместо 4-номилфенола, получают 6-н-бутил-4 -(2 -трет-бутил-4 -метилфенокси)-хинолин-2-карбоновую кислоту в виде красно-коричневой вязкой смолы. Пример 6. По методике примера 3, применяя 2,4-ди-трет-пентилфенол вместо 4-нонилфенола, получают 6-н-бутил-4- ( 2 , 4-ди-трет-Г1ентилфенокси)-хинолин-2-карбоновую кислоту в виде коричневой вязкой смолы. Пример 7. Повторяют методику примера 6, применяя 17 вес.ч. 4-фенилфенола вместо 2,4-ди-трет-пентилфенола. Получают 35,4 вес.ч. 6-н-бутил-4-(4 -фенилфенокси)-хинолин2-карбоновой кислоты в виде вязкого темного масла. Пример 8. Повторяют методику примера 6, применяя 17,5 вес.ч. 4-циклогексил()енола вместо 2,4-ди-трет-пентилфенола. Получают 11,7 вес.ч. 6-п - 4-(4-циклогексилфенокси)-кинолк;1-2--карос;иозоа кисло да очень знлко//с TBf.. мед
П р и ы е о ; . ;.;,-; s ее: -трет-бу1ч-ш-4 ме.силФакопс, и 22,4 вес ч, ед:;огс калы т i воды к б с вес,, ллщг нс; пятят с обратной nepefcnKo фере азота до полного рлстк фенола. , иобс.злнют 4(;С ксилола и STTI,
- б - Н - б у т ил к я Н с л и i Е - ; - е Р R i3
лоты (из примег:;: ji « ;.:с;.--7:-продолжают 2С ч в икерлной ре i После добав.ле;-;ия ;ui; зе воды л гиетанол ;. .. ;: ром и смеси дага- ;;;: ь.-фазу декантиру1о;1р: iiojVy-iciwосадок, 1;:у эате .трог: доя л Су C;je i,bv ру;от . иО -
рОфОрмсР Xj;O;JOQO-pr.iSL;Ky 10 - V С
обрабативаюг 30 вес.ч укс лоты, Смусь D зб:1ЛМ мьа:0л .; и добавляют i(0 3 ас ,- -ouiV-. удаления слоя хлслзс раствор с НОВ;: i:poiv:bib аюл -uP ной уксусной |;мг:лотоп J 200 веер-:,) . затем 1зо,цок ii по 200 вес,ч.) до ;У кислоты и 1-:ад супьРа Хлороформ с-1тонч;от а так у у фильтрованногю рас IHvjca , о
того лролух :;-: ;y-jj-::,C.:: ао.. лизуюУся X ciа;-; 3 i-a-j,, , с, KpHCTa;ulH3iL.pa: из г:с : а, ,:, v,l pa ; т -КУГ , 60- SO СУ iia;.; 42,4 зес.ч. Ь ;- а-.,: ,. л;. / у бутил-;-a.l;-ai.:;V ;;aa: а a-hiбоновой .;ис ic-aj. а ana вых крас .aaiyar;; с:
-карбоксила л ,:: ; масла и б -мет аа зилокс О -хиью/:,-; ту в с с а а л а: г засла .
та С; т уап . л39, S-C (разложение) и
окси-4 - ( 4-чонилфенокск) -хинолин-2-асарбоновую кисло1у к виде светлоaej-airci полутверд;ого продукта,
П р и м е Р 13. о методике пример:- } , применяя О толуилик вместо к - -олуидкна. по/:учают э-;ил-4-0X0 В - i, ;е и лх и Н ол ин-7-карбоксилат р aavjr ;.3«-139°С k 8-метил-4--( 4 ДОдеа,:: лбенэи1и.) - xиl-ioлин-/-кapбoнo ivю кислоту в Е1-{1-;е БЯЗИОГО коричкв- аа:.. маапа ,
Р и и м е р 14, Этил Ч-ОКОЙ--8-.чатилхииолига-2 -харбокоилат ,, лолуaaH;ajft ана; сгичнс; примеру 13, презра:лают г:о покмера 3 :з этил-- 4 ХЛОР-- 8- ь-еаилхиь1олин -2 карбоксипат
.. П,л
а аа :;. С (разложение) л 8-ме ь;.И- - ( --ЧОКИЛфеПОКСИ ; - хин ОЛИ Н-2.raraiava; «аю кисл(;ту а т , пл , 1211 :; i : , ;а:а;,е,г ле:. аутек обработки
a-TpOJ:eH ibiM афИрОМ, в КОТОrajM uepbJjH кислота слабо растворима,.
Ра а. к ;,и я 6 -;чати;а- - { а конилфенокси) a-:Hia:ai,-м 2-ь. apooiioaaft кистюты с: меia;,i;; j и caieTBTOM кооальта а г ипятем
1 о о
192-193 С (раэложес т , пл
м :: р 1 ; , По
;:иг4а1;яя Л --метокск о-толуиа у -т.а; ун aiics., получают
;: :., о а.1С ГОлСа- В - Mela IЛ ХИ Н О
S -;--.атакси-В-:а:агкл-4-(4,.cj алакга- ) --хк нолаи-2-карбо аа -- аоаутаердьа- продукт
J - - т а
. ; а р 16. По методике ./аая: : 4-хлор-о-аолукдик
;-ау- Лика, ло луча.ют этил-:аа- 6-метклхиноа ин-2: г т . па . 12 3-1 24 , и Nic V- а-- 4 { Р-додеди. бензилока.а Р -:ароанопу10 к-с;;оту в -а а аоаутпердао продукта. м ;-: у iP По метэдике при:ричга я а-х;1ора - И.мин змес. .:i.iaсу асаучают эакл-8ж г-.; ; а :-i с ли к - 2 - к арб оке и лат с
; Паа аС име i-:e;ia и вмесf-бенз нахлорада бекзклхлори;к т эти г -В- хлOD--4-бензилхиa)a5oKcv.лат с а „ пл , i4jч г.. г и io. по 1 етодике приpaMera-iK :1а-а;;аа;кеалилг1ропи чаг;: эти;1акаа.1адетата и tt буain EMe:i.:T(; а -толуид -на, пос 1---сго.пь:;оаа 1аем в качестве НОЙ кислоты в начальной стадии конденсации , этил-3-метил-4-окси-6-н -бутилхинолин-2-карбоксилат с т,пл. 15б--157 С и 3-метил-6-к-4-( 4-додецилбензилокси)-хинолин-2-карбоновую кислоту в виде светло-оранжевого вязкого масла. Пример 19. По методике при мера 18, применяя анилин вместо И -бутиланилина, получают этил-3-метил-4-оксихинолин-2-карбоксилат с т.пл. 175-177 -с и 3-метил 4-( 4-додецилбензилоксяхинолин-2-кар5оновуюкислоту в виде светло-желтого масла Пример 20. По методике при мера 18, применяя о-толуидин вместо П -бутиланилина, получают этил-3,8-диметил-4-оксихинолин-2 карбоксилас т.пл. 133-134с и 3,8-диметил-4-(4-додецилбензилокси)-хинолин-2-карбоновую кислоту в виде вязкого светло-желтого масла. Пример 21. Хорошо перемеида ваемую смесь 65,1 вес.ч. этнл-4-оксихинолин-2-карбоксилг1та, 42 вес. ч. безводного карбоната калия 38,4 вес аллилбромида и 800 вес.ч. ацетона кипятят с обратной перегонкой в течение 24 ч. Охлажденную реакционную смесь фильтруют для удаления неорга нических солей, ацетон отгоняют в вакууме. Раствор оставшегося коричневого масла в эфире (360 вес.ч.) промывают сначала 1 н,раствором едкого натра (3 порции по 50 вес.ч.) и водой (4 порции г;о 100 вес. ч.) за тем сушат над сульфатом магния и от гоняют растворитель . Получе:-:ное вяз кое масло кристаллизуется при охлаж дении, кристаллы перекристаг.;:изовы-вают из петролейного эфира (т.кип. 60-80°С) и получают 57,1 вес.ч. эти -4-аллилоксихинолин-2-карбоксилата в виде светло-желтых игл с т.пл. 71-72 С. Хорошо перемеишваемую смесь 61,4 вес .4. этил-4-аллилоксихинолин-2-карбоксилата и 320 вес.ч. Шеллзол Т (алифатический керосин) нагревают при 180-190 С в течение 2 ч в атмосфере азота. После охлаждения реакционную смесь фильтруют и твердый продукт промывают 50 вес,ч. пет ролейного эфира и кристаллизуют из олуола. получают 49,2 sec.ч. этил-3-аллил-4-оксихинолин-2-карбоксилата в виде бесцветных игл с т.пл 146 , 5-147с . После дальнейшей очистки из этанола небольшой порции вещества получают крупные ромбические призмы с т.пл. 148,5-150 С. Найдено,%: С 69,7; Н 4,9;N 5,0. С|5 Н gNOj Вычислено,%: С 70,0; Н 5,9;Ы 5,4 Раствор 49,0 вес.ч. этил-3-аллил - 4 - ок с и X и fi ол ин-2-карбоксилата в 600 вес.ч. кипящего этанола перемешивают 5 ,мин в 3 вес. ч. Зч-могчт -;атализатора - палладий на угле. Затем его фильтруют, фильтрат вместе с 5 вес.ч. свежего катализатора загружают в автоклав из нержавеющей стали и добавляЮТ водород при комнатной температуре до давления 50 атм. После перемешивания в течение 16 ч поглощается 1,38 молей водорода. Реакционную смесь растворяют в горячем этаноле, фильтруют для удаления катализатора и выпаривают, получают 39,3 вес.ч. этил-З-н-пропил-4-оксихинолин-2-карбоксилата в виде светло-желтых игл с т.пл. 155-157с, которые отделяют и сушат, еще 4,8 вес,ч. менее чистого продукта с т.пл. 140146 С выделяют из эта нольного маточного раствора после упаривания в вакууме. После поваорной перекристаллизации из этанола получают очень светло-желтые призматические иглы с т.пл. 15 8-15 9, 5 С. Найдено , % : С 69,3; Н 6 , 3 ; К1 5,2. C. Зычи ел ено , % : С 6 9 , Ь ; Н 6 , 6 ; N 5, 4 . 3-н-Пропил-4-оксихинолин-2-карСоновую кислотч, получе:- (ую обычным способом из ее этилового эфира гидролизом кипящего 12%-:1ого раствора едкого кали с последхН :цим подкислением выделяю из 5 О-i-но го этанола в виде тонких бесцветных игл с т.пл. 194195 0 (разложение) . Найдено, -i: С 67,1; Н 5,7; N 6,2. С 12 НпчОй 1 ычислено, S : С 67,5; Н 5 , 7 ; N 6,1. Хорошо перемешиваемую смес-. 5 вес. ч, этнл- 3-н - пропил-4-оке их и н ОЛИ н - 2-кауЗоксилата, 3 вес. ч. безводного карбоната калия и 3,3 вес. ч. бензилбромнда в безЕО/iH.OM аг;етоне кипятят с обратной перегонкой 16 ч, фильтруют для даления неорганических солей ; отгоняют растворитель. Раствор оставшегося масла в- 75 в ее.ч. эЛира после промывки 1 н. раствором едкого катра (2 порции по 25 вес.ч.), затем водой (4 порции по 40 вес.ч.) сушат над су.чьфатом магния, выпаривают и получа ют 6,4 вес. ч. сырого э т -; л - 3 - н - п р о п и л - 4 - б е н 3 и л о к с и X и н о л и н -2-карбоксил та в виде очень светлого л ел т о го мае;: а. Это вещество растворяют в 32 вес. ч, кипящего этанола и х-идролизуют в течение 2 ч 5 вес.ч. 161-ного водного раствора едкого натра, затем отгоняют этанол, разбавляют 150 вес.ч. Е оды и подк; сляюг ледяной уксусной кислотой. Образовав чийся сначала маслянистый осадок медленно кристализуется при , получаКТ 5,1 вес.ч. сырого продукта с т.пл. 127-129 С, которьлй после перекристаллизации из этанола дает 3,9 вес.ч. 3-н-пропнл- 4 - 6 е н 3 и л о к с и X и н о л и н - 2 - к а р б о н о в у ю .с;1оту в виде бес цветнь х игл с
Найдено , и s С
С gjj H|q N0 J
Вычислено ; % :
N
4,4.
22. Зтил-3-н-пропилПример- 4 ок с и X и н ол и н - 2 гс ар бок с ил ат ,., no/ty ченный аналогично примеру 21,. пре:враК1ают по методике примера 3. применяя температуру обратной перегог кз з первой стадии для окончс;ния р гакции;, в 3 н - пр з п и л -J - :к л ор X и н ол и н - 2 - к а) )0 к силат в виде вязкого масла н j-i-i-пропил- 4- ( 4-ноиилфенокск ) -хкнолин-2-карбоновую кислоту в ни.це ;й:расного полутвердого тела.
Пример 23, По методиц-а примера 1,-применяя этилэтоксэлилЕалерат вместо этилксалацетата и г:нилин вместо Г( -толундипа,, получают, применяя Б-качестве каталиэат : ра в начальной стадии конденсации кесколь-ко капель соляной кислоты, З-к-пропил-- 4-оксихинолин-2-карбоксила.т ,, идентичный продукту, полученному по методике примера 21, и З-н-пр-СПил-4 ( 4-додецилбекзилокси) -хинол ин-2 карбоновую кислоту в виде вязкого светло-оранжевого масла.
Пример 24, По методике примера 21 этил 4-окск-б-н-бутилхинолик-2-карбоксилат превраш.ают в ;)ткл
-4 - аллилок си -6 - к- бу тилхи на.п кн - 2 -карбоксилат в виде коричневого вязкого масла. эткл-З-аллил-д-окол-б-н бу т 11Л хи н Оли н - 2 -к ар 5 ок с мл а т с
т „ пл , 156-l57Cf эткл-3-н-пропи/:-4-окси-б-к-бутилхиколи} -2--карбоксилатс т . пл . 1 36 1 ; З-н-пропил-6-Н бутил-4- ( 4-додеци,гбекзилокси) - :инолин- 2-карбояопую кислоту в зкда светло-желтого масла.
п р
Этил- 1-н-пропилм е D
-6-н-оксихииолии-2-карбоксила:г превращают по методике примера 22 в э тил- 3 - н-пропил- б - н -- буткл- 4 -хл орхи н о л н - 2 - к а р бокс к л а т т . п л ., 4 3 ., 5 -44 С и 3-н-пропил б--н-6уткл -4 - 4- н они л ф - н ок СИ) -- хи н ол i-i н - 2 к а рбо н о в ую кислоту в виде ЕЛЗКОГО коричневого масла,
Пример 26. По методике а 2 J. э : к л --б - н - бу т к.п 4 - ок с и х к н олин-2-карЗГКсилат преоращают с ломощью и зодецилб:)омида вместо аллилбромида в этил--;,-изо,г:е11;клокси-6-н-бутилхинол-ш 2 -кароокси 1ат в ;эиде вязкого коричневого масгта м 4-ИЗодецил-окси-6-н-бутилхг-;нолин --2 --каибоновую кислоту в виде полутвнрдого продукта кремового цвета.
Пример 27. Зтил 3--н-пропил-6-н-бутил-4-окслхинолин 2--карбоксилат превращают по методике примера 26 в этил-,-н- пропил--6-к-бутил-4-иэодецилоксихинолин-- 2-карбокс ллат , 3 -н-пропил - b -н - бутил- 4-из одеци локс ;з{Инолин-2--карбоксклат и 3-н-пропил-5 - :: -О:/ :;и;- -- :.-:Зг;;-е1и-Локсихинолин 2-карбонозуз кислоту з виде светлой:е-гп ого зязчого масла.
П р и м ер 28„ По методике примера 23, применяя зтоксалклфенклаце-тат вмест-о этилэтоксалилвалерата и rt -бутиланилин вместо анилина получают ЗТИЛ- 3-фенил-4-окси-6-н-бутилхннолин- 2-,арбоксилат с т . гш . 164165с и 3--фенил-6-н-буткл-4-( 4-додетдилбензилокси) -хинолин-2 карбс1новую кислоту Б змде вязкого коричневого ма ел а .
п р м м 3 р 29 По методике примера 28, применяя :-тилэтоксалилбензиладетат вместо зтилэтоксалилфенилацетата, получают этил-З-бенэил-6ил- 4 --ОКСИХИНОЛИН-2-карбоксилат
с т.пл. 163,5-164, и З-бензил-6--Н бутил-4- ; 4-додецилбензилокси) -хинолик--2--карОоновую кислоту в виде вязкого желто-оранжевого масла.
П р и м е р 30. По методике примера 1., применяя н-иэодециланилин вместо п--толуидина, получают этил-6-и э одецил-4-ок си хи н ол ин-2 карбоксилат в виде очень вязкого коричневого масла и б-нэодецил-4-( .-додецилок си бен зил) -хинолин-2-карбоновую кислоту в виде вязкой коричневой смолы.
П р и м е р 31. Этил-6--Хлор-4 оксихин-олин-2-карбоксилат превращают по методике примера 1 Е б-хлор-4- (4-додецилбенэилокси) - Хкнолин-2-карбоновую кислоту в виде вязкого светло-коричневого масла.
Интеноивко перемл хлороформенX 10
растаора, содержащего О
г -
МОЛИ хкнолип-2-карбоновой кислоты (лиганд) , и 25 водного кислого раствора соответствующего металлического иона (0.25 к мол я для
,-S двухвалентного металла; О, 1667 к 10 моля для трехвалентного металла), содержащую также О . .2 5 « 10моля надхлоркой кислоты, титруют потен диометрическя л г раствором едкого натра. Такой ие -опыт проводят, применяя 25 i-.U чистого хлороформекного р астворите 1Я, По разнкие между двумя кривыми TSiTpoasHMH рН определяют процент образовавшегОси комплекса между лигаидом к даннык ионом металла для .-диапазона рК (2:1 лиганд/металл - стехиометрия для двухвалентного металла; 3; J. - для трехвалентного металла); третья кривая построена дл зависимости npotieHTa комплекса от рН, По этой последней кривой определяют величину Ph.-j. Зта величина считается как рН, при котором образуется 50% наблюдаемого (не теоретического) комплекса.
Во Е-сех растворах металлов прис у т с; т в ж т с у л ь ф а 7 -- и о ны , так как их по.,чают из соотБ етстяую;аих сульфатов металлов. Однако при применении железа (П иИх) и алюминия имеются также ионы аммония, поскольку приме няются двойные соли металла и аммония . Результаты даны в табл.1, при этом в приведенных в таблице примерах т качестве действующего начала применяете я хинолин-2-карбоновая кислота. Пример 33. 100 мл 3,13%-но го раствора 6-метил-4(4-додецилбен зилокси)-хинолин-2-карбоновой кисло ты в перхлорэтилене (концентрацья эквивалентна концентрации кобальта 2 г/л) интенсивно nepeMeinj-iBaiCT при в течение 10 глин с тремя после довательными порциями раствора суль фата тяжелого металла в разбавленно серной кислоте сначала при pi; 2,0, в котором начальная концентрация ко бальта и железа (II) составляет 2,0 г/л, концентрация цинка и меди 0,2 и 0,05 г/л соответственно, затем им дают разделиться. Концентрацию ионов металлов в трех водных растворах после экстракции (раоинаты) определяют атомным noi ло1дением. Органические слои, содержащие ме таллы, снова промывают порциями по 25 мл разбавленной серной :.;ислоты ,в которой концентраци - серной к;-,с;.г;о ты составляют 10 и 150 г/л сос-ветственно, концентрации металла в дьух полученных кислотных экстрактах опре деляют по ЯМР. Результаты приведены в табл.2. Эти данные показывают лyчiJJyю избирательную обратную промь;вку кобал та и цинка по сравнению с медью гч в меньшей степени железа (11) ;--:з содеркаци:-; металл лигандных растворов слабой серно;-, кислотой (10 г/л), чем крепкой серной кислотой (i50 г/л Пример 34. 25 мл раствора сульфата кобальта и разбавлекной серной кислоты сначала при рН 2 при концентрации кобальта 2 г/л интенсив но перемешивают при комнатной температуре в течение 5 мин с тремя последовательными порциями по 2Ь мл 3, раствора 6-н-бутил-4-( 4-додецилбензилокси) -хинолин-2-кэ-рбоновой кислоты в 1 еллзоле Т (концентрационный эквивалент концентрггции кобальта 2 г/л) и дают разделить ся. Содержание метг;лла и рН водной фазы определяют после каждого смешения и разделения. Результаты приведены э табл.З.
Пример Зь . Повторя от методику примера 33, применяя 3,42%--ный раствор 6-н-бутил-4-(4-додецилфенокси)-хинолин-2-карбоновой кислоты в Шеллзоле Т при комнатной температуре.
Результаты приведены в табл.4.
р 39. 50 мл 2,65%-ноП р к f. е 6 -.ч-бутил-4-( 2-трет . буго jiacTBOoa
I хни олин- 2-карТИ.П - ч -метил фенокси в Шеллзоле Т
бонозой кислоты в нцентрацин кобальта Результаты показывают, что слабая серная кислота (10 г/л) дает лучшее избирательное обратное вымывание кобальта и цпнка, чем меди и в «елезо (III) из лиганменьшей степени дных оастворов, чем крепкая кислота (13С г/л) . П р и м е р 35. Повторяют методику npvnepa 34, пр -:меняя 50 мл растзора сульфата кобальта (2 г/л) при рН 2,0 Т 4г55й-ного раствора 5--ь-5чг:-::л-4 ( -.--конмлфенокси) -хинолин-2-карбоновой х 1слоты в перхлорэтилене (эквквалентгю 3 г/л кобальта). езульта: р:: приведены в табл.5. Пример 37. Порцию 50 мл 3,СЗ-;-:-ого раствора 6-г-бути.г;-4-( 4-нонилфенохси)-хинолин-2-карбоновой кислоты в Миеллзоле Т (эквивалент40 концентрации кобальта 2 г/л) инт: : синно перемешивают при комнатной .--|ературе s течение 5 мин с тремя госле,доЕательньм; по 50 мл раствора сульфатов тяжелых металлов 3 - гсбавленной серной кислоте при рН 2, в котором первоначальная конце: трация кобальта составляет- 2 г/л, а концентрация железа ( .I и III } , цинка и меди, соответстэенко, 1,56, 0,44, 0,2 и 0,05 г/л. Пос.-с разделен:: я концентрацию метг.л.г;ов S трех водных рафинатах опрела ел я ю т по атом:-; ол :у п о г .ч о щ е н и ю . Содер ка1;ин металлы органический раствор разх оляют на две порции равного объег-г; о/дич из низ хорошо промъ1-- д:от в течение 5 мин 25 мп серной кислоты (30 г/;;), а вторую также сс1;абатыБают серной кислотой (15 С r/;i) ; концентрацию металла в осо;:х кислот;-; ;-: про; 1ыкках определяют г;С no; omcHii: J , Рсз/льтаты анализов приведены в таЗл . б . Л р и м ер 33. 25 мл 16,88%-ного раствора. 6- -:-бутн;1-4-( 4 нонилфенокси )-ХИНОЛИН--2-карбоксилата в 11еллзоле Т (экзиБалентно концентрации ме, 12 г/л) перемешивают в течение 5 ; гп:-: с тремя последовательными порция.и по 25 bin раствора сульфатов тяж-з..ых металлов в разбавленной серной кислоте, снача.-.а при рН 2, в которых исхсднач СО;;:;с гграцня меди сосгг;злпет 11,25 г.-л, концентрация железа (III) н кобальта - 0,25, коние:г7рацня цинка - 0,05 г/л, затем ают раздел :ться . Органическую фазу ромывают 2S i.v серной кислоты крепостью 150 г/л. Концентрацию метал;ов Б трех водных рафинатах и. в сер;лотных прог-алЕках определяют по
2 г/л) смешивают при КОМИОГЕ-ЮЙ I-SIMпературе в течение 10 ми ;: последовательными порциями по 50 мл раствора сульфатов тяжелыу. металлов в разбавленной серной кис:иоте сн; ча-ла при рК 2f Б котором исходная коч-центрация кобальта и железа (ИП составляет 2 г/л . а цинка - л1е;1и - и 0,05 г/л соочиетсплачпо , Пос;:1 разделения концентрацию i-.C:. е ап-лов в трех водных рафии этэ::1 ог;;-ед е ЛЯ ОТ по атомному ПОГ ЮГцСПИК: ,
Органический слой lipo UBa-гот юопедояательно аорг.иями не 50 глл разбавленной сергзоя .ci-jcj:oi-;: : с концентраи.ией 30 i-/j. :/; 150 г/,п СОСТБЁТственно, концентрацию MeiJia.nsi ч кис-лоткых экстрйктазс слрадет люг пс iTOr--;ному поглощению„
Результаты прИгэддень и табл„о
Пример 40, noBTOpKiOT f/cj;o-. дику примера 39., применяя б-п-еутил-4™ { 2-трет . бутил- 5-метилфенокеи ) -хкколин 2 карбоковую кислоту.
Результаты приведены в табл,9.
Пример 4 1 „ Повторяют г.е :одику примера 39, применяя 3,1%-ный раствор б н-бутил-4- ( 2, 4--Л 5-тре т . пентклфенокоихиноликJ 2--карбоновоЛ кис-лоты 3 111елпзоле Т ( эквив ал i HTFJO комиентрации коба;зьта 2 г ./л; .
Результаты привецань; э ;абл„1(1.
Пример 42,: ..пт :.с::оцкку примера -39. применят-. ;131- Ьй раствор 4 S 6 ( 4-нонилфе;-к;кс1 ; -Х1г;-к;лкн-2--карбоноБОй ккс;ю7Ь1 я .ппзоле Т ( зквиналемтчо и г;н :ектпа;1ии кобальта 2 г/л) „
Результаты ривепены в :-a6ji 11..
Пример 13, :30 мл . 2 .: 4--::охО раствора 4 , б-ди™ 4-но:г лфе;Юкс--) --хи нолин 2 карбоновой KHc;noTrv я ;1еглзоле ( эквязалектно iCOH .лйи:-ра:...ии кобальта 5 г/л) интенси.в но теремешизают при комнатной температуре в течение 3.0 мик с тремя поо;1едона:.ель«ьгли псрция:/;к по 150 мл раствора су.п.ьфзтоз ТЯжелЫл металлов в р-а збагитен ной оерной кислоте при рН 2- в когором исходная конлектрацля кобальта и желе;:з (П) составляет 2 P/J;, .динка и Г4едр --- О.. 2 г/л х п.СБ .г-/л соответственно. Лссле разделения хояцектрацик ионов :.;с 1 :-;-;:са ;з золдгнпх рафянатах опре.де.1.- . по : - омном;, Х)гло-щению о
« Органический рас твое, сс цер алчий металлы, разделлкд ка , час-о- равного объема; одну :з :г:х .О промывают 3 течение 5 м:.-;- 25мц серчо:; кислоты крепостью 30 , а иторую также обрабатывают сер:- 0й кислотой крепостью 150 г/л; концекчрациг:; 1Ле талла Б обек:к кислотных промывках определяют яо атоиному ,пог-лс- де1- К10 Результат;- прязедены а тз6л.Л2, П р и wi е р 44, Повторяют йШгодику примера 3Sf применя. л б ,
ivacTBtip ti--Mei скск-4- ( 4-додецилбекэклолси ) --хино :ип 2-КЗ рб о и оной кислоты 11 хлирофор1-.1е (зквк валентно кониентРЙП.ИИ меди 11,25 г/;) .
Результаты приведены в табл , 13 ,
Пример 45. 25 мл 3,13%-HOго ра(;твс5ра 8-метр;л 4-( 4-додецилЬензилокси) хииолин-2-карбоновой кислоты в с.пороформе (-кривалентно концанграп.ии коба- Ьга 2 г/л) теремешивают гри комнатной температуре в течение 10 с; 25 мл раствора буферированчот-о при рН 5,0 с помощью ацетата naTpMH/vKc-yrniaa кислота, в котором ,- сходная кспцентра ция меди составля ;т 2 г/л, кобальта. 0,2 г/л, железа Л и III i 0,1 г/п. цинка 0.02 г / л ,
Пос;1е отделе1- ия концентрацию ионо ьтетал.ссБ в водном раЛинате опоеделя;от aTOMHNivi поглощением .
Ортанитеский слой, содержаиий металлы, промывают обратн-ой про- ывкой 25 мл разбав тенной серной кислотк -150 /л); кс1нцентрацию метал.лов в кислотном экстракте определяют методом атомного г-оглоцеЕ-1ИЯ .
Резуль-а 1-, приведены в табл.14.
П р и м е р if,. Повторяют ме7О дику примера 45, применяя раствор, lie содер ка::г-й меди, при этом концентг ацли же.1еза ( II у. } ,. кобальта и цинка га1чие же.
Резу.1П)Тат-гд; приЕ;едень Е табл. 15
:i р и м р 47, 25 мл 3,8 2%-него раствора 8-мeтиJ -4 - ( 4 чонилфенокси) --ХИНОЛИН-2-карбоноЕой кислоты в хлоооформе ( экги палоьтно онцен-ра ши г-1е.ли 3 V/M; перемешиваю- - при комнатной температ ре ь течение 10 мин с 25 мл рд ::г-: ;;;а ,, буферированного при г; 4гС, с омощью ацетата натрия/ук-суснзя кис-:ста. в котором исходная чонпент1)аци F меди составляет 2 г/л, кобальта 0,2 г/л, лселеза (И и 1П ) 0,1 г/л г цинка 0,02 г/л. После отде)гения концерт рацин) ионов металлов в вещных рафинатах сшределяют атомным поглощением,
Орга1- ический с/Ой, содержащий месаллы, последоват5:льно промывают 25 мл разбавленной серной кислоты крепо-стью - 5С г/л; конц.ентр,адию .егалло 3 jii кислотном экстракте опреде.пппт атомным поглощением,
Оргаг-ический CJ-iO , содержаший меаллы, затем про шгвают 25 ;лл разбавленной серной кислоты (150 г/л). Кон:1:ентрацц 0 ;-;еталла Б кислотных вытяжках определяют атомньзм поглощением.
Результаты приведены в табл.16.
П р и ) е р 4 е,, 25 мл рас:твора сульфата меди в разбавленной серной кис,поте при рН 2fO при концентрации меди л 2 г/я схгешквают с тремя последовательньЕ 1И порциями по 25 ivLn -й,11%-кого раствора З-н-цропил-6(изодецчлхинолин) --2-карбоновой кислоты в Эскайде 110 (алисратнческий керосин; экзивалентно концентрации меди 12 г/л) при комна ной температуре по 5 мин. После разделения концентрацию металлов и рН водной фазы определяют после каждого смешения. Результаты приведены в табл.17, Пример 49. 25мл 5,37%-ного раствора 3-н-пропил-6-н-бутил-4-изодецилоксихинолин-2-карбоновой кислоты в Эскайде 110 {эквивалентно концентрации меди 4 г/л) смешивают в течение 10 мин с тремя последовательньоми порциями по 25 мл раствора сульфата тяжелого металла в разбавленной серной кислоте при рН 2, в котором исходная концентрация меди, железа (1П) , кобальта и цинка состав ляет 8,0, 4,0, 2,0 и 0,2 г/Л соответственно. После разделения концентрацию ионов металлов в трех водных рафинатак определяют атомньлм поглощением. Органический слой, содержащий ме-таллы, рнова промьшают 25 мл 25%-ной (вес/объем) соляной кислоты. Концентрацию ионов металлов в кислотных отг сявочных жидкостях определяют атомным поглощением. Результаты приведены в табл.18. Пример 50. Повторяют методику примера 49 с раствором, не содержащим меди, но подобным раствору примера 49 . Результаты приведены в табл.19. Таблица 1















1,6
1,0 1,0 1,0 1,0
1,2 1,0 1,4 1,3
Неопр, 1,1 То же
I
Неопр, 1,0 1,1 1,45 1,0
1,1 2,6
Нет 2,6 То же
2,7
2,8 1,6
1,25
ьо
1,0
1,1
3,2 ,
Нет
2,4
2,0
2,4
2,0 1,8
1,8 2,0 2,3
1,85 1,75
1,6
1,5
1,4 еопр.
1,95 2,15
1,65
1,45
Ь8
1,8
1,3
1,25
2,1
2,2
1,6
1,6
2,0
2,05
Неопр.
2,0
1,85
Неопр.
4,6
Нет
5,95
5,9
4,6
Нет
(ниже рН 6)
4,1
Нет (ниже рН 6)
4,2
То же
Неопр,
4,2 4,5
3,0
2,65 3,2 2,8 2,6 3,2 2,9
2,5
2,1 Нет 6,0
Нет 5,3 (ниже рН 6)
3,0
2, 7 3,3 3 , 2
Кислотн-; i ,PKOC: w : 10 г/л f,;&o, i50 т/л Н;6С,.
Всего металла, казле ченного к:; орган;- чзс фазы дзумл кислотным э к с т р а. к ц и ям и
25
Всего извлечено металла из органической фазы двумя кислотными вытяжками
62985726
Таблица 3
0,081
0,040
0,24
0,33
Показатели
Содержание металла в лигандном растворе
Вод н ый р а ф и н а т
Кислотная экстракци f лигандного растьора, с оде ржаще г о мет аллы
Кислотные экстракты: 30 г/л
150
29
Показатели
Содержание металла в лигандном растворе
Исходный раствор сулфата металла при рН
Водный рафинат I
И
П1
Всего извлечено металла в органическую фазу (по разности)
Кислотное извлечение из лигандного раствора
Кислотная ЖИДКОСТЬ 150 г/л 2,50
Содержание металла в лигандном растворе
Исходный раствор сульфата метсшла при рН 2
Водный рафинат
I
11
III
Всего металлов, экстрагированных в органическую фазу (по разности)
Кислотная отмывка из лигандного раствора
62985:
30 Таблица
Концентрация ионов металлов в
водных жидкостях, г/л
Pejiii)
Со
Си
Zrr
11,2500,2500,2500,050
3,3620,2500,2470,050
11,0830,2400,2510,049
11,8890,2440,2460,049
0,0160,0060,002
7,46
0,003
0,002
0,009
2,413
Таблица 8
2рОО
2,00
0,200
0,05
0,92
0,21
0,022 0,138 Показатели Кислые жидкости; 30. г/л H2.S04 0,120 150 г/л 0,087 Всего извлечено металлов из органической О,2 С 7 фазы двумя OTh/iHBKaMU
Кснцентращ я металлов в водных жидкое т ях, г/л
Показатег.Н
Продолжение табл. 8
Таблица 9
:i:.:
ZH
eviH) Концентрация ионов металлов Б водных жидкостях, r/ji 1 reiltl) I Si7 О,5560,0090 003 0,2760,0040,031 ,0130,03 0,832
Содержание металлов в лигандном растворе
Исходный pacTBCjp сульфата металла при рН 2
Водный pa0vHaT
III
Всего извлечено металла в органическую фазу (по разности)
Кислотная отмывка лигандного раствора
Кислотные жидкости: 30 г/л 150 г/л
Всего извлечено металла из органическо фазы двумя кис.потны-л промывками
0,05
0,0003 0,0024 О ,, О О 1 2
,05
0,044 0,1411
0,0025 0,0290,0315
0,026
33
Содержание металлов в лигандном растворе
Исходный раствор сульфатов металлов при рН 2
Водный рафинат: Всего извлечено металлов в органическую фазу (по разности Кислотная отмывка лигандного раствора Кислотная жидкость: 30 г/л 0,17 0,89 150 г/л 0,063 0,13 Всего извлечено из органической фазы двумя кислотньвли 0,233 1,02 отмывками
Содержание металла в лигандном растворе
Исходный раствор сульфатов металлов при рН 2
Водный рафинат:
629857
34 Таблица 10
0,200 0,05
2,00
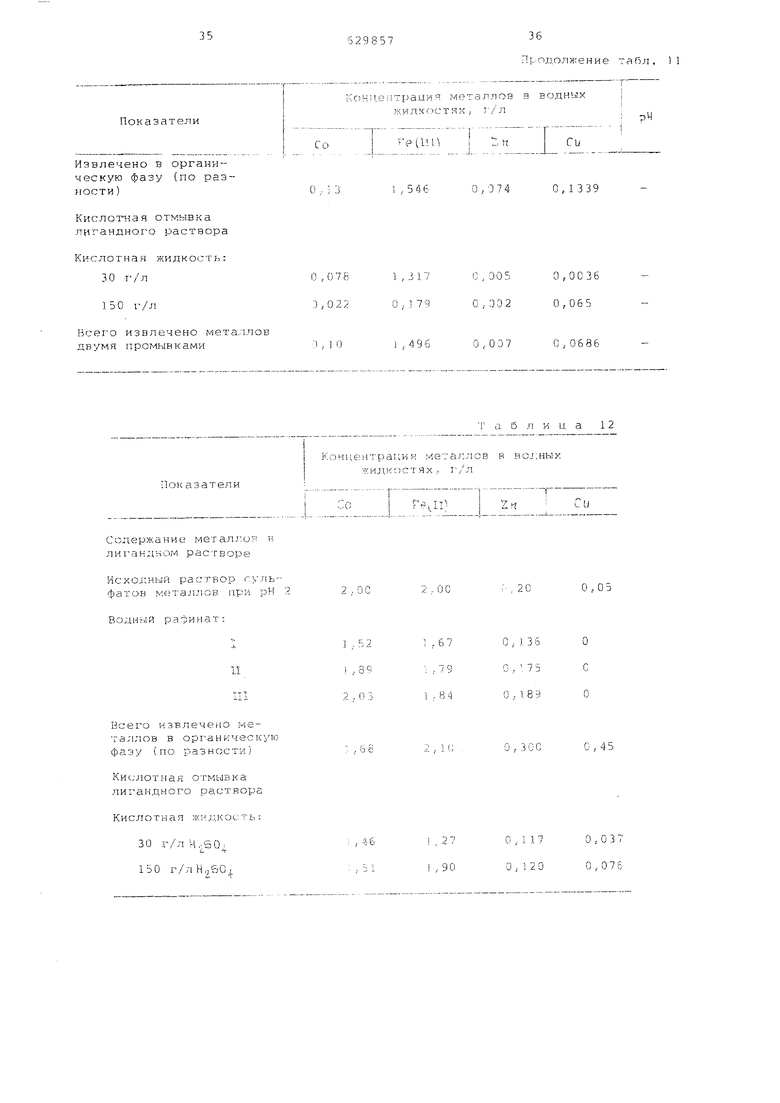
Таблица 11
2,0
0,05
0,20
2,00
0,0005 1,45 0,0045 1,79 0,00э7 2,0 0,01 0,0031 0,002 0,054 0,012 0,0571
35
Показатели
36 Продолжение табл. 11
рЧ
(Ill}
Извлечено в органическую фазу (по раэгЮсти)
Кислотп- ая отмывка лигандного раствора
Кислотная жидкость: 3 О Т / л
150 г/л
Всего извлечено мет двумя промывками
Показатели
II
блина
О f 1. 3 бО
,790,.75С
,840.189О
, 45
Показатели
Содержание метал1;ой в лигандном растворе
Исходный раствор суль-фатов металлов при рН 2
Водный рафинат:
Со
П
11L.40,050
0,500
0,500
II III
Всего извлечено металлов в органическУО фазу (по разности)
Кислотная отмывка лигандного раствора
Кислотная отмызочная жидкость:
150 г/л И.2,50J,
0,0011
0,0008
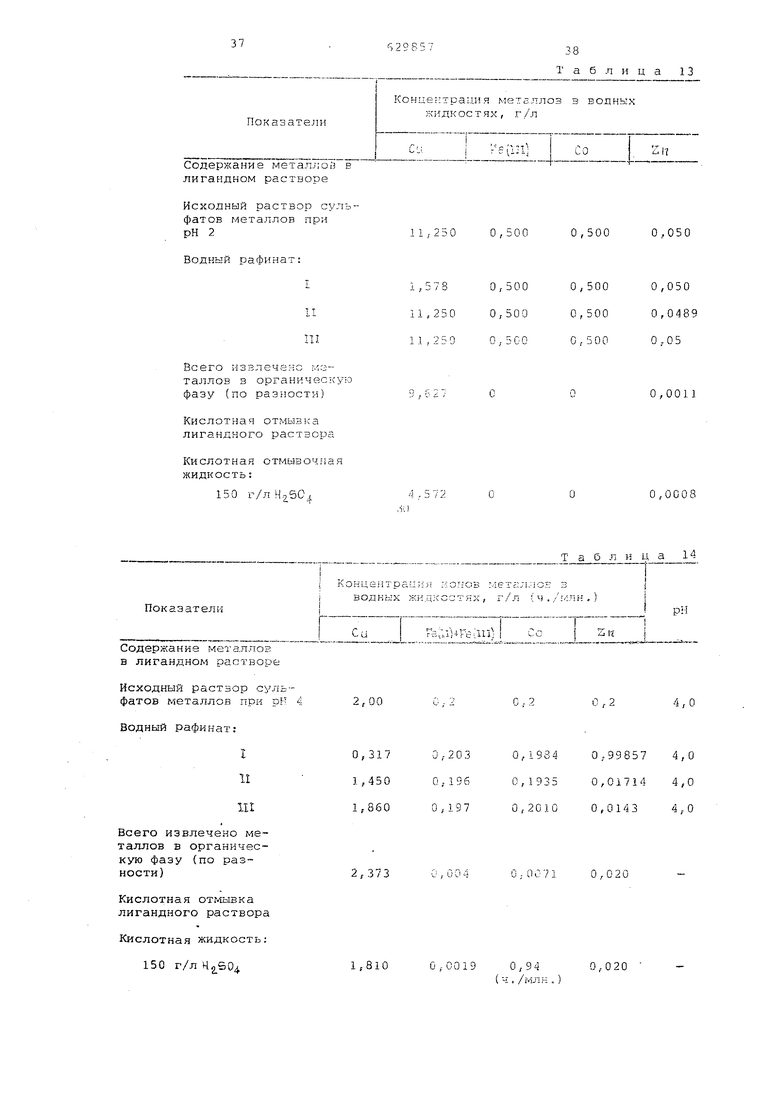
Показатели
Содержание металлов в лигандном растворе
Исходный раствор суль фатов металлов при pF
Водный рафинат:
Всего извлечено металлов в органическую фазу (по разности)
Кислотная лигандного раствора
Кислотная жидкость: 150 г/л
Т а .б,, л н
водных жи,ц:ссстях, г/л ч.
4,0
2f 00
0,2
0,998574,0
0,017144,0
0,01434,0
0,020
1,810
0,94 0,020
0,0019 (ч./млк.)
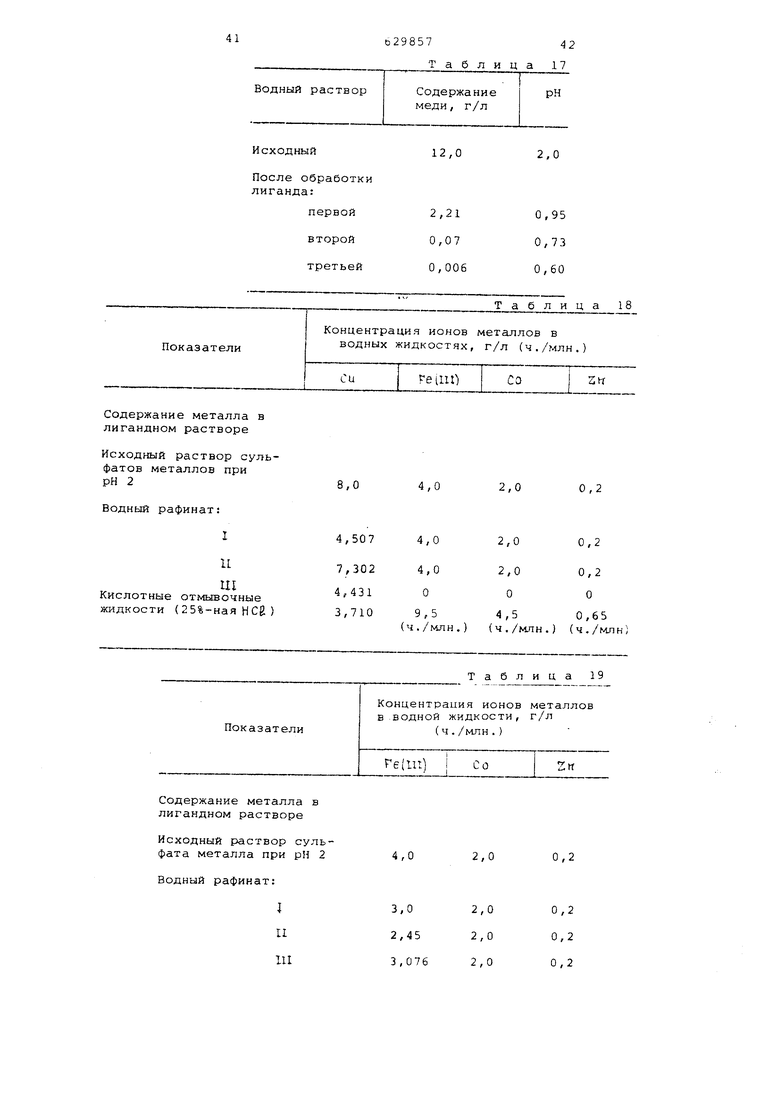
Исходный
После обработки лиганда:
Содержание металла в лигандном растворе
Исходный раствор сульфатов металлов при рН 2
Водный рафинат:
4,507
Показатели
Содержание металла в лигандном растворе
Исходный раствор сульфата металла при рН 2
Водный рафинат:
J
II
III
12,0
4,0
2,0
0,2
2,0
0,2
4,0
Таблица 19
Концентрация ионов металлов в водной жидкости, г/л
(ч./млн.)
re(Iit)
Ztt
Со
0,2
2,0
0,2
2,0 0,2 2,0 0,2 2,0
Всего извлеченс) т/ та.пла в осгьиичес йазу (по разнпс:ч;
Формупа изобретен -;;1 . Состав для изБлэ еиин мгг из ноднкз{ растворов, одсржа,.л-п лэтирую111Ий po;i.iei;T :: ра.ст-ор т о т л и ч а ю 1Ц и :-; с я м егч . целью утгвличения из бирательнос тава, в кз,честве хелат11ру гцег;; агента состап со.цеожмл .viKiM Ffi46oiiOBy;o x icnryry тби,аи р( :-Oj.-OpjIj, С; -Cg -аЛКИл ,
г иуппь при условии f что к ;1 с;одержат всего не pjBt5,;K.;oc..nb:x ;:то:лов ,
: Р; J - 1 ; т 1 J: Н . с . К1
I, -1ТС 3 качестве раствоjp,n6ip;Kj-rr алифат -ч&с 1 lacKn;-) углевсДТрол. ;-т -и-н,-й :; :р-;еиэдорсд ,
- :Pp;N--L 1:.и , ;:;)::ня rtje но
Авторы
Даты
1978-10-25—Публикация
1973-08-03—Подача