ния; подвё|)гают взаимодействию с илидом формуле
(CsHj Sff-CHj-CHs-CHs-COO-i
с получением соединения формулы I,
где Аг, R, rt и Z имеют указанные значения;
/ ОН W - г ис-двойная связь; М - ., ,
и, в случае необходимости, восстанавливают указанное соединение с получением соединения формулы I, где Аг, R, М, « и Z имеют указанные значения, W - простая связь, после чего целевые продукты выделяют известными методами.
Восстановление соединения формулы I проводят предпочтительно с помощью водорода на палладированном угле в качестве катализатора при температуре от -15 до -20° С.
Пример 1. (Исходное вещество). YПолуацеталь 2- {5а-окси-3а-(тетрагидропиран-2 - илокси)(тетрагидропиран-2илокси)-4-фенил-транс - бутен-1-ил-1 -циклопентил-1а)-апетальдегида.
Раствор 605 мг (1,33 ммоль} -лактона-2{ 5а-окси-3«-(тетрагидропиран-2 - илокси) (тетрагидропиран-2-илокси) -4-фенил7ра«с-бутен-1-ил-1 - циклопентил-1а -уксусной кислоты в 8 мл сухого толуола охлаждают до -78° С в атмосфере сухого азота. К полученному охлажденному раствору добавляют 3,0 мл 20%-ного раствора диизобутилалюминия в «-гексане ( Инорганикс) по каплям с такой скоростью, чтобы температура не превышала -65° С (15 мин). После перемешивания в течение еще 45 мин при -78° С Добавляют безводный метанол до прекращения выделения газа и реакционную смесь постепенно доводят до комнатной температуры. Реакционную смесь соединяют с 100 мл эфира, промывают 50%-ным раствором двойного тартрата натрия и калия (4X20 мл), высушивают (сульфатом натрия) и концентрируют.
Получают 615 мг (100%) у-полуацеталя 2- { 5a-oкcи-3 a(тeтpaгидpoпиpaн-2-илoкcи)(тeтpaгидpoпиpaн-2 - илокси)-4фенил-гра«с-бутен-1-ил-1 -циклопентил-1а } ацетальдегида.
Пример 2. 9а-Окси-11а, 15а-быс-(тетрагидроииран-2-илокси)-16-фенил-г{«с - 5транс- 3-( - тетранорпростадиеновая кислота.
К раствору 1760 мг (4,Q ммоль) бромида (4-карбокси-н-бутил) -трифенилфосфония в атмосфере сухого азота в 5,0 мл сухого диметилсульфоксида (ДМСО) добавляют 3,2 мл (7,0 ммоль) 2,2 М раствора метилсульфинилметида натрия в ДМСО. К полученному раствору илида красного цвета добавляют по каплям раствор 615 мг (1,34
ммоль) 7-полуацеталя 2-f 5 а-окси-3а-(тетрагидропиран-2-илокси) - (тетрагидропирап-2-илокси)-4-фенил-г/7анс - бутен-1ил-1 - циклопентил-Iaj-ацетальдегида в 5,0 мл сухого ДМСО в течение 20 мин. После перемешивания в течение еще 2 ч при комнатной температуре реакционную смесь выливают в ледяную воду. Водный раствор основного характера промывают дважды
этилацетатом (20 мл) и подкисляют до рН примерно 3-10%-ным раствором соляной кислоты. Кислый раствор экстрагируют этилацетатом (3X20 мл) и соединенные органические экстракты промывают однократко водой (10 Л1л), высушивают (сульфатом магния) и упаривают с образованием твердого остатка. Фильтрат подвергают очистке колоночной хроматографией на силикагеле (Бэйкер-«Энэлайзд, 60-200 меш) с
применением этилацетата в качестве элюента. После удаления примесей с высоким значением Rf собирают 150 мг 9сб-окси-11а, 15а-быс-(тетрагидропиран-2-илокси)-16-фе1-1ил-цис-5-транс -13-со-тетранорпростадие.новой кислоты.
Пример 3. 9а-0кси-11а, 15р-5ыс-(тетрагидропиран-2 - илокси)-16-фенил-г «с-57-рйнс-13-сй - тетранорпростадиеновая кислота.
К раствору 1760 мг (4,0 ммоль) бромида (4-карбокси-н-бутил) -трифепилфосфония в атмосфере азота в 5,0 мл сухого ДМСО добавляют 3,2 мл (7,Qммоль) 2,2 М раствора метилсульфинилметида натрия в
ДМСО. К полученному раствору илида красного цвета добавляют по каплям раствор 621 мг (1,34 ммоль) -полуацеталя 2(5а-окси-3а-окси- (тетрагидропиран-2-илокси)(тетрагидропиран-2 - илокси)-4фенил-транс-бутеи-1-ил-1 -циклопентил -1а)ацетальдегида в 5,0 мл сухого ДМСО в течение 20 мин. После перемешивания в течение еще 2 ч при комнатной температуре реакционную смесь выливают в ледяную
воду. Водный раствор основного характера промывают дважды этилацетатом (по 20 мл) и подкисляют до рН 3 10%-ным раствором соляной кислоты. Кислый раствор экстрагируют этилацетатом (3x20 мл) и соединенные органические экстракты промывают однократно водой (10 мл), высушивают (сульфатом магния) и упаривают с образованием твердого остатка. Твердый остаток растворяют с этилацетатом и отфильтровывают. Фильтрат подвергают очистке колоночной хроматографией на силикагеле (Бейкер «Энэлайзд, 60-200 меш) с применением этилацетата в качестве элюента. После удаления примесей с высоким значением Rf собирают 300 мг 9а-окси-11а, 15рб«с-(тетрагидропиран-2-илокси)-16 - фенилцис-5-транс- 3-& - тетранорпростадиеновой кислоты.
Пример 4. (Исходное вещество), v
Полуацеталь - окси-За-(тетрагидро11Иран-2 - илокси)(тeтpaгидpoпиpaн-2илoкcи)-4-фeнилбYтил- - циклопентил-1аацетальдегида.
Раствор 1457 мг (3,2 ммоль) 7-лактона-2 5а-окси-3а- (тетрагидропиран-2-илокси) -2р(За- тетрагидропиран-2 - илокси -4 - фенилбутил-1 -циклопентил-1 а-уксусной кислоты в 15 мл сухого толуола охлаждают при -78° в атмосфере сухого азота. К этому охлажденному раствору добавляют 5,0 мл 20%-ного диизобутилалюминия в н-гексане (альфа Ииорганикс) по каплям с такой скоростью, чтобы температура не превышала -65° С (3 мин). После перемешивания в течение еще 30 мин. при -78° С, добавляют безводный метанол до прекращения выделения газа и реакционную смесь постепенно доводят до комнатной температуры. Реакционную смесь смешивают с 150 мл эфира, промывают 50%-ным раствором двойного тартрата натрия и «алия (1x50 мл), высушивают (сульфатом натрия), концентрируют и хроматографируют.
Получают 1200 мг (81,5%) -у-полуацеталя 2-( 5а-окси-За-(тетрагидропиран-2-илокси)(тетрагидропиран-2 - илокси)-4фенилбутил-1 -циклопентил-1а j -ацетальдегида.
Пример 5. 9а-Окси-11а, 15а-бмс-(тетрагидропиран-2-илокси) - 16-фенил-чис-5-(втетранорпростеновая кислота.
К раствору 5150 мг (11,6 ммоль) бромида (4-карбокси-н-бутил) -трифенилфосфония в атмосфере сухого азота в 10,1 ;иуг сухого ДМСО добавляют 10,8 мл (21,1 ммоль) 1,96 М раствора метилсульфинилметида натрия в ДМСО. К полученному раствору красного цвета добавляют по каплям раствор 1200 мг (2,6 ммоль) -прлуацеталя 2{ 5а-окси-За-(тетрагидропиран-2 - илокси)(тетрагидропиран-2-илокси) - 4 - фенилбутил-1 - циклопентил-1а ) -ацетальдегида в 7,0 мл сухого ДМСО в течение 20 мин. После перемешивания в течение еще 2 ч при комнатной температуре реакционную смесь выливают в ледяную воду. Водный раствор основного характера подисляют до рН310%-ным раствором соляной кислоты. Кислый раствор экстрагируют этилацетатом (3X100 мл) и соединенные органические экстракты промывают однократно водой (50 мл), высушивают (сульфатом магния) и упаривают до твердого остатка. Этот твердый остаток растирают этилацетатом и фильтруют. Фильтрат подвергают очистке колоночной хроматографией (реагент Бэйкер «Энэлайзд, 60-200 меш с применением этилацетата в качестве элюента. После удаления прн,месей с высоким значением Rf собирают 880 мг 9а-окси-11сс, 15абмс-(тетрагидропиран-2-илокси)- 16-фенилЧыс-5-й)-тетранорпростеновую кислоту.
ИК-спектр соединения показывает адсорбиию при 1715 CvTj- (карбонил).
Продукт, полученный по указанной методике, можно превращать в 16-фенил.- отет :аг;ор-13,14-дигидро-РОР2.
П р и м е р 6. 9-Оксо-11а, 15а-диокси-13траис-16-фенил-со-тетранорпростеновая кислота.
Гомогенный раствор 178мг (0,328 ммоль) неочищенного тетрагидропиранилового эфира, полученного по методике примера, в 2 мл смеси (65 : 35) уксусной кислоты с водои перемешивают в атмосфере азота при 40 ±2° С в течение 5 ч. Реакционную смесь концентрируют с помощью роторного испарителя, а затем масляного насоса. Неочищенный продукт подвергают очистке колоночной хроматографией на силикагеле.
Пример 7. (Исходное вещество), уПолуацеталь 2- (5а-окси-3а-(тетрагидропиран-2 - илокси)(тетрагидропиран-2илокси)-4-Сп-метилфенил)-транс - бутен-1ил-1 -циклопентил-1а}-ацетальдегида.
Раствор 1,6 г (3,3 ммоль) у-лактона-2{ 5сс-окси-3«-(тетрагидропиран-2 - илокси)2|3- 3а- (тетрагидропиран-2-илокси) -4- (/г-метплфенил)-гранс-бутен-1-ил-1 -циклопентил1а/ -уксусной кислоты в 20 мл сухого толуола охлаждают до -78° С в атмосфере сухого азота. К полученному охлажденному раствору добавляют 8,0 мл 20%-ного раствора гидрида диизобутилалюминия в н-гексане (Альфа Йнорганикс) по каплям с такой скоростью, чтобы температура не превышала -65° С (15 мин). После дополнительного перемешивания в течение 45 мин при -78° С добавляют безводный метанол
до прекращения выделения газа и реакционную смесь доводят до комнатной температуры. Затем реакционную смесь соединяют с 200 мл эфира, промывают 50%-ным раствором двойного тартрата натрия и каЛИЯ (2x50 мл), высушивают сульфатом натрия и концентрируют.
Получают 1,4 г (87,5%) -полуацеталя 2-{ 5а-окси-За-(тетрагидропиран-2 - ил-окси)-2.(тетрагидропиран - 2-илокси)-4(л-метилфенил) - гранс-бутен-1-ил-1 - циклопентил-1сс}-ацетальдегида.
Пример 8. 9а-Окси-11а, 15а-5«с(тетрагидропиран-2-илокси)-16 - (л-метилфенил) г{ыс-5-тра«с - 13 - со-тетранорпростадиеновая кислота.
К раствору 5,3 мг (12,0 ммоль) бромида (4-карбокси-н-бутил) - трифенилфосфония 3 10 мл сухого ДМСО в атмосфере сухого азота добавляют 9,5 мл (21 ммоль) 2,2 М. раствора метилсульфинилметида натрия в ДМСО. К этому раствору илида красного цвета добавляют по каплям раствор -уПолуацеталя 2- 5а-окси-За-(тетрагидропиран-2-илокси) - (тетрагидропиран-2-илокси)-4-(л-метилфенил) - трансбутен-1-ил-1 - циклопентил-1а - ацетальдегида в 5,0 мл сухого ДМСО в течение 20 мин. После дополнительного перемешивания в течение 2ч при комнатной температуре реакционную смесь выливают в ледяную воду и подкисляют до рН - 3 107о-ным раствором соляиой кислоты. Кислый раствор экстрагируют этилацетатом (3X100 мл) и соединенные органические экстракты промывают водой (3x50 мл), высушивают (сульфатом магния) и упаривают до твердого остатка. Этот твердый остаток растворяют с этилацетатом и фильтруют. Фильтрат подвергают очистке колоночной хроматографией на силикагеле (реагент Бэйкер «Энэлайзд, 60-200 меш) с применением в качестве элюента хлороформа, а затем этилацетата. После удаления примесей с высоким значением Rf собирают 1,2 г 9а-окси-11а, 15а-бис-(тетрагидропиран-2-илокси) -16-фенил-г{«с-5-гранс13-со-тетранорпростадиеновой кислоты.
ИК-спектр (СНСЬ) имеет полосы иоглрщеиия при 1710 см (карбопил) и при 965 см (двойная связь транс-конфигурации) .
Пример 9. (Исходное вещество). у-Полуацеталь 2- 5а-окси-3|сс- (тетрагидропираи-2-илокси) - (тетрагидропиран-2илокси) - 4-(/г-метоксифеиил)-г/заяс-бутен1-ил-1 -циклопеитил - 1а-ацетальдегида.
Раствор 2,2 ммоль -лактона 2- 5а-оксиЗа - (тетрагидропирап-2-илокси) - (тетрагидроиирап-2-илокси - 4-(/г-метоксифенил)-транс-бутеи - 1-ил-1 - циклопентил la-уксусной кислоты в 15 мл сухого толуола охлаждают до -78° С в атмосфере сухого азота. К этому охлажденному раствору добавляют 5,0 мл 20%-иого гидрида диизобутилалюминия в «-гексане (Альфа Инорганикс) ио каплям с такой скоростью, чтобы температура не повышалась выше -65°С 15 мин). После дополнительпого перемешивания в течение 45 мин при -78° С добавляют безводный метанол до прекращения выделения газа и реакционную смесь доводят до комнатной температуры. Реакционну смесь соединяют с 100 мл , промывают 50%-ным раствором двойного тартрата натрия и калия (4x20 мл), высушивают (сульфатом патрия), концентрируют и хроматографируют.
Получают 900 мг (84%) 7ПОлуацеталя 2-/5а-окси-За - (тетрагидропирап-2-илокси) - (тетрагидропиран - 2 - илокси) - 4(/г-метоксифенил)-гранс-бутен - 1-ил-1 -циклопентил-1а }- ацетальдегида.
Пример ГО. (Исходное вещество). Y-Полуацеталь 2-(5а-окси - За-(тетрагидропиран-2-илокси)-2р - Эр-(тетрагидропиран2-илокси)-4-«-метоксифенил - транс-буген1-ил-1-(циклопентил-1;а) ) -ацетальдегида.
Раствор 2,68 ммоль у-лактопа 2- 5а-окси-За (тетрагидропиран-2-илокси)-2р - Зр(тетрагидропиран-2 - илокси)-4-(л-метоксифенил)-гранс-бутен - 1-ил - 1- циклопентил1а} -уксусной кислоты в 15 мл сухого толуола охлаждают до -78° С в атмосфере сухого азота. К этому охлажденному раствору добавляют 8,0 мл 20%-ного раствора гидрида диизопропилалюминия в «-гексане (Альфа Инорганикс) по каплям с такой скоростью, чтобы температура не повышалась выше -65° С (15 мин). После
дополнительного перемешивания в течение 45 мин при -78° С добавляют безводный метанол до полного прекращения выделения газа и реакционную смесь доводят до комнатной температуры. Реакционную смесь
смещивают с 100 мл эфира, промывают 50%-ным раствором двойпого тартрата натрия и калия (4X20 мл), высушивают (сульфатом натрия), концентрируют и хроматографируют.
Получают 1150 мг (87%) у-полуацеталя 2-1 5а-окси-3а-(тетрагидроииран - 2-илокси)-2р-(Зр-(тетрагидррпиран-2 - илокси)4-(л-метоксифенил) - гране - бутен-1-ил-1 циклопентил-1а}-ацетальдегида.
Пример И. 9а-0кси-11а, 15а-бис-(тетрагидропиран-2-илокси) - 16 - (п-метоксифенил)- {ыс-5-транс-13 - ш-тетранорпростадиеновая кислота.
К раствору 3720 мг (8,55 ммоль) броМИДа (4-карбокси-н-бутил) - трифенилфосфоиия в атмосфере сухого азота в 7,4 мл сухого ДМСО добавляют 7,9 мл (15,3 ммоль) 1,96 М раствора метилсульфинилметида натрия в ДМСО. К полученному раствору илида красного цвета добавляют по каплям раствор 900 мг (1,84 Л1моль) у-полуацеталя2-( 5а-окси-3а- (тетрагидропиран-2-илокси) - (тетрагидропирап-2илокси) - 4-(л-метоксифепил)-гранс-бутен1-ил-1 -циклопентил - 1а) - ацетальдегида в 5,0 мл сухого ДМСО в течение более 20 мин. После дополнительного перемешивания в течение 2 ч при комнатной температуре реакционную смесь выливают в ледяную воду. Водный раствор основного характера подкисляют до рН - 3 10%-ным раствором соляной кислоты. Подкисленный раствор экстрагируют этилацетатом (3X100 мл) и соединенные органические
экстракты промывают однократно водой (50 мл), высзшивают (сульфатом магния) и упаривают до твердого остатка. Этот твердый остаток растирают с этилацетатом и фильтруют. Фильтрат подвергают очистке колоночной хроматографией, на силикагеле (реагент Бэйкер «Энэлайзд, 60- 220 Meui) с применением в качестве алюата хлороформа, а затем этилацетата. После удаления примесей с высоким значением Rf собирают .762 мг 9а-окси-Па, 15а-бис(тетрагидропиран - 2-илокси)-16-(/г-метоксифенил)-Ч с-5-7-ранс-13 - со - тетранорпростадиеновой кислоты.
ИК-спектр (CHCIs) имеет полосы поглощения при 1715 см (карбонил) и полосу поглощения при 970 см (двойная связь транс-конфигурации).
Продукт, полученный ио методике этого ириме, можно превращать в 16-л-метоксифенил-(о-тетранорпростагландины ряда
F, Р2(1, FICC, Foa. Пример 12. 9а-Окси-11а, 15а-бмс-(тетраг11дропиран-2-илокси) - 16-(л - метоксифенил)-ч«с-5-гранс-13 - со-тетранорпростадиеновая кислота. К раствору 4876 мг (10,95 ммоль) бромида {4-карбокси-«-бутил) - трифенилфосфония в атмосфере сухого азота в 9,7 мл сухого ДМСО добавляют 10,3 мл (20,0 ммоль 1,96 М. раствора метилсульфинилметида натрия в ДМСО. К этому раствору илида красного цвета добавляют по каплям раствор 1150 мг (2,34 ммоль -полуацеталя 2-{ 5а-окси-За-(тетрагидропиран-2илокси)-2|3- 3,р- (тетрагндропиран-2 - илокси)-4-(tt-метоксифенил)-гранс-бутен - 1-ил1 -циклопентил-1а)-ацетальдегида в 7,0 мл сухого ДМСО в течение более 20 мин. После дополнительного перемешивания в течение 2 ч при комнатной температуре реакционную смесь выливают в ледяную воду. Водный раствор основного характера подкисляют до рН 3 10%-ным раствором соляной кислоты. Подкисленный раствор экстрагируют этилацетатом (3X100 мл и соединенные органические экстракты промывают водой (1X50 мл, высушивают сульфатом магния и упаривают до получеТаблица 1 ния твердого остатка. Этот твердый остаток растирают с этилацетатом и фильтруют. Фильтрат подвергают очистке колоночной хроматографией на силикагеле (реагент Бэйкер «Энэлайзд, 60-200 меш с применением в качестве элюента хлороформа, а затем этилацетата. После удаления примесей с высоким значением R} собирают 898 мг 9а-окси-11а, 15а-б«с-(тетрагидропиран-2-илокси) - 16-(л - метоксифенил)-(«с-5-гра«с-13-(о - тетранорпростадиеновой кислоты. ИК-спектр (СНС1з) имеет полосы поглощения при 1715 сл{- (карбонил) и при 975 еж- (двойная связь гране-конфигурации). Исходные соединения общей формулы 1СНг)п-Аг ТНРО полученные по примеру 4, представлены в табл. 1.







| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 15-замещенных простановых производных или их солей | 1973 |
|
SU644384A3 |
| Способ получения производных циклопентана | 1975 |
|
SU645564A3 |
| Способ получения 2-дезкарбокси2-(тетразол-5-ил)-11-дезокси - -пентанорпростагландинов или их магниевых солей | 1976 |
|
SU638255A3 |
| Способ получения аналогов природных простагландинов | 1973 |
|
SU665799A3 |
| Способ получения промежуточных соединений для синтеза простагландинов и их -эпимеров | 1976 |
|
SU640660A3 |
| Способ получения аналогов простагландинов и их с-15 эпимеров | 1976 |
|
SU652890A3 |
| Способ получения 11-дезокси-16арилокси- -тетранорпростагландинов или их солей | 1976 |
|
SU679134A3 |
| Способ получения 11-дезокси- пентанорпростагландинов или их солей | 1976 |
|
SU613719A3 |
| Способ получения производных -тетранорпростагландинов или их эпимеров по с -или их солей | 1973 |
|
SU584766A3 |
| Способ получения диалкилфосфонатов | 1975 |
|
SU584791A3 |

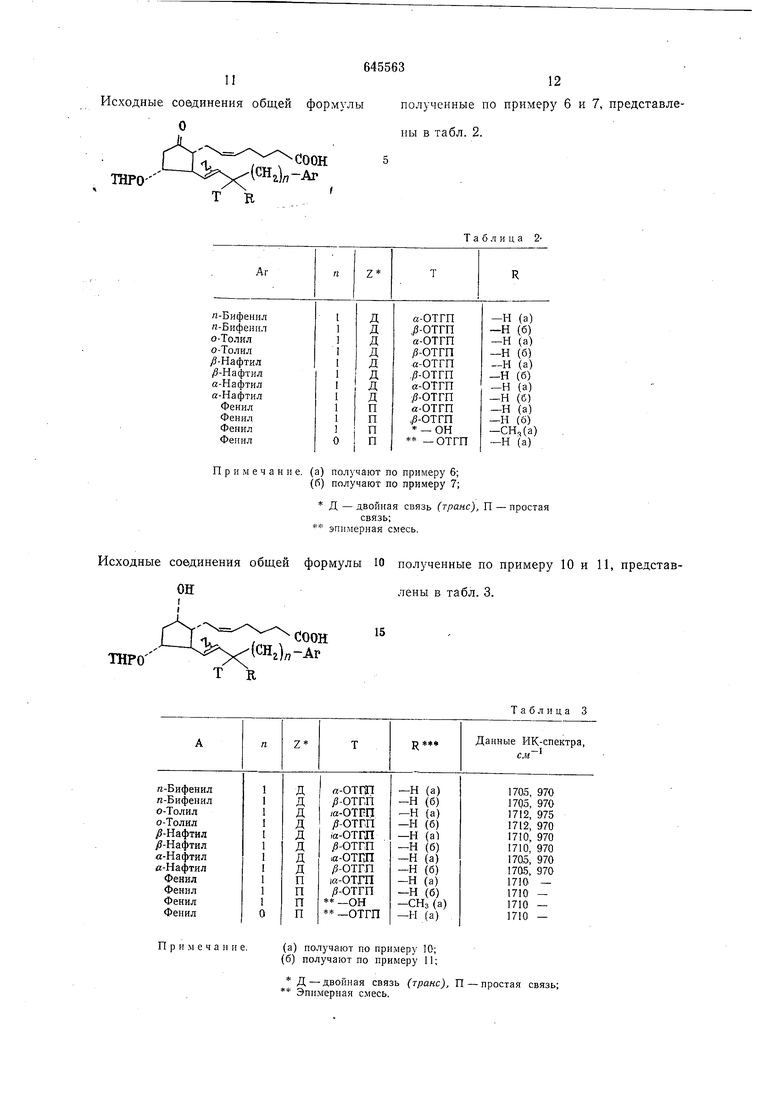
Д-двойная связь (транс), П-простая связь; - эпи.мерная смесь. 11 Исходные соединения общей
соон
Т В
Примечай л е. (а) получают по примеру 6; (6) получают по примеру 7;
Д - двойная связь (транс), П - простая эпимериая смесь. Исходные соединения общей формулы 10
ОЫ
I ,,.СООН
R
(а)получают по примеру 10;
(б)получают по примеру 11;
Д-двойная связь (транс), П - простая связь; Эпимерная смесь.
пы в табл. 2.
Таблица 2связь;
лены в табл. 3.
Таблица 3 формулы полученные по примеру 6 и 7, представле64556312 полученные по примеру 10 и И, представПример 13. (Исходное веиС: т о) у-Полуацеталь 2-{ 5а-окси-3а- (тетрагпдропнран-2-илокси) - (тетрагидропиран-2илокси)-4 - фенил-г/занс-бутен-1-ил-1 - циклопентил-1а |- ацетальдегида.
Раствор 1,2 г у-лактона 2- 5а-окси-3а(тетрагидропиран-2-илокси) - - (тетрагидропиран-2-илокси) -4- (2-тиенил) -трансбутен-1-ил-1) - циклопентил-1а)- уксусной кислоты в 25 мл сухого толуола охлаждают до -78° в атмосфере сухого азота. К этому охлажденному раствору добавляют 3,4 мл 0,8 М раствора гидрида диизобутилалюминия в к-гексане (Альфа Инорганикс) по каплям с такой скоростью, чтобы температура реакционной смеси не поднималась вышг-65° С (). После дополнительного перемешивания 45 мин при -78° С добавляют безводный метанол до прекращения выделения газа и реакционную смесь доводят до комнатной температуры. Реакционную смесь соединяют со 150 мл эфира, иромывают 50%-ным раствором двойного тартрата натрия, и калия (4X20 мл), высушивают (сульфатом натрия) и концентрируют.
Получают с количественным выходом масляиистый у-полуацеталь 2-f 5а-окси-3а(тетрагидропиран-2-илокси) -(тетрагидропиран-2-илокси)-4-(2 - тиенил)- трансбутен-1-ил-1 - циклопентил-1а / -ацетальдегида.
ИК-спектр иоказывает широкую полосу поглощения при 3400 (гидроксил).
Аналогичным образом получают р-тиенильные соединения:
ИК-сиектр: 970
15а-ОТГП; ИК-спектр: 970 см. 15а-ОТГП;
Пример 14. 9а-0кси-11а, 15а-б«с(тетрагидроииран-2-илокси) -16 - (2-тиенил) цис-5-транс-13-а - тетранорпростадиеновая кислота.
К раствору 2,6 г (6 ммоль) бромида (4карбокси-к-бутил)-трифеиилфосфония в атмосфере сухого азота в 5,0 мл сухого ДМСО добавляют 5,7 мл (11,7 ммоль) 2,2 М раствора метилсульфинилметида натрия в ДМСО. К этому красному раствору илида добавляют по каплям раствор 1,03 г (2,2 ммоль) -полуацеталя 2-1 5а-окси-3а-(тетрагидропиран-2-илокси) (тетрагидропиран-2-илокси)-4-(2-тиенил)-гранс-бутен-1ил-1 -циклопентил-1а| -ацетальдегида в сухом ДМСО в течение более 20 мин. После дополнительного перемешивания в течение 2 ч при комнатной температуре реакционную смесь выливают в ледяную воду. Водный раствор основного характера промывают дважды этилацетатом (по 20 мл), подкисляют до рН примерно 3 10%-ньш раствором соляной кислоты. Подкисленный раствор экстрагируют этилацетатом (3X20 мл) и соединенные органические
экстракты промывают однократно водой (10 мл), высушивают (сульфатом магния) и упаривают до получения твердого остатка. Этот твердый остаток растирают с этилацетатом и фильтрат концентрируют.
Получают 1,2 г 9а-окси-11а, 15а-б«с(тетрагидропиран-2-илокси) -16- (2-тиенил) цис-5-транс-13-() - тетранорпростадиеновой кислоты.
ИК-спектр показывает сильную полосу поглощения при 1700 см-, а также полосы поглощения между 2800 и 2600 см (ка|:)боксильная группа).
Продукт, полученный по методике этого
примера, можно превращать в 16-(2-тиенил)-ш-тетранорпростагландины ряда F
(Р2 а , F ,ct , FO (2 ) .
Аналогичным образом получают р-тиенильные соединения.
15а-ОТГП; ИК-спектр: 1710, 970 см 15Р-ОТГП; ИК-спектр: 1710, 970 слгПример 15. (Исходное вещество).
у-Полуацеталь 2-f 5а-окси-3а-(тетрагидропиран-2-илокси) -2:р- 3а- (тетрагидропиран-2илокси)-4 - (2-тиенилбутил-1 -циклопентил1а /-ацетальдегида.
Раствор 1600 мг (3,2 ммоль} у-лактона
2- 5а-окси-3:а - (тетрагидропиран-2-илокси) (тетрагидропиран-2-илоксн) -4- (2-тиенил)-б)тил-1 - циклопенгил-1а /-уксусной кислоты в 5 мл сухого толуола охлаждают до -78° С в атмосфере сухого азота. К этому охлажденному раствору добавляют 5,0 мл 20%-ного гидрида диизобутилалюмииия в н-гексане (Альфа Инорганикс) ио каплям с такой скоростью, чтобы температура реакции не превышала -65° С (3 мин).
После дополнительного перемешивания в течение 30 мин при -78° С добавляют безводный метанол до прекращения выделения газа и реакционную смесь доводят до комнатной температуры.-Реакционную смесь
смешивают со 150 мл эфира, промывают 50%-ным раствором двойного тартрата натрия и калия (1X50 мл), высушивают сульфатом магния, концентрируют и хроматографируют.
Получают 7-полуацеталь 2- f 5а-окси-3а(тетрагидропиран-2-илокси) - (тетрагидроииран-2-илокси) -4- (2 - тиенил) -бутил1 -циклопентил-1а ) -ацетальдегида.
Пример 16. 9а-Окси-11а, 5a-6uc(тетрагидропиран-2-илокси)-16-(2-тиенил)1{ис-5-сй-тетранорпростеновая кислота.
К раствору 5150 мг (11,6 ммоль) бромида (4-карбокси-н-бутил) -трифенилфосфония в атмосфере сухого азота в 10,1 мл
ДМСО добавляют 10,8 мл (21,1 ммоль) 1,96 М раствора метилсульфинилметида натрия в диметилсульфоксиде. К этому раствору илида красного цвета добавляют по каплям раствор 1300 мг (2,6 ммоль)
- -полуацеталя 2- {5а-окси-3а-(тетрагидро15
nT paii-2-ibioKcii) (тетрагидропиран-2 1Л-окс 1)-4-(2 - тиенил)-бутил-lj-циклопентил-1а}-ацетальдегида в 7,0 мл сухого ДМСО в течение более 20 мин. После до1гол1п;тельного перемешизаиня в течение 2 ч при комнатной температуре реакционную смесь выливают в ледяную воду. Водный раствор основного характера подкисляют до рН примерно 3 10%-ным раствором соляной кислоты. Подкисленый раствор экстрагируют этилацетатом (3x100 мл) и соедшюиные органические экстракты промывают однократно водой (50 мл), высушивают (сульфатом магния) и упаривают до получения твердого остатка. Этот твердый остаток растирают с этилацетатом и фильтруют. Фильтрат подвергают очистке хроматографией на колонке на силикагеле (Бэйкер «Энэлайзд, 60-200 меш) с применением этилацетата в качестве элюента.
После удаления примесей с высоким зиачеиием собирают 9а-окси-11а, 15аб«с-(тетрагидроииран-2 - илокси)-16-р-тиеипл)-г(ыс-5-сй -тетраиорпростеновую кислоту.
Продукт, полученный по указанной методике, можно превращать в 16-(2-тиенил)со-тетранор-13,14-дигидро-РОР-2а.
Пример 17. (Исходное вещество). 7-Полуацеталь 2-f 5а-окси-3а-(тетрагидропирап-2-илокси) (тетрагидропираи-2илокси)-5-(2-тиенил)-т/7анс-пеитен-1-ил-1)циклопентил-1а -ацетальдегида.
Раствор 1,28 г {2,7 ммоль) 7-лактона-25а-окси-3а - (тетрагидропиран-2 - илокси)(тетрагидропиран-2 - илокси)-5-(2тиенил)-транс - пентен-1-ил-1 -циклопентил1а J-уксусной кислоты в 13 мл сухого толуола охлаждают до -78° С в атмосфере сухого азота. К этому охлажденному раствору добавляют 3,7 мл 0,8 М раствора гидрида диизобутилалюминия в н-гексане (Альфа Ииорганикс) по каплям с такой скоростью, чтобы температура реакции не была выше -65° С (15 мин). После дополнительного перемешивания в течение 45 мин при -78° С добавляют безводный метанол до прекращения выделения газа и реакционную смесь доводят до комнатной температуры. Реакционную смесь соединяют со 150 мл эфира, промывают 50%-ным раствором двойного тартрата натрия и калия (4x20 мл), высушивают сульфатом натрия и концентрируют. Получают с количественным выходом маслянистый Полуацеталь 2- f 5а-окси-3 а-(тетрагидропиран-2-илокси)2р- За- тетрагидропиран-2 - илокси -5-(2-тиенил-) - пентен-1-ил-1)-циклопентнл1а )-ацетальаегида.
Пример 18. (Исходное вещество). 7-Полуацеталь 2- { 5а-окси-3а- (тетрагидропиран-2-илокси) - (тетрагидропиран-2илокси)-5-(2-тиенил)-гранс - центен-1-ил-1||циклопентил-1а -ацетальдегида.
IG
Раствор 1,47 г (3,1 ммоль) -у-лактона 2{ 5о:-окси-3а-(тетрагидропиран-2 - илокси)2,)- (тетрагидропиран-2-илокси) -5- (2-тиенил)-грая :-пентен-1ил-1)-циклопентил-1а j уксусной кислоты в 15 мл сухого толуола охлаждают до С в атмосфере сухого азота. К этому охлажденному раствору добавляют 4,25 мл 0,8 М раствора гидрида диизобутнлалюминия в н-гексане (Альфа
Инорганикс) по каплям с такой скоростью, чтобы температура реакции была выше -65° С (15 мин). После дополнительного перемешивания в течение 45 мин при -78° С, добавляют безводный метанол до прекращения выделения газа и реакционную смесь доводят до комнатной температуры. Полученную реакционную смесь соединяют со 100 мл эфира, промывают 50%-ным раствором двойного тартрата натрия и калия
(4x20 мл), высушивают сульфатом натрия II концентрируют.
Получают 1,38 г -полуацеталя 2- f 5а-окси-За-(тетрагидропиран-2 - илокси)-2j3- 3j3(тетрагидропиран-2 - илокси)-5-(2-тиеиил)7-раяс-пентен-1-ил-1 -циклопентил - 1а -ацетальдегида.
Пример 19. 9а-Окси-11а, 15а-бис(тетрагидропиран-2-илокси)- 17-(2-тиенил)цис- -транс - 13-0) - триснорпростадиеновая
кислота.
К раствору 1,8 г (4,05 ммоль) бромида (4-карбокси-н-бутил) -трифенилфосфония в атмосфере сухого азота в 5,0 мл сухого ДМСО добавляют 3,2 мл (7,0 ммоль), 2,2 М раствора метилсульфииилметида натрия в диметилсульфоксиде. К этому раствору красного цвета добавляют по каплям раствор 717 мг (1,34 ммоль) -полуацеталя 2{ 5ос-окси-3:а-(тетрагидропиран-2 - илокси)2|5- 3 3- (тетрагидропиран-2-илокси) -5- (2-тиенил)-гранс-пентен-1-ил-13-циклоцентил-1а )ацетальдегида в 5,0 мл сухого ДМСО в течение более 20 мин. После перемешивания в течение еще 2 ч при комнатной температуре, реакционную смесь выливают в ледяную воду. Водный раствор основного характера промывают этилацетатом (2X20 л«.л) и подкисляют до рН примерно 3 10%-ным раствором соляной кислоты. Подкисленный раствор экстрагирзют этнлацетатом (3x20 мл) и соединенные органические экстракты промывают водой (1X10 мл, высушивают сульфатом магния и упаривают до твердого остатка. Этот твердый остаток
растирают с этилацетатом и фильтруют. Фильтрат подвергают очистке колоночной хроматографией на силикагеле (Бэйкер «Эпэлайзд, 60-200 меш) с применением этилацетата в качестве элюента.
После удаления примесей с высоким
значением Rf собирают 740 мг 9а-окси-11а,
15а-бис -(тетрагидропиранил-2- илокси)-17(2-тиенил)-1{нс-5-гранс-13-ш-триснорпростадиеновой кислоты. Пример 20. (Исходное иещество). Полуацеталь 2-; 5а-окс1ьЗа-(тетраг11дропиран-2 - илокси)-2|3- За-{тетрагидропиран-2илокси)-5-(2-фурил)-транс-пентен-1-нл -циклопентнл la. {-ацетальдегида. Раствор 1,6 г (3,4 ммоль) у-лактона 2{ 5а-окси-3 -(тетраг1 Дропиран-2-илокси)-2|3 За - (тетраг; дропиран-2 - илокси)-5-(2-фу ри л) -гранс-пснтен-1 -ил- 1 -циклопентил- 1а уксусной кислоты в 16 мл сухого толуола охлаждают до -78С в атмосфере сухого азота. К полученному охлажденному раствору добавляют 4,68 мл 0,08 М раствора гидрата диизобутилалюмнния в н-гексане (Альфа Инорганикс) ио канлям с такой скоростью, чтобы температура реакции не превышала -65° С (15 мин.. После дополнительиого перемешивания при -78° С в течение 45 мин добавляют безводный метанол до прекращения выделения газа и реакционную смесь доводят до комнатной температуры. Реакционную смесь соединяют с 150 мл эфира, промывают 50%-ным раствором двойного тартрата натрия и калия (4x20 мл), высушивают (сульфатом натрия) и концеитрируют. Получают с количественным выходом маслянистый у-полуацеталь 2-1 5а-окси-3а(тстрагидропиран-2-илокси) - - (тетрагиаропиран-2 - илокси) - 5 - (2-фурил)7ранс-пентен-1-ил-1 - циклопентил-laj-ацетальдегида. Пример 21. 9а-Окси-11а, 5a-6uc(тетрагидропиран-2 - илокси)-17(2-фурил)цис-5-транс - 13-со - триснорпростадиеновая кислота. К раствору 3,36 г (7,6 м.чоль) бромида (4-карбокси-н-бутил) -трифенилфосфония в атмосфере сухого азота в 15,0 мл сухого ДМСО добавляют 7,0 мл (14,0 ммоль) 2,0 М раствора метилсульфинилметида натрия в ДМСО. К полученному раствору илида красного цвета добавляют по каплям раствор 1,3 г (2,81 ммоль) -у-полуацеталя 2-( 5а-окси-За-(тетрагидропиран-2-илокси),о, - (тетрагидропиран-2-илокси)-5- (2-фурил)-гранс-пентен-1-ил-1-циклопентил-1а -} ацетальдегида в сухом ДМСО. В течение более 20 мин. После дополнительного перемешивания в течение 2 ч при комнатной температуре, реакционную смесь выливают в ледяную воду. Водный раствор основного характера промывают дважды атилацетатом (20 мл) и подкисляют до рН примерно 3 10%-ным раствором соляной кислоты. Подкисленный раствор экстрагируют этилацетатом (3x20 мл) и соединенные органические экстракты промывают однократно водой (10 мл), высушивают (сульфатом магния) и упаривают до получения твердого остатка. Этот твердый остаток растирают с этилацетатом и фильтруют. Фильтрат подвергают очистке колоночной хроматографией на силикагеле (Бэйкер «Энэлайзд, 60-200 меш) с применением этилаиетата в качестве элюента. После удаления примесей с высоким значением R,- получают 1,53 г 9а-окси-11а, 15а-б«с-(тетрагидропиран-2-илокси)-17(2 - фурил)-г(«с-5транс-13-сй-триснорпростадненовой кислоты. Пример 22. 9-Оксо-11а,15а-б«с-(тетрагидроиираи-2-шюкси)-16-(/г - дифенил)7 уанс-13-со-тетранорпростеновая кислота. Суспензию 85 мг 9-оксо-11а, 15a-6wc(тетрагидропиран-2 - илокси) - 16-(п-дифенил)-г «с-5-гранс-13-(й - тетранопростадиеновой кислоты и 20 мг 5%-ного палладия на угле в 20 мл абсолютного метанола перемешивают под давлением водорода 1 атм при комиатиой температуре до потребления 1,6 мл водорода. После этого смесь фильтруют через цеолит и концентрируют для получения целевого соединения, в форме вязкого масла весом 84 мг. После удаления защитных тетрагидропиранильных групп (ТНР) спектр ядерного магнитного резонанса (в дейстерированном хлороформе) показал мультиплет при 7,07-7,67 б (ароматические группы), мультиплeJ при 5,33-5,60 б Странс-олефин) и не показал присутствия г мс-олефина. Пример 23. 9-Оксо-11а, 15а-диокси16-фенил-гранс-13-со - тетрапорнростеновая кислота. Раствор 46 мг 9-оксо-11а, 5а-диокси16-фенил - цис-5-транс-13 - со - тетранорпростадненовой кислоты в 5 мл безводного диэтилового эфира обрабатывают при помощи 448 ,мг (3,6 ммоль) диметплизопропилхлорсилана и 360 мг (3,6 ммоль) триэтиламина при температуре 25° С в течение 48 ч. Реакционную смесь охлаждают до 0° С, прибавляют метанол и полученный раствор промывают водой (3 порции по 2 мл), сушат над сульфатом магния и выпаривают до получения остатка (67 мг). Сырой остаток растворяют в 6 мл метано ла, прибавляют 30 лг 50%-ного палладия на угле и полученную суспензию гидрируют в течение 4 ч при температуре -22° С (четыреххлористый углерод - сухая углекислота). После фильтрования через «суперцелль и выпаривания продукт гидрирования подвергают гидролизу в 2 мл смеси уксусной кислоты с водой (3:1) в течение 10 мин, разбавляют водой (20 мл) и экстрагируют этилацетатом (4 порции по 15 мл). Объединенные органические экстракты промывают водой (2 порции по 10лл), сушат над сульфатом магния и выпаривают до получения 44 мг 9-оксо-11а, 15а-диокси-16-фенил-гранс-13-« - тетранорпростеновой кислоты. Температура плавления сгответствую-щего эфира 95-96 С. Формула изобретения 1. Способ получения промежуточиых оединений для получения простагландинов бщей формулы
R
ОТНР
где Ar - а- или |3-фурил, а- или р-тиенил, а- или Р-НЗФТИЛ, фенил, 3,4-диметоксифенил, 3,4-метилендиоксифенил, 3,4,5-триметоксифенил или монозамещенный фенил, в котором заместителем является галоид, трифторметил, фенил, низший алкил или низший алкоксил;
я - целое число от О до 5 при условии, что, если Аг - фенил, замещенный фенил или нафтил, п - I, I;
R - водород или низший алкил;
ТНР - 2-тетрагидропиранил;
W - простая связь или г ыс-двойная связь;
Z - простая связ или транс-двойная связь, если , и Z - простая связь, если
/он
Н - группа.
отличающийся тем, что соединение формулы
ОН
Ч
(СН,)„-Аг
ТНРООТНР 11
где Аг, R, и и Z имеют указанные значения, подвергают взаимодействию с илидом формулы
(СбНз)зР СН-СНз-СНг-СНг-СОО М :III
С получением соединения формулы I,
где Аг, R, л и Z имеют указанные значения;
W - 1{«с-двойная связь;
/ОН
М
н
и, в случае необходимости, восстанавливают указанное соединение с получением соединения формулы I, где Аг, R, М, га и Z
имеют указанные значения, W - простая связь, с последующим выделением целевого продукта.


Авторы
Даты
1979-01-30—Публикация
1975-09-05—Подача