(54) СПОСОБ ПОЛУЧЕНИЯ АНАЛОГОВ ПРИРОДНЫХ ПРОСТАГЛАНДИНОВ
в соотношении 65:35. Обработку ведут при температуре от комнатной до 40-42 С.
Целевые соединения выделяют и очищают известными методами.
Пример 1 (исходный продукт). К раствору 5,82 г (12,0 м,моль) 4-ацетиламинокарбонилбутилтрифенилфосфонийбромида в 6,0 /мл сухого диметилсульфоксида добавляют по каплям 9,8 мл (23,5 ммоль) 2,4 М раствора метилсульфинилметида натрия н диметилсульфоксиде. К образовавшемуся красному раствору илида добавляют по каплям растВОр 1,32 г (3,00 моль) 2- 5ааксИ - За-(тетрагидроииран - 2 - илокси)2р - (За) - тетрагидропиран - 2 - илокси(гране-1 - октен - 1 - ил)-циклопент-1а-ил ацетальдегида, -полуацеталя в 3,0 мл сухого диметилсульфоксида в течение 0,5 ч. После пере1мешивания в течение 20 ч при комнатной температуре реакционную смесь выливают в ледяную воду. К водному раствору добавляют эфир, энергично неремеши,вают и смесь .подкисляют до рН 3 добавлением 10%-ной соляной кнслоты. Подкисленный водный слой далее дважды экстрагнруют эфиром. Объединенные эфирные экстракты сушат безводным сульфатом магния и концентрируют. Получают 4 г твердого вещества. Полученное вещество очищают с помощью колоночной хроматографии на силикагеле с использованием хлороформа, а затем этилацетата BI качестве элюентов. После удаления примесей с высоким Rf собирают 1,15 г (л) (выход 67,8%) М-ацетил-9а-окси-11а, 15сх-бас-(тетрагидропиран - 2 - илокси)-t{wc-5 - транс13-простадиенамида в виде вязкого бесцветного масла.
ИК-спектр (СНС1з) показывает сильное поглощение при 5,80 мк (карбонилы). ЯМР-спектр (CDCIa) показывает мультиплет при 5,,686 для олефиновых протонов, широкий синглет при 4,60-4,806 для ОН и Nn, мультиплеты при- 3,25- 4,305 для -СПО- и -СНгО-, синглет при 2,376 для - СОСНз и мультиплеты при 0,68 - 2,376 для остальных протонов.
Указанный продукт подвергают каталитическому восстановлению для получения М-ацетил-9а - ркси - На, 15а-б«с - (тетрагидропиран - 2 - илокси)-транс-13 - простенамида, который может превращаться с помощью известных реакций в N-ацетилнростагланди.н-Fia - карбоксамид и N - ацетил15 - метилпропостагландин-Егкарбоксамид. Последний может превращаться, как описано в примере VI, в N-ацетил-простагландин-Агкарбоксамид, или восстанавливаться, как описано в примере 36, в N-ацетилпростагландин-р1,з - карбоксамид.
Пример 2. Раствор 108мг (0,192 М1моль) М-ацетил-9а - окси-Па, 15а - бис(тетрагидропиран - 2 - илокси) - цис - 5гранс-13-простадиенамида в 2 мл смеси уксусной кислоты с водой (65:35) перемешивают в атмосфере азота при 42°С 3 ч. Растворитель удаляют при пониженном давлении, и полученное в результате масло очищают с помощью хроматографии на колонке при использовании хлороформа, этилацетата, затем смеси (9:1) метиленхлорида и метанола в качестве элюентов. После удаления менее полярных примесей собирают 42 мг Н-ацетил-9а, Па, 15а-окси-|5-г{«с13-гранс-простадиенамида в виде вязкого бесцветного масла. Выход 89%.
ЯМР (CDCls) Продукта показывает мультиплет при 5,65-5,226 (4Н) для олефиновых протонов, мультиплет при 4,31- 3,806 (ЗН) для СНО, щирокий синглет при 3,20-2,736 (4Н) для ОН и NH, синглет при 2,416 (ЗН) для СОСНз и мультиплеты при 2,60-0,716 (ЗН) для остальных протонов.
Пример 3 (исходный продукт). К раствору, охлажденному до -10°С в атмосфере азота, 1,15 г (2,04 мадоль) Ы-ацетил-9аокси - Па, 15а-бис - (тетрагидропиран - 2илокси) - 5 - гранс-13 - простадиенамида, приготовленного аналогичяо примеру 2, в 30 мл ацетона добавляют по каплям 0,90 мл реактива Джонса. Через 30 мин реакционную смесь рез-ко охлаждают добавлением 0,90 мл изопропанола. Смесь перемешивают на холоду в течение 10 мин, затезд разбавляют этилацетатом. Органический слой промывают дважды водой и один раз насыщенным раствором ,NaCl, сушат безводным сульфатом магния и концентрируют, получая 1,12 г (97% выход) неочищенного маслянистого -9 - оксо - 11, 15абис - (тетратидропиран - 2 - илокси) - цисN-ацетил - 5 - транс-13 - простадиенамида.
ИК-спектр (СНС1з) продукта показывает сильное поглощение при 5,67ц (кетоновый карбонил) и 5,95|д, (.карбонилы имида).
Раствор 5,0 г (8,89 ммоль) продукта примера 1, 5,45 г (26,5 ммоль) дициклогексилкарбодиимида и 1,71 г (8,89 ммоль) трифторацетата пиридиния в 75 мл бензола перемешивают под азотом при комнатной температуре 4 ч. Раствор затем разбавляют 150 мл этилацетата. Выпавшую в осадок дициклогексилмочевину собирают фильтрованием, раствор промывают трижды водой и Насыщенным раствором NaCl, сушат безводным сульфатом магния и концентрируют. Получают 6,56 г (выход 100) маслянистого неочищенного N - ацетил - 9 - оксоПа, 15а-бис - (тетрагидропиран - 2 - илокси) - цис - 5-гране-13 - простадиенамид.
Пример 4. Раствор 1,12 г (0,020 ммоль) N-ацетил - 9 - оксо - Па, 15а - б«с-(тетрагидропиран - 2 - илокси) - 5 - транс13-простадиенамида в 14,0. мл смеси уксусной кислоты и воды (65:35) перемешивают в атмосфере азота при комнатной температуре 18 ч. Затем концентрируют с помощью испарения при вращении. Полученное неочищенное масло очищают с помощью хроматографии на -колонке на силикагеле при использовании смесей хлороформа и этилацетата в (качестве элюента. После элюирования менее полярных примесей кристаллический N-ацетил - 9 - оксо - Па, 15а-диокси-г{нс - 5 - транс - 13 - простадиенамид, N-ацетил - простаглаидин Е карбоксамид собирают и получают 407мг (выход 51,8%) целевого продукта, т. пл. 86- 86,5°С (из этилацетата-гексана).
ИК-спектр (СНС1з) продукта показывает сильные полосы поглощения при 5,78}г (карбонил кетона) и 5,92}д, (карбонилы имида). Спектр-ЯМР (CDMU) продукта показывает два мультиплета при 5,26- 5,726 для олефиновых протонов, мультиплет при 3,85-4,286 - для СНО, синглет при 2,356 для - СОСНз и мультиплеты при 0,68-2,826 для остальных протонов.
Пример 5 (исходный продукт). К раствору 2,03 г (4,00 ммоль) 4-пропиониламинокарбонилбутилтрифенилбромистого фосфония примера 8 (высушенного в вакууме в течение «очи при 110°С) в 5 мл диметилсульфоксида добавляют 8,96 мл (17,0 ммоль) 1,89М раствора метилсульфинилметида натрия в диметилсульфоксиде. К полученному красному раствору илида добавляют по каплям раствор 876 мг (2,00 ммоль) известного - окси - За(тетрагидропиран - 2 - ил окси) - 2р - За(тетрагидропиран - 2 - илокси) - 1 - трансоктен - 1 - илциклопент - 1а - ил -ацетальдегида, -уполуацеталя в 2,0 мл диметилсульфо.ксида. Смесь перем-ешивают 2,5 ч под азотом. Затем выливают в смесь ледяной воды с эфиром. Водный слой подкисляют до с помощью 10|%- ной соляной кислоты, и подкисленный водный слой дважды экстрагируют эфиром. Объединенные эфирные экстракты сущат -безводным сульфатом магния и концентрируют, получают неочищенное масло. Масло очищают с помощью колоночной хроматографии на силикагеле при использовании бензола, хлороформа, затем этилацетата в качестве элюентов. После удаления менее полярных примесей собирают 507 мг (выход 43,6%) бесцветного маслянистого Ы-лропионоил-9аокси - На, 15а - бис - (тетрагидропиран)2 - илокси) - цис - 5 - транс - 13-простадиенамида.
ЯМР-спектр (CDCls) продукта показывает мультиплет при 5,66-5,276 для олефиновых протонов, широкий синглет при 4,70 для -О-СН-О-, мультиплеты при 4,26-3,226 для - СВО, и СНгО, широкий синглет при 9,10 для NH, квадруплет при О II
2,63 для N СНСНг, триплет при 1,206 для СНз, и мультиплеты при 2,83-0,676 для остальных протонов.
Указанный продукт можно подвергать каталитическому восстановлению для получения N - пропионоил - 9а окси - 11а-15абмс-(тетрагидропиран - 2-илокси) - простанамида, соединение А. Соединение А можно гидролиз-овать, по примеру 3 для получения N-пропионоил - 13,14 - дигидропростагландин-Рга-карбоксамида. Соединение А можно подвергать окислению, как описано в примере 4, с последующим гидролизом, по примеру 5, для получения N-npoпионоил - 13,14 - дигидропростагландин-Ег карбаксамида, соединение В. Соединение В можно дегидрировать, как описано в примере 6, для получения N - пропионоил - 13, 14-дигидропростагландин AI карбоксамида
или восстанавливать, как описано в примере 36, получая пропионоил-13, 14-дигидропростагландин-р1|3-карбоксамида.
Указанное исходное вещество можно подвергать каталитическому восстановлению
для получения N - пропионоил - 9а - окси11а-15а - бис - (тетрагидропиран - 2-илокси - транс-13 - простенамида), который можно подвергать превращениям с помощью известных реакций в N-пропионоилпростагландин-Fia - карбоксамид или Nпропионоилпростагла«дин - FI - кар-боксамид. Последний можно превратить (пример 6) в N - нропионоил-простагландин-Аг карбоксамид или (пример 36) в N-пропионоил - простагландин - Fip - «арбоксамид. Указанный продукт можно гидролизовать по примеру 3, для получения N-пропионоилпростагландин - Раа - карбоксавдид. Данное вещества можно подвергать каталитическому восстановлению, как описано в примере 7, в N-пропионоил - 13,14-дигидропростагландин - Pia-карбоксамид.
Пример 6 (исходный продукт). К раствору, охлажденному до -15°С, 749 мг
(1,3 ммоль) хроматографированного спирта примера 5 в 80 мл ацетона добавляют 0,56 мл реактива Джонса. Смесь перемешивают на холоду 15 мин, затем резко охлаждают добавлением 0,56 мл 2-пропанола. Ох.лажденную смесь разбавляют этилацетатом, промывают дважды водой и насыщенным растворОМ NaCl, сушат безводным сульфатом магния и концентрируют, получая неочищенное масло, очищают его с помощью хроматографии на колонке, используя хлороформ в -качестве элюента. Концентрированием первых четырех фракций получают 416 мг (выход 55,6%) N-пропионоил-9 - оксо - На, 15а - бис - (тетрагидропиран - 2 - илокси) - цис - 5 - гране-13простадиенамида в виде бесцветного масла.
Пример 7. Раствор 416 мг хроматографированного кетона примера 6 и 5,0 мл
смеси уксусной кислоты и воды (65 : 35) перемешивают в токе азота при комнатной температуре в течение ночи. Концентрирование смеси дает масло, которое очищают с помощью колоночной хроматографии на
силикагале при использовании смесей хлореформа и этилацетата в качестве элюентов. После удаления менее полярных примесей собирают 76 мг кристаллического N-пропионоил - 9 - оксо - 11а, 15а - диоксицис - 5 - транс - 13 - простадиенамида, Nпропионоилпростагландин - Ег - карбоксамида, т. пл. 49-51°С (из смеси этилацетата и гексана).
ИК-спектр (СНС1з) продукта показывает сильные полосы поглощения при 1735 и 1695 сы для карбонильных групп и среднее поглощение при 970 см для трансдвойной связи. ЯМР-спектр (CDCU) продукта показывает мультиплет при 5,70- 5,436 для гракс-двойной связи, мультиплет при 5,43-5,106 для г{«с-двойной связи, мультиплет при 4,30-3,696 для СНО, широкий синглет при 3,42-2,806 для ОН и NH, квадруплет при 2,606 для СОСН2, триплет, при 1,136 для -СНз и мультиплеты при 2,72-0,606 для остальных протонов.
Пример 8 (исходный продукт). К растводу 1,53 г (3,00 ммоль) 4-циклопропанкарбониламино арбонил) - бутил - трифенил бромистого фосфония, высушенного в вакууме в течение ночи при 110°С в 40 мл диметилсульфоксида, добавляют 3,38 мл (6,93 ммоль) 2,05М раствора метилсульфенилметида натрия в диметилсульфоксиде. К полученному красному раствору илида добавляют по каплям раствор 438 мг (1,00 ммоль) известного - окси - За(тетрагидропиран - 2 - илокси) - 2|3 - (Затетрагидропиран-2-илокси) - 1 - транс - октен - 1 - ил (циклопент - 1а-ил - ацетальдегида, уполуацеталя в 2,0 мл диметилсульфоксида. Смесь перемешивают в течение ночи под азотом, затем выливают в смесь ледяной воды и эфира. Водный слой ПОДКИСЛЯЮТ до 10%-ной соляной кислотой, и подкисленный водный слой экстрагируют эфиром. Объединенные эфирные экстракты сушат безводным сульфатом магния и концентрируют, получая неочищенное масло. Масло очищают с номощью колоночной хроматографии на силикагале при использовании 10% бензола в хлороформе в качестве элюента. После удаления менее нолярных примесей собирают 289 мг (выход 49%) бесцветного маслянистого N - циклопропанолкарбонил - 9а - окси-11 а, 15а - бис- (тетрагидропиран - 2 - илокси)цис - 5 - транс - 13 - простадиенамида.
ИК-спектр (СНС1з) маслянистого продукта показывает сильное поглощение при Г670 и 1720 c.м приписываемое карбонильным группам, и при 970 см, приписываемое транс-двойной связи, ЯМР-спектр (CDCls) маслянистого продукта показывает мультиплет при 5,66- 5,276 для олефиновых протонов, широкий синглет при 4,70 для -О-СН-О-, мультиплеты при 4,26-3,226 для -СНО и СНг-О, широкий синглет нри 9,10 для NH,
и мультиплет при 2,83-0,636 для остальных протонов.
Пример 9. Раствор хроматографированного спирта примера 8 (90 мг) в 2,0 мл смеси уксусной кислоты и воды (65:35) перемешивают при 42°С 4,5 ч в атмосфере азота. Концентрирование реакционной смеси дает масло, которое очищают с помощью колоночной хроматографии на силикагеле.
После элюирования менее полярных примесей этилацетата и бензола (2:1) элЮИрование смесью метиленхлорида и метанола (9:1) дает 39 мг (выход60,7%) бесцветного твердого .продукта N-цИКло-пропанкарбонил-9а. Па, 15а-триокси-1{мс-5-гранс-рпростадиенамида, т. пл. 99-102°С (из эфира).
ИК-спектр (СНС1з) маслянистого продукта показывает сильные полосы поглощения при 1680 и 1720 си- приписываемые карбонильным группам, и при 970 , приписываемые траяс-двойной связи. Снектр-ЯМР (CDCls) показывает широкий оинглет при 9,36 для. NH, мультиплет
при 5,70-5,106 для олефиновых протонов,
мультиплеты при 4,27-3,006 для СНО, и
мультиплеты при 2,84-0,566 для остальных
протонов.
Пример 10 (исходный продукт). К
раствору, охлажденному до -15°С, 200 мг хрОматографированного спирта нримера 8 в 3 мл ацетона добавляют 82 мл реактива Джонса. Смесь перемешивают на холоду 20 мин, затем резко охлаждают добавлением 82 мл 2-пропанола. Охлажденную смесь разбавляют этиладетатом, дваЖды нромывают водой И насыщенным раство.ром NaCl, сушат безводным сульфатом магния и концентрируют, получая 184 м-г (выг
ход 92%) N-циклопрОпанкарбоннл - 9 - оксо-Иа, 15а - бис - (тетрагидропиран - 2илокси) - цис - 5 - транс - 13 - стростадиенамида.
Пример 11. Раствор 184 мг неочищенного кетона примера 10 и 4,0 мл смеси уксусной кислоты и воды (65:35) нагревают в атмосфере азота при 42°С 4,5 ч. Концентрирование смеси дает масло, которое очищают с помощью колоночной хромйтографин на силикагеле. После элюировання смесью этилацетата и бензола (2:1) удаляют менее полярные примеси и затем элюированием этилацетатом получают бесцветный маслянистый продукт, N-циклопропанкарбонил - 9 - оксо - На, 15а-диокси - цис - 5 - транс - 13 - простадиенамид, N-цнклопропанкарбонил - простагландин ЕЗ карбоксамид, весом 83 мг (выход 63,5%).
ИК-спектр маслянистого продукта показывает полосы сильного поглощения .при 1730 для карбонила кетона, при 1680 и 1730 см для карбонилов имида и при 970 см-1 для транс - двойной связи
Спектр-ЯМР (CDCls) маслянистого продукта показывает синглет при 9,176 для NH, мультиплет при 5,70-5,496 для транс-олефина, мулыкплет при 5,49-5,176 для цисолефина, мультиплет при 4,30-3,776 для СН-О, синглет п-ри 3,50 и мультиплеты прИ 3,04-0,636 для остальных протонов.
Пример 12 (исходный продукт). К раствору 1,22 г (2,32 ммоль) 4-гриметилацетиламино - карбонилбутил - трифенилфосфонийбромида в 4,0 мл сух-ого диметилсульфоксида добавляют 2,22 мл (4,54 ммоль) 2,05М раствора метилсульфинилметида натрия в диметилсульфоксиде. К полученному красному раствору илида добавляют по каплям раствор 0,219 г (0,5 ммоль) 2-i 5aокси - За - (тетрагидропиран - 2(илокси)2р - (За - тетрагидропиран - 2 - илоксн)транс - 1 - октен - 1 - ИлАциклопент - 1аил ацетальдегида, -полуа-цеталя в 1,0 мл сухого диметилсульфоксида. После перемешивания при комнатной температуре в атмосфере азота в течение 20 ч реакционную смесь выливают в ледяную воду. К водному раствору добавляют эфир и подкисляют до добавлением 1б%-ной соляной кислоты. Водную смесь далее экстрагируют трижды, , объединенные эфирные экстракты сушат безводным сульфатом магния и концентрируют, получая вязкое масло. Очистку продукта проводят с помощью колоночной хроматографии на силнкагеле при использовании хлороформа в качестве элюеита. Полученное вещество растирают со смесью эфира, и гексана, н-олучая 401 мг маслянистого N-триметил - ацетил - 9а-окси-Иа, 15а - бис - (тетрагидропиран - 2 илокси) - цис - 5 - транс - 13 - простадиенамида.
Спектр-ЯМР (CDCls) показывает синглет при 1,206 для С(СНз)з щирокий синглет при 4,48-4,736 для ОСНО и мультиплет при 5,15-5,606 для олефиновых протонов.
Пример 13 (исходный продукт). К раствору, охлажденному до -20°С в атмоофере азота, 0,40 г N-трИметилацетил - 9а-оксн - Па, 15а-бг;с - (тетрагидропиран.- 2илокси)-1{ыс - 5 - транс - 13 - простадиенамида примера 12 в 4,0 мл ацетона добавляют 0,165 мл реактива Джонса. Смесь неремешивают на холоду 20 мин, затем резко охлаждают добавлением 0,165 мл изопропанола. Смесь перемешивают 5 мин, затем разбавляют этилацетатом. Разбавленный раств-ор промывают дважды водой и насыщенным раствором NaCl, сущат безводным сульфатом магния и концентрируют, получая 352 мг неочищенного маслянистого N-триметилацетил - 9 - ОКсо - На, 15а - бис - (тетрагидропиран - 2 - илокси) цис - 5 - транс - 13 - ппостадненамида.
Пример 14. Раствор 352 мг очищенного N-триметилацетил-9 - оксо - На, 15абис - (тетрагидропираи - 2 - илокси)-ч«с5 - транс - 13 - нростадиенамида примера
13 в 4,0 мл смеси (65:35) уксусной кислоты и воды перемещивают в атмосфере азота 4,5 ч при 40±2°С И затем концентрируют. Полученное в результате масло подвергают колоночной хроматографии на силикагеле и получают М-тримстилацетил-9оксо-Н, 15 - диокси - цис - 5 - транс - 13простадиенамид, триметилацетилпростагландин-Ез-карбоксамид, весом 45 мг.
ИК-спектр (СПС1з) продукта показывавают полосы сильного поглощения при 1680 и 1730 см для карбонильных групп и при 965 для гране-двойной связи. Спектр-ЯМР (CDCls) показывает синглет при 1,226 для С(СНз)з, щирокий синглет при 3,316 для ОН, мультиплет при 3,00- 4,236 для СПО, мультиплет при 5,23-5,526 для у,ас-олефина, мультиплет при 5,52- 5,766 для транс-олефина, щирокий синглет при 8,20 для МП и мультинлет при 0,70- 3,056 для остальных протонов. УФ-спектр (МеОП) после обработки КОН показывает характерное для РСВ поглощение цри 278 мм к.
Пример 15. К раствору (9-метансульфониламинокарбонил - бутил) - трифенилбромистого фосфония (10,4 г, 20,0 ммоль) в 12,0 сухого диметилсульфомсида добавляют по каплям 21,8 мл (39,0 ммоль) л 1,8М раствора метилсульфинилметида натрия в сухом диметилсульфоксиде. Полученный в результате красный раствор илида перемешивают в атмосфере азота 5мип, затем по каплям в течение 30 мин добавляют раствор 2,19 г (5,0 ммоль) известного 2 - 5а - окси - За - (тетрагидропиран - 2илокси) - 2р - (За-) - тетрагидропиран - 2илокси (-гране - 1 - октен - 1 - ил) - циклопент - 1а - ил - а цетальдегида, -у-полуацеталя в 5,0 мл сухого диметилсульфо ксида. Раствор перемещивают в течение ночи, затем выливают в смесь эфира и ледяной воды. Энергично перемещиваемый раствор подкисляют до рН 3 соляной кислотой. Подкисленный водный слой экстрагируют эфиром и объединенные эфирные экстракты сущат безводньш: сульфатом магния и концентрируют, получая неочищенное желтое масло. Масло очищают с помощью колоночной хроматографии на сили-кагале при использовании смесей бензола и хлороформа в качестве элюентов. После удаления менее нолярных примесей собирают бесцветный маслянистый N-метансульфонилва - оксн - На, 15а - бис - (тетрагидропиран - 2 - илокси) - цис - 5 - транс - 13 простадиенамид весом 2,59 г (выход 86,41%).
Спектр-ЯМР (CDCls) продукта показывает мультнплет при 5,70-5,136, приписываемый олефиновым протоном, щирокий синглет при 4,80-4,526для ОСНО, мультиплет при 4,30-3,006 для СНО и СН2О, синглет ори 3, для ЗОгСНз и мультипле11
ты при 2,75-0,686 для остальных протонов.
Пример 16. Раствор 3,16 г б«с-ТНР эфира примера 15 и 32 мл смеси Зксусной кислоты и воды (65 : 35) перемешивают При комнатной температуре в течение ночи в атмосфере азота. Раствор затем концентрируют и полученное масло очищают с помощью колоночной хроматографии на силикагеле при использовании смесей хлороформа и этилацетата в качестве элюентов. После удаления менее полярных поимесей собирают кристаллический (1,4 г) N-метансульфонил - 9а, На, 15а - триокси - цис - 5 - транс - 13 - простадиенамид, N-метаисульфонилпростагландин - Faa карбоксамид; т. пл. 121 - 121,5°С (из смеси этилацетата и эфира).
ИК-спектр (СНС1з) показывает полосы сильного поглощения при 1720 для карбонильных групп и 970 см для трансдвойной связИ. Масс-спектр показывает пики потери одной, двух и трех молекул воды и пик потери HaO+CsHiiПример 17 (исходный продукт). К раствору 2,48 г спирта примера 15 и 14 мл ацетона, охлажденному до -15°С в атмосфере азота, добавляют 1,70 мл реактива Джонса. Смесь перемешивают на холоду 20 мин, затем резко охлаждают добавлением 1,70 мл изопропанола. Смесь разбавляют этилацетатом-; разбавленный раствор промывают водой дважды я насыщенным раствором NaCI, сушат и концентрируют, получая маслянистый -бесцветный N-метансульфонил - 9 - кето - Па, 15а - бис - (тетрагидропиран - 2 - илокси) - цис - 5 - транс13 - простадиенамид (2,45 г выход 98,6%).
Пример 18. Раствор 2,45 г бмс-ТНР эфира примера 17 в 24 мл смеси уксусной кислоты и воды (65:35) нагревают до 40±2°С под аз-отом в течение 6 ч. Смесь затем концентрируют и полученный в результате маслянистый продз кт очищают с помощью колоночной хроматографии на силикагеле при использовании смесей хлороформа и этилацетата в качестве элюентов. После удаления менее полярных примесей получают твердый N-метансульфоНИлпростагландин Eg карбоксамид, весом 865 мг (выход 49,2%), ст. пл. 118,5-119°С (из ацетона и гексана).
ИК-спектр (СНС1з) кристаллического продукта Показывает поглощение при 1720 СМ- для карбонила имида, при 1730 см для карбонила кетона и при 970 см- для транс-двойной связи. ЯМР спектр (CDCls) кристаллического продукта показывает мультиплет при 5,70-5,446 для транс-олефина, мультиплет пр-и 5,44- 5,186 для «(«с-олефина, мультиплет при 4,33-3,80б для СИ-ОН, синглет при 3,236 для ОзСНз и мультиплет при 2,78-1,66 для остальных протонов.
12
Вычислено, % С 58,72; И 8,21; N 3,26; S 7,46.
Пайдено, % С 59,01; И 8,12; N 3,19; S 7,54.
Пример 19 (исходный продукт). К раствору (4-метансульфониламинокарбонил) - бутил трифенилбромистого фосфония 2,68 г (5,1 ммоль), который сушился на протяжении ночи при 144С в 5 м.л сухого диметилсульфоксида, добавляют по каплям: 6,22 мл (9 мм-оль) 1,56 М раствора метилсульфинилметида натрия в сухом диметилсульфоксиде. Полученный красный раствор илида перемешивают под азотом 15 мин, затем добавляют раствор 770 мг (1,50 ммоль) 2-15а - окси - За - (тетрагидропиран - 2 - илокси) - 2р-(33 - метил-За)тетрагидропиран - 2 - илокси) - транс - 1октен - 1 - ил-циклопент - 1а - ил -ацетальдегид, олуацеталь и 2-|5а - окси - За(тетрагидропиран - 2 - илокси) - 2р - (Заметил - 33) - тетрагидропиран - 2 - илокси) - транс - 1 - октен-1 - илциклопент-1аилацетальдегид, у-полуапеталь в 2 мл сухого диметилсульфоксида. Смесь перемешивают в атмосфере азота в течение ночи, затем выливают в смесь ледяной воды и эфира. Водный слой подкисляют 10%-ной соляной кислотой, а затем трижды экстрагируют этилацетатом. Объединенные органические экстракты сушат безводным .сульфатом магния и концентрируют, получая неочищенное желтое масло, которое очищают С помощью колоночной хроматографии на силикагеле, используя смесь хлороформа и этилацетата в качестве элюента. После элюирования менее полярных примесей собирают маслянистые продукты N-метансульфонил - 9а - окси - II а, 15а - б«с-(тетрагидропиран - 2 - илокси) - 15р - метилцис - 5 - транс - 13 - простадеинамид и N-метан-сульфонил - 9а - окси - Па, 15абнс - (тетрагидропиран - 2 - илокси) - 15аметил - цис - 5 - транс - 13 - простадиенаМИД, весом 300 мг.
Спектр-ЯМР хроматографированногопродукта (CDCls) показывает мультиплет при 6,60-5,096 для олефиновых протонов, широкий синглет при 4,74-4.446 для ОМНО, мультиплеты при 4,21-3,926 для СНгО и СНО, синглет при 3,246 для SOpCH, два синглета при 1,30 к 1,116 для С-СНз и мультиплеты при 2,67-0,566 для остальных протонов.
П р и м е р 20 (исходный продукт). К охлажденному до -15°С раствору 0,600 г (0,98 ммоль) быс-ТНР эфиров примера 19 в 11 мл ацетона добавляют 0,83 мл реактива Джонса. Смесь перемеш-ивают в атмосфере азота иа холоду 20 мин. Затем резко охлаждают добавлением 0,83 мл изапропанола, продолжая перемешивание 5 мин, затем разбавляют этилацетатом. Органический слой промывают водой (2 раза) и насыщенным раствором NaCI, сушат безводным сульфатом магния и концентрируют, получая неочищенный маслянистый N-метансульфонкл - 9 - кето - На, 15абис - (тетрагидропиран - 2 - илокси) - 15рметил - цис - 5 - транс - 13 - простадиенамид и N-метансульфонил - 9 - кето - Па, 15р - бис - (тетрагидропиран - 2 - илокси)15а - метил - цис - 5 - транс - 13 - Ьростадиенамид, весом 523 мг (выход 87,1%). Пример 21. Раствор 623 мг (0,855 ммоль) неочищенных 6wc-THP эфиров примера 20 в 5,0 мл смеси уксусной кислоты и ВОДЫ (65 : 35) перемешивают под азотом при комнатной температуре в течение ночи, затем концентрируют. Неочищенный маслянистый продукт очищают с помощью хроматографИи па колонке силикагеля при использовании смесей хлороформа и этилацетата в качестве элюептов. После элюирования менее полярных примесей собирают бесцветный маслянистый N-метансульфонил - 9 - кето - Па, 15а - диокси - 15р - метил - 5 - цис - 13 - транспростадиенамид И N - метансульфонил - 9 кето - Па, 15р - диокси - 15а - метил - 5цис - 13 - транс - простадиенамид, весом 169 мг (выход 42,0%). Спектр-ЯМР (CDCla) продукта обнаруживал мультиплет при 5,72-5,495 для транс-двойной связи, мультиплет при 5,49-5,126 для чмс-двойной связи, мультиплет при 4,37-3,486 для СНО, еинглет при 3,266 для 5О2СНз и мультиплеты при 2,72-0,636 ДЛЯ остальнЫХ протонов. Масс-спектр показывал м/е при 443 для родственной молекулы, м/е при 425 для М-Н2О и м/е при 407 для М-2П2О. Пример 22 (исходный материал). К раствору 835 мг (1,61 ммоль) продукта Г(4-метансульфониламино) - бутил - трифенилфосфонийбромида в 2,0 мл сухого диметиЛСуль:фоксида добавляют по каплям 1,42 мл (2,72 ммоль) 1,91 М раствору метилсульфинилметида натрия в диметилсульфоксиде. К полученному красному раствору илида добавляют по каплям раствор 250 мг (0;54 ммоль) полуацеталя, полученного аналогично примеру 21 в 1,0мл сухого диметилсульфоксида в течение 5 МИн. После перемеш-ивания в течение 20 ч при комнатной температуре реакционную смесь выливают на лед со льдом. К водному раствору добавляют этилацетат и энергично перемешанную смесь подкисляют до рН 3 добавлением 10%-ной соляной кислоты. Подкисленный водный слой далее дважды экстрагируют этилацетатом. Объединенные органические экстр актьг сушат безводным; сульфатом магния -и концентрируют, получая неочищенное масло. Полученное масло очищают с помощью колоночной хроматографии на силикагеле при использовании смесей хлороформа и этилацетата в качестве элюентов. После удаления менее полярных примесей собирают целевой N-метансульфонил - 9а-окси-Па, 15а - бис - (тетрагидропиран - 2 - илокси)16, 16 - диметил - цис - 5 - транс - 13-простадиенамид в виде вязкого масла, весом 249 мг (75,5% выход). ЯМР-спектр (CDCU) хроматографированного продукта показывает мультиплет при 5,70-5,136 для винильных протонов, мультиплет при 4;80-4,466 для ОСНО, еинглет при 3,246 для ЗОзСНз, мультиплеты при 4,26-3,056 для СН20 и СНО, еинглет при 0,806 для гем-диметильных групп и мультиплеты при 2,71-0,506 для остальных протонов. Пример 23 (исходный продукт). К охлажденному до -20°С под азотом раствору 249 мг (0,403 ммоль) N-метансульфонил9а - окси - Па, 15а - бис - (тетрагндрОпиран - 2 - илокси) - 16, 16-димегил - цис-5транс - 13 - простадиенамйда, приготовленного аналогично примеру 22, в 5 мл ацетона добавляют по каплям 0,202 мл реактива Джонса. Через 15 мин реакционную смесь резко охлаждают добавлением 0,202 мл изопропанола. Смесь перемешивают на холоду 5 мин, затем разбавляют этилацетатом. Органический слой дважды промывают водой и насыщенным раствором NaCl, сушат безводным сульфатом магния и концентрируют, N-метансульфонил - 9 - кетоПа, Г5а - бис (тетрагидропиран - 2-илокси)-16, 16 - диметил - цис - 5 - транс - 13простадиенамид в виде масла, весом 220мг (выход 88,4%). Пример 24. Раствор 220 мг (0,36 ммоль) N-метансульфонил - 9 - кетоПа - 15а - бис (тетрагидропиран - 2илокси)-16, 16 - диметил - цис - 5 - транс13 - простадиенам-ида примера 23 в 5 мл смеси уксусной кислоты и воды (65: 35) перемещивают под азотом при комнатной температуре на протяжении ночи, затем концентрируют упариванием при вращеНИИ. Полученное сырое масло очищают с помощью хроматографии на колонке силикагеля при использовании смесей хлороформа и этилацетата в качестве элюентов. После элюирования менее полярных примесей собирают N-метансульфонил - 9-кето - Па, 15а - диокси-16, 16 - диметил-ц«с5 - транс - 13 - простадиенамид в виде вязкого бесцветного масла, весом 73 мг (выход 44,5%). ИК-спектр (СНСЬ) хроматографированного продукта показывает полосы сильного поглощения при 1735 и 1720 см- для карбонильных групп и при 970 см- для транс-двойной связи. Спектр-ЯМР (СОС1з) Продукта показывает мультиплет при 5,78-5,506 для транс-двойной связи, мультиплет при. 5,,206 для- г «с-двойной связи, мультиплеты при 4,29-3,706 для СНО, еинглет при 3,27 для SOaCHs, синглет при 0,866 для гем-диметильных групп и мультиплет при 2,80-0,566 для остальных протонов. Пример 25 (исходный продукт). К раствору 2,60 г (5,36 ммоль) продукта 4-(ацетиламинОКарбонил) - бутил - трифенилфосфонийбром-ида в 20 мл сухогодиметиЛСульфоксида добавляют но канлям 5,45 мл (10,22 Ммоль) 1,88 М раствору метилсульфинилметида натрия в диметилсульфокСиде. К полученному красному раствору илида добавляют по каплям раствор 250 мг (0,54 ммоль) - окси - За(тетрагндроп-иран - 2 - илокси) - 2р - За(тетрагидропирап - 2 - и.токси) - 4,4-диметил - транс - 1 - октен - 1 - илциклонент) 1а-ил -ацетальдегид полуацеталя в 1,0 мл сухого диметилсульфоксида в течение 5 мин. После 20 ч перемешивания при комнатной температуре реакционную смесь выливают в ледяную воду. К водному раствору добавляют этклацетат, и Прн энергичном перемешивании смесь подкисляют до рН 3 добавлением 10%-ной соляной кислоты. Подкисленный водный слой дважды экстрагируют этилацетатом. Объединенные органические экстракты сушат безводным с)ЛБфатом магния и коннентрируют, получая неочиш;енный продукт, который очиШ,ают с помощью хроматографии на колонке силикагеля при использовании бензола и хлороформа в качестве элюентов. После удаления менее нолярных примесей целевой N - ацетил - 9а-окси11а, 15а - бис - (тетрагидропиран - 2-илокси) - 16, 16-диметил - цис - 5 - транс - 13нростадиенамид собирают в виде вязкого бесцветного масла, весоМ 250 мг (выход 78,5%). Спектр-ЯМР (СНС1з) хроматографированного .Продукта показывает синглет при 9,36 для NH, мультиплет пр-и 5,65-5,226 для олефиновых протонов, широкий синглет при 4,653 для ОСНО, мультиплет при 4,20-3,206 для СНО, и СНзО синглет при 2,326 для СОСПз, синглет при 0,80 для гем-диметильных групп и мультиплеты нри 2,69-0,616 для остальных протонов. Приме.р 26 (исходный продукт). К охлажденному до -20°С в атмосфере азота раствору 250 мг (0,424 ммоль) N-ацетил9а-окси-11а, 15а - бис- (тетрагидролиран2 - илокси)-16, 16 - диметил - цис-5-транс13-1Простадиенамида, приготовленного аналогично примеру 25 в 7 мл ацетона добавляют по каплям 0,212 мл реактива Джонса. После 15 мин реакционную смесь гасят добавяением 0,212 мл изопропанола. Смесь перемешивают на холоду 10 мин, затем разбавляют этилацетатом. Органический слой дважды промывают водой и насыщенным раствором NaCl, сушат безводным сульфатом магния и концентрируют, получают N-ацетил - 9 - кето-11а, 15а-бис(тетрагидропиран - 2 - илокси)-16, 16-диметил - цис - 5 - граяс-П-простадиенамид в виде вязкого бесцветного масла, весом 226 мг (выход 90,4%). Пример 27. Раствор 226 мг (N-ацетил9 - кето-11а, 15а-бмс - (тетрагидропиран-2илокси)-16, Гб-диметил - цис - 5 - транс-13простадиенамида nip-иготовленного аналогично примеру 26 в 5,0 мл смеси уксусной кислотЬ и воды (65:35) «перемешивают под азотом при комнатной температуре в течение ночи, затем концентрируют упариванием при вращении. Полученное неочищенное масло очищают с помощью хроматографии на колонке на силикагеле, используя смесь хлороформа и этилацетата в качестве элюентов. После элюирования менее молярных примесей целевой N-ацетил - 9 - кето-Иа, 15а - диокси-16, 16-ди-метил - цис - 5-транс13-простадиенамид собирают в Виде вязкого бесцветного масла, весом 57 мг. ИК-спектр (СНС1з) продукта показывает сильное поглощение при 1745 и 1710 см- для карбонильных групп и меренное ноглощение при 975 см- для транс-двойной связи. Спектр -ЯМР (CDCIs) показывает мультиплет при 5,75-5,486 для гранс-двойной связи, мультиплет при 5,48-5,206 для «wc-двойной связи, мультиплет при 4,16- 3,686 для СНО, сипглет -при 2,266 для СОСНз, синглет при 0,886 для гем-диМетильных грушп и мультиплеты при 2,62- 0,606 для остальных протонов.. Пример 28 (исходный нродукт). К раствору 2,42 г (5,00 ммоль) 4-(ацетиламинокарбонил) - бутил - трифенилброМистого фосфония в 5,0 мл сухого диметилсульфоксида добавляют по кацлям 10,5мл (10,0 ммоль) 0,95 М раствора м.етилсульфинилмвтида натрия в диметилсульфоксиде. К полученному красному раствору илида добавляют по каплям раствор 450 мг (1,00 ммоль) - окси - За - (тетрагидропиран - 2 - илокси) - 2р - (Зр-метил-За)тетрагидро-ПИран - 2 - илокси)-транс - 1-октен-1 - илциклопент - 1а - ил -ацетальдегид, у-полуацеталя и 2-(Зсс - метил - Зя)-тетрагидропиран - 2 - илокси)-2р - (За - метилЗр) - тетрагидропиран - 2 - илокси)-Tpa«c1а - октен - I - ил (у-циклопент - 1 - ил ацетальдегид, 7-полуацеталя в 2,0 мл cvxoго диметиЛСульфоксида в течение 0,5 ч. После 20 ч перемешивания при комнатной температуре реакционную смесь выливают в ледяную воду. К водному раствору добавляют этилацетат и энергично Перем ешанную смесь подкисляют до рП 3 добавением водной соляной кислоты. Подкисленый водный слой дважды экстрагируют этилацетатом. О.бъединенные органические эктракты сушат безводным сульфатом магния и концентрируют, получая сырой продукт. Полученный неочищенный продукт очищают с помощью колоночной хромаографии, что дает целевой N-aцeтил-9aокси-Па, 15а - бис - (тетрагидрооиран)-2илокси) - 15р - метил - цис - 5 - транс - 13простадиенамид и Ы-ацетил-Эа-окси-Па, 15р-быс - (тетрагидропиран) - 2 - илокси)15а-метил - цис - 5 - транс-13-простадиенамид.
Пример 29. (исходный продукт). К охлажденному до -20°С в атмосфере азота раствору 139 мг (0,24 -ммоль) эпимерных . продуктов, приготовленных в примере 28, в 4 мл реактивно чистого ацетона добавляется ПО каплям 0,080 мл (0,213 ммоль) реактива Джонса. Через 15 ми« реакционную смесь гасят добавлением 0,080 мл изопропанола. Смесь леремешивают на холоду 10 мин, затем разбавляют этилацетатом. Органический слой дважды промывают водои и насыщенным pacTBOipoM NaCI, сушат безводным сульфатом магния и концентрируют, что дает неочищенную эпимерную смесь N-ацетил - 9 - «ето - Па, 15а - бис(тетратидропиран - 2 - илокси) - 15|р-метил цис - 5 - транс - 13 - простадиенамид и N-ацетил - 9 - кето-Иа, 15р-быс - (тетрагидропиран - 2 - илокси)-15а-метил - цис5 - транс - 13-1простадненамида.
Пример 30. Раствор 65 мг (0,11 ммоль) эпимерной смеси примера 29 в 2,0 мл смеси уксусной кислоты и воды (65 : 35) перемешивают в атмосфере азота при комнатной температуре в течение ночи, затем концентрируют упариванием- при вращении. Полученное неочищенное масло очищают с помощью колоночной, тонкослойной или жидкость-жидкостной хроматографии, получая N-ацетнл - 9 - кето-Па, 15а - диокси15р-метил - цис - 5 - транс - 13-1прОСтадиенамида и Ы-ацетил - 9 - кето-Па, 15р-диокси - 15а-метил - цис - 5 - транс - 13-.простадиенамида.
Пример 31. (исходный продукт). К раствору {4 - бензолсульфониламинокарбонил - трифенил бромистого фосфония (2,53 г, 4,36 ммоль) в 3,0 мл сухого диметилсульфоксида добавляют по -каплям 5,05 мл (8,72 -ммоль) 1,73 М раствора метилсульфинилметида натрия в сухом диметилсульфоксиде. Полученный красный раствор илида перемешивают в атмосфере азота 5 ми«, затем по каплям добавляют раствор 0,476 г (1,09 ммоль) 2- 5а-оксиЗа - (тетрагидрониран - 2 - илокси) - 2р(За-тетрагидропиран - 2 - илокси)-граяс-1октен - илциклопент - 1а-ил - ацетальдегида, полуацеталя в 2,0 мл сухого диметилсульфоксида. Раствор перемешивают в течение 2,75 ч, затем выливают в смесь этилацетата и ледяной воды. Энергично перемешанный раствор подкисляют до рН 3, добавляя 10%-ную соляную кислоту. Подкисленный водный слой экстрагируют этилацетатом и объединенные органические экстракты сушат безводным сульфатом магния и концентрируют, получая неочищенное желтое . Масло очищают с помощью колоночной хроматографии на силикагеле при использовании смесей хлороформа и этил ацетата в качестве элюентов. После удаления менее полярных лримесей целевой М-бензолсульфоНил - 9а - окси-Па, 15а - 5нс - (тетрагидропиран - 2 - илокси)цис - 5 - транс - 13 - простадиенамид собирают в виде бесцветного масла, весом 294 мг (40,8% выход).
Спектр-ЯМР (CDCIs) хроматографированного продукта показывает мультиплеты при 8,19-7,926 и 7,72-7,376 для ароматических Протонов, мультиплет при 5,70- 5,126 для винильных протонов, мультиплет при 4,83-4,606 для ОСНО, мультиплеты, при 4,29-3.305 для СП2О и СНО и мультиплеты при 2,49-0,706 для остальных topoтонов.
Пример 32. Раствор 104 мг б«с-ТНР эфира примера 31 и 5,0 мл смеси уксусной кислоты и воды (65:35) нагревают до 40±2°С в течение 2,5 ч в атмосфере азота. Раствор концентрируют и полученаюе масло очипдают с помощью колоночной хроматографии на силикагеле. После удаления примесей с более высоким Rf хлороформом, элюирование 10%-ным метанолом в метиленхлариде дает целевой N-бензолсульфонил-9а. Па, 15а-триокси - цис - 5 - транс13-простадиенамид в виде белой пены, весом 30 мг (38,0% выход).
Снектр-ЯМР (CDCls) хроматографированного продукта показывает мультиплеты при 8,10-7,886 и 7,60-7,366 для ароматических протонов, мультиллеты при 5,60- 5,376 и 5,,086 для винильных протонов, -мультиплеты при 4,24-3,736 для СНО и мультиплеты при 2,52-0,696 для остальных протонов. ИК-спектр (СНСЬ) продукта показывает полосы сильного поглощения при 1720 см- для карбонильной группы и 965 см- для транс-двойной связи.
Пример 34. Раствор 175 мг (0,266 ммоль) б«с-ТНР эфира примера 33 в 3 мл смеси уксусной -кислоты и воды (65 :35) нагревают до 40±2°С в атмосфере азота в течение 6 ч. Смесь концентрируют и полученный маслянистый продукт очищают с помощью колоночной хроматографии на силикагеле. После удаления примасей с более высоким Rf хлороформом элюирование смесью 1 : 1 хлороформа н этилацетата дает целевой Н-бензолсульфонил-9кето-Па, 15а - диокси - цис - 5 - транс-13простадиенамид в виде пены, весом 35 мг (26,8% выход).
ИК-спектр (СНС1з) хроматографированного продукта показывает полосы сильного поглощения при 1735 и 1720 см- для карбонильных групп и поглощение при 970смдля транс-двойной связи. Спектр-ЯМР (CDCla) .продукта показывает мультиплеты при 8,10-7,886 и 7,67-7,406 для ароматических протонов, мультиплет при 5,72- 5,506 для гранс-двойной связи и 5,39- 5,106 для ч с-двой ной связи, мультиплет
19
при 4,27-3,886 для СНО и мультиплеты при 2,68-0,686 для ОСтальиых протонов.
Примео 35 (исходный продукт). К раствооу 4- (л-толуолс -льфониламинокарбонилбутил) - трифеиилбромистого фосфония (2,68 г, 4,50 ммоль), котооый сушился в течение ночи при 144°С в 2,0 мл сухого диметиЛСульЛоксида добавляют по каплям 4,65 мл f9.00 ммоль), 1,94М раствора метилсульфинилмет па натпия в сухом диметилсульсЬоксиде. Полученный красный растроо илида перемешивают в атмосфере азота 15 мин. Затем добавляют оаствор 653мг 1,50 ммоль) изрестного 2-Г5а-окси-За(тетпагидропиран - 2 - илокси) - 23 - (За)тетрагидропипан - 2 - ило-кси-(гоанс-1-октен - I - ил)-циклопент - 1а-ил -ацетальдегида, v-полуацеталя, в 20 мл сухого диметилсульфоксида. Смесь перемешивают в атмосфере азота 5 ч, затем выливают в смесь ледяной воды и эфира. Водный слой подкисляют 10%-ной соляной кислотой, затем трижды экстрагируют эфиром. Объединенные эфирные экстракты сушат безводным сульфатом магния и концентрируют, получая неочишенное л елтое масло, которое очищают с помошью колоночяой хроматографии на силикагеле. После удаления менее полярных примесей смесями хлороформа и бензола, элюирование этилацетатом дает бесцветный маслянистый N-л-толуолсульфонил - 9а - окси-Па, 15а-бис(тетрагидропиран - 2 - илокси) - цис - 5транс - 13 - простадивнамид, весом 383 мг (выход 37.9%).
Опектр-ЯМР (CDCU) маслянистого продукта показывает два дублета при 7,89 и 7,236 ( one) для ароматических протонов, мультиплет при 5,64-5,006 для олефинпвых протонов, широкий синглет при 4.636 для О-СН-О, мультиплеты при 4,28-3,206 для -СНО- и -СН,О, синглет ПРИ 2.426 для -СНя и мультиплеты при 2,63-0,486 для остальных шротонов.
ИК-спектр (СНСЬ) показывает полосы сильного поглошения при 1710 , приписываемые карбонильному поглощению и 970 см- приписываемые транс-двойной связи.
Пример 36. Раствор 222 мг (0.329 ммоль) бис-ТНР эфира примера 35 в 2 мл смеси уксусной кислоты и воды (65:351 нагревают до 40±2°С в атмосфере азота 5 ч, затем концентрируют. Маслянистый продукт очищают с помощью колоночной хроматографии на силикагеле. После удаления менее полярных примесей хлороформом элюирование смесью метиленхлорида и метанола (9: 1). Получают целевой N-л-толуолсульфонил - 9а, Па, 15а-триокси - цис - 5 - транс - 13 - ггростадиенамид в виде бесцветного вязкого масла, весом 50мг (30% выход).
Спектр-ЯМР (CDCls) маслянистого продукта показывает два дублета при 7,85 и
20
7,236 (J 7 спс) для ароматических протонов, два перекрывающихся мультиплетапри 5,68-4,946 для олефиновых протонов, мультиплеты при 4,68-2.906 для -СНО- и ОН, синглет ПРИ 2,326 для -СНз и мультиплеты при 2,50-0,436 для остальных протонов.
Пример 37 (исходный продукт). К охлажпенному до -15°С раствору 0,161 г
(0.239 ммоль) бмс-ТНР эфира шримера 35 в 4 мл ацетона добавляют 0,101 мл реактива Джонса. Смесь перемешивают в атмосфере азота на холоду 20 миН, затем гасят добавлением 0,10 мл изопропанола.
Смесь перемешивают 5 мин, затем разбавляют этилацетатом. Органический слой дважды промывают водой и насыщенным раствором NaCl, сущат безводным сульфатом магния и концентрируют, что дает сырой маслянистый М-л-толуолсульфонил-9кето-Иа, 15а-бис - (тетрагидропиран - 2илокси) - цис - 5 - транс - 13 - простадиенамид, весом 156 мг (выход 97,0%).
Пример 38. Раствор 156 мг
(0,232 ммоль) неочищенного бис-ТНР эфира примера 37 в 3,0 мл смеси уксусной кислоты и воды (65:35) нагревают в атмосфере азота ПРИ 40±2°С 4 ч, затем концентрируют. Неочищенный маслянистый
продукт очишают с помощью колоночной хроматографии на силикагеле. После удаления менее полярных веществ хлороформом, элюирование с помощью 2i%-Horo метанола в хлороформе дает бесцветный вязкий маслянистый М-л-толуолсульфонил-9кето-Иа, 15а-диокси - 5 - цис - 13 - транспростадиенамид, весом 32 мг (выход
27,4%).
Спектр-ЯМР продукта (CDCU) показывает два дублета при 7,81 и7,206 () для олефиновых протонов, мультиплет при 5,64-5.316 для транс-олефина, мультиплет при 5,31-4.986 для 1(нс-олефина, мультиплет ппч 4,23-3,556 для -СНО-, синглет
ПРИ 2.236 для -СНз и мультиплет при 2,57-0,376 для остальных протонов. ИКспектр (CDClj) показывает полосы сильного поглощения при 1720 и 1730 см для карбонильных групп и при 970 см для
т/ а«с-двойной связи.
Пример 39 (исходный продукт). К раствору Г4-(2 - тиофенсульфонил)-аминокарбонилбутил -трифенилбромистого фосфония (2,34 г, 4,0 ммоль) в 2,0 мл сухого
диметилсульфоксида добавляют по каплям 3,59 мл (7,5 ммоль) 2,09М раствора метилсульфинилметида натрия в сухом диметилсульфоксиде. Полученный красный раствор нлида перемешивают в атмосфере азота
5 мин, затем добавляют по каплям в тече.ние 10 мин раствор 0,438 г (1,0 ммоль) известного 2-Г5а-окси-За- (тетрагидропиран-2илокси)-23-(3а) - тетрагидропиран-2-илокси (-граяс - 1 - октен - 1 - ил)-циклопент-.
1а - ил1-ацетальдегида, -полуацеталь в 2,0 мл сухого диметилсульфоксида. Раствор перемешивают в течение ночи, затем выливают в смесь этилацетата и ледя«ой воды. Энергично перемешиваемый раствор, ПОДКИСЛЯЮТ до рН 3 10%-ной соляной кислотой. Подкисленный водный слой экстрагируют этилацетатом и объединенные органические экстракты сушат безводным сульфатом магния и концентрируют, что дает неочищенное желтое масло. Масло очиш:ают с номошью колоночной хроматографии на силикагеле. После удаления менее полярных веш:еств с помощью 2%-кого диэтиламина в этилацетате элюированиеэтилацетатом дает бесцветный маслянистый N-(2 - тиофенсульфонил - 9а - окси - Па, 15а-б«с - (тетрагидропиран - 2 - илокси)цис - 5 - транс - 13 - простадиенамид, весом 113 мг. Спектр-ЯМР (CDCls) хроматографированного продукта показывал мультиплеты при 7,86-7,486 и 7,23-6,906 для тиофеновых протонов, мзльтиплет при 5,60-5,066 для винильных протонов, мультиплет при 4,72-4,436 для ОСНО, мУльтиплеты при 4,20-3,146 для СНгО и СНО и мультиплеты при 2,63-0,526 для остальных протонов. Пример 40. Раствор 121 мг (0,178 ммоль) быс-ТНР эфира .примера 39 2,0 мл смеси уксусной кислоты и воды (65 :35) нагревают до 40±2°С в течение 5 ч в атмосфере азота. Раствор концентрируют и полученное масло очищают с помощью колоночной хроматографии на силикагеле. После удаления примесей с более высоким Rf хлороформом, элюирование 3%-ным метанолом в метиленхлориде дает N-(2 - тиофенсульфонил)-9а, а, 15а-триокси - цис - 5 - транс - 13-простадиенамид в виде пены, весом 61 мг. Спектр-ЯМР (CDCla) продукта показывает мультиплеты при 7,84-7,486 и 7,10- 6,906 для тиофеновых протонов, перекрывающиеся мультиплеты при 5,60-5,106 для винильных протонов, мультиплет При 4,28- 3,756 для СНО, и мультиплеты при 2,57- 0,606 для остальных иротонов. Пример 41 (исходный продукт). К раствору 180 мг (0,265 ммоль) спирта примера 39 в 3 мл ацетона, охлажденному до - 5°С под азотом, добавляют 0,20 мл реактива Джонса. Смесь перемещивают на холоду 20 мин. Затем резко охлаждают на холоду добавлением 0,20 мл изопропанола. Смесь разбавляют этилацетатом, дважды промывают водой и насыщенным раствором, сущат безводным сульфатом магния и концентрируют, что дает маслянистый бесцветный (2-тиофенилсульфонил) - 9 кето Па, 15а-б«с - (тетрагидропиран) - 2илокси) - цис -5 - транс-13-простадиенамид, весом 159 мг (выход 88,3%). Пример 42. Раствор 159 мг б«с-ТНР эфира примера 41 в 3 мл смеси уксусной кислоты и воды (65:35) нагревают до 40+2°С в атмосфере азота 4,5 ч. Смесь затем концентрируют и полученный маслянистый продукт очищают с помощью колоночной хроматографии на силикагеле. После удаления примесей в более высоким Kf хлороформом элюирование 2%-ным метаполом в метиленхлориде дает целевой N-(2 - тиофенс льфонил) - 9 - кето - Па, 15а - диокси - 5 - цис - 13 -транс - простадиенамид в виде вязкого масла весом 72мг. Спектр-ЯМР (CDCls) продукта показывает мультиплеты при 7,90-7,556 и 7,16- 6,946 для тиофеновых протонов, мультиплет при 5,72-5,436 для граяс-двойной связи, мультиплет при 5,43-5,106 для иисдвойной связи, шипокий синглет ори 5,60- 4.756 для ОН и Н, мультиплет при 4,32- 3,816 для СНО и мультиплеты при 2,75- 0,636 для остальных протонов. Пример 43. Раствор 75 мг спиота N-метансульфонил - 9а-окси-11а, 15а-б«с(тетрагидропиоан - 2-илокси)-13-транс-простенамид в 1,0 мл смеси ледяной уксусной кислоты и воды перемешивают в атмосфере азота при комнатной температуре 20 ч. Затем концентрируют и перегоняют азеотропно с толуолом. Очистка неочищенного продукта с помощью хроматографии на силикагеле дает целевой N-метансульфонил9а, Па, 5а-триокси-13-гранс - простенамид. Пример 44 (исходный продукт). К охлажденному до -23°С в атмосфере азота раствору 0,218 г (0,371 ммоль) N-метансульфонил - 9а - окси - Па, 15а-бмс-(тетрагидропиран - 2 - илокси)-13-гранс-простенамида в 4,0 мл ацетона добавляют по каплям 0,163 мл (0,408 ммоль) реактива Джонса. Реакционную смесь перемещивают на холоду 15 мин, затем гасят добавлением 0,163 мл изопропилового спирта. Погащенную реакционную смесь перемещивают на холоду 5 мин, затем разбавляют этилацетатом. Органический раствор промывают водой, сущат безводным сульфатом магния и концентрируют, что дает целевой N-метансульфонил - 9 - кето-11 а, 15а-бис-(тетрагидропиран - 2 - илокси)-13-транс-простенамид. Пример 45. Гомогенный раствор 0,190 г неочищенного бнс-ТНР эфира примера 44 в 2,0 мл смеси ледяной уксусной кислоты и воды (65:36) перемещивают в атмосфере азота при комнатной температуре 12 ч, затем концентрируют азеотропно и перегоняют с толуолом. Очистка продукта с помощью хроматографии на силикагеле дает елевой N-метянсульфонил - 9 - кето-11а, 15а-диокси - 13 - транс-простенамид. Пример 46. К раствору 3,21 г (6,25 ммоль) (4-метансульфониламиНОкарбонилбутил) - трифенилфосфоний бромида в 5 мл диметилсульфоксида добавляют 6,0 мл (12,0 ммоль) 2,ОМ раствора метилсульфинилметнда натрия в диметилсульфоксиде. Полученный красный раствор илида перемешивают 10 мин, затем добавляют по каплям раствор 338мг (1,25ммоль) 2-Г2р-(За - окси - транс - 1 - октен - 1-ил)3,5 - дигидроксициклопент - 1а - ил -ацетальдегид, -нолуацеталь в 2,0 мл диметилсульфоксида.
Смесь перемешивают при комнатной температуре в атмосфере азота 4 ч, затем выливают в смесь этилацетата и льда с водой. Водный слой подкисляют 10%-ной соляной кислотой и экстрагируют этилацетатом. Объедкненные органические экстракты промывают водой и насыщенным раствором NaCl, -сушат безводным сульфатом магния и концентрируют. Очистка продукта с помошью хроматографии на силикагеле дает целевой Ы-метансульфонил-9а, Па, 15а-триокси - 5 - цис - 13-гранс-простадиенамид.
Пример 47. К раствору 3,01 г (6,25 ммоль) 4-(ацетиламинокарбонил)бутил -трифенилфосфоний бромида в 4 мл диметилсульфоксида добавляют 6,00 мл (12,0 ммоль) 2,ОМ раствора метилсульфинилметида натрия в диметилсульфоксиде. Полученный в результате красный раствор илида перемешивают 10 мин, затем по каплям добавляют раствор 338 мг (1,25 ммоль) - (За-окси - гранс-1-октен-1-ил)-За, 5а-дигидрооксициклопент - 1а - ил)-ацетальдегид, -нолуацеталь в 2,0 мл диметилсульфоксида. Смесь перемешивают -при комнатной температуре в атмосфере азота 4 ч, затем выливают в смесь этилацетата и ледяной воды. Водный слой подкисляют 10%-ной соляной кислотой и экстрагируют этилацетатом. Органические экстракты промывают водой -и насыш;енным раствором NaCl, сушат безводным сульфатом магния и концентрируют. Очистка продукта с помощью хроматографии На силикагеле дает целевой Ы-ацетил-9а, Па, 15а - триокси-5 цис - 13 - транс-простадиенамид.
Пример 48. К охлажденному льдом в атмосфере азота раствору 75 мг N-ацетил9-кето-Па, 15а - диокси-13 - транс-5 - циспростадиенамида в 1,5 мл метиленхлорида добавляют 350 мл пивалоилхлорида с последующим добавлением 450 мл триэтиламина. После перемешивания при комнатной температуре в течение 5 ч, смесь выливают ва смесь этилацетата и льда. Водный слой экстрагируют этилацетатом. Объединенные органические экстракты промывают 10%-НОЙ соляной кислотой, насыщенным бикарбонатом, водой, сушат безводным сульфатом магния и концентрируют. Очистка продукта с ПОМОЩЬЮ хроматографии дает целевой М-ацетил-9-кето-11а, 1Ба-бисливалоилокси - 5 - г{мс-13-гранс-простадиенамида.
Пример 49. К охлажденному льдом в атмосфере азота раствору 125 мг. N-метансульфонил - 9а, Па, 15а-триокси-5-г{ыс-13транс - простадиенамида в 2,5 мл метиленхлорида добавляют 0,50 мл бензоилхлорида с Последующим добавлением 0,625 мл триэтиламина. После перемешива«ия при комнатной температуре в течение 5 ч смесь выливают на смесь этилацетата и ледяной воды. Водный слой экстрагируют этилацетатом. Объединенные органические экстракты промывают 10%-ной соляной кислотой и водой, сушат безводным сульфатом магния и концентрируют. Очистка продукта с помощью хроматографии дает целевой К-метансульфонил-9а, Па, 15а-трибензоилокси - 5 - ц«с-13-тра«с-простадиенамид.
Пример 50. К раствору 91 мг (0,2 ммоль) N-метансульфонил - 9 - оксо-Па, 15а-дигидроокси-16, 16-диметил - цис - 5 - транс13-простадиенамида в 2 мл сухого тетрагидрофурана добавляют 58 мг (0,66 ммоль) ангидрида муравьиной кислотой и 70 мг (0,66 ммоль) 2,6-лютидина. Раствор перемешивают 4 ч в атмосфере азота при комнатной температуре, затем добавляют 36 мг (2,0 ммоль) воды. Смесь перемешивают при комнатной температуре в течение 1,0 ч, затем разбавляют этилацетатом. Разбавленный раствор промывают 0,1%-ной соляной кислотой, водой и насыщенным раствором NaCI, сушат безводным сульфатом магния и концентрируют. Очистка остатка с помощью хроматографии на силикагеле дает N-метансульфонил - 9 - кето - Па, 15а-быс - форм ил окси-16, 16-диметил-6-г{мс13-т/ анс-простадиенамид.
Пример 51. К раствору 2,73 г (5,0 ммоль) (4-бензоиламинокарбонил-€утил) - трифенилфосфонийбромида в 10 мл сухого диметилсульфоксида добавляют 2,22 мл (4,54 ммоль) 2,05М раствора метилсульфинилметида натрия в диметилсульфоксиде. К полученному красному раствору илида добавляют по каллям раствор 0,219 г (0,5 ммоль) 2-Г5а-окси-За-(тетрагидропиран-2 - илокси)-2|3-(Зр)-тетрагидропиран-2илокси-(транс - I - октен-1-ил) циклопент1г-ил -ацетальдегида, уполуацеталь в 1,0 мл сухого диметилсульфоксида. После перемешивания при комнатной температуре в атмосфере азота в течение 20 ч реакционную смесь выливают в ледяную воду. К водному раствору добавляют эфир и подкисляют до рН 3 добавлением 10%-ной соляной кислоты. Водную смесь трижды экстрагируют эфиром. Объединенные эфирные экстракты сушат безводным сульфатом магния и концентрируют, получая вязкое масло. Очистку продукта ведут с помощью хроматографии на силикагеле, что дает М-бензоил-9а - окси-Па, 5a-6uc - (тетрагидропиран - 2 - илокси)-1{ыс-5-гранс - 13простадиенамид.
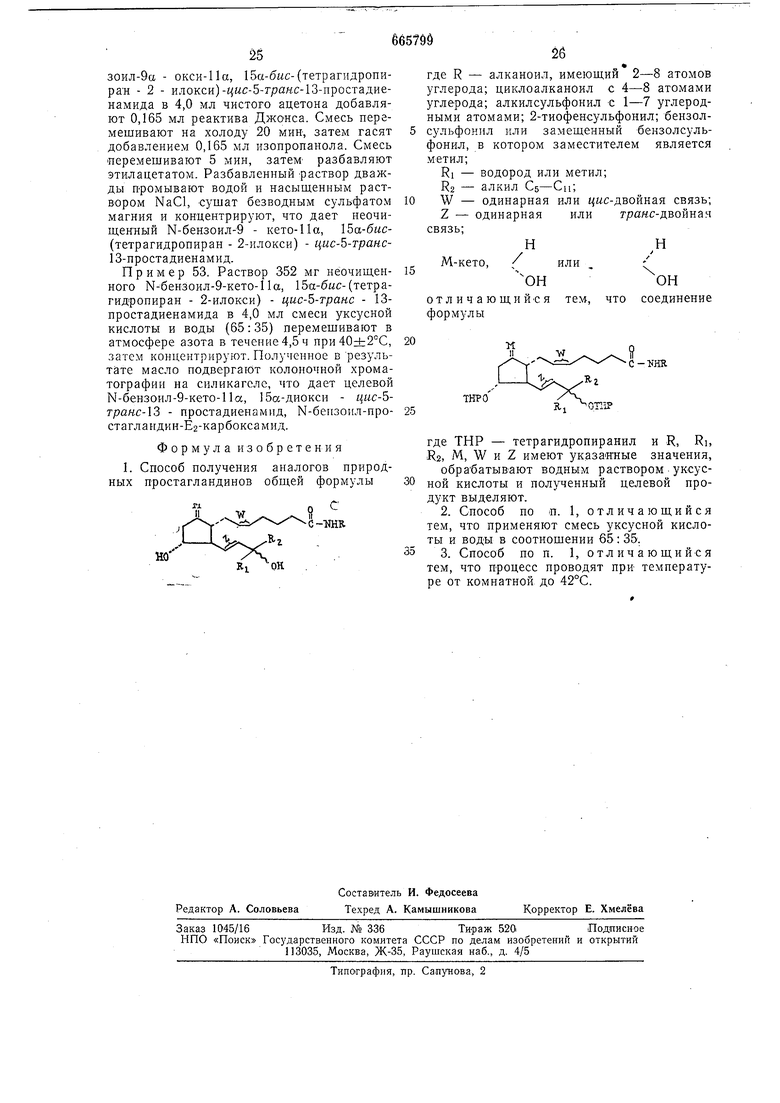
Пример 52. К охлажденному до в атмосАере азота;раствору 0,401 г Ы бензоил-9а - окси-11а, 15а-бмс-{тетрагидропиран - 2 - илокси)-цмс-5-гранс-13-простадиенамида в 4,0 мл чистого ацетона добавляют 0,165 мл реактива Джонса. Смесь перемещивают на холоду 20 мин-, затем гасят добавлением 0,165 мл изопроланола. Смесь перемешивают 5 мин, затем- разбавляют этилацетатом. Разбавленный -раствор дважды Промывают водой и насыщенным раствором NaCl, -сушат безводным сульфатом магния и концентрируют, что дает неочищенный М-бензоил-9 - кето-Па, 15а-б«с(тетрагидропиран - 2-илокси) - цис-5-транс13-простадиенамид. Пример 53. Раствор 352 мг неочищенного Н-бензоил-9-кето-11а, 15а-бис-(тетрагидропиран - 2-илокси) - цис-5-транс - 13простадиенамида в 4,0 мл смеси уксусной кислоты и воды (65:35) перемешивают в атмосфере азота в течение 4,5 ч при40±2°С, затем концентрируют. Полученное в результате масло подвергают колоночной хроматографии на силикагеле, что дает целевой Ы-бензоил-9-кето-11а, 5а-диокси - цис-6транс-13 - простадиенамид, N-бензоил-простаглаидин-Ег-карбоксамид. Формула изобретения 1. Способ получения аналогов природобщей формулы ных простагландинов где R - алканоил, имеющий 2-8 атомов углерода; циклоалканоил с 4-8 атомами углерода; алкилсульфонил -с 1-7 углеродными атомами; 2-тиофенсульфонил; бензолсульфонил или замещенный бензолсульфонил, в котором заместителем является метил; RI - водород или метил; R2 - алкил СБ-Си; W - одинарная или цис-двойная связь; или транс-двойная одинарная М-кето, / отличающийся соединение тем, что формулы где ТНР - тетрагидропиранил и R, Ri, R.2, М, W и Z имеют указанные значения, обрабатыв-ают водным раствором уксусной кислоты и полученный целевой продукт выделяют. 2.Способ по п. 1, отличающийся тем, что применяют смесь уксусной кислоты и воды в соотнощении 65: 35. 3.Способ по п. 1, отличающийся тем, что Процесс проводят при- температуре от комнатной до 42°С.











| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения аналогов природных простагландинов | 1974 |
|
SU522789A3 |
| Способ получения производных трифенилфосфина | 1974 |
|
SU523642A3 |
| Способ получения промежуточных соединений для получения простагландинов | 1975 |
|
SU645563A3 |
| Способ получения 15-замещенных простановых производных или их солей | 1973 |
|
SU644384A3 |
| Способ получения промежуточных соединений для синтеза простагландинов и их -эпимеров | 1976 |
|
SU640660A3 |
| Способ получения 2-дезкарбокси2-(тетразол-5-ил)-11-дезокси - -пентанорпростагландинов или их магниевых солей | 1976 |
|
SU638255A3 |
| Способ получения производных циклопентана | 1975 |
|
SU645564A3 |
| Способ получения 11-дезокси-16арилокси- -тетранорпростагландинов или их солей | 1976 |
|
SU679134A3 |
| Способ получения 11-дезокси- пентанорпростагландинов или их солей | 1976 |
|
SU613719A3 |
| Способ получения аналогов простаглан-диНОВ | 1978 |
|
SU831071A3 |


Авторы
Даты
1979-05-30—Публикация
1973-06-18—Подача