диглицидиловыми эфирами 1,1-быс-(оксиметил)-циклогексена-3 или тетрагидрофталсБЫХ кислот.
Циклоалифатические эпоксиимиды представляют собой твердые вещества с т. пл. 50-70° С, хорошо растворимые в обычных растворителях, что важно ири использовании их в качестве компонентов связуюо),их для армированных иластиков. Эти соедииения можно перерабатывать в полимеры без модифицируюидих добавок и активных разбавителей.
Полимеры, получаемые отверждением циклоалифатических эпоксиимидов формулы (II) ангидридными отвердителями, имеiiOT высокие теплостойкость и температуру начала деструкции, а также повышеиный предел ирочности ири растяжении.
Пример 1. Смесь 141 вес. ч. днгл ;цидилового эфира тетрагидрофталевой кислоты, 151 вес. ч. тетрагидрофталимида и 1,5 вес. ч. N,N-днмeтилбeнзилaмииa нагревают ири 130°С до полного исчезновения глицидных групп (2-3 ч.) После удаления в вакууме катализатора получают с практически количественным выходом триолефин с т. пл. 54° С, йодным числом 129,5% и содержанием гидроксильиых групп 5,64%. Для CsoHseOioN вычислено йодное число 130,2%, гидроксильиое число 5,82%. 292 вес. ч. 1,2-быс-(1-тетрагпдрофталимпдо-2-оксипроиил) - циклогексеи-3-карбоксилата растворяют в 1000 мл хлороформа, прибавляют 34,2 вес. ч. ацетата натрия и по каплям дозируют в течеиие 1 ч 342 вес. ч. 40%-ной надуксусной кислоты, иоддерживая температуру 33- 35° С. Реакционную массу выдерживают при этой температуре 3 ч, после чего отделяют органическую фазу и нейтрализуют ее безводным углекислым натрием. Выпавший осадок хлористого натрия отфильтровывают. После упаривания маточника и вакуумной сушки при 120° С/2 мм рт. ст. в течение 3 ( получают 276 вес. ч. (87%) светло-желтого твердого стеклообразного продукта, содержащего 16,4% эпоксидиых груии и 5,87% гпдроксильных.
После перекристаллизации образца полученного продукта из смеси петролейный эфир /этанол (2 : 1) выделяют 1,2-бас- 1(3,4-эиоксигексагидрофталимидо) - 2-оксипропил -4,5-эпоксициклогексаи - карбоксилат (продукт I) с т. пл. 67° С.
Найдено, %: эпоксидные группы 19,63; гидроксильиые группы 5,16; С 56,81; Н 5,48; N4,12.
С:;,оНзб01з 2.
Вычислено, %: эпоксидиые группы 19,93- гидроксильные группы 5,38; С 56,96; И 5,74; N 4,43.
Пример 2. Смесь 148 вес. ч. диглицидилового эфира (3(4)-метилтетрагидрофталевой кислоты, 165 вес. ч. 3(4)-метилтетрагидрофталимида и 1,6 вес. ч. триэтиламина нагревают при 100-110° С до исчезновения глицидных групп (2-3 ч). После удаления катализатора получают 313 вес. ч. светложелтого вязкого некри5 сталлизующегося продукта с иодиым числом 120,77% и содержанием гидроксильных групи 5,27%. Для СззН42О1оК2 вычислено: йодное число 121,5% и гидроксильное число 5,43%. Эпоксидироваиие полученного
триолефина в условиях примера 1 приводит к триэиоксиду (светло-желтое твердое стеклообразное вещество) с 85-90%-ным выходом п содержащего 15,26% эпоксидных и 5,72%, гидроксильных . После перекристаллизации из смеси иетролейный эфир/ этанол (2:1) получают 1,2-бас- 1-(3(4)-метил-4,5-эиоксигексагидрофталимидо)-2-оксипропил -3(4) -метил - 4,5 - эпоксициклогексанкарбоксилат с т. пл. 52° С (продукт 2).
Найдено, %: эпоксидные группы 18,38; гидроксильные группы 5,17; С 58,45; Н 6,34; N 3,97.
СззН42О1зМ2
Вычислено, %: эпоксидные группы
18,69: гидроксильные группы 5,04; С 58,75; Н 6,27; N 4,15.
Пример 3. Смесь 127 вес. ч. диглицидилового эфира 1,1-бис(оксиметил)-циклогексеиа-3 151 вес. ч. тетрагидрофталимида к 1,4 вес. ч. М,М-диметилбензиламина нагревают при 130° С до исчезновения глицидиых групи (2-3 (). После удалепия катализатора получают 278 вес. ч. светло-желтого вязкого иродукта, кристаллизующегося ио5 еле длительного стояния при комиатной температуре. Т. ил. 37° С, йодное число -Ь 136,2%, гидроксильное число 5,90%. Для C3oH4oO8N2 вычислеио, %: йодное число 136,79; гидроксильиое число 6,11. При
0 эпоксидировании полученного -l-6uc-(тетрагидрофталимидо-2 - оксипропил) оксиметилциклогексена - 3 в Зсловиях иримера 1 иолучают твердый стеклообразный иродукт с 90-95%-ным выходом. Содержание %: эпоксидных групп 16,73; гидроксильных групп 6,34. После перекристаллизации из метанола получают 1,1-б«с- 1-(3,4 - эпоксигексагидрофталимидо)-2-оксипропил - оксиметил-3,4 - эиокси0 циклогексана (иродукт 3) с т. пл. 49° С. Найдено, %: эпоксидные группы 20,64; гидрокспльные группы 5,78; С 59,12; Н 6,50; N 4,42.
C3oH4oOjiN2
5 Вычислеио, %: эпоксидные группы 20.86: гпдроксильные группы 5,63: С 59,59; Н 6.67: N 4.63.
Пример 4. Из 127 вес. ч. диглицидилового зфпоа 1,1-бнс (о1ссимегпл)-циклогек0 сспа-3, 165 вес. ч. 3(4)-метилтетрагидрофталимида и 1,5 вес. ч. триэтиламина в услоц1:я. примера 2, получают 292 вес. ч. трио.чсфпна, светло-желтого вязкого иекристаллизующегося и иеперегоняющегося
5 иродукта с йодным число 128,70% и со5
держащего 5,44% гидроксильиых rpynii. Для C,J2H4408N2 вычислено, %: полное число 130,2, гиароксильное число 5,82. Эпоксидирование полученного трполефнна в условиях примера 1 приводит к триэпоксиду с 85-90%-ным выходом. Содержание, %: эпоксидных групп 16,37, гидроксильных групп 5,94. После перекристаллизации из метанола получают l,l-6iic i (3,4)-мeтил-4,5-эпoкcиreкcaгидpoфтaлимндo)-2 - оксппропил - окспметил-3,4-эпоксициклогексан (продукт 4) с т. пл.44° С. Найдеио, %: эпскспдные группы 19,53; гидроксильные группы 5,56; С 60,21; Н 7,17; N 4,25.
C32H«O,,N2
Вычислено, %: эпоксидные группы 19,23; гпдроксильиые группы 5,38; С 60,75; Н 7,01; N 4,43.
Строение полученных соединений подтверждается анализом их ИК-спектров, которые характеризуются следующими полосами иоглощения: 795 - асимметрические валентные колебания эпоксидного цикла при циклогексановом кольце, 3450 c. - валентные колебанпя ОНгруппы, 1723 и 1780 с.и- - характеристические частоты С О имидного цпкла, 1720-1760 см - поглощение группы С О в сложноэфирной группе (для соедпнений, описанных в примерах 1 и 2), 1000- 1300 - рЯ|Д иолос, характеризующих простую эфирную связь (для соединений, описанных в примерах 3 и 4).
П р и м е р 5. 100 вес. ч. иродукта 1 (см. пример 1) нагревают до 70-80° С, смещ кают с 37,4 вес. ч. расплавленного малеиliCBoro (.VIA) или 63,3 вес. ч. г/зо-метилтстра г :дрофталевого ангидрида (изоМТГФА). Приготовленные композиции заливают в металлические формы и отверждают по режиму: 100° С - до желатинизацип, 140° С - 2 ч, 180° С - 2 ч, 200° С- 12 /.
Пример 6. 100 вес. ч. иродукта 3 (см. пример 3) иагревают до 60-80° С, смешивают с 38,1 вес. ч. рас1:лавлеиио1-о малеииового пли 64,5 вес. ч. «зо-метилтетрагидрофталевого ангидрида и отверждают в условиях примера 5.
Пример 7. 70 вес. ч. продукта 1 или 3 и 30 вес. ч. анилино-феиоло-формальдегидной смолы растворяют в сппртово-ацетоновой смеси (до получения 60-70%-ного ;аствора). Приготовленным раствором пропитывают стеклоткань Т-10-80 и высущипают от растворителя при комиатной тсмпературе 24 (.
Полученный «преирег складывают в пакет и прессуют при удельном давлении 5 по режиму; 140° С - 10 ч., 160° С - 2 (, 180° С - 2 ч, 200° С - 8 /.
Свойства полимеров, полученных при отверждении малеиновым ангидридом соедииений формулы (II) и известных соединений формулы (I) представлены в таблице.
Т а о л 1 ц п
Известны ;
продукт
+ 


| название | год | авторы | номер документа |
|---|---|---|---|
| Бис-(эпоксигексагидрофталимидо)феноксипропанолы-мономеры для термостойких полимеров | 1975 |
|
SU548601A1 |
| Способ получения эпоксидныхолигомеров | 1974 |
|
SU509243A3 |
| Способ получения бромсодержащей эпоксидной композиции | 1980 |
|
SU952917A1 |
| Способ получения глицидных эфиров спиртов | 1979 |
|
SU878767A1 |
| Полимерная композиция | 1977 |
|
SU690044A1 |
| Эпоксидная композиция | 1977 |
|
SU703551A1 |
| 3,4-Эпоксигексагидробензил-/4,5эпоксигексагидро- -фталимидо/ бензоат как мономер для синтеза теплостойких полимеров | 1976 |
|
SU702021A1 |
| -(2",3"-Эпоксипропилоксифенил)-4,5 эпоксигексагидрофталимиды, как мономеры для получения термостойких полимерных материалов | 1974 |
|
SU513033A1 |
| Эпоксидная композиция | 1974 |
|
SU578897A3 |
| Глицидиловые эфиры полиол-3,4эпоксигексагидрофталатов | 1974 |
|
SU522201A1 |

185 210
12СО
1700
500
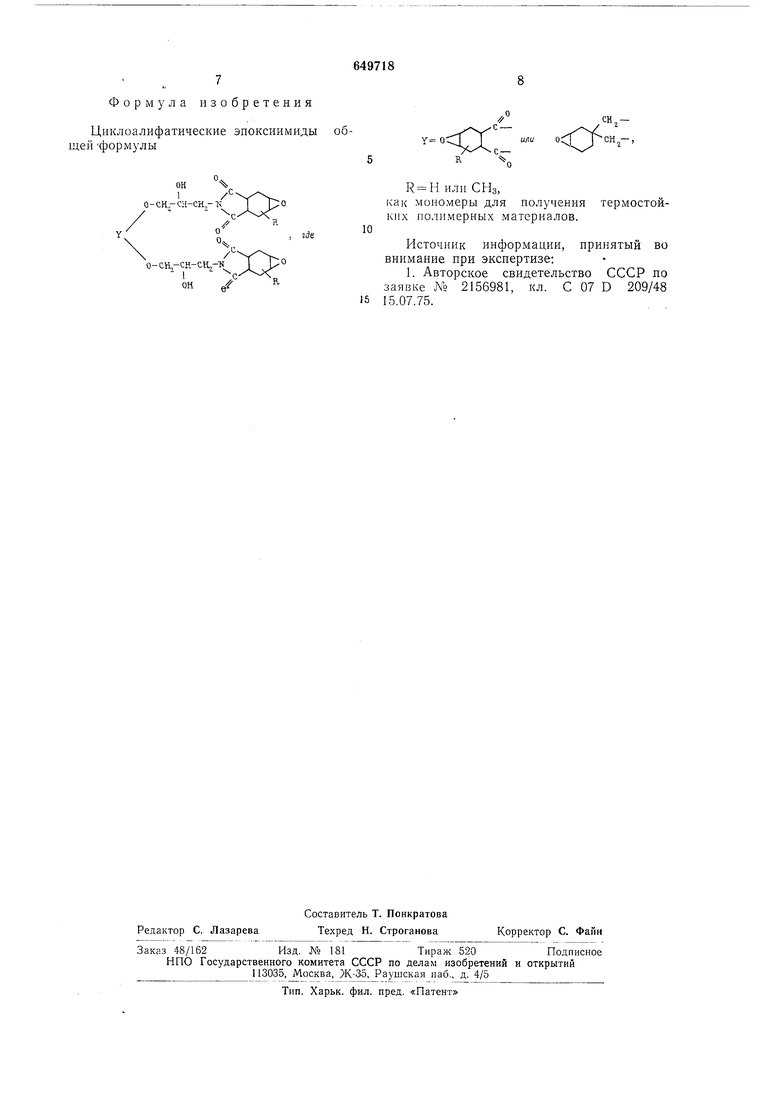
233 Формула изобретения Циклоалифатические эпоксиимиды об- i-формулы f )с.. о-сн„-сн-сн,-гч j €- N1 j, 10 Ч.„ сн-си-™-/Y ° - l ---j,x4x: ок / 5 15 //.сн. н - К НилиСНз, как мономеры для получения термостойких полимерных матевиалов. ких полимерных материалов, Источник информации, принятый во внимание при экспертизе: 1. Авторское свидетельство СССР по заявке N° 2156981, кл. С 07 D 209/48 15.07.75.
Авторы
Даты
1979-02-28—Публикация
1976-09-10—Подача