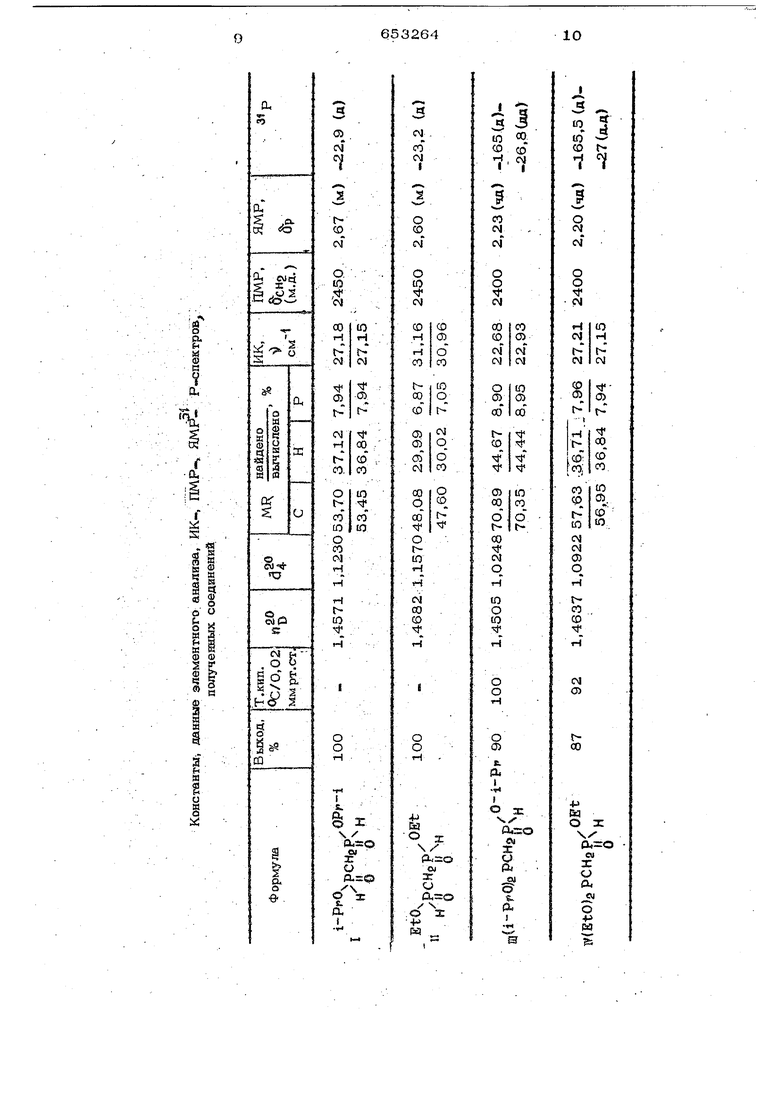
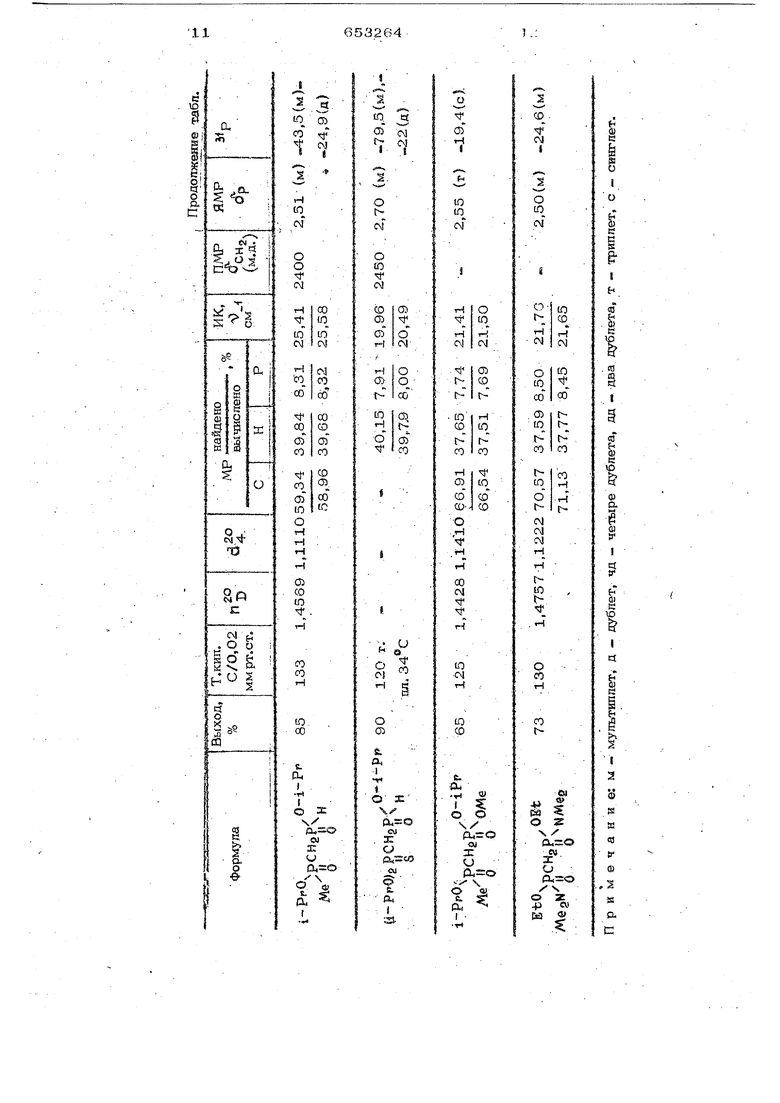
Поставленная цель достигается описываемым способом получения неполных эфиров фосфорзамещенной мегнлфосфонистой кислоты формулы (1 ), который заключается в том, что полный эфир фосфорзамешейной метипфосфонистой кислоты подвергают взаимодействию с водой или хлористым водородом в среде инертного органи еского растворителя при охлаждении до тем пературы от минус 70 до в атмосфере HHeftTHoro газа.,: В качестве растворителя могут быть использованы, например, эфир, диметокси этан и другие. Исходные соединения - полные эфиры фосфорзамещенной метилфосфонистой кис- лоты - легкодоступные соединения, которые могут быть получены с высоким выходом из тетрахлорметилендифосфина. Целевые продукты представляют собой устойчивые бесцветные жидкости или белые кристаллы. Строение и состав полу чемных соединений подтверждены данными эйаментного анализа, ИК-, ПМ1Р- и ЯМР Р-ч;пектроскопией, а также химичес кйШ йреврашениями - реакцией Тодда-Ат тертЬна со спиртом и-амином, которая приводит к смешанным эфирам или эфироамийам метилендифосфоно,вой кислоты. Неамотря на кажущуюся аналогию с из ВёСТ1п.1ми способами получения соединений одной гйДрофосфорильной группой в молекуле получить целевые продукты (неполные эфиры фосфорзамещенной метилфосфонистой кислоты) известными способами не удаетсй. Это связано с большей реаквшжной спрсобйострью по отношению к гид ррййзуюЩим реагентам как исходных соединений, так и целевых продуктов, по сравнению с соединениями, содерх ащими одну гидрофосфорильную группу в молекуле. И оэтомУ в. жестких условиях, характерных для известных способов получения неполных эфиров фосфонистых кислот, целе1эые продукты быстро разлйгйются с получением смеси фосфорсодержащих соединений, в том числе полимеров. Предлагаемый способ получения неполных эфиров фосфорзамещенной метилфосфонисгой кислоты отличается мягкими усло ВИЯМИ (разбв1вление, пониженная температура, отсутствие избытка гидролизующего реагента), что обеспечивает получение соединений нового типа с колйчественны:МИ ИЛИ ВЬЮОКИМЙ ЬЫХОДвМЙ, Все реакции проводят в атмосфере инертного газа (сухого аргона) в абсолютных растворителях. Пример 1, Диизоаропиловый эфир метилендифосфонистой кислоты ( 1 ). В раствор 19 г (0,061 моля) тетраизопропилового эфира метилеидифосфонистой кислоты в 150 мл эфира, охлажденный до , медленна барботируют в токе сухого аргона сухой хлористый водород, полученный из 7 г (0,13 моля) хлористого аммония и избытка серной кислоты. Затем смесь доводят до комнатной температуры, растворитель отгоняют, следы растворителя удаляют в вакууме 0,5мм рт.сг. Получают 14 г (100%) соедине ния (I ). п| 1,4571; df 1,1230; MRHanfl 53,70; 53,43. Найдено, %:С 37,12; И 7,94; Р 27,18. Вычислено, %: С 36,84; Н 7,94; Р 27,15.. . ИК-спектр: Dp 2450 см , ПМРспектр: дсна - 2,67 мульгиплет.. ЯМР Р-спекТ|р: рн -22,9 м.д. дублег, Гц. Аналогично получают диэтиловый эфир метилендифосфонистой кислоты (II), константы которого приведены в таблице. Пример 2, Триизопропиловый эфир метилендифосфонистой кислоты (HI). К раствору 10 г (0,032 мола) тетраизопропилового эфира метилендифосфонистой кислоты в 100 мл диметоксиэтана, охшлсденному до -4О С, при перемешива-, НИИ медленно добавляют 0,58 г воды в 20 мл диметоксиэтана. Затем смесь доводит до комнатной температуры и оставляют на сутки. Растворитель отгоняют, остаток перегоняют в вакууме. Получают 7,8 г (90%) соединения (Ш). Т. кип. ,О2 мм pT.ct.; of 1,4505; &4 1.0248. 70.89; MRabw 70,35,; Найдено, %: С 44,67; Н 8,9О; Р 22;68. Вычислено, %: С 44,44; И 8,95; Р 22,93. , ИК-спектр )рн 2400 см , ПМРспектр: ficHg 2,23 м.д. четыре дублета, JpUHICH« 6 Гц, ;:(v) Гц,3нрсм 2 Гц, ЯМР- Р-спектр: dj)(iiJ| -165 м.д. дублет,3рср - 40 Гц, Jpty; -26,8 м.д. два дублета, Зрср 40 Гц.Зри - 555 Гц. Аналогично получают триэтиловый эфир метилендифосфонистой кислоты (IV), константы которого приведены втаблице. Пример 3. Ия тфопиловый эфир (метилизопропоксифосфиноксидо) метилфос- фойистой кислоты (у ). К раствору 14,2 г (О,О5 моля) диизрпропилового эфира (метилнзопропоксифосфнноксидо)метилфосфонистой кислоты в 50 мл диме1;оксиэтана добавляют при ох лаждении до ОС 0,9 г {0,05 моля) во ды в 20 мл диметоксиэгана и оставляю на сутки. Затем-растворитель отгоняют, остаток перегоняют в вакууме. Получаю 10,3 г (85%) соединения (V). Т.кип. С/0,02 мм PT.CT.I 1,4569; 64 1,1110. 59,34;МНвыч 58,96. Найдено, %: С 39,84; Н 8,31; Р 25,41, Вычислено, %: С 39,68; Н- 8,32; Р 25,58. ИК-спектр н 2400 см , .IIMP . спектр:5сн2 2,51 м,д. мультиплеК ЯМР- F -спектр , -Д(широкий сигнал)),9 м.д. дублет, JpH 575 Гц.. Аналогично получают изопропиловый эфир (диизопропоксифосфин ги.орксидо)ме тилфосфонистой кислоты (VI), константы которого приведены в таблице. П Р и м ер 4. Симметричный диме тилдиизопропилметилендифосфонат (Ш). К раствору 14 г (0,061 моля) дииз пропилового эфира метилендифосфонистой кислоты ( I ) в 150 мл эфира, охлажден ному до , медленно, при перемеши вании добавляют раствор 4 г (О,1 мрлн метилового спирта, 18,8 г (0,12 мола) четыреххлористого углерода, 12,3 г (о,12моля)триэтиламинав 50 мл эфира. Затем смесь при перемешивании доводят до комнатной температуры и оставляют на .12 ч. Добавляю-р 100 мл гексана, ос док фильтруют, растворитель отгоняют, о таток перегоняют в вакууме. Получают 11,5 г (65%) соединения (Vli). Т.кип. 125°С/0,01 мм рт.ст.; n|f 1,4428; а 1,1410; МКнаид 66,91; ШЧ -66,54. Найдено, %: С 37,65; Н 7,74; Р21,41, Вычислено, %: С 37,51; Н 7,69; Р 21,50. ПМР-ч;пектр: «Зсна 2,55 триплет,3рсн 20 Гц, -19,4 м.д. синглет. Аналогично получают симметричный те раметилдиамидодиэтилметилендифосфонат (), контакты которого приведены в та лице. Пример 5. Диэтиловый эфир ме тилендифосфонистой кислоты (Ц). К раствору 25,6 г (0,1 моля) тетра этилового эфира метиленяифосфонистой кислотыв 200 мл диметоксиэтана, охпажденному до -30 С, при перемешива6532646
НИИ медленно добавляют 3,6 г (0,2 моля) ВОДЫ В 50 мл диметоксиэтана. Затем смесь доводягг до комнатной темпера туры и оставляютна сутки. Растворитель отгоняют, следы растворителя удаляют в вакууме 0,5 мм рт.ст. Получают 20 г (100%) соединени:я П. П,,4682; 1,1570. МНнайд 48,08; MRstoW 47,60. Найдено, %; С 29,99; Н 6,87; Р 31,16. Вычислено, %: С 3О,02; .Н 7,05; Р 30,96. ЙК- :пектр cvf, ПМРспектр: .д. мультиплет, ЯМР З Р спектр: 5р 23,2 м.д. дублет, :7рн 570 Гц. Аналогично получают диизопропиловый эфир метилендифосфонистой кислоты ( I ). П Р и м е Р 6. Триэтилов ь1й эфир мв« тилендифосфонистой кислоты (ГУ). В раствор 12,8 г (0,05 моля) тетраэмл-ового эфира метилендифосфонистой кислоты в 200 мл эфира, охлажденный до -70 С, медленно барботируют в токе сухого аргона хлористый водород, полученный из 2,7 г (О,О5 моля) хлорис- . того аммония и избытка серной кислоты. Затем смесь доводят до комнатной темпе ратуры, растворитель отгоняют, остаток перегоняют в; вакууме. Получают 9,9 г (87%) соединения IV. Т.кип. ,02 мм рт.ст.; 1, c3f 1,0922. МКнайд 57,63; МНвыч 56,95. Найдено, %: С 36,71; Н 7,96, Р 27,21. Вычислено, %: С 36,84; Н 7,94; Р 27,15. ИК-спектр: 9ри 2400 см. ПМР-спектр: ,2O м.д. четыре дублета, Эршисн б Гц. 3piy)CH 17 Гц, Зцрсн 2 Гц, ЯМР-3 Р-спекгр: §p«fif-165.5 м.д. дублет, Зрср-40 Гц,б|яу) м.д. два ублета, Гц, Эри 56О Гц. Аналогично получают триизопропиловыё эфир метилендифосфонистой кислоты 0И). Пример 6. Изопропиловый зфнр (диизопропоксифс сфинтиооксидо)метилфос« онистой кислоты (ч ) в раствор 34,4 г (0,1 моля) Д1шзо ропилового эфира (диизопропоксифосфин«° гиооксидо)метилфосфонистой. кислоты в 00 мл эфира, охлаждают до -7О®С, меденно барботируют в токе сухого аргона ухой хлористый водород, полученный нз ,4 г хлористого аммония и избытка сер ой кислоты. Затем смесь доводят до ком- 7 6532 напРйбй темпераг5фы Растворитель ОТГОНИ ют, остаток перегоняют в вакууме. Получают . г (90%) (1 ). Т.кйп, 120 /OjO2 мм рт.ст., т.пл, Найдено. %: С 40Д5; Н 7,91;S Р 19,69. Вычислено, %: С 39,79; Н 8, Р 20,49. ЙК -спектр: рн 2450 , 648 ПМР - спектр: ficHg 2,70 м.д. мультштлет, ЯМР- Р-спектр: ,5 м.д. мультиплет, dVo)r-2S,O м.д. дублет, Эрм / 575 Гц. Аналогично получают изопропиловый эфир (мегилизопропоксифосфиноксидо)ме гияфосфонистой кислоты ( V ).
Формула изобретения
Способ получения Henonifbfx эфиров фосфорзамешенной мегилфосфонисгой кислоты обшей формулы;
§V
где R низший алкил,
ЛЦйО)вР-, j)P-,
ОН
(ROjgP-11 группа,
.,-. ,
заключающийся в том, что полный эфир
фосфорзамё ценной метилфосфопнсгой кислоты подвергают взаимодействию с водой или хлористым водородом в среде инертвочго органического растворителя прв охлаждении до температуры от -70 до 0 в атмосфере инертного газа.
Источники информации, принятые во внимание при экспертизе
1.Пурдела Д., Вылчану Р. Химия ор ганических соединений , М., Хвмия. 1972, с. 181-183.
2.Лупенко И. Ф. и др. О производных карбалк1жсиметилфосфонистых кислот, ЖОХ, 1967, 37. с. 1330-1332.




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения замещенных виниловых эфиров кислот трехвалентного фосфора | 1977 |
|
SU687078A1 |
| Способ получения фосфорзамещенных метилфосфинатов | 1976 |
|
SU653261A1 |
| Способ получения элементзамещенных фосфэтиленов | 1980 |
|
SU910639A1 |
| Способ получения фосфорилированных полуацеталей полуаминалей кетена | 1989 |
|
SU1682358A1 |
| Способ получения -фосфор /ш/ замещенных кетонов | 1977 |
|
SU697520A1 |
| Способ получения дифосфор (у) замещенных фосфинов или их бис-аналогов | 1980 |
|
SU910645A1 |
| Способ получения ди-( -алкоксивиниловых) эфиров кислот пятивалентного фосфора | 1976 |
|
SU586176A1 |
| 4-ТРИМЕТИЛСИЛОКСИМЕТИЛФОСФИНИЛ-2-ТРИМЕТИЛСИЛОКСИ -2- ЦИАНОБУТИРОНИТРИЛ В КАЧЕСТВЕ ПОЛУПРОДУКТА СИНТЕЗА 4-МЕТИЛГИДРОКСИФОСФИНИЛ-2-АМИНОБУТАНОВОЙ КИСЛОТЫ, ОБЛАДАЮЩЕЙ ГЕРБИЦИДНОЙ АКТИВНОСТЬЮ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1992 |
|
RU2054430C1 |
| Способ получения дигалогенангидридов 2-алкоксиалкенилфосфонистых кислот | 1982 |
|
SU1033498A1 |
| Способ получения 2,6-диэтинилпиперазинов | 1973 |
|
SU492518A1 |


Авторы
Даты
1979-03-25—Публикация
1977-01-18—Подача