Изобретение относится к получению новых производных халькона, обладающих фармакологической активностью.
Известны некоторые производные халькона, обладающие фармакологической активностью против язвы желудка.
Так, известен 2,2,4 ,4-тeтpaoкcи-6-мeтoкcи-3- (5-метил-2-изопропенилгекс-4-енил)-халькон.
Однако данное соединение получают экстракцией из растительного сырья с низким выходом и невысокой чистотой по сложной методике.
Целью изобретения является получение новых производных халькона, обладающих более высокой активностью против язвы желудка наряду с низкой токсичностью, npocTfcavi и удобным для промышленного осуществления способом основанным на известной реакции конденсации замещенного ацетофенона с замещенным бензальдегидом в щелочных или кислых условиях.
Способ получения новых производных халькона общей формулы
г,. /гК ,KI
где R,- 4 водород, оксигруппа, низшие алкил, алкокси, ацилоксигруппы; Z - 2„- группа общей формулы
СКз -0-Г СНг-Сн С-СИгД5 31
где п 1 или 2, или группа формулы
-бНг-(1Н й-ЙНэ ЙНз
заключается в том, что соединение общей формулы
СоСн,
Ш)
где RJ 2 имеют вышеуказанные значения, конденсируют с соединением общей формулы
IL
ОНИ
30 где R, R 2 и Z - как указано вьдце, в среде органического растворителя в ггрнсутствии щелочи или минеральной кислоты гфи О-ЮО С. Ко)денса11,ию можно проводить путем добавления щелочи, такой, как гидроокись натрия и гидроокись калия, или кислоты, такой, как соляиая и серЕ1ая кислота, к раствору или суспензии ис хоянь х веществ в органическом растворителе, таком,, как метанол, этанол и этилацетат, и перемешивания полученной смеси при в- течение нескольких часов или нескольких дней Полученные конденсаты отделяют от .маточной жидкости и очищают, если необходимор при помощи перегонки, п рекристаллизации или хроматографии. Полученные соединения обладают активностью против различных видов язвы желудка, а именно уксуснокислой язвы, аналогичной хронической язве желудка, стрессовой язвы Шея язв, вызванных в.ведением лекарств, напри.мер аспирина, стероидов и других противовоспалительных и жаропонижающих препаратов. Целевые соединения превосходно предотвращают и вылечивают различны виды экспериментальных язв желудка у крыс: лечение хронических язв желудка (уксуснокислая язва при инъек циях уксусной кислоты) ускоряется, развитие язв и эрозий (язва Шея при перевязывании пилоруса, стрессовая язва при сдавливании или опускании животных Б воду, аспириновая язва . при введении аспирина) задерживаетс При введении патентуемых соединений не наблюдается нежелательного побоч ного действий на центральную и веге тативную нервную систему. Токсичность настоящих соединений чрезвычайно мала и при введении 5 г/кг Орально или 2 г/кг внутрибрю шинно и крысам не наблюдается смертных случаев в течение 96 ч, по этому соединения можно вводить без опасений в течение длительного времени, не наблюдая никакого побочног действия. Пример 1. К суспензии 218 мг 4 (3-метил-2 бутенилокс1г)-ац тофенона и 200 мг 4(3-метил-2-бутенилокси) --бензальдегида в 8 мл эта нола добавляют 3 мл 50%-иого .раство ра гидроокиси калия, перемешивают 1ч при комнатной температуре, подкисляют разбавленной соляной кислотой, растворитель выпаривают, остат экстрагируют 3 х 30 глп эфира, экстракт про14ывают водой и сушат 6езвод ным сульфатом натрия. После выпаривания эфира остаток перегоняют под /вакуумом и получают 333 мг 4,4-6ис- - (3-метил--2-бутенилокси) -хапькона, т,кип, 99-102 С/0,08 шл; т.пл, 95Вычислено, %: С 79,75 г И 7,50, С. f,C Най.аено, %: С 79,77.; Н 7,48. 4 Пример 2. К раствору 3 г салицилового альдегида в 20 м.п ацетона добавляют 4,1 г карбоната калия и 4,9 г З-метил-2-бутенилбромида, перемешивают 2 ч при комнатной температуре и получают 3,5 г 2-(3-метил-2 бутенилокси) -.бензальдегида. К раствору 3,3 г п-(З-метил-2-бутенилокси)-ацетофенона и 3,0 г полученного 2-{З-метил-2-бутенилокси)-бензальдегида в 5 мл этанола добавляют 30 мл 50%-ноГо раствора гидроокиси калия, перемешивают 3 ч при комнатной температуре, добавляют 200 мл воды, подкисляют соляной кислотой и экстрагируют эфиром. Экстракт перегоняют под вакуумом и выделяют 3,6 г 2 ,4-бис-(З-метил-2-бутенилокси)-халькона, т.кип. lOB-llO C/ /О,1 мм; т.пл. , Вычислено, %: С 79,75; Н 7,50. О 3 . Р айдено, %: С 79,35; Н 7,49. Пример 3. К раствору 3,3 г п-(З-метил-2-бутенилокси)-ацетофенона и 3,0 г м-(З-метил-2-бутенилокси)-бензальдегида в 5 мл этанола добавляют 30 мл 50%-ного раствора гидроокиси калия и перемешивают 3 ч при комнатной температуре. После добавления воды реакционную смесь подкисляют соляной кислотой и экстрагируют эфиром. Экстракт перегоняют под вакуумом.и получают 3,1 г 3,4-бис-(З-метял-2-бутенилокси)-халькона, т. кип, 111-11 а С/0,1 мм. Пример 4. К суспензии 260 мг 2-ОКСИ-4-(3-мeтил-2-бyтeнилoкcи) -ацетофенона и 219 мг 4-(3-метил 2 6утенклокси)-бензальдегида 3 8 мл этанола добавляют 3 мл 50%ного раствора гидроокиси калия и перемешивают 1 ч при комнатной температуре. Реакционную смесь подкисляют соляной кислотой, растворитель выпаривают, остаток экстрагируют 3x30 мл эфира, экстракт промывают водой и сушат безводным сульфатом нат- рия« После выпаривания эфира остаток перегоняют под вакуумом и получают 390 мг 2-ок:си-4,4-бис-(З-метил-2-бутенилокси)-халькона, т.кип, 109- -114С/0,1 мм; т.пл. 87-88,5°С. Вычислено, %; С 76,50; Н 7,19. Со- Н-д О Найдено; %: С 76,94; Н 7,12, Пример 5. К раствору 130 мг 2-метокси-4-(З-метил-2-бутенилокси)-ацетофенона и Г20 мг п-(З-метил-2 бутенилокси)-бензальдегида в 2 мл этанола добавляют 3 мл 50%-ного раствора гидроокиси калия и с-перемешивают 1 ч при комнатной температуре. Реакционную смесь подкисляют разбавленной соляной кислотой, растворитель вьатаривают, остаток экстрагируют эфиром, экстракт промывают водой и суш.ат безводным сульфатом натрий. После удаления эфира остаток перегоняют под вакуумом и вьщеляют 130 мг 2-метокси-4,(3-метил-2-бутенилокси)-халькона, г,кип. 117-119 С/О,09 мм. Пример 6.К раствору 418 м 4-окси-З- (3--метил-2.-бутенил) -ацетофенона и 390 мг 4-(З-метил-2-бутенилокси)-бензальдегида в 2 мл этано ла добавляют 20 мл 50%-ного раствора гидроокиси калия, перемешивают 3 ч при комнатной температуре, добавлжот воду, подкисляют до рН 2 разбавленной соляной кислотой и экстрагируют эфиром. Растворитель выпаривают, остаток пропускают чере колонку с силикагелем, элюируя смесью ацетон-гексан, и получают 310 м бесцветного порошка 4-окси-З-(3-метил-2-бутенил)-4-(З-метил-2-бутенил окси,)-халькона, т.пл. 145-147 С. Приме р 7. К суспензии 440 мг 2,4-диокси-З-(3-метил-2 буте нил)-ацетофенона и 380 мг п-(3-метил-2-бутенилокси)-бензальдегида в 2 мл этанола добавляют 8 мл 40%-пог раствора гидроокиси калия, перемеши вают 72 ч при комнатной температуре добавляют воду, подкисляют до рН 2 разбавленной соляной кислотой и экстрагируют эфиром. Растворитель выпаривают и остаток пропускают через колонку с силикагелем, элюируя бензолом, и получают 95 мг желтых иголок 24-диокси 3-(З-метил-2-бутенил)-4-{З-метил-2-бутенилокси)167-168,. -халькона, т.п: С 76,50; Н 7,19. Вычислено, %. Найдено, %: С 76,53; Н 7,17. Пример 8. К суспензии 660 мг 2,4-ДИОКСИ-5-(З-метил-2-буте нил)-ацетофенона и 571 мг п-(3-метил-2-бутенилокси)-бензальдегида в 3 мл этанола прибавляют 12 мл 40%-н го раствора гидроокиси калия, перемешивают 1 ч при 6 Ос, поступают далее, как в примере 7, и получают 280 мг оранжевых иголок 24-диокси-5- {З-мэтил-2-бутенил) (З-метил-2 -бутенилокси)-халькона, т.пл. 145- 146°С. Пример 9. Раствор 9,9 г 2,4-диацетокси 3-(З-метил-2-бутенил -ацетофенона и 9,6 г 2-метил-4-(3метил-2-бутенилокси)-бензальдегида 160 мл безводного этилацетата насыщают хлористым водородом при 0 С и перемешивают при комнатной температ ре в течение 12 ч. Затем растворите выпаривают на водяной бане. После охлаждения остаток растворяют в эфи и эфирный раствор промывают водой и сушат безводным сульфатом натрия, з тем эфир выпаривают. Остаток загружают в колонку с силикагелем и элюи руют смесью ацетон-гексан, получая 2,1 г 2, 4-диацетокси-2-метил-3-( 3-метил-2-бутен1и1) -4-(З-мепгд-З-бутенияоксн)-халькона, т.кип. 13013зс/о,ое мм. Пример 10, к раствору 3,1 г 2-окси-- (З-метил-2-бутенилокси) -ацетофенона и 3,2 г 4-метокси-З(З-метил-2-бутенил)-бензальдегида в 6 мл этанола добавляют 30 мл 50%-ного раствора гидроокиси калия и перемешивают 3 ч при комнатной температуре/ прдкисляют разбавленной соляной кислотой, растворитель выпаривают, остаток экстрагируют эфиром, экстракт промывают водой и сушат безводным сульфатом натрия. После удаления эфира остаток перекристаллизовывают из смеси метанол-ацетон и получают 4,7 г желтых иголок 2-окси-4-ме- токси-3-{З-метил-2-бутенил)-4-(З-метил-2-бутенилокси)-халькона, т.пл, 9192 0. Пример 11. К раствору 3,2 г 2-метокси-4-(З-метил-2-бутенилокси)-ацетофенона и 3,4 г 2-окси 4-метокси-3-(З-метил-2-бутенил)-бензальдегида в 6 мл этагнола прибавляют 30 мл 50%-ного раствора гидроокиси калия и перемешивают 3 ч при комнатной температуре, подкисляют разбавленной соляной кислотой, растворитель выпаривают, остаток экстрагируют эфиром, экстракт промывают водой и сушат безводным сульфатом натрия. После удаления эфира остаток перегоняют под вакуумом и получают 4,5 г 2-окси-2, 4-диметокси-З- (З-меткл-2-бутенил) -4- (З-метил-2-бутенилокси) -халькона, т.кип, 131-133°С/0,09 мм. Пример 12. к раствору 7,6 г 2,6-диметокси-4-(3-метил-2-бутенилокси)-ацетофенона и 7,0 г 4-ацетокси-З-(3-метил-2 бутенил) -бензальдегида в l40 мл безводного этилацетата добавляют 40 мл 40%--ного раствора серной кислоты и перемешивают в течение 6 ч при 0°С. Растворитель выпаривают, к остатку добавляют воду и экстрагируют эфиром. Экстракт промывают водой, сушат безводным сульфатом натрия, эфир выпаривают, остаток перегоняют под вакуумом и получают 1,9 г 4-ацетокси -2,6-диметокси-З- (З-метил-2-бутенил) -4-(З-метил-2-бутенилокси)-халькона, т.кип. 129-131° С/О,09 мм. Н 7,16, Вычислено, %: С 72,78; Найдено , %: С 72,31; Н 7,22, Пример 13, К раствору 2,7 г п-(3,7-диметил-2,6-октадиенилокси)-ацетофенона и 2,6 г п-(3,7-диметкл-2,б-окстадиенилокси}-бензальдегида в 10 мл этанола прибавляют 30 1лл 50%-ного раствора гидроокиси натрия .и перемешивают в течение 1 ч при
SO С. После добавления холохчгоп воды реакц; окнуго смесь гкодк-псляют соляной кислотой и экстрагирушт эфИ-ром, Экст ракт перегоняют под ватчуумои л полу- чают 3,2 г 4 , 4-бис-(3, 7 1:1 неГИл- 2 , G-окгадиенилоксн)Халькона, Т..КИП. Ы4. -116°С/0,06 №л т.пл. 6970° С.
Вычислено, % С 8.1,9 9 j И .
ч
Найдено, %s С 81,89; Н 8,70,
Пример 14, К расГБОр5 3 г 2, 4 Дкметокси 3- {3-нети.л 2™6утенил) -ацетофенона и 3,5 г 4-метоксгг-2 - (3 ,7 димвтил-2 ,б-октадиенилокси) - -бензальдегида в 10 мл метанола добавляют 40 мл 50%-иого раствора гидроокиси калия -перемешивают 3 ч при комнатной температуре, после добавления воды подкисляют соляной кислотой я зкстрах чруют эфиром Эксгракт перегоняют под вакуумом и получают 3,7 г 24 f 4 триметокси-3-{3-метнл 2 бутенил),7 Диметил-2,б октадиеиилокси)Калькона, т.кип. 122- 125°С/0,08 MVJ,
Вычислено, %: С 76,41 Н 8,16.
Найдено , %s С 76,49 Н 8,11.
Особенно полезными являются соедмнания, полученные в примерах 1-14, а также .
f 4 бис-- (З-метил-2-бутенилокси)-халькон, . 1JO--112 С/ . /ОД мм
4 Окси-3-{3-нетил-2 бутенил)-4(3 Метил-2-бутенилокси)-халькон, т.ккп„ 5.30-132 С/О,О2 №t; т.пл. 139™ 140°С;
J 2 4-диокси-3(З-метил-2-бутенил)-4-(3™метил 2-бутекилокси)-халькон, т,кип с 14 5-14 7° С/О,11 мм т,пл. 14 2 143 С|
3 -метил-4 ,4-бис- (3, 7-диметиЛ 2, б -октадненилокси)-халькон, т,кип, 119121 0/0,11 Mivi,- /
4 Окси 4™метокси 3(3 метил-2 -бутенил) -2 (3, .метил- 2, 6 октадиенилокси)-хальконf т,кип. 133-135°(:/0,09 мм;,
4--ОКСИ-2, 4 диметокси 3 {3 метил 2 бутенил)-2-{3,7 диметил-2,6 ьктадиенилокси)-халькон, т,кип, 131- мм.
Формула изобретения
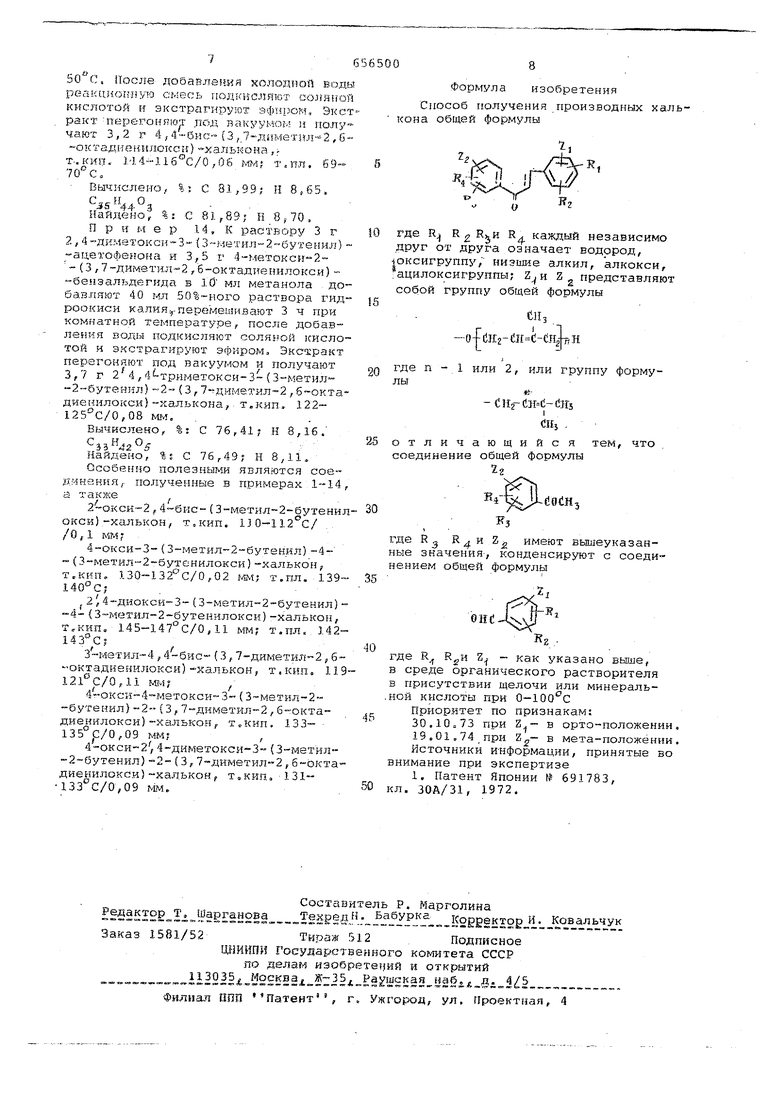
Способ получения производных халь кона общей формулы
где R R 2 R каждый независимо друг от друга означает водород, ноксигруппу, низшие алкил, алкокси, ацилоксигруппы; Z представляют собой группу общей формулы
С11з
-О-ГйЛ.2- (Лф7 Н
i
g где п - 1 или 2, или группу формулы
- H2-C№i;-(;jij (III},
отличающийся тем, что . соединение общей формулы Zg
щйойн.
Кз
где R R и Z
имеют выьиеуказанные значения-, конденсируют с соеди нением общей формулы
ОНИ
где R Z как указано выше, в среде органического растворителя в присутствии щелочи или минераль.ной кислоты при 0-100 0
Приоритет по признакам:
30. при Z в орто-положении.
19,01,74 при в мета-положении.
Источники информации, принятые во внимание при экспертизе
1, Патент Японии № 691783, кл. ЗОА/31, 1972,


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения хальконовых эфиров | 1975 |
|
SU633466A3 |
| Способ получения хальконовыхэфиРОВ | 1975 |
|
SU799643A3 |
| Способ получения карбостириловых производных (его вариант) | 1982 |
|
SU1779249A3 |
| Способ получения 7-замещенных 3-винилцефалоспоринов или их аддитивных солей с кислотами | 1983 |
|
SU1309911A3 |
| Способ получения производных 7-ацетамидо-3-цефем-карбоновой кислоты | 1974 |
|
SU668607A3 |
| Способ получения гетероциклических соединений | 1986 |
|
SU1493105A3 |
| Способ получения производных 1,8-нафтиридина или их солей | 1984 |
|
SU1482527A3 |
| Способ получения производных фурилоксазолилуксусной кислоты или их фармацевтически приемлемых солей | 1983 |
|
SU1169536A3 |
| Способ получения гетероциклических соединений | 1986 |
|
SU1491337A3 |
| Способ получения производного хинолина или его фармацевтически приемлемого сложного эфира или фармацевтически приемлемых солей указанного производного или его сложного эфира | 1988 |
|
SU1582986A3 |


Авторы
Даты
1979-04-05—Публикация
1974-10-04—Подача