Изобретение относится к способу получения новых производных хинолина, обладающих высокой бактерицидной активностью.
Целью изобретения является способ получения новых производных хинолина, которые проявляют более высокую активность против грамположительных и грамотрицательных бактерий по сравнению с известными структурными аналогами.
Пример 1 (ссылочный).
1-Циклопропил-5,6,7,8-тетрафтор- -1,4-дигидро-4-оксохинолин-3-карбоно- вая кислота.
1.1 Смесь этилового эфира пента- фторбензоилуксусной кислоты (25 г), этилортоформиата (20 г) и уксусного ангидрида (23 г) кипятят 2 ч. Реак-. ционную смесь упаривают при пониженном давлении досуха. Остаток растворяют в диэтиловом эфире и вводят в
реакцию с циклопропиламином (5,1 г) i с получением этилового эфира 2-пента- фтсрбензоил-3-циклопропиламиноакри- ловой кислоты (28 г), т.пл, 89°С,
1.2. Полученное выше соединение (28 г) растворяют в сухом тетрагидро- фуране и вводят в реакцию при комнат- ной температуре с 60%-ным гидридом
фтор-1,4 дигидро-4-оксохинолин-3-кар- боновая кислота, т.пл. 255-256°С;
d)7-(цис-3-трифторацетиламино-4- -фторме тил-1-пирролидинил)-1-цикло- пропил-5,6,8-трифтор-1,4-дигидро-4- -оксохинолин-3-карбоновая кислота;
e)7-(транс-3-амино 4-фторметил- 3-метил-1-пирролидинил)-1-циклопро




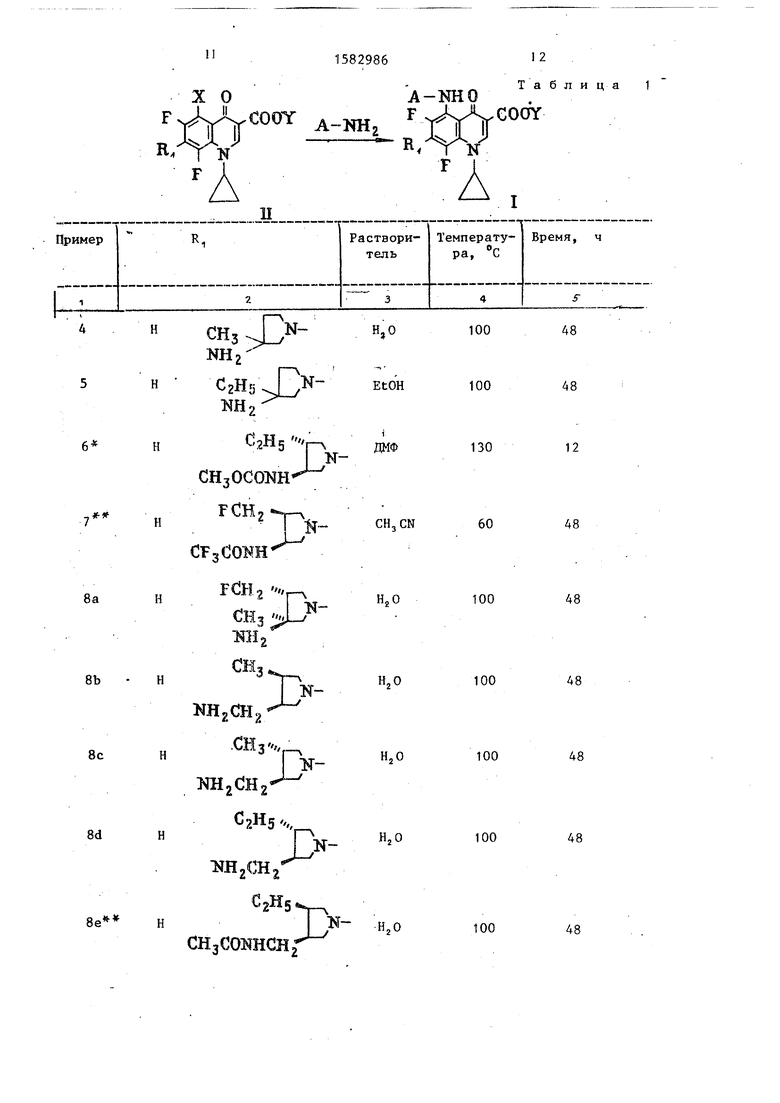

Изобретение касается производных хинолина, в частности соединений общей ф-лы N .H 2 C=CF-CR, =CF-C=C-C[O]-C[C/O/OH]=CH-N - C-CH 2-CH 2, где R 1= =N-CH 2 @ -CH 2 @ -CHK-CH 2 при K= -[CH 2] N-NH R 4
R 2-низший алкил, галоидалкил
R 3=R 4=H или низший алкил, N=0 или 1, их эфиров или солей, обладающих бактерицидной активностью, что может быть использовано в медицине. Цель - создание более активных веществ указанного класса. Синтез ведут введением группы NH 2 с помощью обработки производного хинолина, содержащего галоген, аммиаком с последующим, при необходимости, гидролизом [в случае когда карбоксил этерифицирован] с получением целевого продукта либо в виде кислоты, либо в виде необходимой фармацевтически приемлемой соли. Новые вещества в сравнении с аналогами проявляют более высокую активность в отношении грамположительных и грамотрицательных бактерий и имеют низкую токсичность (LД 50*982000 мг/кг). 4 табл.
натрия (3,85 г) с получением этилово-JQ пил-5,6,8-трифтор-1,4-дигидро-4-оксого эфира 1-циклопропил-5,6,7,8 тетра ,;фтор-1,4-дигидро-4-оксохинолин-3-кар боковой кислоты (18,4 г), т.пл. 170171°С.
Пример 2 (ссылочный). 7-(3-Амино-3-метил-I-пирролидинил) -1-циклопропил-5,6,8-трифтор-1,4-ди- гидро-4-оксихинолин-З-карбоковая кислота.
Смесь 1-циклопропил-5,6,7,8-тетра- фтор-1,4-дигидро-4-оксохинолин-3-кар- боновой кислоты (0,8 г), З-амино-3- -метилпирролидина (0,8 г) и ацетонит- рила (35 мл) перемешивают 30 мин при 50°С. Выпавшие кристатлы отделяют фильтрованием и промывают водой, растворяют в 10%-ном водном аммиаке, обрабатывают активированным углем и концентрируют при пониженном давлении. Выпавшие кристаллы отфильтровывают, промывают водой и сушат с получением 7-(З-амино-3-метил-1-пирролидинил) -1-циклопропил 5,6,8-трифтор- -1,4-дигидро-4-оксохинолин 3-карбо- новой кислоты (0,81 г), т.пл, 280 - 282°С.
30
хинолин-3-карбоновая кислота, т.пл. 300°С;
f)7-(цис-3-аминометил-4-метил-1- -пирролидинил)-1-циклопропил-5,6,8- -трифтор-1,4-дйгидро-4-оксохинолин- -3-карбоновая кислота;
g)7-(транс-3-аминометил-4-метил- -1-пирролидинил)-1-циклопропил-5,6,8- -трифтор-1,4 дигидро-4-оксохинолин- -3-карбоновая кислота;
Ь) 7-,(транс-3-аминометил-4-этил-1- -пирролидинил)-1-циклопропил-5,6,8-ТрИфТОр-1,4-ДИГИДРО-4-ОКСОХИНОЛИН-3-карбоновая кислота;
i) 7-(цис-3-ацетиламинометил-4- -этил-1-пирролидинил)-1-циклопропил- -5,6,8-трифтор-1,4-дигидро-4-оксохи- нолин-3-карбоновая кислота;
j) 7(цис-3-трифторацетилэтилами- нометил-4-этил-1-пирролидинил)-1-циклопропил-5, 6,8-дифтор-1,4-дигидро-1- -оксохинолин-3-карбоновая кислота
Пример 4. 5-Амино-7-(3-ами- но-3-метил-1-пирролидинил)-1-цикло- пропил-6,8-дифтор-1,4-дигидро-4-оксо- хинолин-3-карбоновая кислота и ее соли,
35
45
Пример 3 {ссылочный).
Используя методику примера 2, получают следующие соединения:
а) 7-(3-амино-3-этил-1-пирролидинил) -1-циклопропил-5,6,8-трифтор-1,4- -дигидро-4-оксохинолин-З-карбоновая кислота;
50
б) 7-(транс-3-метоксикарбониламино-4-этил-1-пиРРолидинил)-1-циклопро-55 Я° Осажденные кристаллы отфиль- пил-5,6„8-трифтор-1,4-дигидро-4-оксо- хин олин-3 -к ар боковая кислота;
с) 7-(транс-3-амино-4-метил-1 ролидинил)-1-циклопропил-5„6,8-тритровывают, промывают водой, затем этанолом и сушат. Получают 5-амино- -7-(3-амино-3--метил-1-пирролидинил)- -1-циклопропил-6,8-дифтор-1,4-дигидрО
Q
0
хинолин-3-карбоновая кислота, т.пл. 300°С;
f)7-(цис-3-аминометил-4-метил-1- -пирролидинил)-1-циклопропил-5,6,8- -трифтор-1,4-дйгидро-4-оксохинолин- -3-карбоновая кислота;
g)7-(транс-3-аминометил-4-метил- -1-пирролидинил)-1-циклопропил-5,6,8- -трифтор-1,4 дигидро-4-оксохинолин- -3-карбоновая кислота;
Ь) 7-,(транс-3-аминометил-4-этил-1- -пирролидинил)-1-циклопропил-5,6,8-ТрИфТОр-1,4-ДИГИДРО-4-ОКСОХИНОЛИН-3-карбоновая кислота;
i) 7-(цис-3-ацетиламинометил-4- -этил-1-пирролидинил)-1-циклопропил- -5,6,8-трифтор-1,4-дигидро-4-оксохи- нолин-3-карбоновая кислота;
j) 7(цис-3-трифторацетилэтилами- нометил-4-этил-1-пирролидинил)-1-циклопропил-5, 6,8-дифтор-1,4-дигидро-1- -оксохинолин-3-карбоновая кислота
Пример 4. 5-Амино-7-(3-ами- но-3-метил-1-пирролидинил)-1-цикло- пропил-6,8-дифтор-1,4-дигидро-4-оксо- хинолин-3-карбоновая кислота и ее соли,
5
5
0
Я° Осажденные кристаллы отфиль-
тровывают, промывают водой, затем этанолом и сушат. Получают 5-амино- -7-(3-амино-3--метил-1-пирролидинил)- -1-циклопропил-6,8-дифтор-1,4-дигидрО
-4-оксохинолин-З-карбоновой кислоты (480 мг), т.пл. 271-273°С (с разложением) .
(145 мг), т.пл, 293-297°С (с разложением) .
с уксусной киспотой (т.пл. 272-274°С, с разложением) и соль с метансульфо- новой кислотой (т.пл. 300°С).
Пример 5. 5-Амино-7-(3-ами- но-З-этил-1-пирролидинил)-1-циклопро- пил-6,8-дифтор-1,4-дигидро 4-оксохи- нолин-3-карбоновая кислота.
По методике примера 4, используя 7-(З-амино-3-этил-1-пирролидинил)-1- -циклопропил-5,6,8-трифтор-1,4-дигид- ро-4-оксохинолин-З-карбоновую кислоту (1,19 г) для взаимодействия аммиака в этаноле при 48 ч,
100°С в течение
получают названное соединение (580 мг), т.пл. 205-206°С.
Пример 6. 5-Амино-7-(транс- -З-амино-4-э тил-1-пирролидинил)-1-ци- клопропил-6,8-дифтор-1,4-дигидро-4- -оксохинолин-3-карбоновая кислота.
40
амиде при 130°С в течение 12 ч в запаянной трубке с получением 5-амино1Г р и м е р 8. По методике при-1 мера 4 получены следующие соединения: а) 5-амино-7-(транс-3-амино-4-фтор.-, ,о45 метил-З-метил-1 -пирролидинил)-1-цик-1-циклопропил-7-(транс-3-метоксикар- 0 .,,
,. лопропил-о,о-диЛтор-1.4-ДИГИДРО-4-ОКбониламино-4-э тил-1 -пирролидинил)- м Mi
-6,8-дифтор-1,4-дигидро-4-оксохинолин- -3-карбоновой кислоты (620 мг), т.пл,
231-232°С
50 метил-1-пирролидинил)-1-циклопропнлсохинолин-3-карбоновая кислота, т.пл. 299-301°С;
Ь) 5-амино-7-(цис-3-аминометил-4f
-6,8-дифтор-1,4-дигидро-4-оксохинолин- -3-карбоновая кислота, т.пл. 221- 223°С (хлоргидрат, т.пл. 268-271°С (с разложением);
с) 5-амино-7-(транс-3-аминометил- -4-метил-1-пирролидинил)-1-циклопропил-6 ,8-дифтор-1,4-дигидро-4-оксохи- нолин-3-карбоновая кислота, т.пл. 223-225°С;
0
следовательно промывают водой и этанолом и после высушивания получают 5-амино-1-циклопролил-7-(транс-3-ами- но-4-этил-1-пирролидинил)-6,8-дифтор- -1,4-дигидро-4-оксохинолин-3-карбо- новую кислоту (490 мг), т.пл. 195 - 196°С.
Пример 7. 5-Амино-7-(цис-3- -амино-4-фторметил-1-пирролидинил)-1- -циклопропил-6,8-дифтор-1,4-дигидро-- -4-оксохинолин-З-карбоновая кислота.
5 7.2. Смесь полученной выше карбо- новой кислоты (500 мг) и 10%-ной водной гидроокиси натрия (5 мл) кипятят на кипящей водяной бане. Полученную смесь подкисляют 10%-ной водной укQ сусной кислотой, после чего добавлением концентрированного водного аммиака делают слабо щелочной. Смесь концентрируют при пониженном давлении и выпавшие кристаллы отфильтровывают, промывают водой и сушат. Перекристаллизацией из диметилформамида получают 5-амино-1-циклопропил-7-(цис-3-амино- -4-фторметил-1-пирролидинил)-6,8-дифтор- 1 ,4-дигидро-4-оксохинолин-3-кар- боновую кислоту(310 мг), т.пл. 248- 249° С.
0
м Mi
сохинолин-3-карбоновая кислота, т.пл. 299-301°С;
Ь) 5-амино-7-(цис-3-аминометил-4
-6,8-дифтор-1,4-дигидро-4-оксохинолин- -3-карбоновая кислота, т.пл. 221- 223°С (хлоргидрат, т.пл. 268-271°С (с разложением);
с) 5-амино-7-(транс-3-аминометил- -4-метил-1-пирролидинил)-1-циклопропил-6 ,8-дифтор-1,4-дигидро-4-оксохи- нолин-3-карбоновая кислота, т.пл. 223-225°С;
715
d)5-амино-7-(транс-3-аминометил -4-ЭТИЛ-1-пирролидинил)-1-циклопро- пил-6,8-дифтор-1,4 дигидро-4-оксохи нолин-3-карбоновая кислота, т.пл. 121-122°С, в виде хлоргидрата т.пл. 183-184°С;
e)5-амино-7-(цис-3-ацетиламиноме тил-4-этил-1-пирролидинил)1-цикло- пропил-6,8-дифтор-1,4 дигидро-4-оксо хинолин-3-карбоновую кислоту гидроли зуют по методике примера 7.2, получают 5 амино-7-(цис-3-аминометил-4- -этил-1-пирролидинил)-1-циклопропил- -6,8-дифтор-1,4-ДИГИДРО-4-ОКСОХШ-ЮЛИ -3-карбоновой кислоты, т.пл. 220 - 222°С (с разложением);
f)5-амино-7-(цис-3-трифторацетилэтиламинометил-4 этил-1-пирролидинил-1 -циклопропил- б, 8-дифтор-1,4-дигид- ро-4-оксохинолин-З-карбоновую кислоту, т.пл. 145-146°С;
По методике примера 7.2 получают 5-амино-7-(цис-3 этиламинометил-4- -этил-1-пирролидинил)-1-циклопропил- -6,8-дифтор-1,4-дигидро-4-оксохино- лин-3-карбоновую кислоту, т.пл. 171- 172°С.
В табл. 1 представлены соединения формулы I, полученные по примерам 4-8
Хемотерапевтическое действие соединений, полученных по предлагаемому способу, иллюстрируется примерами 9-11 .
;,
Использованы следующие соединения: Соединение 1 - 5-амино-7-(3 амино- -3-метил-1-пирролидинил)-1-циклопро- пил-6,8-дифтор-1,4-дигидро 4-оксохи- нолин-3-карбоновая кислота.
Соединение 2 - 5-амино-7-(3-амино- -3-этил-1-пирролидинил)-1-циклопро- пил-6,8-дифтор-1,4-дигидро-4-оксохи- нолин-3-карбоновая кислота.
Соединение 3 - 5-амино-7-(транс-3- -амино-4-метил-1-пирролидинил)-1-цик- лопропил-6,8-дифтор-1,4-дигидро-4-ок- сохинолин-3-карбоновая кислота.
Соединение 4 - гидрохлорид 5-ами- но-7-(цис-З-аминометил-4-метил-1-пирролидинил) -1-циклопропил-6,8-дифтор- -1,4-дигидро-4-оксохинолин-3-карбоно- вой кислоты.
Соединение А - 5-амино-1-этил-6,8- -дифтор-7-(1-пиперазинил)-1,4-дигид- ро-4-оксохинолин-З-карбоновая ки слота
соон
С2Н5
Соединение В - хлоргидрат 1-цикло- пропил-6-фтор-7-(1-пиперазинил)-1,4- -дигидро-4-оксохинолин-3-карбоновой кислоты
соон
HC1-HN
П р и м е р , 9. Бактерицидное действие in vitro иллюстрируется табл. 2, Указанные в табл. 2 значения соответствуют минимальной ингибирующей концентрации (МИК) (в пересчете на свободное основание). Минимальная инги- бирующая концентрация определена методом двукратного разбавления агара (с использованием агара Мюллера-Хинто- на). Одну петельку выращиваемой в течение суток культуры испытуемого организма в бульоне Мюллера-Хинтона наносят на содержащие лекарство слои в 10 мл агара в чашечках Петри. Бактериальная инокула содержит примерно 10 колониообразующих единиц. Рост бактерий наблюдают через 20 ч инкубирования при 37°С. МИК определяют как самую низкую концентрацию лекарства, предотвращающую видимый рост бактерий.
Как видно из данных табл. 2, соединения 1 - 4 показывают очень высокую бактерицидную активность против грамположительных и грамотрицательных бактерий, лучшее in vitro действие против грамположительных и грамотри- цательных бактерий по сравнению с соединением А.
Пример 10. Действие in vitro против общих инфекций на мышах (табл, 3).
Каждое соединение растворяют в де- ионизированной воде. Каждый раствор вводят перорально мышам, зараженным испытуемым организмом, в приведенных ниже условиях и на основе анализа проб подсчитывают значение средней эффективной дозы (ЭД$о).
Приведетше в табл. 3 цифры соответствуют значения 3/7fo (мг/кг) в пересчете на свободное основание.
Экспериментальные условия.
Мыши - мужские особи (ddy-S) весом около 20 г.
Заражение.
Staphylococcus aureus 50774. Вну- тривенное заражение 5 х 10 клеток на мышь, суспендированных в солевом растворе.
Streptococcus pyogenes A65. Заражение внутрибрюшинно 3 х 10 клеток на мышь, суспендированных в сердечно-мозговом бульоне для вливаний.
Pseudoraonas aeruginosa 12. Заражение внутрибрюшинно 5 х 10 3 клеток на мышь, суспендированных в триптосоевом бульоне с 4% муцина.
Медикация дважды: сразу же после заражения и спустя 6 ч,
Наблюдения в течение 14 дней для Staphylococcus aureus 50774 и в течение 7 дней для других организмов.
Как видно из табл. 3, соединение 1 оказывает более сильное терапевтическое действие на общие инфекции, вызы
ваемьш грамположительными и грамотри цательными бактериями по сравнению с соединениями А и В.
Пример 11 (острая токсичность) .
Мужским особям мышей (ddy) вводят перорально растворы, содержащие каждый в различной концентрации соединение, полученное по предлагаемому способу, в дозировке 0,1 мл на 10 г веса тела. Спустя 7 дней подсчитывают число мертвых мышей и в соответствии с методом Гейренса-Кэрбера подсчитывают значение средней летальной дозы (ЛД5&, мг/кг)(см. табл. 4).
Как видно из приведенных результатов, соединения 1, 2, 3 (полученные по предлагаемому способу) по- казывают низкую токсичность при перо- ральном введении.
Как показали исследования, предлагаемые соединения оказывают сильное терапевтическое действие на экспери- ( ментальные инфекции, вызываемые грам
положительными и грамотрицательными . бактериями,, обладают низкой токсич- костью,а также хорошей адсорбируемо- стью и метаболической устойчивостью, низкой цитотоксичностью и при парентеральном введении вызывают низкое местное раздражение.
Таким образом, соединения,полученные по предлагаемому способу, применимы в качестве бактерицидных средств для перорального введения или введения в виде инъекций, Формула изобретения ,Способ получения производного хи- нолина общей формулы
A-NHO
F
20
i
25
где А - водород;
R, - группа формулы
Кз
30
R4HN-(CH2)n
Ј
5
0
где R2 - низший алкил или галоидал- кил;
R3 - водород или низший алкил;
R - водород или низший алкил;
п 0 или 1,
или его фармацевтически приемлемого сложного эфира или фармацевтически приемлемых солей указанного производного или его сложного эфира, отличающийся тем, что.соеде- нение формулы
X О
45
где X - галоген;
Y - водород или низший алкил;
R - имеет указанные значения, подвергают взаимодействию с аммиаком с последующим, в случае необходимости, гидролизом сложного эфира до карбоно- вой кислоты с выделением целевого продука в свободном виде или в виде фармацевтически приемлемой соли.
X 0
1582986
, у N F
A-NHO COOY А--1Ш, F -COOY
--R,
2 Та
OH3 NHZ
С2н5 JIX ш2
ГА
C2HS
CH3OCO:NH
FCH2«
CFgCONH
Nft
FCH2
CH3
™2
CH3,
n
N
г-л
TH
jm2CH2 С И5ч
J-
СНч
2ЪЛ2
C2H5
KСН3СОШ1СНГ
OY
2 Таблица
100
48
EtOH
100
48
ДМФ
130
12
CH3CN
60
48
H00
100
48
H20
100
48
H20
100
48
H20
100
48
H20
100
48
13
Соединение
1 2 3
1582986
14 Продолжение табл. I
Таблица 3
ДД , мг/кг
2000 2000 2000
| Патент США Р 3458519, 287, опублик | |||
| Солесос | 1922 |
|
SU29A1 |
| кл, 260(54) СПОСОБ ПОЛУЧЕНИЯ | |||
| ПРОИЗВОДНОГО ХИНОЛИНА ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМОГО СЛОЖНОГО ЭФИРА ИЛИ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ УКАЗАННОГО ПРОИЗВОДНОГО ИЛИ ЕГО СЛОЖНОГО ЭФИРА | |||
Авторы
Даты
1990-07-30—Публикация
1988-03-28—Подача