где R - R 3 - как указано выше; Y - анион неорганической кислоты, образующийся продукт последовательно обрабатывают слабым основанием, гидроокисью щелочного металла и кислотой, полученное соединение общей формулы
СНгСООН
f.
То
где G, n, R,
- R g имеют вышеуказан.ные значения, обрабатывают сильной кислотой и выделяют целевой продукт.
В этом случае нет необходимости выделять получаемые на одной из стадий продукты перед проведением еледующей стадии.
Производные 2-нафтол-1 сульфокислоты могут быть получены сульфированием замещенного 2-нафтола, например при обработке концентрированной серной кислотой при (-10)-(+10)°
Взаимодействие производного 2-нафтол-1-сульфокислоты Q арилдиазсниевой солью проводят предпочтительно при (-20)(+50)С, например при (-10)-(+10)С.
Стадию обработки слабым основанием, таким как карбонат щелочного металла или аммония,проводят при (-20) (f20)c, лучше при (-10)-(-1-10)°С. В качестве карбоната щелочного металла обычно используют карбонат натрия
Время реакции определяется природой заместителей в арилдиазониевой соли и в случае электроноакцепторных заместителей, таких. как галоген или трифторметил, составляет от 1 до 30 мин; в случае электронодонорных заместителей, таких как аЛкил, время реакции от 30 мин до 24 ч, обычно от 1 до 6 ч .
Стадию обработки гидроокисью щелочного металла, такой как гидроокись натрия, обычно проводят при (-20)- (+50)° С, предпочтительно при (-5)-(+30)«С.
Стадию обработки промежуточного соединения сильной кислотой, как правило, неорганической, такой как соляная, проводЯ.Т при 20-200 с, предпочтительно при 50-120°С, при кипячении с обратным холодильником.
Время этой стадии составляет от 1 до б ч.
Целевые соединения получают в виде рацемической смеси, которая может быть обьзчными методами разделена на оптически активные стереоизомеры.
Пример 1.В концентрированную серную кислоту, охлажденную до , порциями при непрерывном перемешивании добавляют 44 г 6-бром-2-нафтрла. После затвердевания смесь вьщержквают при комнатной температуре в течение ночи, добавляют 250 мл воды перемешивают и фильтруют. К
фильтрату при непрерывном перемешивании добавляют 40 г хлорида натрия, ВЕДцерживают в течение ночи и фильтруют. Твердый продукт с фильтра промывают 350 мл насыщенного раствора хлорида натрия, сушат и экстрагируют кипящим абсолютным этанолом. Экстракт фильтруют, этанол упаривают, а остаток перемешивают с 500 мл диэтилового эфира в течение 2 ч. 1ри. последующем фильтровании получают 6-бром-2-нафтол-1-сульфонат натрия. Часть его (6,3 г) растворяют в 250 мл воды, фильтруют раствор/ охлаждают и медленно добавляют к диазониевой соли, Последнюю получают при добавлении
охлаждаемого льдом раствора 1,7 г нитрита натрия в 5 мл воды к раствору 8 мл концентрированной соляной кислоты в 30 мл воды. Аелтый осадок отфильтровывают, промывают 250 мл
холодного насыщенного раствора хлорида натрия и превращают в пасту при смешивании с 100 мл холодной воды. Пасту охлаждают до , принепрерывном перемешивании добавляют
6 г карбоната натрия, через 1,5 мин добавляют хрлодный раствор гидроокиси натрия. После образования красного раствора перемешивают на ледяной бане в течение 3 ч и при комнатной температуре в течение ночи. Концентрированной соляной кислотой подкисляют до рН 2-3, добавляют насыщенный водный раствор карбоната натрия до рН 8, фильтруют и фильтрат
подкисляют до рН 1 концентрированной соляной кислотой при перемешивании. Твердый продукт отфильтровывают, растворяют в 250 мл теплой воды, кипятят раствор с обратным холодильником в течение 2 ч и в течение этого
времени добавляют 15 мл концентрированной соляной кислоты. Затем смесь охлаждают, твердое вещество отфильтровывают и перекристаллизовывают из смеси уксусная кислота - вода (2:1
по объему). Получают 7-бром-4-гидрокси-2-(3 трифторметилфенил)-1,2-дигидрофталазин-1-уксусную кислоту, т.пл. 217-219 с.
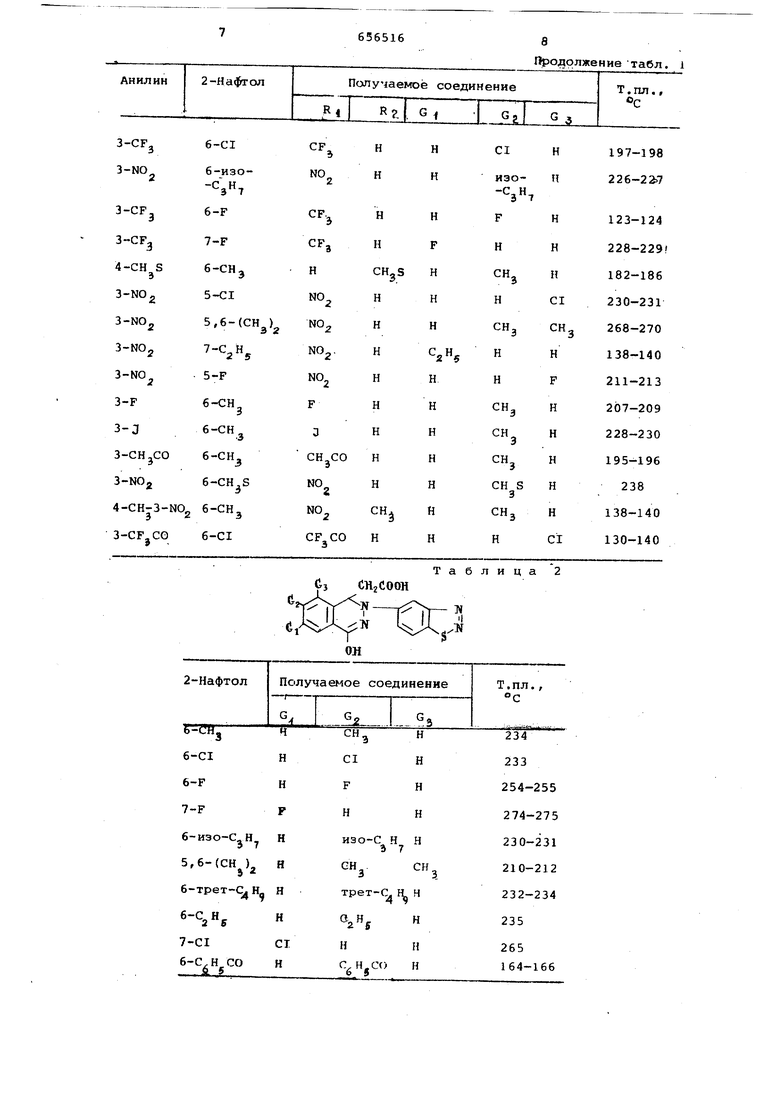
Примеры 2-36, Аналогично
примеру 1 из соответствующего 2-нафтола и анилина получают соответствующую уксусную кислоту. Полученные соединения перечислены в табл. 1.
В ряде случаев разбавленную реакционную смесь из стадии сульфирования 2-нафтола или раствор неочищенного нафтолсульфоната натрия обрабатывают раствором диазониевой соли без очистки. Внекоторых случая ; нейтральные
и фенольные примеси из конечного
продукта удаляют обработкой растворителем, не смешивающимся с водой, обычно диэтиловым эфиром, и водным раствором бикарбоната натрия. Затем продукт извлекают из водной фазы при ее
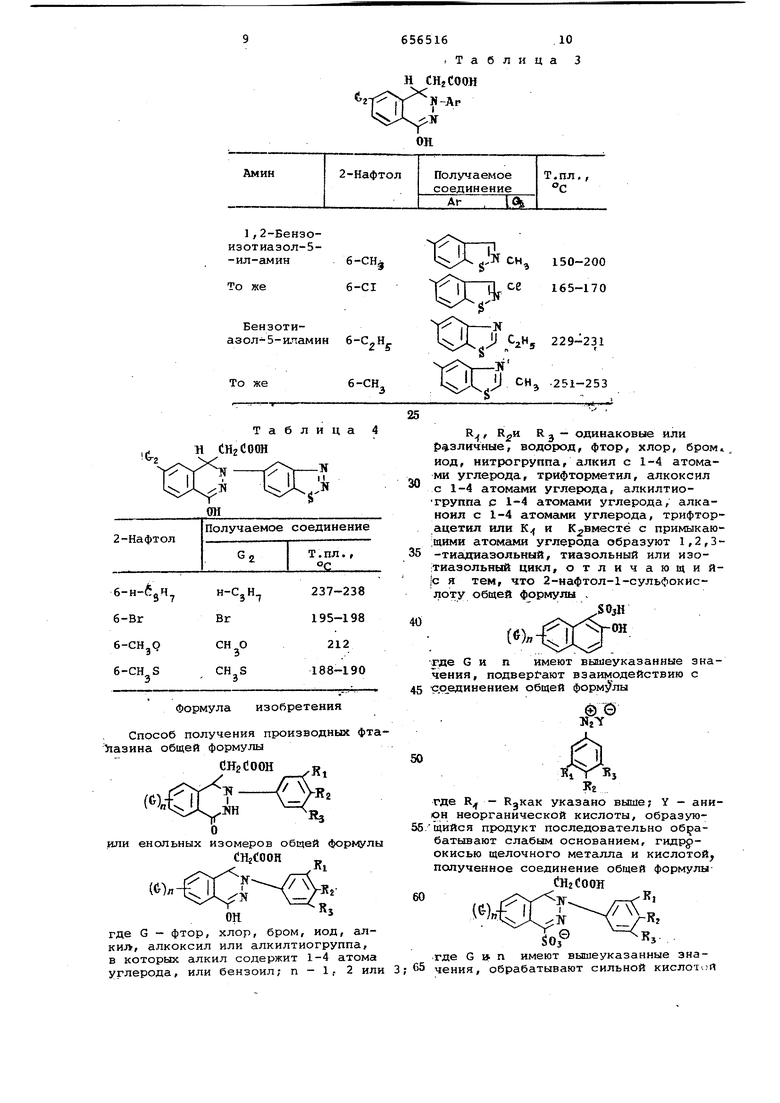
подкислении. В табл. 1 указаны исходный анилин для соли диазония, и сходный нафтол и целевые продукты, полученные на их основе. Примеры 38-4/. Аналогично примеру 1 из 1,2 , 3-бензотиадиазол-5-иламина и соответствутацего нафтола синтезируют кислоты, перечисленные в табл. 2. Продукт получают в двух формах с различными ИК-спектрами. Перекристаллизацией из уксусной кислоты по- „ лучают продукт 1710, 1680 см tj Н а перекристаллизацией из этиладетата - продукт с 1.700, 1635 (диск из КВр) . Примеры 48-51. Подобно примеру 1 из соответствующих нафтола и ароматического амина получают кислоты, которые перечислены в табл. 3 Примеры 52-55. В соответствии с методикой примера 1, исходяиз 1,2,3-5ензотиадиазол-5-иламина и соответствующего нафтола, получают кислоты, указанные в табл. 4. Таблица 1 ООИ
Продолжение табл. l



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения хинолонов | 1980 |
|
SU1124886A3 |
| Способ получения производных имидазола | 1973 |
|
SU576042A3 |
| Способ получения замещенных 1-(1-фенилциклобутил)-алкиламинов или их фармакологически приемлемых солей | 1982 |
|
SU1482522A3 |
| Способ получения хинолонов | 1981 |
|
SU1192617A3 |
| СПОСОБ ПОЛУЧЕНИЯ АЗОКРАСИТЕЛЕЙ | 1968 |
|
SU435615A1 |
| Способ получения гетероциклических производных циклобутиламинометана | 1983 |
|
SU1274622A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 4,9-КСАНТЕНИЛАМИНО-4Н-1,2,4-ТРИАЗОЛА ИЛИ 1,9-КСАНТЕНИЛАМИНОИМИДАЗОЛА | 1972 |
|
SU327681A1 |
| Способ получения производных 5-замещенных @ -пиронов | 1980 |
|
SU976850A3 |
| 2,3,4,5-ТЕТРАГИДРО-1,4-БЕНЗОТИАЗЕПИНЫ, ИХ СТЕРЕОИЗОМЕРЫ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОСУДОРОЖНЫМ ДЕЙСТВИЕМ | 1993 |
|
RU2115650C1 |
| ПРОИЗВОДНЫЕ СУЛЬФОНАМИДОВ, СПОСОБ ИХ ПОЛУЧЕНИЯ, КОМПОЗИЦИЯ И СПОСОБ УНИЧТОЖЕНИЯ СОРНЯКОВ | 1992 |
|
RU2266904C2 |

6-CI
CFHH
6-ИЗОNOHH
6-F
CF.jHH
7-F
CF,HF G-CHj
HCHjS H 5-CI
5,6-(CH).
NO,HH
N0.
5-F
FHH
6-CH
nHH
6-CH
3
CH COHH
6-CH.
NOHH
6-CH,
O2
CFjCOHH
6-CI
6-CI
6-F
7-F
6-ИЗО-С.Н
5,6-(CH)
6-трет-С.Н
«-S«5 7-CI 6-C,H CO
-& ,g
H
197-198 226-22 7
П
123-124
H
228-229
H
182-186
H
230-231
CI
268-270
CHg
138-140
H
211-213
F
207-209
H
228-230
H
195-196
H
238
H
138-140
H
ci 130-140
Таблица 2
CHjCOOH
233
H
254-255
H
274-275
H
230-231
H H 7
210-212
CH,
232-234
С. R H
235
H
265
H 164-166
) H
1,2-Бензоизотиаэол-5-ил-амин6-СНа
То же6-CI
Бензотиазол-5-иламин 6-С-Н
То же
Г Формула изобретения Способ получения производных фта Мазина общей формулы CHgdooH j /TNA или енольных изомеров общей формулы СНгСООН где G - фтор, хлор, бром, иод, алкил, алкоксил или алкилтиогруппа, в которых алкил содержит 1-4 атома углерода, или бензоил; п - 1г 2 или
g СН, С-е
S-
-К
,j S
-jj
IC С«Э
6-СН,
R.
R.
, 3 одинаковые или различные, водород, фтор, хлор, бром иод, нитрогруппа, алкил с 1-4 атомами углерода, трифторметил, алкоксил с 1-4 атомами углерода, алкилтиогруппа с 1-4 атомс1ми углерода, алканоил с 1-4 атомами углерода, трифторацетил или К и К вместё с примыкаю:1цими атомами углерода образуют 1,2,3-тиадиазольный, тиазольный или изо;тиазольный цикл, отличаюадий|с я тем, что 2-нафтол-1-сульфокислоту общей формулы .
ОзН
(«)jrj™
где Сип имеют вышеуказанные значения, подвергают взаимодействию с ср единением общей формулы где R - RgKaK указано выше; Y - анион неорганической кислоты, образующийся продукт последовательно обрабатывают слабЕЛм основанием, гидр окисью щелочного металла и кислотой, полученное соединение общей формулы tlHaCOOH -Кг 50з Где G п имеют вышеуказанные значения, обрабатывают сильной кислотой 11 с последующим выделением целевого продукта. Источники информации, принятые внимание при экспертизе 1, Гетероциклические соединения, воранная литература , 1960, т. 6, 65651612 под ред. Р. Эльдерфильда, Иностс. 170.
Авторы
Даты
1979-04-05—Публикация
1974-10-31—Подача