Изобретение относится к синтезу биологически активных химических соединений, конкретно S-метилсульфониевых солей 3,5-дифенил-2-тиабицикло[4,4,0] декана или дец-5-ена, проявляющих антимикробную активность.
Указанные свойства позволяют предполагать возможность применения их в медицине.
Известны соли 5,6,7,8-тетрагидротиохромилия общей формулы
где X- - J- или ClO
обладающие антимикробной активностью [1]. Однако указанные соединения проявляют незначительную активность.
Целью изобретения является, во-первых, усиление антимикробной активности, во-вторых, расширение арсенала средств воздействия на живой организм.
Указанные свойства определяются новой химической структурой S-метилсульфониевых солей 3,5-дифенил-2-тиабицикло[4,4,0]декана (Iа, Iб) или 3,5 - дифенил-2-тиабицикло[4,4,0]дец-5-ена (II) общей формулы I
где символ  - одинарная или двойная связь, причем в случае одинарной связи X-- AgI
- одинарная или двойная связь, причем в случае одинарной связи X-- AgI
Способ получения указанных солей (Ia, II) заключается во взаимодействии 3,5-дифенил-2-тиабицикло[4,4,0] декана (III) или 3,5-дифенил-2-тиабицикло[4,4,0] дец-5-ена (IV) с иодистым метилом в присутствии 5 - 10% молярного избытка азотнокислого серебра. Иодид AgJ• 2-метил-3,5-дифенил-2-тиониабицикло[4,4,0]декана (Ia) подвергают обменной реакции с HClO4 в CH3COOH, получая перхлорат (Iб).
Синтез осуществляется по следующей схеме:
Пример 1. 2-Метил-3,5-дифенил-2-тиониабицикло[4,4,0]деканиодид•AgJ (Ia).
В трехгорлую колбу емкостью 50 - 100 мл, снабженную механической мешалкой, газоподводной трубкой и хлоркальциевой трубкой, вносят 20 мл иодистого метила и при охлаждении (0oC) в атмосфере азота добавляют 1 г 3,5-дифенил-2-тиабицикло[4,4,0] декана. При энергичном перемешивании в реакционную смесь вносят 0,67 г азотнокислого серебра. Раствор перемешивают при комнатной температуре 1,5 - 3 ч. Затем реакционную смесь разбавляют эфиром. Выпавший осадок отфильтровывают и промывают на фильтре горячим хлористым метиленом. Из экстрактов хлористого метилена эфиром высаждают аналитически чистый 2-метил-3,5-дифенил-2-тиониабицикло[4,4,0] декан иодид•AgJ (Ia). Выход 2,23 г (количественный), т.пл. 162oC (CH2Cl2 - эфир).
Найдено, %: S 4,59; 4,59.
Вычислено, %: S 4,67.
ИК-спектр сульфониевой соли (Ia) характеризуется полосой поглощения при 1415 см-1, которая относится к симметричным деформационным колебаниям метильной группы, присоединенной к атому серы.
Пример 2. 2-Метил-3,5-дифенил-2-тиониабицикло[4,4,0]дец-5-ен-иодид•AgJ (II).
В трехгорлую колбу, снабженную механической мешалкой, газоподводной трубкой и хлоркальциевой трубкой, помещают 20 мл иодистого метила и при охлаждении (0oC) в атмосфере азота вносят 1 г 3,5-дифенил-2-тиабицикло[4,4,0] дец-5-ена. При интенсивном перемешивании в реакционную смесь добавляют 0,67 г азотнокислого серебра. Раствор перемешивают при комнатной температуре 6 ч и оставляют на сутки. Через 24 ч реакционную смесь разбавляют эфиром, выпавший осадок отфильтровывают, фильтраты отбрасывают. Осадок промывают на фильтре горячим спиртом и диметилсульфоксидом. Фильтраты частично упаривают в вакууме и разбавляют эфиром, при этом выделяют 0,8 г (30%) 2-метил-3,5-дифенил-2-тиониабицикло[4,4,0] дец-5-ен-иодида•AgJ (II), т.пл. 185oC (DMCО - эфир).
Найдено, %: S 4,73; 4,70.
Вычислено, %: S 4,30.
ИК-спектр сульфониевой соли (II) характеризуется полосой поглощения при 1410 см-1, относящейся к симметричным деформационным колебаниям метильной группы, присоединенной к атому серы.
Пример 3. 2-Метил-3,5-дифенил-2-тиониабицикло[4,4,0]деканперхлорат (Iб).
В колбу помещают 0,3 г (0,00043 моль) 2-метил-3,5-дифенил-2-тиониабицикло[4,4,0]деканиодида•AgJ (Iа) и 0,3 мл 70%-ной HClO4 в 3 мл ледяной уксусной кислоты. Через двое суток реакционную смесь обрабатывают 10 мл эфира. Кристаллы отделяют на фильтре, сушат. Выход перхлората (Iб) 0,17 г (95%), т. пл. 240oC (DMCO - спирт).
Найдено, %: S 7,42; 7,45.
Вычислено, %: S 7,58.
Пример 4. S-Метилсульфониевые соли 3,5-дифенил-2-тиабицикло[4,4,0]декана (Iа, Iб) или 3,5-дифенил-2-тиабицикло[4,4,0]дец-5-ена (II) обладают высокой антимикробной активностью (см. табл.1).
Следует особо отметить, что названные S-метилсульфониевые соли проявляют высокую активность в отношении грамнегативной флоры, в том числе таких природоустойчивых бактерий, как протей и синегнойная палочка.
Высокая активность указанных соединений подтверждена на примере 2-метил-3,5-дифенил-2-тиониабицикло[4,4,0]деканиодида•AgJ на клинических штаммах бактерий, выделенных от больных гнойно-септическими заболеваниями (см. табл. 2).
Антимикробная активность исследованных солей превосходит активность химиопрепаратов - фуразолидона [2], левомицетина [3], обычно применяемых для лечения дизентерии, салмонеллезов и инфекций, обусловленных протеем и синегнойной палочкой.
Так, сравнительное исследование чувствительности 16 штаммов Shigella к левомицетину, фуразолидону и 2-метил-3,5-дифенил-2-тиониабицикло[4,4,0]деканиодиду•AgJ (Iа) показало, что к 12,5 мкг/мл левомицетина чувствительно только 2 штамма Shigella, для большинства же штаммов минимальная ингибирующая концентрация (МБсК) составляет 25 - 100 мкг/мл левомицетина. Все исследованные штаммы устойчивы к 100 мкг/мл тетрациклина. МБсК фуразолидона для большинства штаммов равны 12,5 мкг/мл. Тогда как 2-метил-3,5-дифенил-2-тиониабицикло[4,4,0] деканиодид•AgJ (Iа) подавляет рост всех 16 штаммов Shigella в концентрации 0,78 - 6 мкг/мл, причем для большинства штаммов эта концентрация равна 0,78 - 3 мкг/мл и только для одного 6 мкг/мл (см. табл. 3). \\2 Токсичность S-метилсульфониевых солей невысока. Белые мыши без каких-либо токсических проявлений переносят парентеральное (подкожное, внутримышечное и внутрибрюшинное) введение препаратов в дозах 250 - 300 мг/кг веса.

S-Метилсульфониевые соли 3,5-дифенил-2-тиабицикло[4,4,0]декана или дец-5-ена общей формулы
где символ  - одинарная или двойная связь, причем в случае одинарной связи X--AgJ
- одинарная или двойная связь, причем в случае одинарной связи X--AgJ
проявляющие антимикробную активность.
S-Метилсульфониевые соли 3,5-дифенил-2-тиабицикло [4,4,0] декана или дец-5-ена общей формулы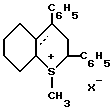
где символ  - одинарная или двойная связь, причем в случае одинарной связи X--AgJ
- одинарная или двойная связь, причем в случае одинарной связи X--AgJ
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Куликова Л.К | |||
| и др | |||
| Антимикробная активность конденсированных производных тиапирилия | |||
| Химико-фармацевтический журнал, 1976, N 1, с.73 - 75 | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| Рубцов М.В | |||
| и др | |||
| Синтетические химико-фармацевтические препараты | |||
| М.: Медицина, 1971, с.56 | |||
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Там же, с | |||
| Паровозный золотник (байпас) | 1921 |
|
SU153A1 |
Авторы
Даты
1998-07-10—Публикация
1977-04-01—Подача