Изобретение относится к синтезу дииодидов серебра S-метил-3-фенил-5R-2-тиониабициклоалканов, проявляющих антимикробную активность и ингибирующее действие в отношении антибиотико-резистентных стафилококка и кишечной палочки.
Указанное свойство позволяет предполагать возможность применения их в медицине.
Известны соли 2,4-дифенил-5,6,7,8-тетрагидрохромилия общей формулы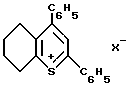
где X- - J- или ClO4 _,
обладающие антимикробной активностью [1].
Однако указанные соединения обладают незначительной антимикробной активностью.
Известны также S-метилсульфониевые соли формулы
которые являются близкими по структуре к новым соединениям, но отличаются наличием различных заместителей при C4 и размером алицикла, проявляющие антимикробную активность [2].
Целью изобретения является, во-первых, синтез веществ, обладающих высокой антимикробной активностью, в частности активных против таких природноустойчивых бактерий, как протей и синегнойная палочка, во-вторых расширение арсенала средств воздействия на живой организм.
Указанные свойства определяются новой химической структурой дииодидов серебра S-метил-3-фенил- 5R-2-тиониабициклоалканов, включающих S-метилсульфониевую группировку, общей формулы I
где
(I) R = H, n = 2; (II) R=CH2C5H5, n=2; (III) R=C6H4OCH3-4, n=2; (IV) R= C6H3(OCH3)2-3,4 n=2; (V) R=C6H5, n=1; (VI) R=CH2C6H5, n=1.
Указанные соединения общей формулы I получают взаимодействием 3-фенил-5R-2-тиабициклоалканов с иодистым метилом в присутствии 5-10%-ного молярного избытка азотнокислого серебра при охлаждении до 0oC в атмосфере азота
Пример 1. S-Метил-3-фенил-2-тиониабицикло[4,4,0] декан дииодид серебра (I).
В трехгорлую колбу емкостью 50 мл, снабженную механической мешалкой, газоподводной и хлоркальциевой трубками, вносят 20 мл иодистого метила и при охлаждении льдом в атмосфере азота добавляют 1 г 3-фенил-2-тиабицикло[4,4,0] декана - изомера с т.пл. 58 - 59oC. При энергичном перемешивании в реакционную смесь вносят 0,67 г азотнокислого серебра. Раствор перемешивают при комнатной температуре 1,5 - 3 ч. Затем реакционную смесь разбавляют эфиром. Выпавший осадок отфильтровывают и промывают на фильтре горячим хлористым метиленом. Из маточного раствора эфиром высаживают аналитический чистый S-метил-3-фенил-2-тиониабицикло[4,4,0] декан дииодид серебра (I), выход 2,34 г (количественный), т.разл. 52oC (хлористый метилен - эфир).
Найдено, %: S 5,17; 5,20.
C16H21AgJ2S
Вычислено, %: S 5,26.
В ИК-спектре сульфониевой соли I имеется полоса при 1415 см-1, соответствующая деформационным колебаниям метильной группы при гетероатоме.
Пример 2. S-Метил-3-фенил-5-бензил-2-тиониабицикло[4,4,0]декан дииодид серебра (IIа).
Опыт проводят, как описано в примере 1. Из 10 мл иодистого метила, 0,3 г 3-фенил-5-бензил-2-тиабицикло[4,4,0]декана - изомера с т.пл. 105 - 107oC - и 0,2 г азотнокислого серебра получают 0,58 г S-метил-3-фенил-5-бензил-2-тиониабицикло[4,4,0]декан дииодида серебра (IIa), выход количественный, т. разл. 130oC (хлористый метилен - эфир).
Найдено, %: S 4,32; 4,40.
C23H29AgJ2S
Вычислено, %: S 4,57.
В ИК-спектре сульфониевой соли IIa имеется полоса поглощения при 1410 см-1, соответствующая деформационным колебаниям метильной группы при атоме серы.
Пример 3. S - Метил-3-фенил-5-бензил-2-тиониабицикло[4,4,0]декан дииодид серебра (IIб).
Опыт проводят, как описано в примере 1. Из 10 мл иодистого метила, 0,2 г 3-фенил-5-бензил-2-тиабицикло[4,4,0] декана - изомера с т.пл. 94 - 96oC - и 0,1 г азотнокислого серебра получают 0,2 г (50%) S-метил-3-фенил-5-бензил-2-тиониабицикло[4,4,0]декан дииодида серебра (IIб), т. разл. 120oC (хлористый метилен - эфир).
В ИК-спектре S-метилсульфониевой соли IIб имеется полоса поглощения при 1410 см-1, соответствующая деформационным колебаниям метильной группы при атоме серы.
Пример 4. S-Метил-3-фенил-5-(4-метоксифенил)-2-тиониабицикло[4,4,0]декан дииодид серебра (III).
Опыт проводят, как описано в примере 1. Из 10 мл иодистого метила, 0,6 г 3-фенил-5-(4-метоксифенил)-2-тиабицикло [4,4,0]декана - изомера с т.пл. 121 - 122oC - и 0,5 г азотнокислого серебра получают 0,5 г (45%) S-метил-3-фенил-5-(4-метоксифенил)-2-тиониабицикло[4,4,0] декан дииодида серебра (III), т.разл. 99oC (хлористый метилен - эфир).
Найдено, %: S 4,43; 4,47.
C23H29AgJ2S
Вычислено, %: S 4,47.
В ИК-спектре S-метилсульфониевой соли III имеется полоса поглощения при 1410 см-1, соответствующая деформационным колебаниям метильной группы при атоме серы.
Пример 5. S-Метил-3-фенил-5-(3,4-диметоксифенил)-2-тиониабицикло[4,4,0] декан дииодид серебра (IV).
Опыт проводят, как описано в примере 1. Из 10 мл иодистого метила, 0,5 г 3-фенил-5-(3,4-диметоксифенил)-2- тиабицикло[4,4,0]декана - изомера с т.пл. 140 - 141oC - и 0,4 г азотнокислого серебра получают 0,65 г (65%) S-метил-3-фенил-5-(3,4-диметоксифенил)-2-тиониабицикло[4,4,0] декан дииодида серебра (IV), т. разл. 109oC.
Найдено, %: S 4,18; 4,19.
C24H31AgJ2O2S
Вычислено, %: S 4,49.
В ИК-спектре S-метилсульфониевой соли IV имеется полоса поглощения 1410 см-1, соответствующая деформационным колебаниям метильной группы при атоме серы.
Пример 6. S-Метил-3,5-дифенил-2-тиониабицикло[4,3,0]нонан дииодид серебра (Va, Vб).
Опыт проводят, как описано в примере 1. В реакцию берут 15 мл иодистого метила, 0,84 г 3,5-дифенил-2-тиабицикло[4,3,0]нонана с т.пл. 115 - 116oC и 0,6 г азотнокислого серебра. Через трое суток отделяют на фильтре осадок, который промывают сначала горячим хлористым метиленом, затем диметилсульфоксидом, собирая экстракты отдельно.
Из экстрактов хлористого метилена эфиром высаждают 0,74 г (42%) S-метил-3,5 - дифенил -2-тиониабицикло[4,4,0]нонан дииодида серебра (Va) - изомера с т.разл. 105oC.
Найдено, %: S 4,69; 4,73.
C21H25AgJ2S
Вычислено, %: S 4,76.
Из диметилсульфоксида водой высаживают 0,93 г (50,6%) изомера Vб с т.разл. 115oC.
Найдено, %: S 4,61; 4,65.
Вычислено, %: S 4,76.
В ИК-спектрах изомерных S-метилсульфониевых солей Vа и Vб имеются полосы поглощения при 1410 и 1415 см-1, соответствующие деформационным колебаниям метильной группы при атоме серы.
Пример 7. S-Метил-3-фенил-5-бензил-2-тиониабицикло[4,3,0]нонан дииодид серебра (VIа, VIб).
Опыт проводят, как описано в примере 6. В реакцию берут 12 мл иодистого метила, 0,47 г 3-фенил-5-бензил-2-тиабицикло[4,3,0] нонана с т.пл. 142 - 143oC и 0,45 г азотнокислого серебра. Из хлористого метилена эфиром высаждают 0,42 г (40%) S-метил-3-фенил-5-бензил-2-тиониабицикло [4,3,0]нонан дииодида серебра (VIб) - изомера с т.пл. 186 - 187oC.
Найдено, %: S 4,55; 4,48.
C22H27AgJ2S
Вычислено, %: S 4,67.
Из диметилсульфоксида водой высаждают 0,27 г (25%) изомера VIа с т.разл. 120oC.
Найдено, %: S 4,61; 4,58.
Вычислено, %: S 4,67.
В ИК-спектрах изомерных S-метилсульфониевых солей VIа, VIб имеются полосы поглощения 1410 и 1415 см-1, соответствующие деформационным колебаниям метильной группы при атоме серы.
Пример 8. Антимикробную активность исследуют методом двукратных серийных разведений в отношении следующих тест-микробов: St. aureus 209p, E. coli 675, Pr. vulgaris 477, Ps. pycceaneum 165, Cand. albicans 37.
Препараты растворяют в ДМФА (диметилформамид) из расчета 1:1000 с последующим разведением их стерильной дистиллированной водой. Данные испытаний представлены в табл.1.
Среди исследованных соединений предпочтительны соединения III и IV, поскольку они растворимы в воде, что при прочих равных условиях значительно расширяет границы их применения.
Следует также отметить, что исследованные соли I - VI проявляют высокую активность в отношении грамнегативной флоры, в том числе таких природоустойчивых бактерий, как протей и синегнойная палочка.
Высокая активность указанных соединений (I - VI) подтверждена на примере соединения III на клинических штаммах бактерий, выделенных от больных гнойно-септическими заболеваниями (см. табл.2).
S-Метилсульфониевые соли (I - VI) повышают чувствительность антибиотико-резистентных стафилококков и кишечных палочек, устойчивых к тетрациклину, хлорамфениколу, бензилпенициллину и стрептомицину [3], к названным антибиотикам (см. табл.3).
Коэффициент ингибирования устойчивости к антибиотикам колеблется от 2 до 66 и зависит от видовой принадлежности тест-микроба. Наибольшее ингибирование фенотипического проявления плазмидной устойчивости у E. coli K-12, R-19 отмечалось в отношении тетрациклина и хлорамфеникола, а для St. aureus 1074 - бензилпенициллина.
Обнаруженная способность дииодидов серебра S-метил-3-фенил-5R-2-тиониабициклоалканов повышать чувствительность микроорганизмов к антибиотикам за счет ингибирования фенотипической экспрессии внехромосомных генов антибиотико-резистентности делает предлагаемые соединения весьма перспективными в борьбе с лекарственной устойчивостью микроорганизмов.
Токсичность S-метилсульфониевых солей I - VI невысока. Белые мыши без каких-либо токсических проявлений переносят парентеральное (подкожное, внутримышечное и внутрибрюшинное) введение препаратов в дозах 250 - 300 мг/кг.


Дииодиды серебра S-метил-3-фенил-5R-2-тиониабициклоалканов общей формулы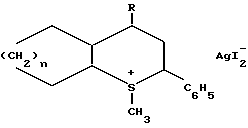
где
(I) R = H, n = 2;
(II) R = CH2C6H5, n = 2;
(III) R = C6H4OCH3-4, n = 2;
(IV) R = C6H3(OCH3)2-3,4, n = 2;
(V) R = C6H5, n = 1;
(VI) R = CH2C6H5, n = 1,
проявляющие антимикробную активность и ингибирующее действие в отношении антибиотико-резистентных стафилококка и кишечной палочки.
Диодиды серебра S-метил-3-фенил-5R-2-тиониабициклоалканов общей формулы
где
(I) R = H, n = 2;
(II) R = CH2C6H5, n = 2;
(III) R = C6H4OCH3-4, n = 2;
(IV) R = C6H3(OCH3)2-3,4, n = 2;
(V) R = C6H5, n = 1;
(VI) R = CH2C6H5, n = 1,
проявляющие антимикробную активность и ингибирующее действие в отношении антибиотикорезистентных стафилококка и кишечной палочки.
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Куликова Л.К | |||
| др | |||
| "Антимикробная активность конденсированных производны х тиапирилия", Химико-фармацевтический журнал, 1976, N 1, с | |||
| Способ подготовки рафинадного сахара к высушиванию | 0 |
|
SU73A1 |
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
| СПОСОБ ПРОИЗВОДСТВА КОНСЕРВОВ "ТРЕСКА ОБЖАРЕННАЯ С МОРКОВЬЮ И ФАСОЛЬЮ В ТОМАТНОМ СОУСЕ" | 2011 |
|
RU2467621C1 |
| Способ восстановления хромовой кислоты, в частности для получения хромовых квасцов | 1921 |
|
SU7A1 |
| Переносная печь для варки пищи и отопления в окопах, походных помещениях и т.п. | 1921 |
|
SU3A1 |
| Машковский М.Д | |||
| Лекарственные средства, М., Медицина, 1972, ч.II, с | |||
| Ножевой прибор к валичной кардочесальной машине | 1923 |
|
SU256A1 |
Авторы
Даты
1998-07-10—Публикация
1977-07-12—Подача