1
Изобретение относится к способу получения новых производных 6-амиHo-sp, 19-циклоандростана общей формулы I
Y
R.O
где Rj метил или ацетил;
9-СНг
у - СО-или 6 I -групп -СНг
Rj- водород или линейная, или разветвленная, незамещенная или замещенная гидроксильной или Сг -алкоксигруппой, Cg-алкильная группа; Cj- Cg-алиииклическая группа, аллильная группа или бензильная группа;
водород или линейная Су-алкильная группа,
Rjвместе с атомом азота образуют пирролидинр-, пиперидине-, морфолино-, пиперазйно-, N-алкилпиперазино-, N-оксиалкилпиперазиноили N-бензилпиперазино группу.
или их солей, обладающих биологической активностью.
В литературе описан способ получения производных 6-аминоциклоандростанов, заключающийся в получении ИЗ соответствующего оксосоединения оксима, его восстановления .и ацилирования 1, однако, отсутствуют какие-либо сведения о получении соединений общей формулы I.
Соединения общей формулы I обладают некоторыми преимуществами по своему действию по сравнению с известными соединениями.
. Целью изобретения является рас-: ширение ассортимента соединений с биологической активностью и-получение воцеств общей формулы I.
. Способ согласно изобретению заключается в том, что соединения общей формулы II
Н(-$Ог-0-СНг1 j
HiO-4..,
где R и У имеют указанные значения;
R4.- алкильная группа или толильная группа, подвергают взаимодействию с первичным или вторичным амином общей формулы III -Кг ги, ныСГ где Кги Кз имеют указанные знйчения при 50-18О с и мольном соотношении исходных продуктов, равном соответственно 1:2-20 в течение 1-20 ч. Процесс проводят предпочтительно в полярном органическом растворителе, таком как Ы,Ы-димётилформамид, N,N-димeтилaцeтaмид, или алифатический Cg-C -спирт, при температуре предпочтительно 50-180 С, предпочтительно в течение 1-10 ч, целевые продукты выделяют известными приемами в свободном виде или виде соли. Пример 1. Перхлорат 3 р) -ацетокси-б -диметиламино.-17-ОКСО-5 р-циклоандростана 5,00 г (0,01 моль) 3/5-ацетокси-17-ОКСО-19-ТОЗИЛОКСИ- д 5-андростена и 20 мл безводного К,Ы-диметилацетамида, содержащего 22 вес,% диметиламина, нагревают в запаянной трубке до 110 С и ВЕадержив-ают при этой температуре в течение 7 ч. После нагревания содержимое запаянной трубки выливают в 400 мл ледяной йоды и перемешивают в течение 15 мин Образующийся осадок отфильт ровывают, промывают водой, а затем растворяют в 150 мл бензола. Бензольный раствор промывают водой, высушивают и выпаривают под вакуумо После растворения остатка в 20 мл безводного этанола раствор нейтрал зуют этанолом,содержащим хлорную ки оту,Раствор после вьщерживания в т ||ение 2 ч при О-(-5) С фильтруют, кристаллическое вацество промывают безводным этанолом и высушивают по вакуумом при 60 С. Выход 1,70 г, т.пл, 200-203с; после перекристал лизации из метанола т,пл.208-209°С П р и м е р 2. Перхлорат 3 --ацет си-6 -диэтиламино-17-оксо-5р-19 -циклоандростана 10 г (0,02-моль) 3 р -aцeтoкcи-1 roкco- 9-тoзилoкcи- Д 5-андростена и 25 мл (0,24 моль) свежеперегнанного диэтиламина нагревают запаянной трубке до 130с и выде в живают при этой температуре.в тече ние 5 ч. После охлаждения реакцион ную смесь выпаривают под вакуумом, остаток растирают вместе с 50 мл бензола. Образунвдийся осадок отфильтровывают и промьшают бензолом. Объединенные фильтраты промывают водой, высушивают и выпаривают под вакуумом. Полученное вязкое масло растворяют в 20 мл безводного этанола и нейтрализуют хло ной кислотой, содержащей этанол. После вьщерживания раствора.в тече ние нескольких часов образующиеся кристаллы фильтруют, промывают безводным этанолом и высушивают под вакуумом при 60°С. Продукт весит 3,20 (32%), т.пл. 181-183С, после перекристаллизации из метанола т.пл. 184-185 0. П р и м е р 3. Перхлорат Эр -ацетокси-6 -пиперидино-17-оксо-5 р, 19-циклоандростана , . А. 20 г (0,04 моль) Зр-ацетокси-17-ОКСО-19-ТОЗИЛОКСИ- д 5-андростена растворяют при нагревании в 20 мл (0,2 моль) свежеперегнанного пиперидина, затем реакционную смесь кипятят с обратным холодильником в ; течение 5 ч на масляной бане при 150°C. После охлаждения избыток пип еридина отгоняют под вакуумом и остаток от выпаривания растирают вместе с 50 мл бензола. Вьтадакнцую в осадок пиперидиновую,соль отфильтровывают и промывают (2x10 мл) бензолом. Следы пиперидина удаляют из ильтрата встряхиванием его с водой. Бензольную фазу высушивают сульфатом натрия, затем выпаривают под вакуумом. Полученное вязкое масло растворяют в 20 мл безводного этанола, а раствор нейтрализуют хлорной кислотой, содержащей этанол. После выдерживания раствора в течение 2 ч образующиеся кристаллы отфильтровывают и промывают некоторым количеством безводного этанола. После высушивания продукта в вакууме при выход 10,5 г (51%),т.пл. 20б-210С,после перекристаллизации из метанола т.пл. 2l4-2l6 c. Т пл. малеината 20 -205°С (из этанола). Б. 20 г (0,04 моль) Зр-ацетокси-17-ОКСО-19-ТОЗИЛОКСИ- Д 5-андростена растворяют в 200 мл безводного диметилформамида и добавляют 12 мл (0,12 моль) свежеперегнанного, пиперидина. После нагревания реакционной смеси до ее выдерживают при этой температуре в течение 10 ч, затем выпаривают досуха в вакууме. Далее поступают согласно методике А. Продукт идентичен проДУКту из метода А, выход 41%. В. 20 г (0,04 моль) Зр-ацетокси-17-ОКСО-19-ТОЗИЛОКСИ- Л 5-андростена растворяют в 80 мл безводного изопропанола, затем добавляют 12 мл (0,12 моль) свежепёрегнанного пиперидина. После кипячения с обратным холодильником в течение 3ч реакционную смесь охлаждают и выпаривают досуха под вакуумом. Далее поступают согласно методике А. Продукт идентичен с продуктом метода А, выход 40%. П р и м е р 4. Хлоргидрат 3/3-ацетокси-б-| (N-метилпиперазино) -17-ОКСО-5Р -19-циклоандростена.
Исходя из 20 г {0,04 моль) Зр-ацетокси-17-оксо-19-тоэилокси- д5-андростена и 20 мл N-метилпиперазина, реакцию проводят точно так же как это представлено в методе А примера 3, однако продукт выделяет в виде хлоргидрата. Выход 9,00 г (48%), т.пл. 213-215С. П р и м е р 5, Перхлорат 3 -.ацетокси-б ё морфолино-17-оксо- 5 ( -19-циклоандростана
Исходя из 20 г (0,047 моль) 3 р-ацетокси-17-рксо-19-мезилокси-д5-андростена и 20 мл (0,23 моль) свежеперегнанного морфолина, проводят реакцЙ1о так же, как это представлено в методе А примера 3 и получают продукт с выходом 11,80 г (49%), т.пл. 202-204°С, после перекристаллизации из смеси метанола и воды т.пл. 202-208°С, т.пл. хлоргидрата 214-217 С (из этанола).
П р и м е р 6. Хлоргидрат 3 р-ацетокси-6 -трет.бутиламино-17-оксо-5р -19-циклоандростана.
10 г (0,02 моль) Зр-ацетокси-17-оксо-19-тозилокси- д 5-андростена и 22 мл (0,21 моль) свежаперегнанного трет бутиламина нагревают в запаяннойтрубке до и выдерживают при этой температуре в течение 5ч, Затем реакционную смесь обрабатывают так же, как это описан в примере 2, однако с тем отличием, что остаток, полученный после вцпаривания досуха бензольного раствора растворяют в безводном эфире и хлоргидрат получают с помощью безводного эфира, насЕлденного сухим газообразным водородом. Выход 3,9 г (45%),т.пл. 207-208с, после перекристаллизации из безводного этанол т.пл. 208-210с.
П р и м е р 7. Хлоргидрат 3 р-ацетокси-6 Ц -бензиламино-17-этилендиокси-5р, 19-циклоандростана
1,00 г (1,84 ммоль)3 -ацетокси-17-этилендиокси-19-тозилокси- Д5-адростена растворяют в 3,00 мл Ы,М-дйметилацетамида и 1,00 мл (9,10 ммоль) свежеперегнанного бенэиламина путем нагревания, затем реакционную смесь нагревают до 110 С и выдерживают при этой температуре в течение 3,5 ч. После охлаждения гомогенный раствор приливают медленно при непрерьшном перемешивании к 150 мл ледяной воды, затем осадок, образующийся после перетлешиагшия в течение 15 мин отфильтровывают, растворяют в 60 мл бензола и промЁвают водой После высушивания раствор выпаривают в вакууме, остаток растворяют в 15 мл безводного этанола, нейтрализуют этанолом, насыщенным сухим газообразным хлористым водородом, и выпаривают досуха в вакууме при температуре не выше 50с. Полученное вязкое масло становится кристаллическим при растирании вместе с небольшим количеством ацетона. Кристаллы фильтруют, промывают ацетоном и высучивают в вакууме при 60°С, получая при этом 0,45 г (44%) продукта, т.пл. 234-236 С, после перекристаллизации из метанола, т.пл. 239-241с.
Пр и м е р 8. Хлоргидрат 3 р -ацетокси-б -циклогексиламино-17-этилендиокси-5 р, 19-циклоандростана.
1,00 г (1,84 ммоль) 3р.-ацетокси-17-этилендиокси-19-тозилокси- Д 5-гандростена растворяют при нагрева ии в 3,00 мл Ы,М-диметилацетамида и 1,00 мл (8,74 ммоль) евёжеперегнанного циклогексиламина. Реакционную смесь нагревают до и выдерживают- при этой температуре
в течение 2,5 ч.
В последующем реакционную смесь обрабатывают так же, как и в примере 8. Выход-0,50 г (50%), т.пл. 21В-220с, после перекристаллизации из смеси ацетона и гексана т.пл. 224-227 с.
Пример9, Хлоргидрат 3 р -ацетокси-17-этилендиокси-6 -циклог пропиламино-5 р -19-циклоандростана
10 г (18,4 ммоль) 3 |г-aцeтoкlCи-17-этилeндиoкcи- 9-тoзилoкcи- Л 5-андростена и 6,4 мл (92 ммоль) свежеперегнанного циклопропиламина растворяют при слабом нагревании в 50 мл N,N -диметилацетамида. Полученный растйор подогревают до и выдерживают при этой температуре в течение 5ч, После охлаждения раствор медленно приливают при постоянном перемешивании к 1.л ледяной воды «Выделяющийся Осадок быстро отфильтровывают ,прО1Мывают водой и растворяют в 150 мл бензола. Бензольный раствор промывают водой, высушивают сульфатом натрия и выпаривают досуха под вакуумом. Остаток от перегонки растворяют в 30 мл эфира и нейтрализуют рфиром, насыщенным сухим газообразным хлористым водородом. Выпадакадий осадок отфильтровывают, промывают эфиром, петролейным эфиром и высушивают под инфракрасным облучением. Полученный таким образом неочищенный продукт (4,80 г) суспендируют в бензоле, фильтруют, промывают смесью 1:1 из бензола и петролейного эфира и высушивают при в вакууме. Выход 3, (44%), т.пл. 212-214 С,после перекристаллизациииз изопропанола т.пл. .218-220 Со
Пример 10. Хлоргидрат 3 -ацетокси-6f -(2-оксиэтиламино)-17-этилендиокси-5 Э-19-циклоандростана
1,00 г (1,84 ммоль) 3 -ацетокси-17-этилендиокси-19-тозилокси- Д 5-андростена растворяют путем .нагревания в 5 мл Н,Ы-диметилацетамида и 0,5 мл (8,40 ммоль) свёжеперегнанного 2-оксиэтиламина, Реакционную смесь нагревают до и выдерживают при этой температуре в течение 5 ч. После охлаждения раствор медленно приливают при непрерывном перемешивании к 50 мл 26%-ного водного раствора хлористого натрия и перемешивают в течение 15 мин. Образующийся осадок фильтруют и растворяют в 30 мл бензола. Бензольный раствор промывают насыщенным водным раствором хлористого натрия, высушивают сульфатом натрия и выпаривают досуха в вакууме. Остаток растворяют в 10 мл безводного этанола и нейтрализуют этанолом, насыщенным сухим газообразным хлористым водородом. Нейтральный раствор выпаривают досуха в вакууме и остаток растирают вместе с ацетоном. Образующиеся кристаллы фильтруют, промывают ацетоном и высушивают в вакууме при 60°С, получая -при этом 0,35 г (40%) продукта с т.пл. 119-202°С, после перекристаллизации из ацетона, т.пл. 203 20бс
Пример. Хлоргидрат 3fi -ацетокси-.17-оксо 6 6 -аллиламино-5| , 19-циклоандростана.
5,44 г (0,01 моль) 3 -ацетокси-17-этилендиокси-19-тозилокси- Д5-андростена и 3 мл (0,04 моль) свежперегнанного аллиламина растворяют при слабом нагревании в 20 мл безводного Ы,Н-диметилацетамида. Температуру раствора повышают до 110°С и вьздерживают при этой температуре в течение 2,5 ч. После этого реакционную смесь охлаждают до комнатной температуры и приливают по каплям 200 мл леДяной воды при энергичном перемешивании. Выпадающий осадо быстро отфильтровывают, а затем растворяют бензолом прямо на фильтр Бензольный раствор промывают водой, высушивают сульфатом натрия н выпаривают под вакуумом. Остаток растворяют в бензводном этаноле. рН раствора доводят до величины 4 с помощью этанола, насыщенного сухим газообразным хлористым водородом, и раствор оставляют стоять в течение ночи при комнатной температуре. После этого его выпаривают досуха при . в вакууме. Остаток является в язким маслом, который становится твердым при растирании вмесгге с эфиром. Неочищенный продукт от- фильтруют,промывают эфиром и высушивают под инфракрасным излучением Выход 2,00 г (47,5%), т.пл. 208211 С, после перекристаллизации из изопропанола т.пл. .
Пример12. Хлоргидрат 3/3-ацетокси-17-оксо-6 -пиперидино-5р 19 циклоандростана.
5 г (0,013 моль) 3 И-метокси-17-оксо-19-мезилокси- д5-андростена растворяют при слабом нагревании в 15 мл безводного Ы,Ы-диметилацетамида и 5,2 мл (9,052 моль) свежеперегнанного пиперидина. Реакционную смесь наг{эевают до ИО°С и выдерживают при этой температуре в течение 4ч. После охлаждения раствор медленно приливают при
постоянном перемешивании к 500 мл ледяной воды. После перемешивания в течение 10 мин выделяющийся осадок отфильтровывают и растворяют в 100 мл бензола. Бензольный раствор промывают водой, высушивают
сульфатом натрия и выпаривают в вакууме. Остаток растворяют в 20 мл безводного этанола и нейтрализуют этанолом, насыщенньм сухим газообразным хлористым водородом. Нейтральный раствор выпаривают досуха
в вакууме и остаток растирают вместе с бензолом. Затвердевший продукт промывают некоторым количеством
0 бензола и посла этого смесью из ацетона и петролейного эфира (1:1), затем высушивают.в вакуум-эксикаторе при . выход 2,70 г (51%), т.пл. 217-220с, после. перекристаллизации из изопропанола т.пл. 2 2-224°С.
Пример 13. 3 р -Ацетокси-6 -амино-17-этилендиокси-5р, 19-циклоандростангидрохлорид.
5,0 г (9,1 ммоль) Зр -ацетокси-17-этилендиокси-19-тозилокси- А 50-андростена и 20 мл безводного Н,Ы-диметилацетамида, который содержит 25 вес.% аммиака, нагревают в тугоплавкой трубке до 10°С и выдерживают в течения 4 ч при этой температуре. После охлаждения тугоплавкую трубку вскрывают и испаряют большую часть непрореагировавшего аммиака. Оставшийся раствор выливают в 400 мл ледяной воды. Выпавший осадок отфильтровывают, промывают водой, и затем растворяют в 150 мл бензола. Бензольный раствор промывают водой,высуши вают и выпаривают в вакууме. Остаток растворяют в 20 мл безводного этанола, нейтра5лизуют с помощью этанола, насыщенного сухим газообразнБи хлористым водородом, и выпаривают в вакууме. Получают аморфное вещество, которое перекристаллизуют из изопропано т.
0 Выход 1,70 г (43%), т.пл. 189-192 С.
Пример 14. Зр -Ацетокси-6 -пирролидино-17-оксо- 5 (%, 1 Э-циклЬанростан НСЮ.
5,0 г (0,01 моль) 3(5-ацетокси-17-оксо-19-тозилокси- Л5-андростена растворяют в 15 мл безводного N,N- иметилацетамидаи 3 мл (0,04 моль) свежеперегнанного пирролидина при
нагревании. Реакционную смесь нагревают до и выдерживают при этой температуре в течение 4 ч. После охлаждения раствор при постоянном перемешивании медленно выливают в 250 мл ледяной воды. Выпавший
осадок отфильтровывают и растворяют в 100 мл бензола. Бензольный раствор промывают водой, высушивают и выпаривают в вакууме. Остаток раст воряют в 10 мл безводного этанола и padTBOp нейтрализуют этанольным раствором хлорной кислоты. Вьаделив шиеся кристаллы отфильтровывают и промывают небольшим количеством безводного этанола. После высушива вания в вакууме при 60 С получают 5,35 г (44,5%) продукта, т.пл. 226 228-С, после перекристаллизации из метанола, т.пл. 229-23lc. Гидрохлорид - т.пл. 244-247°С (из изопропанола). Пример15. 3| 1-Ацетокси-6 -N- (2-оксиэтил)-пиперазино-17-оксо -5р, 19-циклоандростан-гидрохлорид Следуют методике примера 14 с тем отличием, что используют в качестве исходных веществ 5,0 г (0,01 моль) Зр|-ацетокси-17-оксо-19 -тозилокси-А 5-антростена и 5 мл (0,04 моль) 4-(2-оксиэтил)-пиперазина и продукт выделяют в виде солянокислой соли. Выход 2,1 г (42,5%), т.пл. 19б-198с, После перекристаллизации из изо пропанолат.пл. 203-2С5°С. Пример 16°. Зр-Ацетокси-6 -Ы-бензилпиперазино-17-оксо-5р , 19-циклоандростан-гидрохлорил. Следуют методике примера 14 с т отличием7 что в качестве исходньрс соединений используют 5,0 г (0,01 моль) З ацетокси-17-оксо-1Э-ТОЗИЛОКСИ- 5-андростена и 5,2 (0,03 моль) -N-бензилпиперазина и продукт выделяют в виде его соляно кислой соли. Выход 2,40 г (44,5%),т.пл, 222224 0. Перекристаллизовывают из из прюпанола, т.пл. 226-229°С. Пример 17. Зр-Ацетокси-6 -изопропиламино-17-оксо-5 jb , 19-ци лоандростан-гидрохлорид . Следуют методике предыдущего пр мера 16 с тем отличием, что в качестве исходных соединений используют 5,0 г (9,2 ммоль) 3 | -aцeтoкcи -17-этилeндиoкcи-19-т(5§илoкcи-д5-aдpocтeнa и 16 мл (184 моль) изопропиламина и продукт получают в виде его солянокислой соли в безводном этаноле с помощью этанола, насыщенного сухимгазообразным хло ристым водородом, при рН 4. Выход 1,7 г (43,5%), т.пл. 200-202°С-. После перекристаллизации из смеси ацетона с гексаном т.пл. 203-205°С Пример 18, 3 (Ъ -Ацетокси-6 -(2-метоксиэтил)-амино-17-оксо -5р, 19-циклоандростан-гидрохлори Следуют методике примера 11 с тем отличием, что в качестве исходных веществ используют 1,00 Г (1,84 мм 3 J -ацетокси-17-этилендиокси-19-тозилокси- Д.5-андростена и 0,7 м.п (6,60 ммоль) 2-метоксиэтиламина. 10 Выход 0,43 г (53%), т.пл.218-222с. После перекристаллизации из изопропанола т.пл, 226-227°С. П г и м е р 19. 3 р -Метокси-6 -амино-17-оксо-5 Ь, 19-циклоандростан-гидрохлорид. Следуют методике примера 13с тем отличием, что в качестве исходных веществ применяют 5,0 г((0,01 .моль) 3 р -ацетокси-17-этилендиокси-19мезилокси-л 5-андростена и 20 мл безводного Ы,Ы-диметилацетамида, который содержит 25 вес.% аммиака, и солянокислая соль образуется при значении рН 4. Выход 1,70 г (48%), т.пл. 162-165 С. После перекристаллизации из изопропанола т.пл. 164-166°С. Пример 20. 3 р -Метокси-6 -диэтиламино-17-оксо-5 р, 19-циклоандростан-гидрохлорид. Следуют методике примера 12 с тем отличием что в качестве исходных веществ применяют 5,0 г (0,01 ммоль) 3J -метокси-17-оксо-19-мезилокси- Д5-андростена и 5,3 мл (0,05 моль) диэтиламина. Выход 2,80 г (52,5%), т.пл, 184186 С. После перекристаллизации из смеси ацетона с гексаном т.пл, 18б-188°С. , Пример 21. 3(5 -Метокси 6 -бензиламино-17-этилендиокси-Ь р , 1У-циклоандростан-гидрохлорид. Следуют методике примера 12 с тем отличием, что в качестве исходных веществ используют 5,0 г (0,01 моль) 3 Р)-мeтoкcи-17-этилeндикocи-19-мeзилoкc k- Д5-андростена и 5 мл (0,04 моль) бензиламина и продукт выделяют из этанола. Выход 2,95 г (54,6%), т.пл, 216-218с. После перекристаллизации из этанола т.пло 222 224С. Формула изобретения 1„ Способ получения производных 6-амино-5 р, 19-циклоандростана общей формулы Т JC гжг де jмeтил или ацетил; О-СИ 2 А/ I - SCO- или - группа; Ь-СНг R2- водород или линейная, или разветвленная, незамещенная или замещенная гидроксильной или С,алкоксигруппой, С алкильндя группа; Cj- С -алициклическая группа, аллильная группа или бензильная группа; R- - водород или линейная Су-алкильная группа, R вместе с атомом азота образуют пирролидино-, пиперидино-, морфолино-, пипераэино-/ N-aлкилпипepa-5 ЗИНО-, N-оксиалкилтгаперазино или N-бен3илпипера3иногруппу, или их Ьолей, о тличающийся тем, что, стероид общей формулы П R,-$Ot-0-(iHt где R и У имеют указанные значения; R CY - С4-алкильная группа или толильная группа, подвергают взаимодействию с первич680650 15 20 12 ным или вторичным амином общей формулы III R,имеют указанные значе депри 50-180°с и мольном соотношении исходных продуктов, равном соотретственно 1:2-20, с последующим выделением целевого продукта в свободном виде или в виде соли. 2f Способ ПОП.1, отличающийся тем, что процесс проводят в полярном органическом растворителе, таком как N,Ы-димeтилфopмамид, Ы,Ы-диметилацетамид или алифатический Су-спирт. Источники информации, принятые во внимание при экспертизе 1. Патент США №3189606, кл. 260-239.55, опублик. 15.06.65.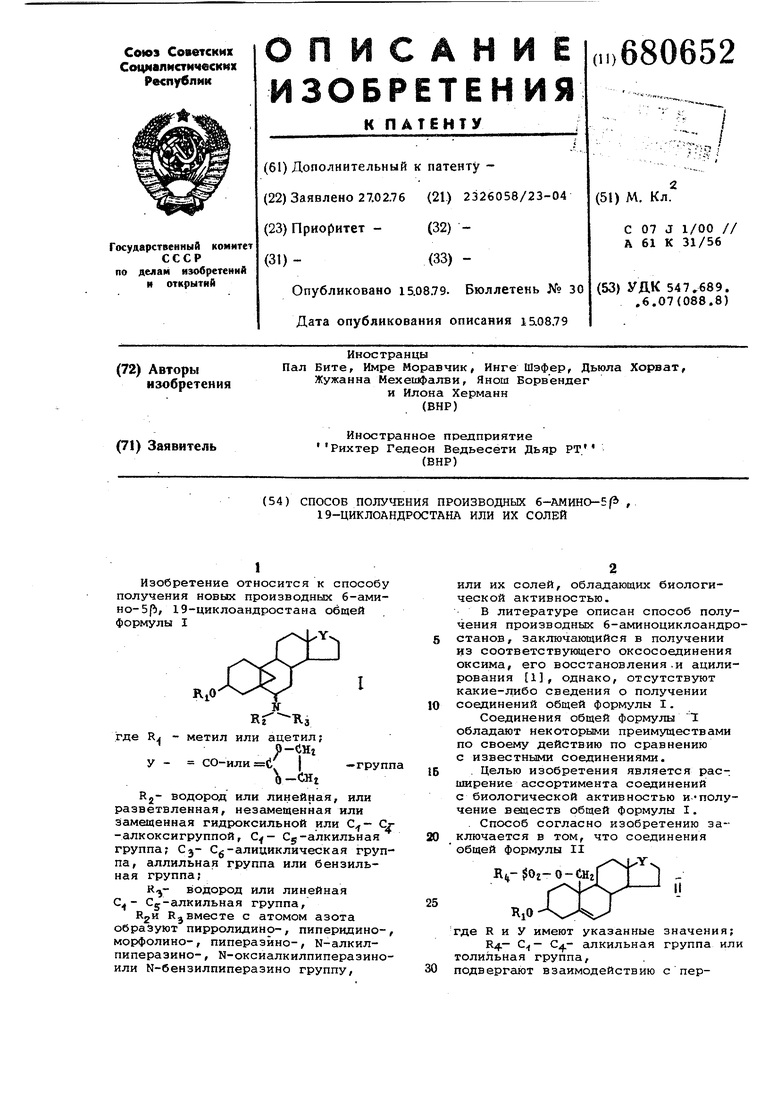





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных стероидспирооксатиазолидинов в виде их стереоизомеров или их смесей или их солей | 1981 |
|
SU1079177A3 |
| Способ получения стероидных спирооксазолидинов или их стереоизомеров | 1978 |
|
SU931109A3 |
| Способ получения производных стероид-СпиРО-ОКСАзОлидиНОНА | 1979 |
|
SU852176A3 |
| Способ получения 5 ,17 -диацетокси6 -хлор-2 ,3 ,16 ,17 диэпоксиандростана | 1976 |
|
SU612635A3 |
| Способ получения производных 1,1,2-трифенилпропена или их стереоизомеров,или смеси стереоизомеров,или их кислотно-аддитивных солей | 1980 |
|
SU1253426A3 |
| Способ получения производных 16-амино-18,19,20-тринор-простагландина или их кислотно-аддитивных солей | 1981 |
|
SU1093244A3 |
| Способ получения 17 оксалилстероидов | 1974 |
|
SU602120A3 |
| Способ получения производных 1,1,2-трифенилпропена в виде смеси изомеров или трансизомера,или их солей | 1981 |
|
SU1114332A3 |
| Способ получения производных 1,1,2-трифенилпропана или 1,1,2-трифенилпропена, или стереоизомеров, или смеси стереоизомеров, или их гидрохлоридных солей | 1981 |
|
SU1097192A3 |
| Способ получения 1- @ 2-(5-(ди-метиламинометил)-2-(фурилметилтио)-этил) @ амино-1-(метиламино)-2-нитроэтилена или его гидрохлорида и способ получения дигидрохлорида 2-(2-аминоэтил)-тиометил-5-(диметиламинометил)-фурана или его моногидрохлорида | 1984 |
|
SU1384197A3 |


Авторы
Даты
1979-08-15—Публикация
1976-02-27—Подача