литийтри-- 7С/ -бутилборгидрида в, нейтральной среде или натрийцианборгидрида в сильпокислой области значений рН и выделяют целевой продукт в свободном виде, или в виде соли,
или в виде стереоизомеров, или соединение формугш I, где R и Rg водород, переводят в соединение 1, где R-, - водород . или С - С.-алкил и Rg - С - Сс--алкил.








| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 3-амино-1-бензоксепин-5/2н/-она или их солей | 1980 |
|
SU955860A3 |
| Способ получения производных 2,3,4,5-тетрагидро-1-бензоксепин-3,5-диона | 1981 |
|
SU963468A3 |
| Способ получения (1,2)-анеллированных 1,4-бензодиазепинов или их оптических изомеров или кислотно-аддитивных солей | 1982 |
|
SU1331431A3 |
| Способ получения 1-фенил-2-аминокарбонилиндольных соединений или их кислотно-аддитивных солей | 1983 |
|
SU1223843A3 |
| Способ получения производных @ -аминоалкилиндола или их солей | 1980 |
|
SU1119606A3 |
| Способ получения 2-ациламинометил-1 @ -2,3-дигидро-1,4-бензодиазепиновых соединений,а также их оптических изомеров и их солей кислотного присоединения | 1982 |
|
SU1245259A3 |
| Способ получения /1,2/-аннелированных 7-фенил-1,4-бензодиазепинов или их солей | 1979 |
|
SU904526A3 |
| Способ получения 1-фенил- 2-аминокарбонилиндольных соединений или их солей присоединения кислот | 1982 |
|
SU1195903A3 |
| 1,7-АНЕЛЛИРОВАННЫЕ ПРОИЗВОДНЫЕ 3-(ПИПЕРАЗИНОАЛКИЛ)-ИНДОЛА, СПОСОБ ИХ ПОЛУЧЕНИЯ (ВАРИАНТЫ), СОДЕРЖАЩАЯ ИХ ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И ПРОМЕЖУТОЧНЫЙ ПРОДУКТ ДЛЯ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2083580C1 |
| Способ получения 2-ациламинометил-1Н-2,3-дигидро-1,4-бензодиазепинов или их солей присоединения кислот | 1980 |
|
SU1253430A3 |
.Способ получения производных З-амино-1-бензоксёпина общей формулы I V ..в R где R и Rj, независимо друг от друга - водород, С -С -алкил, незамещенный или замещенный фенилом, или Сл - Си-алкил, содержащий на концах в качестве заместителей метоксильные остатки, или один из Rxj и R j, - водород или С - С -алкил, а другой из лих - С2 - Са-алкил, имеющий на конце в качестве заместителя группу - В которой К и Rg независимо друг от друга - водород или С - Сс-алкил, или R и R, вместе с атомом азота, с которым они связаны, образуют пирролидиновое, пиперидиновое или морфолиновое кольцо; один из Нз и R4 - водород, а другой из них - оксигруппа,. или оба R и R совместно - кислород; Rg- и R независимо друг от друга - водород или галоген, С - С -алкил или С С -алкоксигруппа, или их стереоизомеров, или их солей, о т л и ч. а и и с я тем, что производное 3-амино-1-бензоксепинона-5

Изобретение относится к способу лолучени.я новых соединений: производных З-амино-1-бензоксепина общей формулы где R, и 5 независимо друг от друга водород, С - С5 алкил, незамещенный или яамещенный фенилом, или С - С -алкил, содержащий на концах в качестве заместителей метоксильные остатки, или один из R;, и R,,, - водород или Ц - С -алкил, а другой из них С2 С -алкил, имекхций на конце в качестве заместителя группу в которой Rf и К g независимо друг от друга - водород или С - Сд--алкил или R и R вместе с атомом азота, ,с которым они связаны, образуют пирролидиновое, пиперидиновое или морфолиновое кольцо; один из R и R водород, а другой из них - оксигруппа, или оба Rt- и R совместно кислород; Rg- и R независимо друг от друга - водород или галоген, С Сф-алкил или С - С4-алкоксигруппа, или их стереоизомеров, или их солей. Эти соединения обладают фармакологической активностью, оказывая хорошее действие на подвижность мышц желудка. Известен способ получения 2-этил-4-оксихромана или 2-этилхромана каталитическим восстановлением 2-этилхромена в присутствии никеля РенеяГ Цель изобретения - получение новы производных З-амино-1-бензоксепина общей формулы I, обладающих ценными биологически активными свойствами. Указанная цель достигается способом, который заключается в том, что производное З-амино-1-бензоксепинона -5(2Н) общей формулы « (Д). 1 имеют указанные RF 6 где Н , R значения. подвергают восстановлению боргидридом натрия при рН 4-7 или натрийцианборгидридом при рН 3-4 при температуре от до температуры окружающей среды или каталитическому гидрированию водородом в присутствии никеля Ренея, предп4)чтительно при давлении водорода 2-150 бар, в среде протонного растворителя, предпочтительно этанола или изопропанола, и выделяют целевой продукт формулы I, где R - водород и R. - оксигруппа, в свободном виде, или в виде соли, или в виде стереоизомеров, или соединение формулы II подвергают восстановлению натрийцианборгидридом при рН 4-6 при температуре от (f С до температуры окружающей среды или каталитическому гидрированию водородом, предпочтительно при давлении водорода 50-150 бар, в присутствии никеля Ренея в среде апротонного растворителя, предпочтительно толуола или бензола, и выделяют целевой продукт форму ты I, где R и R совместно - кислород, в свободном виде или в виде соли, или переводят его в соединение формулы I, где R - водород и R - оксигруппа, действием натрийборгидрида, литийборгидрида, литийалюмогидрида, натрий- 5к -(2-метоксиэтокси)-алкмогидрида или литийтри-й 7С1 -бутилборгидрида в нейтральной среде или натрийцианборгидрида в сильнокислой области значений рН и выделяют целевой продукт в свободном виде, или в виде соли, или в виде стереоизомеров, или соединение формулы 1, где R7 и Rg - водород, переводят в соединение формулы Т, где R-, - водород или Q - С -алкил и R0, - Q - С -алкил. Производные З-амино-1-бензоксепина формулы 1, в которых один из двух остатков R и R представляет собой атом водорода, а другой из них обозначает гидроксильную группу, могут быть разделены на рацематы с и,ис- кяктранс -конфигурацией карбинольного остатка и аминоостатка. Соединения формулы 1 содержат по крайней мере один хиральный атом углерода и находятся в D- или L-форме, а также в виде рацемической .
В одну стадию происходит гидрирование двойной связи, расположенной в положении 3, 4,и восстановление 5-кетогруппы, в расположенную в положении 5 гидроксильную группу в том случае, когда соединение формулы П восстанавливают боргидридом натрия . в нейтральной или слабокислой среде, в особенности в области значений рН от 4 до 7, или цианборгидридом натрия S кислой среде/ преимуществен но при значениях рН от 3 до 4, в качестве растворителя могут быть применены, например, ,диоксан, тетрагидрофуран, диметилфорамид, диметиловый эфир этиленгликоля или диметиловый эфир диэтиленгликоля. Кроме того, могут быть применены такие ниэкомолекулярные спирты, как метиловый спирт, этиловый спирт и изопропиловый спирт. Для создания зна- чения рН,-лежащего в благоприятной области, могут быть применены такие органические или неорганические кислоты, как, например, уйсусная кислота, паратолуолсульфокислота, бен30лсульфокислота, соляная кислота, или серная кислота.
Одновременное гидрирование и восстановление также происходит в том случа1е, когда соединение формулы П подвергают восстановлениюводородом в присутствии никеля Ренея в среде протонного растворителя, в качестве которого преимущественным образом
применяют этиловый или ИЗОПрОПИЛО,вый спирт.
При этом образуется рацемический 2,3,4,5-тетрагидро-3-амино-1-бензоксепинод-5 формулы 1. Он может быть вицелен из реакционной смеси в форме свободного основания или в виде соли с кислотой.
Для разделения на рацематы сцмс-я соответственно,/7&лс -конфигурациями карбинольных остатков и аминоостатков полученное свободное основан или его аддитивная соль с кислртой известными способами может быть подвергнута фракционной кристаллизации в подходящем растворителе, в качест которого может быть применен, напри мер, низший спирт. Предпочтительно в качестве кислоты при получении соли используют малеиновую кислоту, паратолуолсульфокислоту и циклогексаминосульфокислоту. Разделение изо меров MpmjsT быть произведено с помощью хроматографии свободного основания подходящим растворителем на силикагеле или окисИ алюминия.
..-цга и рац - ум /С-2,3,4,5-тётрагидро-З-амино-1-бензоксепинолы-5 формулы I в результате взаимодействия с подходящей оптически активной кислотой, например винной кислотой, о, (/-дибензоилвинной кисл
той, миндальной кислотой, ди-О-изопропилиден-2-оксо-Ь-гулоновой кислот той, и последующе.й фракционной кристаллизации полученной соли могут быть разделены на оптически активные антиподы. Из этих солей могут быть выделены свободные основания, которые при желании могут быть переведены в пригодные с фармакологической точки зрения соли. Б рзезультате перекристаллизации из такого растворителя, как низший спирт и/или простой эфир, рацемические соединения и их изомеры, а также их аддитивные соли с кислотами могут быть очищены. 1идрирование расположенной в положении 3, 4 двойной связи в соединениях формулы 11 проводят в слабокислой среде, преимущественным образом при значениях рН от 4 до 6, при применении цианборгидрида натрия в таком растворителе, как, например, низший спирт, диоксан, тетрагидрюфуран, диметилформамид, диметиловый эфир этиленгликоля или диметиловый эфир диэтиленгликоля. В качестве подходшцей кислоты применяют, например, уксусную кислоту, паратОлуол сульфокислоту, бензосульфоКислоту, соляную или серную кислоту. ГидрирЬвание- водородом в присутствии никеля Ренея а таком апротонном растворителе, как толуол или бензол, равным образом приводит к селективному гидрированию 3,4-двойной связи в соединениях формулы II. В результате взаигмодействия с кислотой в среде .9Рганического растворителя могут быть получены аддитивные соли производных рац.-3-амино-3,4-дигидро-1-бензоксепинона-5 (2Н). Разделение на . оптически активные антиподы может быть I осуществлено описанными способами.
Пример. К охлажденному на .-бане со льдом 1,8,8 г (0,1 моль) З-метиламино-1-бензоксепинона-5(2Н) в смеси, состоящей из 125 мл диоксана и 125 мл уксусной кисло ы, прибавляют при охлаждении небольшими порциями боргидрид. натрия до завершения, реакции 0,4 моль рН 4-5. Затем реакционный раствор выливают в воду со льдом, смесь доводят до щелочной реакции посредств прибавления углекислого натрия, после чего производят экстрагирование дихлорметаном. Органический раствор промывают насыщенным раствором поваренной соли и сушат над сернокислым натрием. После отгонки растворителя получают 16,4 г (85% от теоретического) рац.-2j3,4,5-тетрагидро-З-. -метиламино-1-бензоксепинола-5 в . виде маслообразного остатка.
Температура плавления гидрохлорида полученного соединения составляе 152-157 С (из изопропилового спирта Для разделения изомеров полученный описанным способом маст1Ообразны продукт растворяют в изопропиловом спирте и раствор смешивают с избыточ ным количеством малеиновой кислоты, В результате фракционной кристаллизации малеината из изопропилового спирта и последующего переведения полученного соединения в гидрохлорид получают гидрохлорид рац.-чмг-2, 3, 4 5-тетрагидро-З-метиламино-1-бензоксепинола-5, температура плавления которого составляет (метиловый спирт) диэтиловый, эфир, и гидрохлорид рац.-транс -2,3,4,5-тетрагидро-3-метиламино-1-бензоксепинола-5, температура плавления которого 170173 С (метиловый спирт) диэтиловый эфир. Эти соединения формулы I, которые сами обладают ценной фармакологичесКОЙ Активностью, представляют собой промежуточные продукты, применяемые для получения соответствующих 5-гидроксисоединений формулы 1. Восстановление кетогруппы может быть осуществлено с применением обычных восстановителей, например, в нейтрально области значений рН с применением боргидрата натрия, боргидрата лития литийалюминийгидрида, натрий-гЯкс-(2-метоксиэтокси) -алюминийгидрида или три- 77го/ -бутилгидрида лития или э силънокислой области значений рН с применением цианборгидрида натрия в указанных растворителях и при применении указанных кислот для поддержания требуемого значения рН. При этом посредством выбора подходящегси растворителя и восстановителя может быть достигнуто увеличение количества желаемого рацемата. П р и м е р2.18,8 г (0,1 моль) 3-метиламино-1-бензоксепинона-5(2Н) перемешивают с 40 г никеля Ренея в 400 мл этилового спирта в течение 5 ч при давлении водорода 55 бар. Непосредственно после этого от реакционной смеси отфильтровывают ката лизатор, от фильтрата отгоняют растворитель, в результате чего получают 7,7 г (40% от теоретического) рад. -2, 3,4,5-тетрагидро-З- метиламино -1-бенэоксепинола-5 в виде, маслообразного остатка. По аналогии с описанным полученное соединение может быть разделено на изомеры. П р и м е р 3. К раствору 94,2 г (0,5 моль) З-метиламино-1-бензоксепинона-5(2Н) в смэси, состоящей из 300 мл дйоксана. и 300 мл ледяной уксусной кислоты, при охлаждении прибавляю небольшими порциями 18,9 г (0,3 моль) цианборгидрата натрия таким образом, чтобы температура реакционной смеси не превышала . Непосредственно после этого реакционную массу перемешивают при комнатной температуре до : авершения реакции, после чего реакционный раствор выливают в зоду со льдом, смесь доводят до щелочной реакции посредством прибавления углекислого натрия и затем производят экстрагирование дихлорметаном. Органическую фазу промывают насьвденным раствором поваренной соли и сушат над сернокислым натрием. Посредством введения в раствор хлористого водорода осаждают гидрохлорид рац.-3-метиламино3,4-дигидро-1-бензоксепинона-5(2Н), который непосредственно после этого отфильтровывают. Выход продукта составляет 89,9 г (79% от теоретического), т.пл. 184-18бс ( метиловый спирт/диэтиловый эфир). Пример4.К раствору 2,3 г (0,01 моль) 3-(rt.-бyтилaминo)-l бeнзoкceпинoнa-5 (2Н) в 10 мл метилового спирта прибавляют следы бромкрезолового зеленого. К смеси по каплям прибавляют раствор хлористого водорода в метиловом спирте (3 н.) до перехода индикатора (рН 4-6). Непосредственно после этого к смеси медленно прибавляют при комнатной температуре раствор 0,65 г цианборгидрида натрия (0,01 моль) в 10 мл метилового спирта, после чего реакционную массу дополнительно перемешивают в течение 1-2 ч до .завершения реакции. При этом посредством прибавления по каплям раствора хлористого водорода в метиловом спирте поддерживают желтую окраску индикатора. Затем раствор упаривают, остаток экстрагируют водой, посредством прибавления диметиламина реакцию t)acTBopa доводят до щелочной, после чего производят .экстрагирование диэтиловым эфиром. Эфирные растворы объединяют и сушат над сернокислым натрием. Посредством введения в раствор хлористого водорода производят осаждение гидрохлорида рац.-3(и.-бутиламино)-3,4-дигидро-1-бенэоксепинона-5(2Н). Полученный продукт отфильтровывают и перекристаллизовывают. Выход продукта составляет. 2,0 г (74,1% от теоретического), т.пл. 154-158с (изопропиловый спирт/диэтиловый эфир). Приме р 5. 27,9 г (0,1 моль) 3-фенэтиламино-1-бензоксепинона-5(2Н) перемешивают с 25 г никеля Ренея в 350 мл толуола в течение 20 ч при давлении водорода 150 бар. Непосредственно после этого .от реакционной смеси отфильтровывают катализатор, от фильтрата отгоняют раствс ритель и остаток экстрагируют метиловым спиртом. Посредством введения в раствор хлористого водоррда получают 14,6 г (46% от теоретичёского) гидрохлорида рац.-3-фенэтиламино-3,4-дигидро-1-6енэоксепинона -5(2Н) с температурой плавления (разл.) из метилового спирта Пример 6. Способами, описанными в примерах 3-5, соединения 3-Метилс1Мино-7-метил-1-6ензоксе пинон-5{2Н) 3-Кетиламино-7-этил-1-бензоксеп нон-5(2Н) 3-Метиламино-7-бром-1-бензоксеп нон-5{2Н) 3-Метиламино-7-метокси-1-бензок сепинон-5 (2Н) 3-Метиламино-8-метокси-1-бензок сепинон-5(2Н) З-Иирролидино-Ыгбензоксепинон-5t2H) 3-Матиламино-7,8-дихлор-1-бенз сепинон-5(2Н) 3-Метиламино-7,8-диМетил-1-бен ксеп11нон-5 (2Н) З-Изопропиламино-1-бензоксепин -5{2Н) 3-Бензиламино-1-бензоксепинон-5 2Н) З-Диметиламино-1-бензоксепинон -5(2Н) З-Пиперидино-1-бензоксепинон-5(2Н) 3-Морфолино-1-бензоксепинон-5( 3- (ЗГ-Диметиламинопропиламино)-хлор-1-бензоксепинон-5(2Н) 3-(Диметиламинопропиламино)-бензоксепинон-5(2Н) 3- (|3-Диметиламиноэтиламино}-1-бёнзоксепинон-5{2Н) 3-Амино-1-бензоксепинон-5(2Н) 3- (1 -Метоксиэтиламино)-1-бензо пинон-5(2Н) переводят в следующие соединения: т,пл. , Гидрохлорид рац.-3-метиламино-3,4-дигйдро-6-метил-1-бензоксепинона-5(2Н) 183-185 Гидрохлорид рац.-Зметиламино-3,4-дигидро-7-этил-1-бензоксепинона-5{2Н) 146-148 Гидрохлорид рац.-3мeтилaминo- 3 , 4-дигидро-7-бром-1-бензоксепинона-5(2Н) 193-195 Гидрохлорид рац-3- -метиламино-3,4-дигидро-7-метокси-1-бензоксепинона-5(2Н) 178-180 Гйдрохлорид рац,-3-метиламино-3,4-дигидро-8-метокси-1-бензоксепинона-Т-5{2Н)168-170 Гидрохлорид рац.-З-пирролидино-3,4-дигидро-1-бензоксепинона-5(2Н) 128-130 Гидрохлорид рац.-З-метиламино-3,4-дигидро-7,8-дихлор-1-бензоксепинона-5(2Н) 194 Гидрохлорид рац.-З-метиламино-3,4-дигидро-7,8-диметил-1-бензоксепинона-5(2Н)206 Гидрохлорид рац.-З-и 3 опропиламино-3,4-дигидро-1-бензоксепинона-5(2Н)171-175 Гидрохлорид рац.-З-бензиламино- 3,. гидро-1-бензоксепинона-5(2Н)141-145 Малеинат рац.-3-диметиламино-3,4-дигидpo-l-бeнзoкceпинона-5(2н)107-109 Гидрохлорид рац.-З-пиперидино-3,4-дигидро-1-бензоксепинона-5(2Н)154-156 Гидрохлорид рац.-З-морфолино-3,4-дигидро-1-бензоксепинона-5(2Н)148-150 Моногидрат дигидрохлррида рац„-3(у-диметиламинопропиламино)-3,4-дигидро-7-хлор-1-бензоксепинона-5(2Н)150-154 Дигидрохлорид рац.тЗ-(-Диметилс1минопропиламино)-3,4-дигидро-1-бензоксепинона-5(2Н) :154-158 Дигидрохлорид рац.-З-((Ь-диметиламиноэтиламино) - 3,4-дигидро-1-бен.зоксепинона-5(2Н)150-157 Гидрохлорид рац.-З-амино-3,4-дигидро-1-бензоксепинона--5(2Н)211 Гидрохлорид рац.-3-{ Ь-метоксиэтиламино)-3,4-дигидро-1-бензоксепинона-5(2Я)133-135 ример 7. К раствору 33,5 г моль) дигидрохлорида рац.-Здиметиламинопропиламино)-3,4идpo-l-бeнзoкceпинoнa-5 (2Н) в мл метилового спирта при охлажи прибавляют небольшими порцияоргидрид натрия до завершения ций рН 7. Затем реакционный растподкисляют посредством прибавлесоляной кислоты и производят ивание досуха. Полученный остаэкстрагируют водой, раствор до щелочной реакции посредством
прибавления водного раствора аммиака, после чего производят экстрагирова.ние дихлорметаном. После промывки органического раствора насыщенным раствором поваренной соли, сушки над сернокислым натрием и упаривания получают 23,8 г (90% от теоретического) рац.-2,3,4,5-тетрагидро-З-( -диметиламинопропиламино)-1-бензоксепинола-5 в виде маслообразного остатка.
С помощью хроматографии на силикагеле и последующего образования дималеината получают дималеинат pau,-i4wr-2,3,4, 5-тетрагидро-З- (у-дкметиламинопропилг мино)-1-бензоксепинола-5 с температурой плавления leg-lTO C (метиловый спирт) и дималеинат рац.-w/3 7Wc-2, 3,4,5-тетрагидро-3- (9-Диметиламинопропиламино)-1-бензоксепинола-т5 с температурой плавления 157-159с (метиловый спирт).
Пример 8. К нагретому до температуры кипения раствору 80 г (0,5 моль) рац.-З-метиламино-3,4-дигидро-1 бензоксепинона-5(2Н) в смеси, состоящей из 550 мл толуола и 300 мл гексана, прибавляют по каплям 550 мл 1 М три- w y-бутилборгидрид а лития в тетрагидрофуране таким образом, чтобы раствор поддерживался в состоянии кипения. После завершения прибавления по каплям указанного раствора реакционную массу нагревают при температуре кипения в течение последующего часа. После охлаждения реакционную смесь доводят до кислой реакции посредством прибавления по каплям метанольного раствора хлористого водорода, непосредственно после этого метаноль ную фазу отделяют и смесь толуола и гёксана еще раз экстрагируют метрнольиым раствором хлористого водорода. Экстракт упаривают, остаток экстрагируют дихлорметаном и раствором углекислого натрия (10%), органическую фазу промывают насыщенным раствором поваренной соли, сушат над сернокислым натрием и упаривают досуха.В результате получают 67,6 г (70%.от теоретического) рац.-2,3,4, 5-тетрагидро-3-метиламино-1-бензок-, сепинола-5 в виде маслообразного остатка, в котором содержится 32 ч. рац. -Ц.с-2,3,4, 5-тетрагидро-З-метиламино-1-бензоксепинола-5 и 18 ч. рац. fn/yaMC-2,3,4, 5-тетрагидро-3-метиламино-1-бензоксепинола-5. Указанные соединения можно разделить и охарактеризовать по аналогии с описанным.
Пример 9. К раствору 3,9 г (0,02 моль) рац.- / сгхс-2,3,4,5-тетрагидро-З-метиламино-1-бензоксепинола-5 в 80 мл ацетонитрила и 17,1 мл
водного раствора формальдегида (35%) прибавляют 3,9 г (0,06 моль) цианборгидрида натрия. Непосредственно после этого к реакционной смеси прибавляют 2,1 мл ледяной уксусной кислоты -и смесь перемешивают в течение 2. ч при комнатной температуре. Затем реакционный раствор разбавляют 270 мл диэтилового эфира, промывают разбавленным раствором гидроокиси натрия, сушат над сернокислым натрием и упаривают. Полученный остаток растворяют в метиловом спирте, после чепо производят выделение рац.-луга -2,3,4,5-тетрагидрю-З-диметиламино-1-бензоксепинола-5 в виде малеината. Выход продукта составляет 3,9 г (60% от теоретического), т. пл. 157-158 С (метиловый спирт/диэтиловый эфир).
П р и м е .р 10. По аналогии с описанными примерами из
3-Амино-1-бензоксапинона-5(2Н) 3-( -0утиламино)-1-бензоксепинона-5(2Н)
З-Бензиламино-1-бензоксепинона-5(2Н)
3-Фенэтиламино-1-бензоксепинона-5(2Н)
3-Диметиламино-1-бензоксепинона-5 UH)
З-Диэтиламино-1-бензоксепинона-5(2Н)
З-Пирролидино-1-бензоксепинона-5(2Н)
З-Пиперидино-1-бензоксепинона-5(2Н)
З-Морфолино-1-бензоксепинона-5(2Н)
3-Метиламино-7-этил-1-бензоксепинона-5(2Н)
3-Метиламино-7-хлор-1-бензоксепинона-5(2Н)
3-Метиламино-8-хлор-1-бензоксепинона-5(2Н)
3-Метиламино-7-бром-1-бензоксепинона-5(2Н)
3-Метиламино-7-метокси-1-бензоксепинона-5(2Н)
3-Метиламино-7-хлор-8-метил-1-бензоксепинона-5(2Н)
Диметиламинопропиламино) - 7-хлор-1-бензоксепинона-5(2Н) 3-(р,р -Диметил- -диметиламинопропиламино) -1- бензоксепинона-5(2Н)
3-(Э-Метоксиэтиламино)-1-бензоксепинона-5(2Н) 3-Мётилги«1ино-7гметил-1-бензоксепинона-5(2Н)
3- Метиламино-8-мётокси-1-бензоксепинона-5(2Н)
3-Метиламино-7,8-дихлор-1-бензоксепинона-5(2Н) 3-МетИламино-7,8-диметил-1-бензоксепинона-5(2Н) получают следующие соединения: Гидрохлорид рац.-Чг«;-2,3 ,.4,5-тетрагидро-3-амино-1-бензоксепинола-5Гнщюхлорид рац.- ty&cu c-2,3,4,5-тетрагидрс-3-амиио-1-6енэоксепинола-5 Толуол-4-сульфонат рац.-4ttc-2,3,4,5тетрагидро- 3- (Н,-бутиламиио)-1-бензоксепинола-5Толуол-4-сульфонат рац.-ifpzwc-2, 3,4,5 тетрагидро-3- (Н-бутиламино)-1-бензоксепинола-5Мешеннат рац.,3,4,5-тетрагидро-3-бензиламнно-1-бензоксепинола-5Малеинат рац. -2,Э,4,5-тетрагндро-З-бензняамйно-1-бензонсёпинола-5Иалеинат рац.Ч «с-2,3,4,5-тетрагидро-З-фенэтилаютно- 1 -бвнзоксепииола-5 Малеинат pau. -2,3,4,5-тетрагидро- 3- фенэти лами но- 1 -бензохсепинола-5 Малеинат рац. -TfUc -2,3,4,5-тетрагидро-3-диметйламино-1-бензоксепинола-5 Малеинат pan. -2,3,4,5-тетрагидро -диметиламино-1-бен зоксепинола-5 Толуол-4-сульфонат рац .-IfUC-2,3,4,5-тетрагидро-3-диэтиамино-1-бензоксепнн ла-5 Толуол-4-сульфонат рац.,3,4, 5-тетрагидро-3-диэтиамино-1-бензоксепин ла-5 Толурл-4-сульфонат рад .Чис.- 2,3,4,5-тет ро-3-пиppoлидинo-l-бeнзoкceпинoлa-5Толуол-4-сульфонат рац.-«y cwo-2,3,4,5тетрагидро-3-пиррЬлидино-1-бензоксепинола-5 Толуолг4-сульфонат рац.,3,4,5-тетрагидро-3-пипериди но-1-бензоксепинола-5 Толуол-4-сульфонат рац. 2,3,4 / 5-тетрагидро-3-пиперидино-1-бвнэоксепинола-5142-144Толуол-4-сульфонат рац.-VZffi-2, 3,4, 5-тетрагидро-3-морфолино-. -1-бензоксепинола-5154-156 Толуол-4-сульфонат рац.-« /галс-2, 3 , 4 ,5-тетрагидро-3-морфолино-1-бензоксепинола-5. 145-146 Гидрохлорид рац.-Чггс-2,3,4,5-тeтpaгндpo-3-мeтилaминo -7-этил- -бeнзoкceпинола-5138-140Гидрохлорид рац.- iyb«wc-2,3,4,5-тетрагищю-З-метила но-7-этил-1-бензоксепинола-5197-198ГидрохлоЕясд рац. -H«f-2,3,4,5-тетрагидро-3-метиламино-7-хлор-1-бензоксепинола-5172-173Гидрохлорид рац.- . -wyW.wc-2, 3,4,5-тетрагидро-З-метиламшно-7-хлор-1-бензоксепинола-5242 (разл.) Гидрохлорид рац,-I Zir-2,3,4, 5-тетра-, гидро-3-метиламино-8-хлор-1-бензоксепинола-5194-195Гидрохлорид . 2,3,4,5-тетрагидоо-З-метиламино-8-хлор-1-бензоксепинола-5189-190Гидрохлорид рац.,3,4,5-тётрагидро-З-метиламино-7-бром-1-бензоксепинола-5 186-188 Гидрохлорид рац.-w/ aAc-2,3,4,5-тетрагидро-З-метиламино-7-бром-1-бензоксепино- : ла-5 .243 (разл.) Гидрохлорид рац.- fftc-2,3,4,5-тетрагидро- . ггЗ-метиламино-7-метокси-1-бензоксепинола-5198-200Гидрохлорид рац.- с;Ьеглс-2,3,4,5-тетрагидро-З-метиламино-7-метокси-1-бензоксепино223-22SГидрохлорид рац,-е{йЕ г 2,3,4,5-тетрагидро-3-метиламино-7-хлор-8-метил-1233 (разл. -бензоксепинола-5
Гидрохлорид рац.- л/ «злс-2 , 3, 4 , 5-тетрагидро-3-метиламино-7-хлор-8-метил-1-бензоксепинола-5
Дигидрохлорид рац.-1 -ис-2,3,4, 5-тетрагидро-3-(Т диметиламинопропиламино)-7-хлор-1-бензоксепинола-5
Дималеинат рац.-г мс-2р3,4,5-тетрагидро-3- (1, (Ь -диметил-диметиламинопропиламино)-бензоксепинола 5
Дималеинат рац.-inpcMC-2 ,3,4, 5-тетрагидро-3- ( , / -диметил- диметиламинопропиламино)-1-бензоксепинола-5
Циклогексиламиносульфонат рац. -2,3, 5-тетрагидрогЗ- -метоксйэтиламино)-1-бензоксепинола-5Циклогексиламиносульфонат рац.-йчл 2лс-2,3,4,5-тетрагидро-3(-метоксиртиламино)-1-бензоксепинола-5 : Гидрохлорид рац. - 2 , 3,4 , 5г тетрагидро-3-метиламино-7-метил-1-б;ензоксепинола-5 ;
Гидрохлорид рац.(, 3,4;, 5-тетрагидро-3-метиламино-7-метил-1-бензоксепинола-5
Гидрохлорид рац.- $гл:-2, 3,4, 5:-тетрагидро-3-ме;ти|ламино-8-метокси-1-бензоксепинола-5Гидрохлорид рац.- г;5САС-2,3, 4|, 5-тетрагидро-3-ме тиламино-8-метокси|-1-бензоксепино/ а- 5Гидрохлорид |рац.-Ц-ис -2,3,4 ,|5-тетрагидро-3-мети;ламино-7,8-дихлор- 1-бензоксепинола-5
Гидрохлорид-|рац, -t f ciHc-l, 3,;4, 5тетрагидро-3:-метиламино-7 ,8-ди;Xлop-l-бeнзoкceпин:Oлa-5Ридрохлорид ;рац.-iA,tfC -2,3,4 5-тетрагидро-З-метиламино-7,8-диметил-1-бензоксепинола-5198 (разл.)
Гидрохлорид рац.- и/эсг;л:-2,3,4,5тетрагидро-3-метил5 амино-7,8-диметил-1-бензоксепинола-5 208 (разл.)
Пример 11. К раствору 1,9 г (0,01 моль) З-метиламино-1-бензоксепин(2Н)-она в 10 мл метанола добавляют небольшое количество метилоранжа, после чего прибавляют к нему по каплям метанольный раствор хлористого водорода ( 3 н.) до изменения окраски индикатора. К подкисленному раствору медленно при
комнатной температуре добавляют раствор 1,3 г (0,02 моль) цианборгидрида натрия в 20 мл метанола и перемешивают еще 6 ч до окончания реакQ ции. При этом к нему добавляют по
каплям метанольный раствор хлористого водорода таким образом, чтобы индикатор все время был окрашен в красный цвет (рН 3-4). Раствор упаривают, растворяют остаток в воде, добавляют диметиламин до щелочной реакции и проводят экстракцию диэтиловым эфиром. Эфирные вытяжки объединяют и высушивают сульфатом натрия. После отгонки растворителя по лучают рацемат 2, 3, 4, 5-тетрагидро-3-метиламино-1-бензоксепин-5-онав виде маслянистой жидкости.
Выход 71%, т. пл. 152-157 С (после перекристаллизации из изопропано5 ла). Для разделения изомеров полученную маслянистую жидкость обрабатывают так же, как в примере 1.
Соединения формулы Г или их соли обладают ценными терапевтическими 0 свойствами, причем прежде всего они проявляют ярко выраженную активность при нарушении двигательной способности в желудочно-кишечном тракте.
с В проведенных на животных экспериментах под их влиянием усиливаются перистальтические волнообразные движения желудка, причем частота движения уменьшается в пользу возникновения более сильных и более глубоко затянутых волнообразных движений. Подобная активность проявляется в улучшенном опорожнении желудка.
Описание методов фармакологических исследований.
0 посредством анализа проб.
5 Vena ugularis сосуд-катетер и в
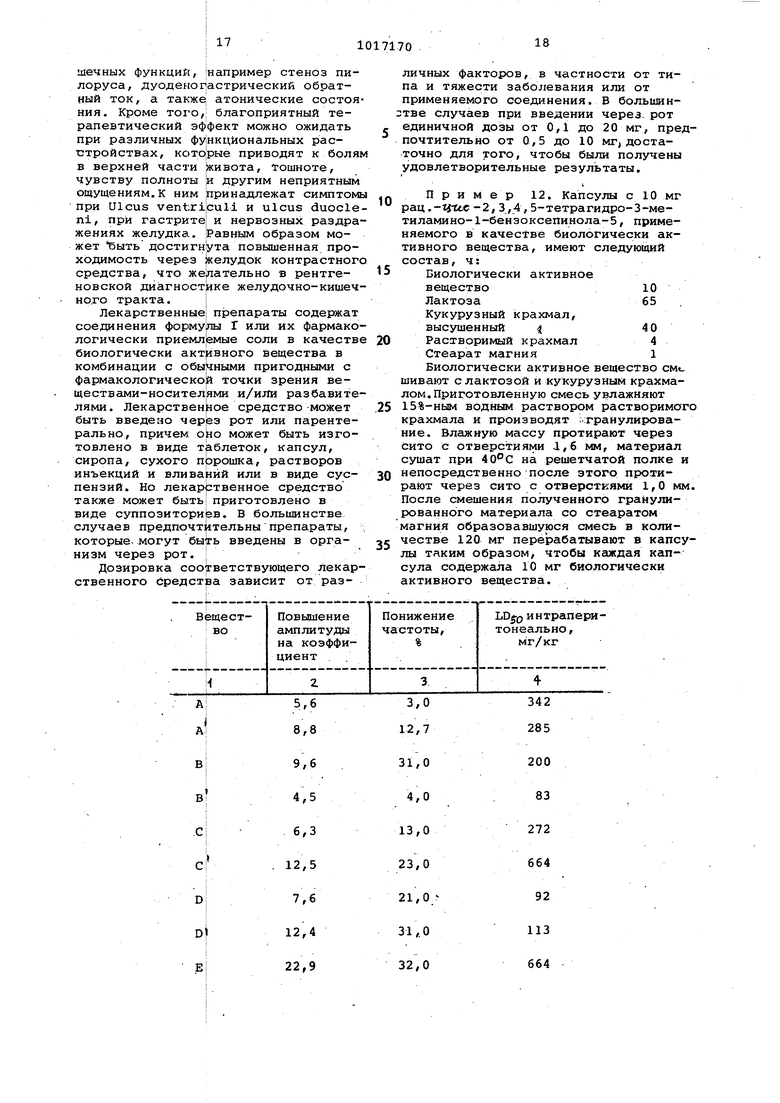
трахею - трахеаяьный катетер, в желудок вводили желудочный зонд, который через трехходовой кран соединяли с датчиком давления (Р 23 DB).. Желудок у пилоруса и у входа в желудок перетягивали лигатурной нитью. Желудок заполняли 3 мл 0,9%-ного водного раствора хлористого натрия. Производимые желудком волнообразные движения непрерывно регистрировали мультикордером Ватайабе (МС 641). Для определения активности исследуемых веществ последние растворяли в физиологическом растворе.хлористого натрия Hjm суспендировали в тилозе МН50, причем введение производили интраперитонеально в дозе 20 мг/кг. Затем сравнивали возникающие до и после введения веществ амплитуды и частоты волнообразных движений желудка. . , .
Оценка показала, что вскоре после введения соот ветствующих соединений формулы 1 наблюдается значительное увеличение амплитуд. Этот эффек в соединении с различно вырс1женным понижением частоты приводит к улучшенной проходимости желудка.
По описанной методике исследовали следующие соединения:
А) рац. ,3,4,5-тетрагидро-3-метиламино -1-бензокеапин-5-оя,
А ) рац.-««/гсг/ с-С2,3,4, Б-тетрагидро-З-метиламиноД -1-бензоксепин-5-ол
В), рац. - ;2,3,4 ,5-тeтpaгидpo-3-мeтилaминo -8-xлop-l- eнзoкceпин-5-oл
в ) рац. -C2,3,4,5-тeтpaгидpo-3-мeтилaминo -8-xлop-l-бeнзoкceпин-5-pл
C)рац.-tfUc -2,3,4,5-тетрагидро-3-изопропиламино -1-бензоксепин-5-ол
с ) рац.-(р12ис-1 2,3,4,5-тетрагиро-З-изопропиламин }-1-бензоксепин
D)рац.- ягглг- 2,3,4,5-тетрагидро-З-бензиламино}-1-бензоксепин-5-ол
D ) рац. 2,3,4,5-тетрагидро-З-бензиламиноЗ-1-бензоксепин-5-ол
E)рац. 2,3,4,5-тетрагидро-3- (з -димeтилaминoпpoпилaминo)J-l-бензоксепин-5-ол
Е ) рац. -wfyOHC -12,3,4,5- тетрагиро-3-(у-диметиламинопропиламино) -1-бен.зоксепин-5-ол
F) a.u.,-ifuc- 2,3,4,5-тетрагидро-3-диэтиламино -1-бензоксепин-5-ол
F) рац. 2,3,4,5-тeтpaгидpo-3-диэтилaминoJ-l-бeнзoкceпин-5-oл
G) рад.-tittc ,3,4, 5-тeтpaгидpo-3-мeтилйминo-7-xлopj- -бeнзoкceпин-5-ол
G ) рац. -wfiOifc С2,3,4,5-тетрагидро-З-метиламино-Т-хлорЗ-1-бензоксепин-5-ол
Н) рац. -L2,3,4,5-тeтpaгидpo-3- (|г-бутиламино)3 -1-бе 13окселин-5-ол
Н ) рац. - 7/гсг.,3,4, Б-тетрагнд;РО-3-(п--бутиламино) -1-бензоксепин-5-ол
D) рац. ,3,4, 5-тетрагидро-3-морфолиноJ-1-бечзоксепин-5-ол
3} рац. 2,3,4,5-тетрагидро-3-морфолино -1-бензоксепин -5-ол
К) рац., 3, 4, 5-тетрагидро-3-пирролидино -1-бензоксепин-5-ол
к ) рац..л с-С2, 3,4 ,5-тетра- . гидро-З-пирролидинсЗ-1-бензоксепин-5-ол
5L) рац.,3,4,5-тетрагидро-5-фенэтиламиноЗ 1-бензоксепин-5-ол
L ) рац. -inpcLHC -2,3,4,5-тетрагидро-5-фенэтиламино -1-бензоксепин-5-ол
0М) pau.-i{-ac -L 2,3, 4,5-тетрагидро.-З-метиламино-7,8-дихлор -1-бензоксепин-5-ол
М ) рац. ,3 ,4, 5-тетрагидро-З-метиламино-7,8-дихлор}-1-бен о5 ксепин-5-ол
N) рац.--«ле-t2,3,4,5-тeтpaгидpo-3-aминo -1-бензоксепин-5-ол
N) рац.--fti /OKc- 2,3,4 ,5-тетрагидро-З-аминоЗ-1-бензоксепин-5-оя0О) рац.,3,4 ,5-тетрагидро-3-диметиламино1-1-бензоксепин
оИ рац.-Ш77а с- 2,3,4, 5-тeтpaгидpo-3-димeтилaминo -l-бeнзoкceпин
1)рац.-3-метиЛамино-З,4-дигидрос -1-бензоксепин-5(2Н)-ОН
2)рац.-3-изопропиламиио-3,4-дигидро-1-бензоксепин-5(2Н)-ОН
3)рац.-3-бензиламино-3,4-дигидро-1-бензоксепин-5(2Н)
4)рац.-З-О-диметиламинопропил амино)-3,4-дигидро-1-бензоксепин-5(2Н)-ОН
5)рац.-3-диметиламино-3,4-дигидро-1-бензоксепин-5(2Н)-ОН
6)рац.-З-СЗ-диметиламинопропил5 амино)-7-хлор-З,4-дигидро-1-бензоксепин-5(2Н)-ОН
7)рац.-3-(ц-бутиламино)-3,4-дигидро-1-бензоксепин-5(2Н)-ОН
Данные проведенных tja желудке измерений представлены в таблице. I .
Из таблицы видно, что уже незначительные дозы соединений формулы Т или их аддитивных солей с кислотами вызывают значительное усиление перистальтических волнообразных движений желудка, причем высокая активность и незначительная токсичность веществ (п.в) указывают на их хорошую переносимость организмом. Другим
0 преимуществом являеах:я быстро наблюдаемое проявление активности.
Наблюдаемая фармакологическая активность может быть объяснена тем, что соединения формулы I устраняют
5 У человека нарушения желудочно-кишечных функций, например стеноз пилоруса, дуоденог|астрический обратный ток, а также атонические состояния. Кроме того,| благоприятный терапевтический эффект можно ожидать при различных фу|нкцйональных расстройствах, приводят к болям в верхней части Ьсивота, тошноте, чувству полноты другим неприятным ощущениям.К ним принадлежат симптомы при Ulcus ventriculi и ulcus duocleni, при гастрите| и нервозных раздражениях желудка. |Равн ым образом может быть достигнута повышенная проходимость через |желудок контрастного средства, что желательно в рентгеновской диагностике желудочно-кишечHO.ro тракта. |
Лекарственные препараты содержат соединения форму|лы Г или их фармакологически приемлемые соли в качестве биологически активного вещества в комбинации с обычными пригодными с фармакологической точки зрения веществс1ми-носител;Ями и/иЛИ разбавителями. Лекарственное средство может быть введено через рот или парентерально, причем о1но может быть изготовлено в виде таблеток, капсул, сиропа, сухого порошка, растворов инъекций и вливаний или в виде суспензий. Но лекарственное средство также может быть приготовлено в виде суппозитори|эв. В большинстве случаев предпочтительныпрепараты, которые- могут введены в организм через рот. |
Дозировка соо|гветствующего лекарственного ередстЬа зависит от раз9,6
4,5
6,3
12,5
7,6
12,4
22,9
личных факторов, в частности от типа и тяжести заболевания или от применяемого соединения. В большин::тве случаев при введении через, рот е1диничной дозы от 0,1 до 20 мг, предпочтительно от 0,5 до 10 мг, достаточно для того, чтобы были получены удовлетворительные результаты.
Пример 12. Капсулы с 10 мг рац. -2, 3,4, 5-тетрагидро-З-метиламино-1-бензоксепинола-5, применяемого в качестве биологически активного вещества, имеют следующий состав, ч:
Биологически активное вещество10
Лактоза65 .
Кукурузный крахмал, высушенный 40
Растворимый крахмал 4 Стёарат магния1
Биологически активное вещество см« шивают с лактозой и кукурузным крахмалом. Приготовленную смесь увлажняют 15%-ным водным растворюм растворимого крахмала и производят ,-:гранулирование. Влажную массу протирают через сито с отверстиями 1,6 мм, материал сушат при 40с на решетчатой полке и 0 непосредственно после этого протирают через сито с отверстиями 1,0 мм. После смешения полученного гранулированного материала со стеаратом магния образовавшуюся смесь в количестве 120 мг перерабатывают в капсулы таким образом, чтобы каждая капсула содержала 10 мг биологически активного вещества.
200
83
272
664
92
113
664
191017170
Продолжение таблицы
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Гетероциклич ские соединения | |||
| Аппарат для очищения воды при помощи химических реактивов | 1917 |
|
SU2A1 |
Авторы
Даты
1983-05-07—Публикация
1980-08-01—Подача