СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ТРИАЗОЛА
(54) ИЛИ ИХ СОЛЕЙ Целевой продукт выделяют в свободном виде или в виде соли. В качестве солей соединений формулы I пригодны соли с физиологически переносимыми кислотами, предпочтительно галогенводородные кислоты, например хлористоводородная и бромистоводородная, фосфорная, азотная, а также моно- и бифункциональные карбоновые и окси карбоновые кислоты, например, уксусная, малеиновая, янтарная, фумаровая, винная, лимонная, салициловая, сорбиновая и молочная кислоты и наконец, сульфокислоты, как 1,5-нефталиндисульфокислота. Соли соединений формулы 1 могут быть получены обьтными методами солеобразования, например путем растворения основания в простом эфире, например диэтиловом эфире, и добавления кислоты, например хлористого водорода, с последующим выд.еле1шем соли путем фильтрации. При этом соль можно очищать. Алканолать щелочных металлов формулы II можно получать тем, что соответствую дие производные 1-окси-1-фенил-2-триазолш1Этана подвергают взаимодействию с пригодными силь ными основаниями, как амидами или гидридами щелочных металлов, в индифферентных рас творителях. Производные 1-окси-1-фе1шл-2-триа золилэтана получают восстановлением соответствующих триазолилалкононов формулы IV rVc-CH где R и п имеют указанные значения, изопропилатом алюминия, формамидсульфон вой кислотой и гидроокисью щелочных металлов или ком1тексными гидридами. Соединение формулы IV получают путем взаимодействия гапогенкетонов формулы V ,-на1 11 о В которой Пип имеют указанные значет я На - хлор или бром, с 1,2,4-триазолами в присутствии связывающего кислоту средства. Галогенкетоны формулы V получают извест HbiMH методами. Способ поясняется нижеследующими примерами. Пример 1. 1-(2,4Дихлорфешш)-2-(1, 2,4-триазолил)-этил -2,4-дихлорбеизиловьш эфи 25,8 г (0,1 моль) 1-окси-1-(2,4-дихлорфени -2-(1,2,4гтриазоп-1-ип)-этана раст180ряют в 125 мл диоксана и, размешивая, каплями доб ляют в смесь из 4 г 80%-ного гидрата натрия 100 мл диоксана. Затем в течение 1 ч нагреают с обратным холодильником. После охлаждеия при комнатной температуре к получаемой аким образом натриевой соли каплями добавяют 20 г {0,1 моль) 2,4-дихлорбензолхлорида. Затем нагревают в течение нескольких часов с обратным холодильником, охлаждают и сгуща- ют путем отгонки растворителя. В остаток добавляют воду и метиленхлорид, органическую фазу отделяют, сущат над сульфдтом натрия и сгущают. Твердый остаток перекристаллизовывают из лигроина. Получают 29 г (70% от теории) 1- (2,4-дихлорфенил)-2- (1,2,4-триазол-1-ил)-этил - 2,4-дихлорбензиловый эфир; тлл. 84°С. А. Получение исходного соединения. J-Окси-1-(2,4-дихлорфенил)-2-(1,2,4-триазол-1-ил)-этан. 25,6 г (0,1 моль) uJ-(1,2,4-триазол-1-ил)-2,4-дихлорацетофенона растворяют в 300 мл метанола и при температуре от 5 до 10°С, размещивая, норщшми добавляют 4 г (0,1 моль) бората натрия. Затем в течение часа при комнатной температуре дополнительно размещивают и в течение часа нагревают до кипения. После отгонки растворителя остаток короткое время нагревают с 200 мл воды и 40 мл концентрированной соляной кислоты. Реакционную смесь подщелачивают натровым щелоком, затем твердый продукт реакции отфильтровывают. После перекристаллизации из лигроина - изопропанола получают 21,3 г (82% от теории) 1-окси-1-(2,4-дихлорфенил)-2-(1,2,4-триазол-1-ил)-этана; т.пл. 90°С. Б. W- (1,2,4-Триазол-1-ил)-2,4-дихлорацетофенон. 269 г (1 моль) а;-бром-2,4-дихлорацетофенона растворяют в 250 мл ацетонитрила. Этот раствор каплями добавляют в нагреваемую с обратным холодильником суспензию 69 г (1 моль) 1,2,4-триазола и 150 г карбоната калия в 2 л ацетонитрила. По истечении 20-часового нагревания с обратным холодильником охлажденную суспензию фильтруют, фильтрат освобождают от растворителя и остаток поглощают уксусным эфиром, промывают водой, сущат над сульфатом натрия и освобождают от растворителя. Уксусноэфирный остаток выкристаллизовывается после добавления изопропанола. После перекристаллизации из лигроина - изопропанола получают 154 г (60% от теории) и-(1,2,4-триазол-1-ил)-2,4-дихлорацетофенона; т.пл. 117°С. П р и м е р 2. 1-(214 Дихлорфекил)-2-(1, 2,4-триазол-1-ил)-этил -аллиловый эфир.. 25,7 г (0,1 моль) 1-окси-1-(2,4-дихлорфеш1л)-2-(1-,2,4-триазол-1-ил)-этана растворяют в 125 мл диоксана и, размеип1вая, каплями добавляют в суспензию 4 г 80%-ного гидрида
натрия в 150 мл диоксана. Затем в течение 1 ч нагревают с обратным холодильником. После охлаждения при комнатной температуре к получаемой таким образом натриевой соли добавляют 22,1 г (0,1 моль) аллилбромида. .Затем нагревают в течение 8 ч с обратным холодильником, охлаждают и сгущают путем отгонки растворителя. В остаток добавляют воду и метиленхлорид, органическую фазу отделяют, сушат над сульфатом натрия и сгущают. Получают 29,5 г 1-(2,4-дихлорфенил)-2- (1,2,4-триазол-1 -ил) - этил 1 - аллилового эфира с показателем преломления п 1,545. Выход количественный.
П р и м е р 3. (1-(2,4-Дихлорфенил)-2-(1,2,4-триазол-1-ил)-этил -аллиловый эфир. 29,5 г (0,1 моль) 1-(2,4-дихпорфенил)-2-(1,2,4-триазол-1-ил)-этил аллилового эфира
6836196
растворяют в 200 мл хлороформа и добавляют 6,4 г 95%-ной азотной кислоты. Добавляют 250 мл простого эфира для окончания выкристаллизации солн. После отфильтровьшакия и 5 сушки подучают 34 г (95% от теории) нитрата 11 - (2,4-дихлорфенил) - 2- (1,2,4- триазол-1 - ил) -этил -аллилового эфира; тлл. 131°С.
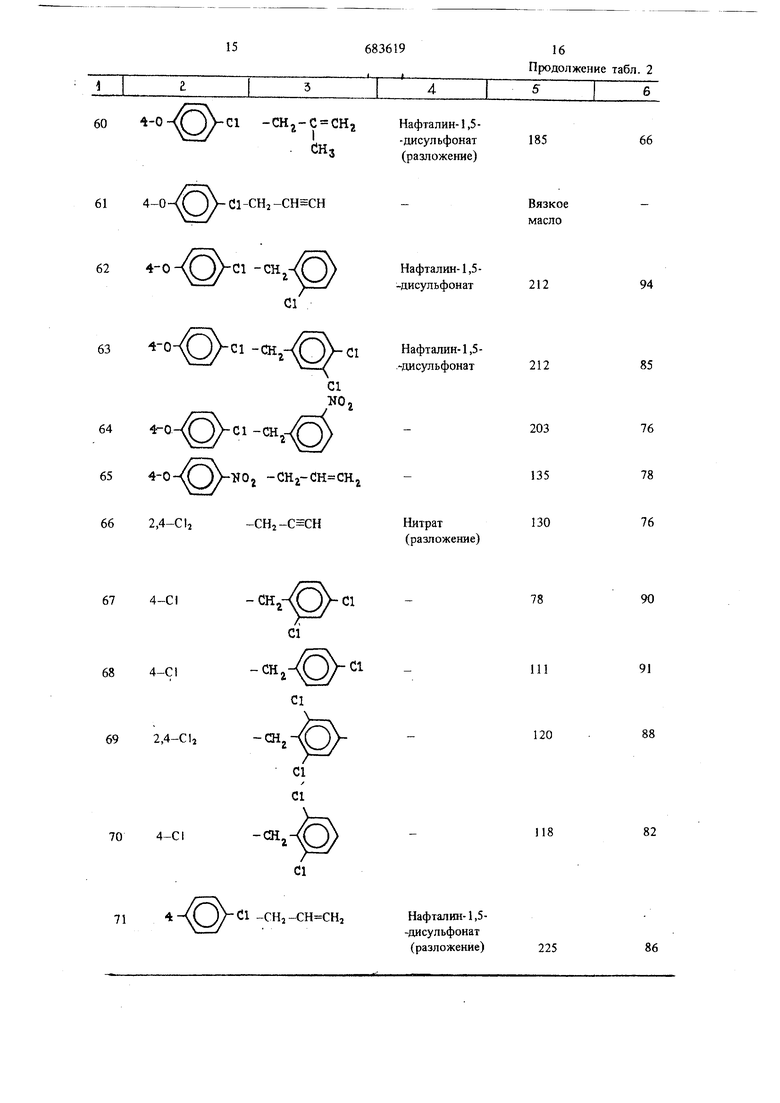
Аналогично примерам 1-3 получают привеto денные в табл. 1 и 2 соединения общей формулы Г
При этом реакции проводят при температуре 20-150°С в среде различных разбавителей.
и -GHj-CHeOHjt 15 4-0-v VGI
,6 r
-ci
Cl
68 Нафталиндисульфоновая кислота-(1,5) 184
95 Нафталиндисульфоновая кислота-(1,5) 213 85 Шфталиндисульфоновая кислота-(1,5) 200


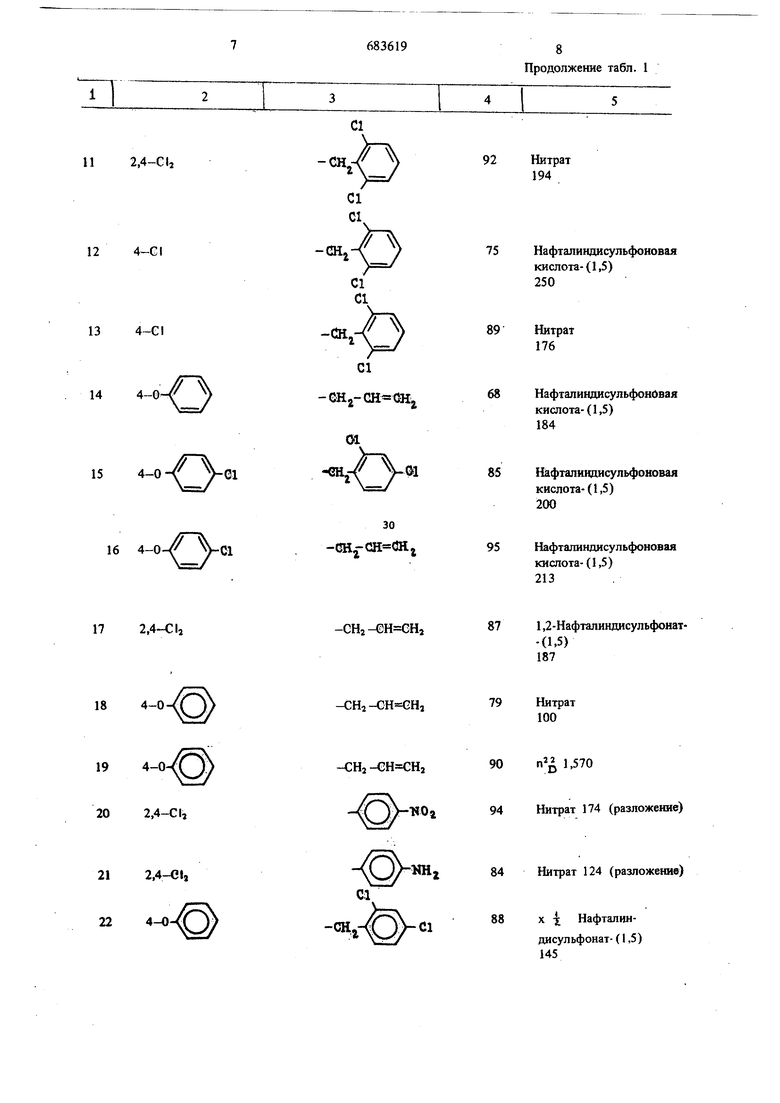
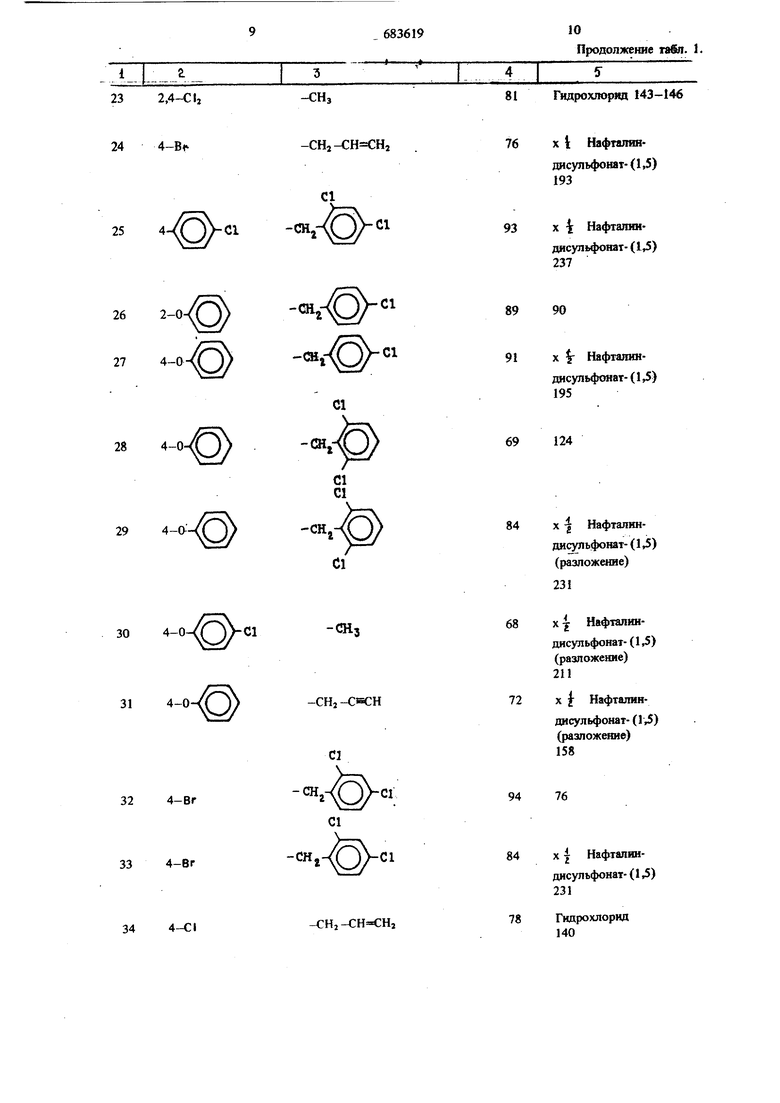
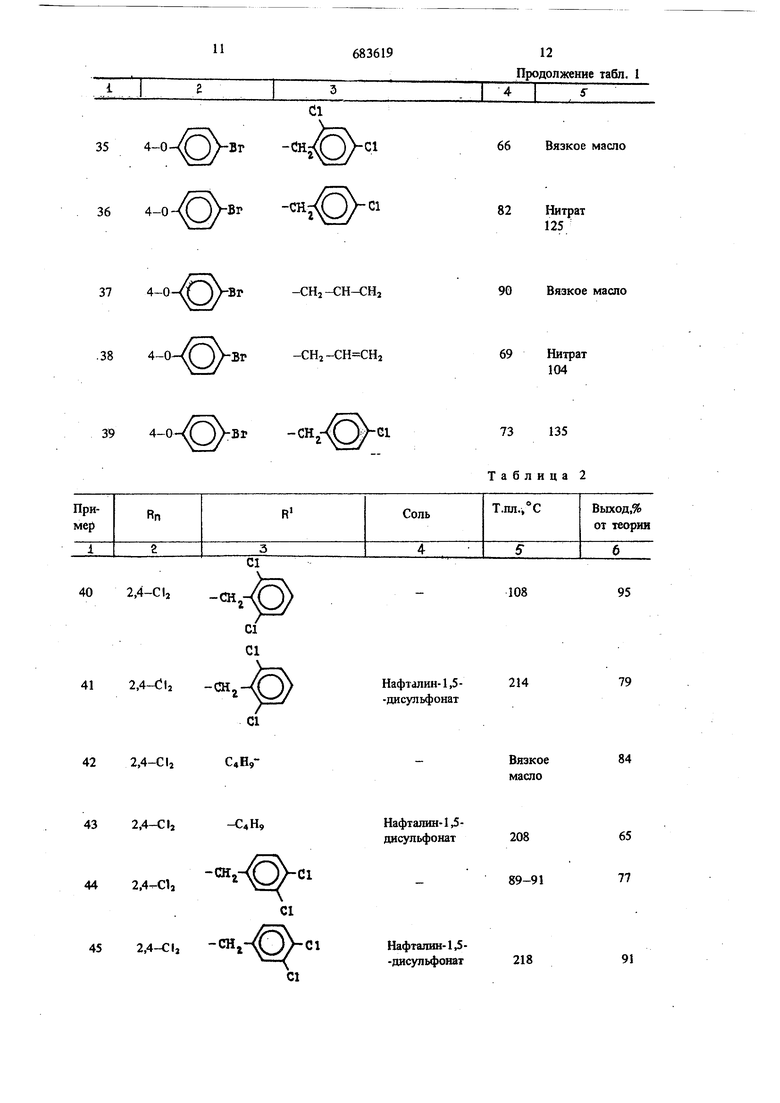



-cH2-eH eHj 17 2,4-Cl2 -CH2-CH CHi 184-0 -cHj 194-0 202,4-CI, 212,4-CI, 224-0 -HOa NH, 71,2-Нафталиндисульфонат79 Нитрат 100 90 п 1,570 94 Нитрат 174 (разложение) 84 Нитрат 124 (разложение) 88XI Нафталнндисульфонат-(1,5) 145
С1-СНз
304-0
-CHj-СвСН
4-0 CJ
г- О 4-Вг
С1 334-8Г -CHj-€H CH, 344-CI
Продолжение габя. 1.
231
X Нафталиндисульфонат-(1,5) (разложение) 211
X Нафталнндисульфонат- (1,5)
(разложение)
158
9476 84 X { Нафталиндисульфонат-(1,5) 231 78Гидрохлоркд
11
Вг-СН
35 4-0
12
683619 Продолжение табл, 1
66 Вязкое масло
Вг-ОН
36 4-0
82 Нитрат 125
37 )Увг-CHj-CH-CHi
38 4-0-(( )Увг-СН,-СН-СН2
90 Вязкое масло
Нитрат
69 104
39 4-0-( ))-ВГ-СН,
73135
40 2.4-CI2 сн
С1 С1
95
108
412, -СН,
79
214
Нафталии-1,5дисульфонат
42 2,4-Cl2С+Н,43 2,4-Clj-С4Н,
С1
44 2,4-СЬ
84
Вязкое масло
65 77
208
89-91
Нафталин-1 91
218 -дисульфонат
15
С1 -CHj-CH CHj
71
16
Продолжение табл. 2
i, . 1
Нафталш -1,5-дисульфонат
86 (разложение) 225
17 Формула изобретения
Способ получения производных триазола общей формулы
СМ 0-R N
где R - хлор, бром, фенил, замещенный хлором, феноксигруппа, незамещенная или замешенная хлором, бромом или нитрогруппой;
R - метил, бутил, аллил, пропаргил, бутенил, бензил, однократно или двукратно замещенный хлором, бензил, замещенный нитроили аминогруппой;
п 1 или 2,
или их солей, отличающийся тем, что соединение общей формулы
683619
18
ом
где R и п имеют указанные значения; М - катион щелочного металла, подвергают взаимодействию с соединением общей формулы R - Hal,
где R имеет указанное значение; Hal - галоген,
при температ)фе 20-150° С в среде разбавителя с последующим выделением целевого продукта в свободном ввде или в виде соли. Источники информации, принятые во внимание при экспертизе

Авторы
Даты
1979-08-30—Публикация
1977-08-02—Подача