h последующим кипячением реакционной смеси.
Предпочтительно взаимодействие проводить в среде диэтилового эфира.
Тетрагалогениды селена или теллура синтезируют, исходя из SeOg или ТеОг и соответствующей концентрированной галогенводородной кислоты. Полученный таким образом в водном растворе тетрагалогенид селена или теллура добавляют при интенсивном перемешивании и охлаждении реакгде А - Se; X - Вг (1а);
А - Se; X - CI (16);
А - Те; X - Вг (1в)7
А - Те; X - CI (1г). Соединения, полученные взаимодействием аллилового муравьиной {иcлoты с тетрагалогенидом селена или теллура, идентичны соеяикениям, полученным при взаимодействии диаллилового эфира и тетрагалогенидов селена или теллура.
Таким образом, расширен круг реакций получения указанных вецеств представлякядих значитапьный интерес в качестве физиологически активных .соединений, а также в качестве промежуточных продуктов тонкого органи ческого синтеза ;
J Пример 1. 1,l-дибpoм-2,б-дибpoммeтил-l,4-ceлeнoкcaн (1а).
11,72 г (0,02 моль) аллилового эфира муравьиной кислоты растворяют в 200 МП эфира и охлаждении льдом и интенсивном перемеошвании добавляют раствор 1,11 г (0,01 моль SeOjt, растворенного в 20 мл НВг. После прибавления SeBr смесь кипят
2ч, затем сушат 1 сут над CaCl, отгоняют растворитель под вйкуумои. Из маслообразного остатка через
1 сут выпадают кристгшлы. Выхбд 0,55 г (11%), т.пл. 105-10б С (из ацетонитрила). Желтые крнсталлш, RI . 0,71 (СЯС1, :С%ОН, 11:1).
Найдено, %t BrBr 65,21.
OSeBrj .
Вычислено,: ВгВг б4,38.
По известной методике получают целевой продукт после многократной кристаллизации из хлороформа с т.пл 124-124,. Это объясняется следуюищм образом. .
В результате разделения продукта, полученного взаимодействием
Ционной массы к эфирному раствору аллилового эфира муравьиной кислоты.
Отличие предлагаемого способа состоит в использовании в качестве непредельного соединения аллилового эфира муравьиной кислоты и проведение взаимодействия при охлаяиении с последующим кипячением реакционной смеси.
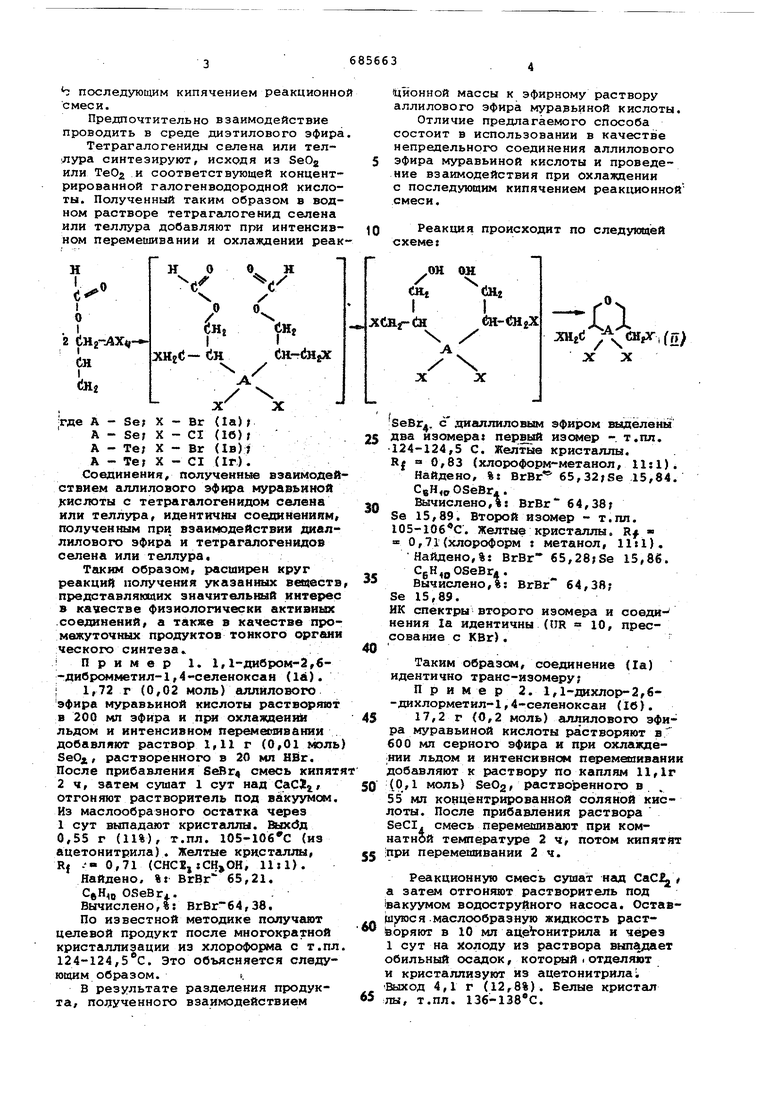
Реакция происходит по следующей схемег
он (2U2
ен-й12Х
:шг« / й1рГ|(й;
/
XX
X
SeBr, с диаплиловым эфиром выделены 5 Двз изомера первый изсмер -. т.пл. 124-124,5 С. Желтые кристаллы. Rf 0,83 (хлороформ-метанол, 11:1).
Найдено, %: ВгВг 65,32;Se 15,84.
CeH pOSeBrj;.
g Шлчислено,%: BrBr 64,38; Se 15,89. Второй изомер - т.пл. 105-106 С. Желтые кристаллы. R 0,71(хлороформ : метанол, 11tl).
Найдено,%: ВгВг° 65,28;Se 15,86.
CgH oOSeBr.
Вычислено,%: BrBr 64,38; Se 15,89.
ИК спектры второго изомера и соединения 1а идентичны (HR 10, прессование с КВг).
Таким образом, соединение (1а) идентично транс-изомеру;
П р и м е р 2. 1,1-дихлор-2,6-дихлорметил-1,4-селеноксан (16). 17,2 г (0,2 моль) аллилового зфира муравьиной кислоты растворяют в 600 мл серного эфира и при охлажде;нии льдом и интенсивном перемешивании добавляют к раствору по каплям 11,1г (0. 1 моль) SeO2 f растворенного в
55 мл концентрированной соляной кислоты. После прибавления раствора SeCI смесь перемв1швают при комнатной температуре 2ч, потом кипятят :при перемешивании 2ч.
Реакционную смесь сушат над а затем отгоняют растворитель под вакуумом водоструйного насоса. Остав|шуюс я маслообразную жидкость раст оряют в 10 мл ацетонитрила и через 1 сут на холоду из раствора выпадает обильный осадок, который - отделяют и кристаллизуют из ацетонитрила; йлход 4,1 г (12,8%). Белые кристал
лы, т.пл. 136-138С.
R OjVeCCHC ojrCjHsOH, 11:1).
Найдено,%: CpCE 44,50.
Cj,H OSeCt . Вычислено,%: CJCt 44,54.
Полученное соединение идентично транс-изомеру, выделенному при разделении продукта, полученного известным способом.
В результате разделения продукта полученного по известной методике, выделе|ш два изомера: первый т..од. 140-141,БС. Белые кристаллы, R. 0,76(CHCJj Cj,H50H, 11:1).
Найдено,: CJCI 44,52,
.
Вычислено, %: crCjT 44,54. Второй изомер - т.пл. 71,5-72,5С. Белые кристаллы, R 0,69(СНС1.:C,HgOH, 11:1).
Найдено,%: 44,50.
СвН оОЗеСТЕд.
Вычислено,%: 44,54.
Таким образом, соединение (16) идентично первому изомеру.
Пример 3. 1,1 дибром-2,6-дибромметил-1,4-теллуроксаи (1в).
17,2 г (0,2 моль) аллилового эфира муравьиной кислоты растворяют в 600 мл серного эфира и при охлаждении льдом и интенсивнее перемешивании прикапывают к раствору 16 г (0,1 моль) ТеО, растворенной в 120 мл бромистоводородной кислоты. После окончания прибавления ТеВг смесь перемешивают при .комнатной температуре 2 ч, а затем кипятят 80 ч. Затем реакционную смесь сушат над GaCtj 1 сут, после чего отделяю верхний эфирный слой от нижнего водно-эфирного и сушат каждый в отдельности над CaCEj 1 сут. Растворитель отгоняют под вакуумом водоструйного насоса. Из эфирного слоя выпадает незначительное количество осадка. Большую часть ветцества выделяют из водноэфирного слоя. Выход 4,8 г (8,7%). Кристаллы желто-зеленого цвета, т.пл. 128-130 с (из бенэола). R{ 0,75 (гексан:эфир, 2:1)
Найдено,%: ВгВг 58,88.
CjHjo ОТеВг..
Вычислено,%: ВгВг 58,65.
С помощью дробной кристаллизации из ацетонитрила проведено разделение изомеров, полученных по известной методике.
Выделено два изомера. Первый т.пл. 107,5-108 с. Желто-зеленые кристаллы. R, 0,06 (гексан:зфир, 2:1).
Найдено,%: ВгВг 58,76.
CjHio ОТеГагд.
Вычислено,%: ,65. Второй изомер - т.пл. . Желто-зеленые кристаллы. Rf 0,75(гексан:эфир, 2:1).,v
Найдено,%: ВгВг 58,81.
CgH,oOTeBr.
Вычислено, %1 ВгВг 58,65.
Соединение (1в) идентично трансизомеру.
Пример 4. 1,1-дюслор-2,6дихлорметил-1,4-теллуроксан (1г).
Получают из аллилового зфира муравьиной кислоты и ТеО«, растворениоЙГ в соляной кйслотеЫ 1,19г/см) по методике примера 1. Выход 50%. Белые кристаллы , т.пл. .140-142 0 (из бензола).
Найдено,%: С 38,90; 38,70. Ce taOTeCe. Вычислено,%} сг 38,62.
Преимуществом данного процесса является возможность получения индивидуального вещества транс-изомера. Формула изобретения
1. Способ получения 1,1-дигалоген-2,б-дигалогенметил-1,4-селен (теллур) океанов общей формулы 1
ОXKid,
йЯ(Х
где А - селен или теллур;
X - хлор или бром,
взаимодействием водного раствора тетрагалогенида селена или теллура с непредельньш соединением в среде растворителя, отличающи йс я тем, что, с целью упрощения технологии процесса, в качестве непредельного соединения используют аллиловый эфир муравьиной кислоты и взаимодействие проводят при охлаждении с последуюсцим кипячением реакционной смеси.
2. Способ по п. 1, отличающий с я тем, что взаимодействие проводят в среде диэтилового эфира.
Источники информации принятые во внимание при экспертизе
1. Lautenchlagen F., Reachlons and propoties of derivatives selen (II). J.Org.chem., 34, 4002 (1969).
2 f Авторское свидетельство
450806, кл. С 07 D 345/00, Ьпублик. 1973 (прототип).

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения пяти- или шестичленных селен (1у) - или теллур (1у) - содержащих гетероциклических соединений | 1973 |
|
SU450806A1 |
| Способ получения симметричных органилселенидов | 1988 |
|
SU1616901A1 |
| ПРОИЗВОДНЫЕ ДИАЗЕПИНОНА, СМЕСИ ИХ ИЗОМЕРОВ И ИХ СОЛИ | 1992 |
|
RU2017740C1 |
| Способ получения 2,5-диметил-4-фенил-4-пропионилоксипиперидина | 1983 |
|
SU1165679A1 |
| Способ получения производных алкилмелатонинов | 1988 |
|
SU1553011A3 |
| Способ получения 9-оксибицикло-(3.3.1)нонен-2-ил-9-фосфонистых кислот | 1974 |
|
SU518499A1 |
| Гербицидный состав | 1977 |
|
SU810066A3 |
| ТРИ- ИЛИ ТЕТРАЗАМЕЩЕННЫЕ 4Н-СЕЛЕНОПИРАНЫ, ПРОЯВЛЯЮЩИЕ АНТИМИКРОБНУЮ И АНТИФАГОВУЮ АКТИВНОСТЬ | 1984 |
|
SU1246566A1 |
| Способ получения 1,1-дизамещенных октагидроиндол-хинолизидинов или их солей или оптически активных изомеров | 1976 |
|
SU657749A3 |
| ПРОЛЕКАРСТВА 3-АЦИЛ-2-ОКСИНДОЛ-1-КАРБОКСАМИДОВ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1993 |
|
RU2124514C1 |


Авторы
Даты
1979-09-15—Публикация
1976-06-21—Подача