1.Медный порошок или порошкообразная медь, полученный измельчением медных болванок, мелких кусков или проволоки.
2.Восстановленная медь, например, получаемая восстановлением соединения меди, например окиси меди, гидроокиси меди, хлорида меди и т. п., при помощи водорода и/или окиси углерода при температуре от
О до 500°С;
3.Восстановленная медь, например, получаемая восстановлением соединения меди, например окислов меди, гидроокиси меди, хлористой меди (хлорной меди) и т. п., с применением обычных восстановителей, например гидразина, боргидрида натрия и т. п., в жидкой фазе.
4.Восстановленная медь, например, получаемая обработкой соединения меди, например окисла меди, гидроокиси меди, хлорида меди и т. п., при помощи металла с большей степенью ионизации, чем у меди, например цинка, алюминия, железа, олова и
т. п., в жидкой фазе.
5.Медь Ренея, например, получаемая через получение сплава Ренея, содержащего медь и алюминий, цинк или магний.
6.Медь, получаемая, например, термокрекингом соединения меди, например, медной псевдокислоты или щавелевокислой меди при температуре от 100 до 400°С.
7.Миогоэлементный катализатор, получаемый, например, сочетанием другого металла, например хрома, цинка, никеля, марганца или молибдена, с одним из указанных медных материалов в процессе получения катализатора.
3. Любой из указанных катализаторов на подложке из инертного материала, например глинозема, кремнезема, кизельгура, пемзы, диатомовой земли и т. п., получаемый нанесением или отложением катализатора на инертную подложку в процессе получения катализатора.
Одним из соответствующих методов получения каталитической меди Ренея является метод Ренея, сходный с методом получения никеля Ренея. Технические или коммерческие формуляции подобных катализаторов легко доступны, например сплав алюминия и меди. Катализаторы обрабатывают или активируют известными способами и получают медный металлический катализатор, пригодный для применения по предлагаемому способу. Обычно подобные методики включают контактированием сплава с сильным основанием в условиях, обеспечивающих выщелачивание алюминия или другого металла.
Различие между указанными катализаторами заключается не столько в селективности реакции, сколько в 11нте 1сивности их действия. Так, например, при гидратировании акрилонитрила в обычных условиях, при соответствующем подборе катализатора и получении его исключительно чистым,
фактор избирательности реакции составляет для акриламида 97% или выше, а эгиленциангидрина он составляет 2% или меньше.
Количество металлического медного катализатора, вносимого по предлагаемому способу, составляет 0,01 -1000 г на 1 моль нитрила при использовании его в суспендированном слое. Такие медные металлические катализаторы пригодны для применения как при серийном, так и непрерывном процессе. При любом методе нитрил и вода контактируют с катализатором в соответствующих условиях реакции, после чего извлекают целевой продукт - амид.
Целесообразно, как правило, подвергать металлический медный катализатор действию реакционной смеси в жидкой фазе. Его можно также подвергать действию реакционной смеси в газообразной фазе.
Соотнощение нитрила и воды в реакционной смеси может колебаться в широких пределах, так как допускается любое количество воды, лишь бы она обеспечивала гидратацию. Важнее, чем соотношение нитрила и воды, является степень взаимодействия между реагентами и высокая степень контакта. При газообразных реагентах нитрил и вода смешиваются во всех соотношениях. При жидких реагентах, однако, полезны некоторые мероприятия, обеспечивающие тесный контакт между нитрилом и водой, например растворение нитрила в воде или воды в нитриле. Кроме пределов растворимости одного реагента в другом, реакционную смесь можно перемещивать или можно вносить подходящий совместимый растворитель, или использовать различные другие средства. К соответствующим инертным совместимым растворителям относятся алканолы, например метанол, диоксан, диметилсульфокснд, ацетон, диметиловый эфир, этиленгликоль, тетрагидрофуран и т. п. Рекомендуемым соотношением нитрила и воды является, как правило, такое, при котором вода берется с избытком, например вода составляет 50-90 вес. % от веса реакционной смеси.
Температура реакции может колебаться в широких пределах в зависимости от нитрила. Реакцию ведут, как правило, при температуре от О до . При температуре, ниже указанного интервала, реакция протекает медленно, а при температуре, выше указанного интервала, увеличивается количество образующихся побочных продуктов реакции. Предпочтительный температурный интервал 50-300°С. Однако при реакциях с возможной побочной реакцией или полимеризацией, например, при конверсии акрилонитрила в акрпламид предпочтительным температурным интервалом является 50-150°С.
Получаемые водные растворы амидопроизводных содержат ничтожные количества
используемых нитратов, и поэтому их можно использовать непосредственно в качестве промежуточных продуктов без необходимости в очистке. Разумеется, что любые вносимые ионы можно вывести при надобности, например, путем использования ионообменной смолы. Далее, в случае, когда целевым продуктом является водный раствор акриламида, его можно непосредственно использовать для получения полимеров, пригодных, например, для использования в производстве бумаги или укреплении почвы, а также для получения кристаллического акриламида. Точно также, в случае, когда целевым продуктом является никотинамид, его можно эффективно использовать в качестве материала для получения сельхозхимикалиев, а также фармацевтических препаратов.
Другим преимуществом данного способа является значительное удлинение срока службы металлического медного катализатора в процессе получения амида из нитрила, так что любое производное амида можно получить в промышленном масштабе, причем эффективным образом.
Конкретнее, соответствующее сочетание медного металлического катализатора и нитратного промотора в соответствии с настоящим изобретением, в отличие от известных сочетаний медного металлического катализатора и промотора в виде медной соли, в значительной мере предохраняет катализатор от порчи или старения, в результате чего можно уменьшить расход медного катализатора, повышая тем самым экономичность процесса.
Нижеследующие примеры иллюстрируют, но не ограничивают изобретения. В примерах все части даны в весовом отношении, а все весовые данные подразумевают сухой вес, если нет особых указаний. Во все.х таблицах количество промотора в промилях дается в весовом соотношении от общего веса жидкого сырья, включающего нитрил и воду.
Пример 1. На месте приготовляют обычным способом 150 г меди Ренея в реакторе емкостью 1 л (из нержавеюшей стали SUS-27), снабженном мешалкой и сепаратором катализатора. Воду и акрилонитрил, очищенные на 90% от растворенного в них кислорода, путем дезоксидации
в дезоксидирующем аппарате, подают в реактор непрерывным процессом со скоростью 700 г/ч и соответственно 300 г/ч п вводят во взаимодействие при 120°С. Вода содержит 39 ррш нитрата натрия, предварптельно внесенного в нее, что соответствует 20 ррт промотора от общего веса жидкого сырья, содержащего акрилонитрил и воду. Реакцию ведут 14 дней и реакционную жидкость анализируют методом газовой
хроматографии; результаты представлены в виде коэффициента конверсии акрилонитрила в акриламид (табл. 1) и коэффициентов конверсии в примеси, особенно в акриловую кислоту, акрилат, этиленциаигидрин, и -оксипропионамид, которые в сумме составляют 0,5% или даже меньше. Для сравнения повторяют реакцию и анализы, но в качестве промотора берут известный промотор - сульфат меди, в количестве 10 ррт иона меди от общего веса жидкого сырья, вместо нитрата натрия. Третью реакцию и анализы осуществляют без участия промотора.
Результаты реакций и анализов представлены в табл. 1.
Таблица I



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения амидов | 1985 |
|
SU1575935A3 |
| Способ получения акриламида или метакриламида | 1971 |
|
SU469243A3 |
| Способ получения акриламида | 1987 |
|
SU1757461A3 |
| Способ получения акриламида | 1972 |
|
SU456408A3 |
| Способ очистки водного раствора акриламида | 1976 |
|
SU703015A3 |
| Способ получения акриламида или метакриламида | 1970 |
|
SU454737A3 |
| Способ получения кристаллического акриламида | 1986 |
|
SU1491331A3 |
| Способ получения амидов карбоновых кислот | 1974 |
|
SU560529A3 |
| Способ получения производных ароматических алканов | 1984 |
|
SU1524808A3 |
| Инсектоакарицидная композиция (ее варианты) | 1981 |
|
SU1477230A3 |

Приведенные в табл. 1 результаты подтверждают повышенные результаты, полученные при использовании промотора - нитрата натрия, по сравнению с известным промотором.
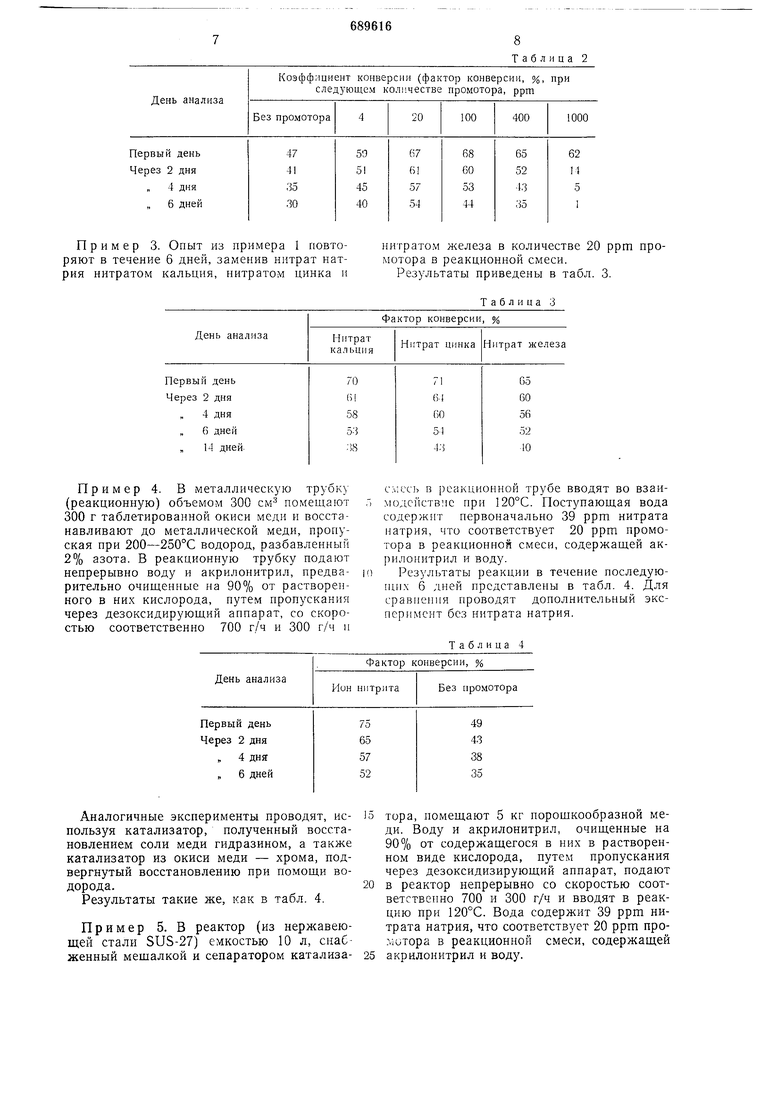
Пример 2. Описанный в примере 1 опыт повторяют в течение б дней, но вместо
Промотора - нитрата натрия берут различные количества нитрата аммония в количестве от 4 до 1000 ррт от веса реакционной жидкости.
Результаты приведены в табл. 2, причем данные колонки «без промотора взяты из табл. 1.
Пример 3. Опыт из примера 1 повторяют в течение 6 дней, заменив нитрат натрия нитратом кальция, нитратом цинка и
Пример 4. В металлическую трубку (реакционную) объемом 300 см помещают 300 г таблетированной окиси меди и восстанавливают до металлической меди, пропуская при 200-250°С водород, разбавленный 2% азота. В реакционную трубку подают непрерывно воду и акрилонитрил, предварительно очищенпые па 90% от растворенного в них кислорода, путем пропускания через дезоксидирующий аппарат, со скоростью соответственно 700 г/ч и 300 г/ч и
Аналогичные эксперименты проводят, используя катализатор, полученный восстановлением соли меди гидразином, а также катализатор из окиси меди - хрома, подвергнутый восстановлению при помощи водорода.
Результаты такие же, как в табл. 4.
Пример 5. В реактор (из нержавеющей стали SUS-27) емкостью 10 л, снабженный мешалкой и сепаратором катализаТаблица 2
нитратом железа в количестве 20 ррт промотора в реакционной смеси.
Результаты приведены в табл. 3.
Таблица 3
Фактор конверсии, %
смесь в )еакционной трубе вводят во взаимодействме при 120°С. Поступающая вода содержит первоначально 39 ррт нитрата натрия, что соответствует 20 ррш промотора в реакционной смеси, содержащей акрилоиитрил и воду.
Результаты реакции в течение последующих 6 дней представлены в табл. 4. Для сравиення проводят дополнительпый эксперимент без нитрата натрия.
Таблица 4
Фактор конверсии, %
тора, помещают 5 кг порошкообразной меди. Воду и акрилонитрил, очищенные на 90% от содержащегося в них в растворенном виде кислорода, путем пропускания через дезоксидизирующий аппарат, подают в реактор непрерывно со скоростью соответственно 700 и 300 г/ч и вводят в реакцию при 120°С. Вода содержит 39 ррт нитрата натрия, что соответствует 20 ррт промитора в реакционной смеси, содержащей акрилонитрил и воду.
Результаты реакции анализируют в течение 6 последующих дней; они представлены в табл. 5. Факторы конверсии в примеси, в особенности в акриловую кислоту, акрилат, этиленциангидрин и р-оксипропионамид сосПример 6. Опыт из примера 1 повторяют в течение 6 дней, заменив акрилонитрил метакрилонитрилом и бензонитрилом. Нитрат натрия введен в количестве, обеспеПример 7. Повторяют опыт по примеру 1, заменив акрилонитрил пропионитрилом и никотинонитрилом (т. е. 3-цианопиридином). Нитрат натрия берут в количетавляют 0,5% или меньше. Дополнительные эксперименты проводят без добавки нитрата натрия для сравнения. Результаты также приведены в табл. 5.
Т а б л II ц а .5
чивающем содержание в реакционной смеси 20 ррш промотора. Для сравнения проводят реакцию без промотора.
Результаты представлены в табл. 6.
Таблица 6
стве, обеспечивающем содержание в реакционной смеси 20 ррт. Для сравнения проводят опыт без добавки промотора. Результаты представлены в табл. 7.
Таблица 7 Как видно из приведенных данных, степень конверсии нитрила в амид повышается до порядка 80%, а активность катализатора с предлагаемым промотором менее снижается во времени, чем без промотора или с известным промотором. Формула изобретения 1. Способ получения амида алифатической или ароматической одноосновной карбоновой кислоты гидратацией нитрила, выбранного из группы: акрилонитрил, метакрилонитрил, бензонитрил, пропионитрил, никотинонитрил, в присутствии медьсодержащего катализатора, например меди Ренея, восстановленной меди, и промотора каталнзатора - нитрата металла, отличающийся тем, что, с целью повыщения степени конверсии нитрила в амид, в качестве нитрата металла используют нитрат аммония, натрия, кальция, цинка или железа в количестве 4-1000 ррт в расчете на реакционную массу. 2. Способ по п. 1, от л и ч а ю щ и и с я тем, что гидратацию ведут при 50-300°С. Источники информации, принятые во внимание при экспертизе 1.Патент США № 3361104, кл. 260-261, опублик. 1971. 2.Патент Японии по заявке № 1724583/ /23-04, кл. С 07С 102/08, с конв. приорит. от 14.12.70 (прототип).
Авторы
Даты
1979-09-30—Публикация
1974-06-05—Подача