(54) СПОСОБ ПОЛУЧЕНИЯ Y-ИЗОМЕРА 2,6-ДИОКСИMETИЛПИPИДИП- ЯC-(N-METИЛKAPБAMATA)



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 2,6-диоксиметилпиридин-бис-( -метилкарбамата) или кристаллической модификации | 1977 |
|
SU697051A3 |
| Способ получения оксиметилпиридинов | 1974 |
|
SU510998A3 |
| Способ получения 2,6-диацилоксиметилпиридинов | 1976 |
|
SU648089A3 |
| Способ получения азотнокислых эфиров 21-спиртов прегнанового ряда | 1972 |
|
SU493963A3 |
| СПОСОБ ПОЛУЧЕНИЯ СТЕРОИДОВ, НЕНАСЬЩЕННЫХ В ПОЛОЖЕНИИ 9 | 1971 |
|
SU421183A3 |
| Способ получения 22 /R, S/-11 @ , 21 - дигидрокси-16 @ , 17-бутилиденбисоксипрегна - 1,4-диен-3,20-диона | 1988 |
|
SU1711675A3 |
| Способ получения производных 17 @ -окси-прегн,-4-ен-3,20-диона | 1982 |
|
SU1132791A3 |
| Способ получения производных 6-оксо-17 @ -этинил-17 @ -трифторацетоксигонана | 1982 |
|
SU1176845A3 |
| Способ получения 1,1-дизамещенных октагидроиндол-хинолизидинов или их солей или оптически активных изомеров | 1976 |
|
SU657749A3 |
| Способ получения 2,6-бис-(хлорметилоксикарбонилоксиметил)-пиридина | 1987 |
|
SU1510717A3 |

1
Изобретение относится к способу получения уИЗомера, одной из полиморфной модификации 2,6-диоксиметилпиридин-быс(N-метилкарбамата), который может найти применение в качестве лекарственного средства.
Известен способ получения 2,6-диоксиметилпиридин-б«с-(1М-метилкарбамата) в виде неоднородного рыхлого порошка путем взаимодействия 2,6-диоксиметилпиридина, растворенного в 10-кратном количестве пиридина, с 1,5 моль метилизоцианата в органическом растворителе при температуре от комнатной до температуры кипения реакционной смеси с последующей отгонкой пиридина и перекристаллизацией целевого продукта из метанола 1.
Продукт, получаемый этим способом, представляет смесь различных кристаллических структур, и его таблетирование является сложной технологической задачей.
Однако с помощью известного способа невозможно получить -изомер 2,6-диоксиметилпиридин-бис- (N-метилкарбамата).
Цель изобретения - способ получения -изомера 2,6-диоксиметилпиридин-бис- (Nметилкарбамата), не требующего грануляции при его таблетировании.
Поставленная цель достигается способом получения Y1зомера 2,6-д1юксиметилпиридин-бнс- (К-метилкарбамата) взаимодействием 2,6-диоксиметилпиридина гидрохлорида с метилизоцианатом в присутствии третичного аммониевого основания, взятого в количестве 1-4 моль на 1 моль гидрохлорида в среде орган1 ческого растворителя, упаривания реакционной смеси и перекристаллизации сырца из воды, а затем из смеси алифатического спирта с 1-3 атомами углерода с водой в соотношении 1 : 1-2 и высушивания при 50-100°С.
Б качестве третичного аммониевого основания предпочтительно использование триалкиламина, например триэтиламина.
Предпочтительно использование в качестве органического растворителя третичного аммониевого основания, тетрагидрофурана, ацетонитрила, галогенированного углеводорода, таких как хлороформ или четыреххлористый углерод, или их смесей.
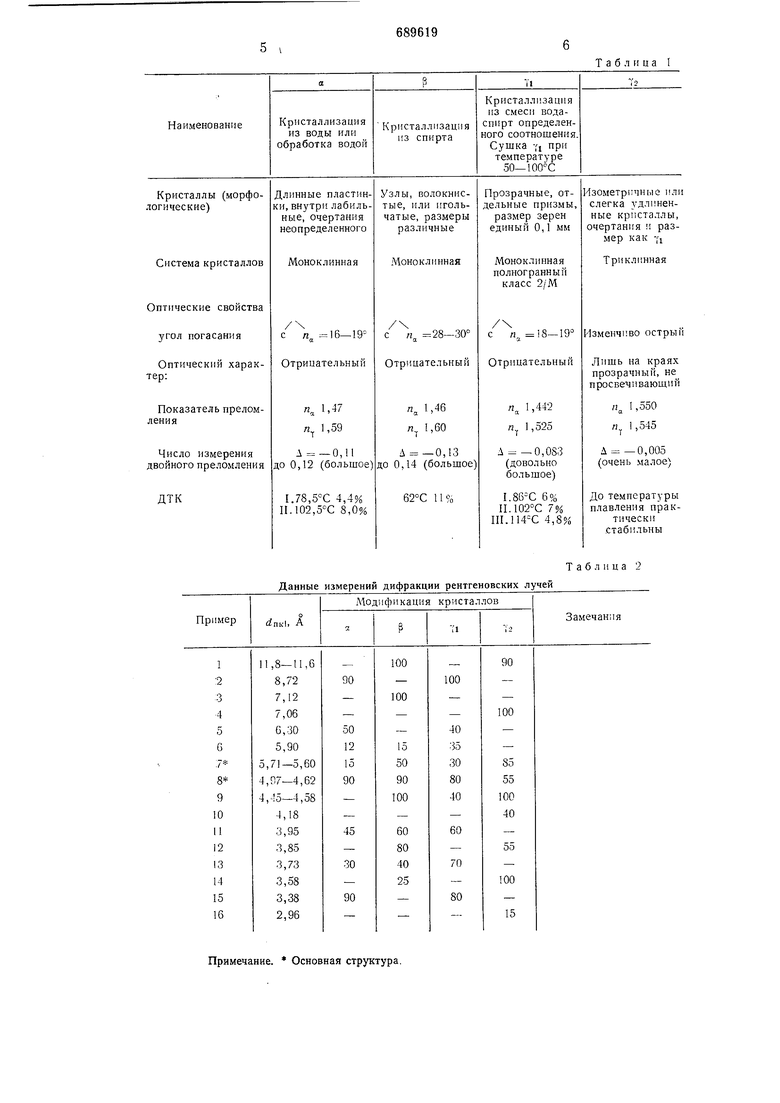
Предлагаемый способ позволяет использовать сырец 2,6-диоксиметилпиридина гидрохлорида, содержащий до 20% органических или неорганических загрязнений, нолучениый при гидролизе 2,6-диацетоксиметилпиридина. Предпочтительно проведение способа ио изобретению нри мольном соотношении 2,6-диоксиыетилииридина, триэтиламина и метилизоцианата, равном 1 : (2-3) : (2- 4), в среде ацетоиитрила. Оитимальным является проведение ироцесса, при котором в начале реакции реакционная смесь находится при комнатной температуре, а затем ее температуру повышают до температуры кипения смеси. С помощью перекристаллизации 2,6-диоксиметилпиридин- (Ы-метилкарбамата) из различпых растворителей, получены различные полиморфные модификации доказанные при рентгеноанализе. а-форму получают кристаллизацией 2,6диоксиметилпиридин - быс-(Ы - метилкарбамата) из воды. Эта модификация образуется и тогда когда кристаллы 2,6-диоксиметилпиридин- (N-метилкарбамата) получают кристаллизацией из органического растворителя. а-форма представляет собой длинные пластинки неодинаковых размеров с моноклинной системой кристаллов. Светопреломление этой формы небольшое, а двойное преломление высокое. Угол погашения (преломления) 16-19°. При сушке поляризационно-оптические свойства вещества практически ие меняются. Другая форма кристаллов - р-форма образуется ири кристаллизации из спирта. Кристаллы этой формы также относятся к моиоклинной системе, однако имеют вид волокон, иногда с узлами. Угол погашения у этих кристаллов 28-30°. Кристаллы сольватированы, и сольватация отличается большой прочностью. При сушке оптические свойства этой формы не меняются. При кристаллизации 2,6-диоксиметилпиридин-(N-метилкарбамата) из смеси алифатического спирта с 1-3 атомами с водой в соотношении 1 : 1, получают угформу кристаллов, морфологические и оптические свойства которой отличаются от свойств аи р-форм. Система кристаллов 2/М полногранная, угол погашения составляет 18- 19°. Показатель преломления Па равен 1,55; пу- 1,442, двойное нреломление большое. Это небольшие, плотные, неагломерированные прозрачные кристаллы; размер их 2: 1, не содержат включений и маточного раствора. Кристаллы ограничены несколькими фасонными поверхностями, размер их 0,1-0,3 мм. При высушивания кристаллического продукта Yi-формы образуется уг-форма, которая может подвергаться без грануляции таблетированию. У2-форма также отличается По своим оптическим свойствам от свойств а, р и уг форм. При сушке 7гформь1 происходит перестройка кристаллов в триклиино-симметричные кристаллы, внутри монокристаллов просматриваются мозаикообразно расположенные различно ориентированные скопления кристаллов. Показатели преломления в продольном направлении (Ла ) приближаются к показателям, преломления л и л,, г. е. двойное преломление на порядок меньше, чем у указанных модификаций. Кристаллы у2-формы, не просматриваются, у2-форму кристаллов не удается получить при высушивании а- или р-формы. В табл. 1 приведены данные различных: модификаций кристаллов 2,6-диоксиметилииридин-(5ыс- (N-метилкарбамата). В табл. 2 представлены данные по измерению дифракции рентгеновских лучей для этих кристаллов. Для получения угформь: 2,6-диоксиметилпиридин-бис-(Ы - метилкарбамата) используют при перекристаллизации смесь спирта с 1-3 атомами углерода с водой в соотношении от 1:1 до 1:2, обычно в 4- 6 раз больше веса перекристаллизовываемого вещества. Предпочтительно использование 4-6-кратного количества 50%-ногО) .метанола. Непосредственно таблетируемого модификацию - 72-форму получают высушиванием угформы при температуре 50-100°С до постоянного веса. Пример 1. А. 15,7 г (0,1 моль) 2,6-диоксиметилпиридин гидрохлорида суспендируют в 176 мл ацетонитрила и затем добавляют 20,8 мл (0,15 моль) триэтиламина. После этого при 20-25°С к реакционной смеси прибавляют. по каплям 13 мл (0,22 моль) метилизоцч-. аната. Реакционную смесь в течение ча.са-. перемешивают при 20-30°С и затем кипя-тят в течение 3 ч. После этого растворитель, упаривают в вакууме. Получают 35-40 г серой кристаллической массы смеси 2,6-диоксиметилпиридинбыс-(N-метилкарбамата) и триэтиламин гидрохлорида. Продукт растворяют в 80 мл кипящей воды, кипятят с 2 г активированного угля в течение 30 мин и фильтруют. После охлаждения выпавшие кристаллы при О-5°С перемешивают в течение 3 ч, а затем фильтруют. Отфильтрованное вещество сушат при 50-60°С. Получают 23,3 г 2,6-диоксиметилпири-. дин-бмс-(N-метилкарбамата) (94,4% теоретического выхода). Продукт плавится при t-135°С; содержание чистого вещества по данным УФ-спектроскопии составляет 99,8% и не обнаруживает примесей при онкослойной хроматографии. Б. 23,3 г полученного продукта растворяют в кипящей смеси 46,6 мл воды с 46,6 мл
Данные измерений дифракции рентгеновских лучей
Примечание. Основная структура.
Таблица I
Таблица 2
метанола. По окончании растворения расTROp пои медленном перемешивании охлажтрют боз нрименония наружного охлажгтриия. При 48-50°С начинаетея кристаллизация. После того, как темнература смеси упадет ниже .35°С. применяют наружное охлаж.денне до О-5°С и смесь при этой температуре оставляют стоять в течение 8 ч После этого фильтруют и суHifiT прн 50--ЛПО°С.
Получают 22.65 г 2.б-т,иоксиметилпирилии-бис- (N-метнлкарбамата), соответствуюгнего трсбовартиям к медицинскому препапату.
Выход нерекристаллнзации составляет 95.7%. Полученный продукт представляет собой моднфикан.ию vs консталлов, пригодHFjix к непосредственному таблетированию. Те лпрратура плавления составляет 134- 13б°С. Содеол ание чистого вегцеетва, определенное УФ-спектросЬотометрическнми измспониями, составляет 99.9%.
П р tf м е р 2. Аналогично нримеру 1, с тем отличием, что вместо анетонитрила в качестве растворителя применяется тетрагкдоофуран. Кипячение проводят не 3, а 5-б ч. Разделение смеси и кристаллизацию проводят так же. как описано в примере I.
Подучают 23,15 г (93,7% теоретического 2.6-диоксилгетилпиридии-бнг-fN - метилкарбамата), который плавится при 134 - 136°С. Содержание вещества, определенное с номощью УФ-снектрогЬотометрических измерений, составляет 99,7%.
П р и м е р 3. 20 г сырна 2,б-диокс1 метилпиридин гидрохлорида (степень чистоты 91,7%) суспендируют в 160 мл ацетонитрила. К суспегтзип прибавляют по каплям 20 мл трнэтиламича и 20 мл метилнзог;ианата. Реакгиюнную смесь перемешивают в течет ие часа при 20-30°С, затем в течение одного ча-а нагревают до температуры кипения и в течение 3 ч кипятят. Затем при уменьпгенном давлении выпаривают досуха. Полученные 38 г продукта перекристаллизовывают по примеру 1 из 76 мл
- -.
ВОДЫ.
Получают 24,4 г 2,6-дтюксиметилпиридинб«с-(КТ-метилкарбамата), который плавится при 134-136°С. Содержание чистого вещества, определенное УФ-спектрометрическими измерениями, составляет 100%. Выход составляет 92,2% (от теоретического).
Продукт перекристализовывают из смеси метиловый спирт - вода по примеру 1 и cyujBT. С тем же выходом получают модификацию кристаллов, пригодных для непосредственного таблетирования. Качество то же, что у продукта, перекрпсталлизованного из воды.
Пример 4. 5,25 г (0,03 моль) 2,6-диоксиметилпиридин гидрохлорида растворяют в 25 мл пиридина и подвергают реакции с
5,3 мл (0,09 моль) метилизоцианата по примеру 1.
Реакнлгонную смесь
раЗуЧеляют, как в примере 1.
Получают 7,65 г (94,0% теоретического выхода) 2,6-диоксиметилпиридин - 6uc-{Nлстилкарбамата), который плавится при 135-137°С. УФ-спектрометрические измерения дают 99% основного вещества и хро rлтoгpaфия в тонком слое показывает отсутствие примесей.
Пример 5. Аналогично примеру 1 с тем отличием, что вместо апетонитрила в качестве растворителя используют 200 мл че--ыреххлористого углерода.
Получают 23,5 г 2,6-диоксиметилпирилпн-бнс-(N-метилкарбамата), степень частоты соответствует продукту, полученному по нримеру I.
Форм у,та изобретения
высунгивают при 50-100°С.
. Способ по пп. 1-3, отличающийс я тем, что в качестве исходного 2,6-диоксиметилпиридина гидрохлопида используют сырец, полученный при гидролизе 2,6-дианетоксиметилпиридина.
тем, что 7гизомер 2,6-диоксиметилпири910
дин-б«с-(М-метилкарбамата) получают пе-быc-(N-мeтилкapбaмaнa) получают из vr
рекристаллизацией из смеси спирта с 1-изомера высушиванием при 50-100°С.
3 атомами углерода и воды в соотношенииИсточники информации,
1 : 1-2.принятые во внимание при экспертизе
тем, что 72-изомер 2,6-диоксиметилпиридин-опублик. 1965.
689619
Авторы
Даты
1979-09-30—Публикация
1977-01-24—Подача