1
Изобретение относится к области органической химии, конкретно к усовершенствованному способу получения органических перекисей, которые на ходят применение в химической промышленности.
Известен способ получения органических перекисей реакцией нуклеофильного замещения при углеродном центре под действием перекисного реагента по сХеме:
R OOR
2.2
где X - ОН, ОВОгОН, , Н ИЛИ алкил 1.
Данный способ требует использования в качестве реагента спиртов, либо их сульфатов или алкилсульфонатов.
Ближайшим по технической сущности и достигаемому результату к изобретению является способ получения органических перекисей взаимодействием алкигтбромидов (третичных и вторичных) или иодидов (первичных) и перекиси . водорода или алкилгидроперекиси с трифторацетатом сеоебра в среде органического растворителя при охлаждении льдом. 2 .
Недостатком способа является использование в качестве реагента малодоступного трифторацетата серебра, а также получение только перекисных соединений алифатического ряда. Выходы перекисей составляют 38-60%.
Цель изобретения - упрощение процесса получения перекисных соединений, увеличение выхода целевых про+ НХ дуктов и расширение универсальности способа. .
Поставленная цель достигается описываемым способом получения органи-ческих перекисей общей формулы
20.
(I)
,
где RJ - изопропил, -бутил или
трифенилметил; 25 Rg водород,трет -бутил, диметилЦиклогексилметил или с.-кумил,
Путем взаимодействия, органического галогенида общей формулы 30R-«X (II)
где R имеет вышеуказанные значении;
К - хлор, бром или иод, и перекиси общей формулы
(III)
RgOOH,
где R- имеет вышеуказанные значения, с солью алифатической карбоновой кислоты в среде органического растБОритепя, отличительной особенностью которого является то, что в качестве соли алифатической карбоновой кислоты используют ацетат одновалентной ртути. Реакция протекает по схеме:
2R.X + 2R,jOOH + Нд,(ОСОСНз)2 - + 2CHjCOOH + ,
где R. - С(СНз)з , СН(СНз)2 / С(), R - Н, С(СНз)} , С(СН,)2 , .
С(СНз)2 СбН ;
X .- CI, ВГ/ J.
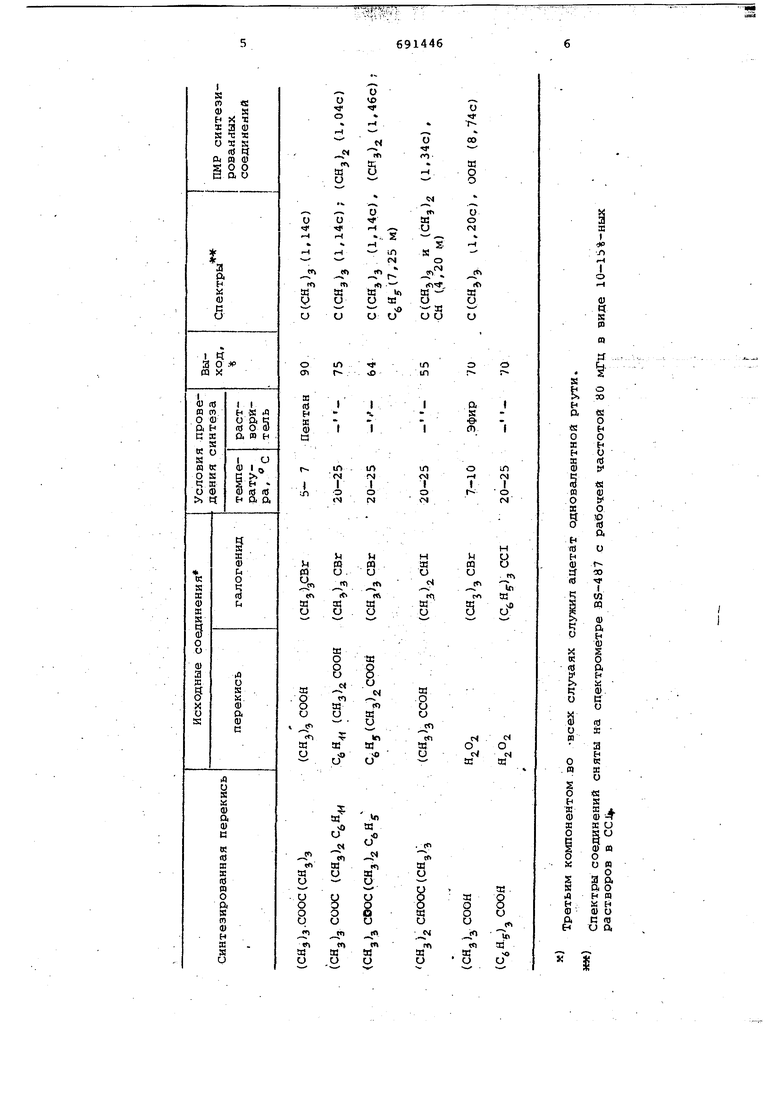
Полученные индивидуальные перекисные соединения и их ПМР спектры приведены в таблице.
Пример 1. Синтез Перекиси третичного бутила. , ,
В реактор, снабженный механичёской мешалкой и,термометром,помещают 50 мл пёнтана, 0,1 г- моль {9,0 г) гидроперекиси, -бутила и 0,1 гк
моль (13,7 г) бромистог о трег -бутила. Смесь охлаждают до , пОрцй ями прибавляют 0,05 г моля (25,9 г) ацетата однова лентной ртути и перемешивают.3-4 ч при комнатной тёМПёра-..
. Образовавшийся осадок бромида одновалентной.ртути отфильтровывают, в фильтрате нейтрализуют уксусную
кислоту раствором б 1карбОната натрия органический слой отделяют и сушат
.над безводным сернокислым магнием. После удаления растворителя остаток разгоняю.т в вакууме (30 мм рт.ст.) и выделяю т при 30°С целевой продукт перекись г/5ег-бутила в количестве 14,7 г 1,3881, выход 90%.
Пр им ер 2. Синтез трет -бутил гексагидро-Л-кумилперекиси.
Целевой продукт получают согласно примеру I из 0,05 г. моль (8,0 г)
.Тйдроперекиси гексагидро-сС кумила, 0,05 г моль (6,8 г) бромистогоr/Jer бутила и 0,025 г МОЛЬ (13,0 г) ацетате, одновалентной ртути. Вакуумной разгонкой вьвде 1яют 7,51 г целевого продукта, т. кип. 62-64с (2 мм рт.с выход 75%, 1,4610.
Пример 3.Синтез трет-бутил-кумилперекиси. .
Целевой продукт получают согласно .примеру 1 из 0,05 (7,6 г) гидроперекиси «А-кумйла, 0,05 г моль (6,8 г) бромистогот/ етбутила и 0,025 г . моль (13,0 г) ацеЬгата одновалентной ртути. Уксусную
кислоту отмывают водой до ее полного отсутствия. Цепевой продукт вьщеляют вакуумной разгонкой, т. -кип. 58-60°С (2 мм рт.ст), выход 64%, п д° 1,4825
П р и м е р 4. Синтез изопропил-т/ ег-бутилперекиси.
Целевой продукт получают согласно примеру 1 из 0,15 г- моль fl3,5 г) гидроперекиси r Jer-бутила, 0,15 г«мол (25,5 г) изопропилиодида и 0,75г мол (39,0 г) ацетата одновалентной ртути. Для сокращения времени реакции в реакционную смесь прибавляют 0,2 мл трифторуксусной кислоты. Вьзделяют 10,92 целевого продукта, т. кип. 5lc (123 мм рт.ст) , выход 55%.
Пример 5. Синтез гидроперекиси ГуОег -бутила.
В реактор, снабженный механической .мешалкой и термометром, помещают 50 мл«абсолютного эфира, 0,05 г-моль (6,8 г) Tfier-бутилбромида, 0,05 г -моль (6 мл) эфирного раствора перекиси водорода (с концентрацией 0,29 г В.1 мл). Смесь охлаждают до 7-10°С и порциями прибавляют 0,025 г. моль (13,0 г) ацетата одновалентной ртути Затем перемешивание продолжают ч при комнатной тем.пературе. Образовавшийся осадок бромида одно.валентной ртути отфйльтровывайт. В фильтрате нейтрализуют уксусную кислоту раствором бикарбоната натрия, смесь переносят в делительную воронку, отделяют органический слой и сушат его над безводным сернокислым магнием. Послё удаления растворителя остаток разгонют в вакууме и вьщеляют при (20 мм рт.ст) целевой продукт - гИдponepeKHcbT/Jeг-бутила, выход 70%.
Пример 6. Синтез гидроперекиси трифенилМетила..
Целевой продукт получают согласно примеру 5 в среде абсолютного эфира при 20-25 С. В реакцию берут 0,02 г« хмоль (5,56 г) трифенилхлорметана, 0,02 г.МОль (2,5 мл) эфирного раст- . вора , (с концентрацией 0,29 гв 1 мл раствора) и 0,01 г моль (5,2 г) ацетата одновалентной ртути. Кристаллизацией из смеси эфира и пёнтана выделяют 3,96 г целевого продукта - гидроперекиси трифенилметила, выход 70%, т. пл. 82С. :
Из приведенных примеров и данных таблицы видно, что целевые продукты получают с хорошими выходами и высокой степенью чистоты. Применение в качестве реагента ацетата одновалентной ртути значи±ельно упрощает процесс получения целевых продуктов и дает возможность получать перекисные соединения с алифатическими, циклоалифатическими и аралифатическими радикалами. 7 69 Формула изобретения Способ получения органических перекисей общей формулы. 12 . ( где R - изопропил, гяег -бутил или трифенилметил; R - водород, трет -бутил, диметилциклогексилметил или « -ку путем взаимодействия органического галогенида общей формулы : . ( где R имеет вышеуказанные значения,-. X - хлор, бром или иод; и перекиси общей формулы R2OOH , . (Ill) 1446 g гяе R2. имеет вышеуказанные значения; с солью алифатической карбоновой кислоты в среде органического растворителя, отличающийся тем, что, с целью упрощения процесса, увесличения выхода целевых продуктов и 5расширения универсальности способа, качестве соли алифатической карбо.. j, используют ацетат одноралентной ртути. ,f4 Источники информации, принятые во Ш экспертизе . Хавкинс Э. Дж. Органические перекиси, М. , 1964, с. 19-249. 2. Cobkson P. G., Davies A. G., t,.Roberts B. P, A convenient and 15general preparation of alkyl hydroperoxides and dialkyi peroxides. . j, hem Soc., Chem Cortmun., 1976, p. 24, 1022-3 (прототип).


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения перекисных соединений, содержащих металлорганические группировки | 1974 |
|
SU502895A1 |
| Способ получения 2-(6 @ -карбоксигексил)-циклопент-2-ен-она | 1985 |
|
SU1334644A1 |
| Способ получения простых олигоэфиров с концевыми перекисными группами | 1978 |
|
SU763374A1 |
| СПОСОБ ПОЛУЧЕНИЯ БЕНЗИЛХЛОРИДА | 2005 |
|
RU2291144C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПЕРЕКИСНЫХСОЕДИНЕНИЙ, СОДЕРЖАЩИХ МЕТАЛЛООРГАНИЧЕСКИЕ ГРУППИРОВКИ | 1972 |
|
SU425914A1 |
| Способ получения -оксидиалкилперекисей | 1977 |
|
SU767095A1 |
| Способ получения ацетальсодержащих олигомеров | 1976 |
|
SU597208A1 |
| СПОСОБ ПОЛУЧЕНИЯ АЛКАНСУЛЬФОХЛОРИДОВ | 2002 |
|
RU2231524C2 |
| СПОСОБ ПОЛУЧЕНИЯ МЕРКАПТАНОВ | 1973 |
|
SU381219A1 |
| Способ получения смеси алифатических кетонов | 1977 |
|
SU679570A1 |


Авторы
Даты
1979-10-15—Публикация
1978-03-13—Подача