водных 3-карбамоилоксиметил-7 фурил(тиенил или фенил)ацетамидоцеф 3-ем-4-карбоновой кислоты, обладающих физиологической активностью, ацилированием 3 карбамоил-7-аминоцеф 3-ем-4-карбоновой кислоты 1 ,
Целью изобретения является синтез новых производных цефалоспорина, рас1аиряющих ассортимент средств воздействия на живой организм.
Предлагаемый способ заключается в том, что соединениеОбщей формулы
NHR,
.хЧ.
( 1 /Х
15H-J--j %
,OC-«H
N I OR
II о
(3)
где R. - группа, удаляемая кислым ..гидролизом или гидрогенолизом, или хлорацетил; 1 - имеет указанные значения,, в виде сии-изомера обрабатывают кислым агентом гидролиза или гидрогенолиза .или тиомочевиной и выделяю целевЪй продукт в виде свободной .йислрты или ее соли (щелочного Металла, щелочно-земельного металла магния или аьшнированного Органического основания.
в качестве кислого агента гидролиза, действию которого подвергают при необходимости продукты Обшей формулы 3 можно назвать трифторуксусную, муравьиную или уксусную кислоты.;Эти кислоты. мож- но применя ь безводными или в сутствии воды. В качестве агента гидрогенолиза можно назвать систему цинк-уксусная кислота.
Используют преимущественно такой кислвзтй агент г адролиза, как беэводяая трифторуксусная кислота, водная муравьиная кислота или водная уксусная кнслота,-чтобы удалить группы третичного бутоксикарбонила ЙЛ.И тритила.
Используют преимущественно систему цинк-уксусная кислота, чтобы удалить группу трихлорэтила, и катлитическое гидрирование, чтобы удалить №Уппу бензила, дибензила и карбобензшюксигруппу.
Солеобразование продуктов общей формулы 1 можно осуществлять, например, действием на кислоту минерального основания {гидроокиси натрия или калия, или карбоната, или кислого карбоната натрия) или органического основания, такого как триэтиламин.
Солеобразование преимущественно проводят в растворителе или в смеси растворителей (вода7 метанол, этанол, ацетон, диоксан).
В приводимых далее примерах описаны способы получения как целевых, так и исходных продуктов.
Пример 1. 3-Карбамоилоксиметил-7- 2(2-тритиламино-4-тиазолил)-2- (метоксиимино)ацетамидо1 цеф-З-ем-4-карбоновая кислота.
А. Натриевая соль З-оксиметил-7-Г2- (2-тритиламино-4-тиазолил) -2- -- (метоксиимино)ацетамидо1 цеф-З-ем-4-карбоновой кислоты.
Смешивают в атмосфере азота 85 мл
5 метанола и 1,7 г диэтиламиновой соли З-ацетоксиметил-7- 2-(2-тритиламино-4.-тиазолил) -2-{метоксиимино}ацетамидо1 цеф-З-ем-4-карбоновой кислоты Доводят раствор до -25°С и добавляют за
0 2 мин 380 г метилата натрия. Перемешивая при.-20°С в т,ечение 4 ч 30 мин, добавляют 126г г метилата нат-рия и смесь перемешивают еще в течение 4 ч. Насыщают ,массу льдом,
5 затем .выливают при .-20°С в 680 мл эфира.
После выдержки в течение ночи в холодильнике производят обезвоживание и промывку эфиром. Получают
0 А,89 г белого вещества с 210230°С с разложением.
Б. 3-Карбамоилоксиметил-7- 2-(2-тритиламино-4-тиазолил)-2-(метоксиимино)aцeтaмндo цeф-3 eм-4 кap 5 боковая кислота
Смецшвают в атмосфере азота 30 мл хлористого метилена и 0,75 мл трихлорацетилизоцианата. Поддерживают температуру О- и добавляют
за 4 мин 1,5 г продукта, полученного на стадии А.
После введения половины полу(ченного продукта добавляют 0,25 мл трихлорадетилиэоциаЕШта, в конце введения опять добавляют еще 0,25 /lл
5 После 10 мин перемешивания при О - 5 С добавляют 1 мл метанола и концентрируют почти досуха в вакууме. Снова растворяют в 30 мл -метанола и добавляют раствор 915 мг
0 кислого карбоната натрия в 22,5 воды, Массу перемешивают 3 ч при комнатной температуре, декантируют, концентрируют, подкисляют до рН 2 нормальной соляной кислотой, обез5 воживают осадок, промывают водой, затем эфиром, замешивают в.эфире и сушат в вакууме.
Получают 600 мг твердого вещеQ ства, т.пл. 210°С (разложение), , 0,28 (этилацетат:этанол1воца 7г2:1) .
Диэтиламиновую соль 3 ацетоксиметил-7-Г2-{2-тритиламино-4-тиазо5 лил)-2-(метоксиимино) ацетамидо) ;1еф- -З-ем-4-карбоновой кислоты получаю следующим образом.
2-(2-Амино-4-тиазолил)-2-метоксииминоэтилацетат. Загружают 1 г }(-хлор-о(- метоксииминоэтилацетата, 3 мл абсолютного этанола и 0,42 г измельченной мочевины и перемешивают при комнатной температуре прилизительно 2 ч. Разбавляют 60 мл эфира, кристаллизуют полученный хлоргидрат, перемешивают, обезвоживают, промывают, сушат и получают 685 мг хлоргидрата. Растворяют их в 4 мл воды при 50°С, добавляют ацетат калия до получения величины pri 6, свободный амин кристаллизуется. Охлаждают, обезвоживают, промывают водой, сушат и получают 27Q мг ожидаемого продукта, т.пл. 161°с:
2-(2-Тритиламино-4-тиазолил)-2-метоксииминоэтилацетат.
4,6 г продукта, полученного на предшествующей стадии, растворяютпри 30°С Б 92 мл хлористого метилена. Охлаждают до -10°С, добавляют 2,9 мл триэтиламина, охлаждают еще до -35°С, добавляют за 15 мин 6,1 г хлористого тоитила. оставляют смесь до достижения комнатной температуоы йли на 2 ч 30 мин. Промывают водой, затем 0,5 н. соляной кислотой и ацетатом натрия в воде. Сушат, концентрируют, поглощают эфиром, снова концентрируют, растворяют в метаноле, добавляют воду и эфир, оставляют для кристаллизации, обезвоживают, промывают эфиром и получают 6,15 г ожидаемого продукта, т.пл. .
2-(2-Тритиламино-4-тиазолил)-2-метоксииминоуксусная кислота.
7,01 г полученного эфира растворяют в 35 мл диоксана, доводят до 110®С на масляной бане и добавляют, за 5 мин 9 мл 2 н.раствора гидроокиси натрия, промывают 30 мин с флегм при перемешивании. Натриевая соль кристаллизуется. Охлаждают, обезвоживают, промывают диоксаном, затем эфиром и получают 5,767 г соли. Концентрируют маточный раствор и получают еще 1,017 г,всего собирают 6,784 г соли.
Добавляют 3,06 г соли в 65 мл хлористого метилена и 6,5 мл 2 н. соляной кислоты, промывают водой, сушат и концентрируют досуха, чтобы получить количественно свободную кислоту.
Диэтиламиновая соль 3-ацетоксимеТИЛ-7-Е2- {2-тритиламино-4-тиазолил -2-метоксииминоацетамидо цеф-З-ем-4-карбоновой кислоты.
Кислоту, полученную на предыдущей стадии из 153,6 г натриевой соли, растворяют в 450 мл хлористого метилена в инертной атмосфере.
Охлаждают на ледяной бане. При добавляют 36 г дициклогексилкарбодимида. Перемешивают 40 мин при 5°с и 30 мин при . Обезвоживают осажденную дициклогексилмочевину. г Охлаждают при температуре между и предьщущий раствор и добавляют к нему при -1СГС раствор из 40,8 г 7-аминоцефалоспорановой кислоты в 600 мл хлористого ме.- тилена и 41 мл триэтиламина. Смесь оставляют до достижения комнатной температуры, перемещивают, промывают два раза 1 н. соляной кислотой и 3 раза водой. Сушат, концентрируют, поглощают этилацетатом и выпаривают 15 досуха. Продукт растворяют в 350 мл эфира, затем 33 мл .диэтиламина, перемешивают 20 мин, фильтруют, концентрируют фильтрат и добавляют приблизительно 2,5 л эфира. Перемешивают, обезвоживают и получают 110,3 г ожидаемой соли.
Jf -Хлор-с -метоксииминоэтилацетилацетат, используемый ранее, приготовляют следующим образом. 25 Берут 22,5 г -у-хлор-йС-оксииминоэтилацетилацетата в 100 мл хлористого метилена. Помещают на ледяную баню и медленно добавляют при перемешивании свежий раствор диазомета30 на (21,6г/л или 275 мл). Оставляют на 5 мин раствор и разрушают избыток диазометана небольшим количеством окиси алюминия. Концентрируют, затем очищают элюированием на дву25 оккси кремния с хлористым метиленом. Получают 11,93 г ожидаемого продукта.
Пример 2. 3-Карбамоилоксиметил-7- 2-(2-тритиламино-4-тиазолил) -2- (метоксиимино) ацет.амидо цеф -З-ем-4-карбоновая кислота.
А. Натриевая соль 3-оксиметил -7-С2-(2-тритиламино-4-тиазолил)-2-(метилоксиимино)ацетамидоЗ цеф-З-ем-4-карбоновой кислоты. 5. а) Смешивают в атмосфере азота 15 мл сухого метанола и 272 мг 7-аминоцефалоспорановой кислоты. Доводят температуру до и добавляют за 3 раза 136 мг метилата 0 натрия. Перемешивают 7 ч 30 мин при -15 С, затем используют продукт непосредственно в ходе синтеза.
б) Вводят 1 г натриевой соли 5 2-(2-тритиламино-4-тиазолил)-2-метоксииминоуксусной кислоты и 8 мл хлористого метилена, 1 мл эфира и 4 мл 1 н.соляной кислоты. Перемешивают до растворения, декантируют Q и повторно экстрагируют хлористым .метиленом. Промывают водой, сушат и выпаривают досуха.
Полученный продукт снова растворяют в 4 МП сухого хлористого метилена, добавляют 235 мг дициклогекилкарбодиимида, перемешивают 30 мин ри комнатной температуре, обезвожиают образовавшуюся дициклогексилочевину и промывают хлористым меиленом.
в) Раствор б добавляют к проукту а, предварительно насыщенноу льдом. Перемешивают 30 мин при , затем оставл яют на ночь при °С. Осаждают продукт добавлением зопропилового эфира. Получа1от 800 мг продукта, идентичного проукту, полученному на стадии А приера 1. .
В. З-Карбамоилоксиметйл-7-t2-(2-Тритиламино-4-тиазолил) -2- (меток-аиимино) ацетамидо1-цеф-3-ем-4-кар-боновая кислота.
Процесс ведут аналогично стадии В примера 1 для получения указанного продукта.
Пример 3. 3-Карбамоилоксиметил-7- 2 {2-тритиламино-4-тиазо-лил) -2 (метоксиимино) ацетамидо деф--3-ем-4-карбановая кислота.
2-(2-Тритиламино-4-тиазолил)-2-метоксниминоуксусную кислоту, полученную, как описано ранее, из 1,81 г ее натриевой соли, растворяют в 20 мл- сухого хлороформа, добавляюг 0,48 г дициклогексилкарбодиимида и перемешивают 45 мин при комйатной температуре. Обезвоживают Образовавшуюся мочевину, охлаждают до.-Ю-с и добавляют раствор из 0,5 г 3 карбамоилоксиметил-7 аминоцеф-З-ем-4-карбоноБОй кислоты в 8 мл хлороформа и 0,5 мл тризтиламина.
После выдержки в течение ночи при смесь экстрагируют 4%ным раствором бигсарбоната натрия. Водный раствор промывают эфиром, затем подкисляют до рН 2, осадок обезвоживают, промывают водой и эфиром, сушат и получают продукт, идентичный продукту, полученному в примере 1.
Пример 4. 2-{2-АМИНО-4-тиазолил)-2-(метоксиимино)-этилацетатр син-изомер.
Смешивают 1 г З-хлор-об-метоксииминоэтйлацетилацетата3 мл абсолютного этанола и 0,42 г измельченной тиомочевины. Смесь перемешиваю при комнатной температуре приблизительно 2 ч. Разбавляют 60 Mji зфира, полученный хлоргидрат кристаллизуется, иго перемешивают, обезвоживают, промывают, сушат иполучают 685 г хлоргидрата, который растворяют в 4 мл воды при 50°С, добавляют ацетат калия до получения рН .6, свободный амин кристаллизуется. Смесь охлаждают, обезвоживают, промывают водой, сушат и получгиот 270 MI ожидаемо;го продукта, т.пл. 161 °с..
2-(2-Хлорацетамидо-4-тиазолил);-2-(метбТ сиимино) этилацетат, синГ-изомер.
Смешивают. 45,8 г 2 -(2-амино-4--тиазолил) -2- (метоксиимино) этилацетата, син-изомера, и 200 ivui хлористого метилена. Отгоняют 20 мл для сушки, охлаждают до 10°С и добавляют 50 мл пиридина. Добавляют 41 г ангидрида монохлоруксусной кислоты и слегка нагревают до растворения. Оставляют на 6 ч при 20°С в атмосфере азота,добавляют 5 мл во перемешивают и выливают в 300 мл 2 ледяной соляной кислоты. Декантируют, экстрагируют хлористым метиленом, промывают водой, кислым карбонатом натрия, водой, сушат, пропускают через активированный уголь, концентрируют и добавляют 300 1ЛЛ изопропилового эфира Продукт кристаллизуется. Концентрируют до получения густой пасты, охлаждают, обезвоживают, промывают изопропиловым эфиром, сушат и получают 45,4 г продукта, т.пл. 113с,
Получают чистый образец перекрис,таллизацией из смеси хлористого метилена и изопропилового эфира, т.пл. 118°С.
2- (2-Хлорацетамидо-4-тиазолил)-2-(метоксиимино)уксусная кислота, син-изомер.
Вводят 46 г продукта, полученного на предыдущей стадии, в 250 мл абсолютного этанола. Добавляют при в атмосфере азота 30 мл чистого натрового щелока. Продукт растворяют, соль натрия начинает кристаллизоваться, затем среда схватывается. Через 16 ч обезвоживают и промывают этанолом.. Полученную соль растворяют в воде, охлаждают, добавляютЮО мл 2 н. соляной кислоты насыщенной хлористым натрием, экстрагируют, этилацетатом, содержащим 10% этанола. Сушат, пропускают через активированный уголь, отгоняют в вакууме, удаляют воду бензолом, поглощают в хлористом метилене, перегоняют досуха, поглощают хлористым метиленом, охлаждают, обезвоживают, промывают хлористым метиленом, сушат и получают 34,5 г ожидаемого продукта, т . пл . , Очищают продукт перекристаллизацией из смеси ацетона и изопропилового эфира.
Найдено,%: С 34,8; Н 2,8;
N 14,8;С#12,6; S 11,5.
(мол,в. 277,68)
Вычислено,%: С 34,60; Н 2,90;
N 15,13; СС 12,77; S 11,55.
З-Ацетоксиметил-7- (2-хлорацетамидо-4-тиазолил)2-(метоксиимино; ацетамидо цеф-3-ем-4-карбоновая кислота, син-изомер. : Вводят 15,3 г продукта, получейного на предьщущей стадии, в 80 мл хлористого метилена. При 5 добавляют 8 мл триэтиламина. При Ос и в атмосфере аёота, вводя 3,8 МП хлористого тионила и 26 мл хлористого метилена. CMBCJ ост&вляют на 15 мин при , затем , добавляют 7 мл триэтиламина,, Вво дят.при 0°С и Е атмосфере азота 13,6 г 7-аминоцефалоспорановой кислоты в 100 мл хлористого метилена и 14 мл триэтиламина. Повы Шают температуру до 20°С, перемешивают 1 ч. Этот раствор перегоняют досуха в вакууме при 30-35°С Растворяют остаток в 250 мл воды, .пропускают, через активированный уголь, добавляют 5 мл 2 н, соляной кислоты, Обезвоживают осадок , промывают водой. Полученный сырой продукт суспендируют в 80 мл этанола. При 5°С добавляют 7 мл триэ тиламина. Добавляют сразу при пере мешивании и при 15 мл 4 н.сер кислоты, продукт кристаллизуется. Через 15 мин обезвоживают, промывают этанолом замешиванием, затем эфиром, сушат в вакууме и получаю 18,6 г ожидаемого продукта , Л. jj 26t. (1%, в дкметилформамкде) . 3-ОКСИМРТИЛ-7-С2- {2 хЛоратдета™ мидо 4-тиа5олкл)2(метоксиимино) .ацетаг-.мдо цеф-З-е.м-4-карбоновая -, .кислота , ск.:1-:ч:.зомерс Смеш11вают 240 мл дистиллирован ной воды при 37°С и 40 г обезжире ного ростка гш;еницы, перемешивают 30 мин при , центрифугируют п и получают всплывшую массу (205 см) при рН 6,S, Вводят в 96 мл дистиллирозанной воды 1,6 г -3-ацатоксиметлл--7- 2- (2-хлорацет М11ДО-4 -тиаэолил) -2- {метоксиимино) а ; а ./1идо цеф-3-ем 4--карбоновой кисло ты, син-иэомера. Получают суспензию с рН 4,3, которую доводят до рН 6,7 добавлением 11,9 мп 0,2 н.е кали. Раствор становится прозpa.4HHf4. Вводят при перемешивании, при и в атмосфере азота192 см свежего ферментативного раствора, описанного раньше, затем пре.дыдуэдий. кислый раствор с рН 6,7. Величину ЪН поддерживают 6,5 автоматическим добавлением 0,2 н. едкого кали. Контролируют реакцию хроматографией в тонком .слое. Прекращают реакцию по прошествии 4ч, центрифугируют при 5°С, растирают осадок в 19 мл ледяной воды, затем центрифугируют при в течение 30 tJOiH, ВсплЕлвшую массу соединяют и концентрируют цо 61 мл. ДобайляJ9T 168 мл ацетона, «тобы осадить протеины, фильтруют, промывают замешиванием 3 раза по 16 мл раствора воды и ацетона (1:2,5). Соединяют фильтрат и промывные-воды и добавляют 640 мг газовой сажи, перемешивают 1 ч при комнатной температуре, затем фильтруют, промыв;1ют смесью воды и ацетона, соединяют промывочные воды и фильтрат концентрируют на водяной бане, затем добавляют 5 мл муравьиной кислоты .Происходит кристаллизация. Смесь оставляют на ночь при 5° с и обезвоживают кристаллы, промы-, вают водой и получают 76,1 г ожидаемого продукта, который перекристашлизовывают следующим образом. Добавляют 727,4 мл полученного продукта к 28 мл дистиллированной /воды. Вводят 134 мг кислого Kap6q-. ната натрия, перемешивают, отделяют нерастворившуюся часть, снова..добавляют 50 мг кислого карбоната натрия, перемешивают 15 мин, добавляют 142 мг газовой сажи, перемешивают 30 мин при комнатной температуре, фильтруют, промывают 3 раза 2 мл воды. Соединяют промывочные воды и фильтрат, добавляют 1 мл уксусной кислоты, затем 0,5 мл муравьиной кислоты, продукт медленно кристаллизуется. .Его обезвоживагст, промывают дистиллированной водой и получают 635,9 мг продукта посл-з сушки. fiCjjj ,63,4 (0,5%, в i кислом карбонате натрия с 0,5 М). Ядерный магнитный резонанс (диметилсульфо ;сид, 60 МгЦ)-: 7,48 протона в тиазоловом цикле, 3,91ррт метоксиоксима, 4,28 ррт метилена группы . З-Карбамилоксиметил-7-: 2-{2-хлорацетамидо-4-тиазолил)-2-jMeтоксиимино)ацетамидо цеф-З-ем-4-карбоновая кислота, cин-изoмept Смешивают 1,56 г З-оксиметил-7 2-(2-хлорацетамидо-4-тиазолил)(метоксиимино)ацетамидо цеф-З-ем-4-карбоновой кислоты, син-изомера, полученного на предыдущей стадии, 18 мл пиридина и 60 мл тетрагидрофурана. Доводят температуру до -25°С и добавляют за один раз 3 мл трихлорацетилизоцианата. Температура повышается до , затем снова падает. Выливают 600 мл раствора, насыщенного кислым карбонатом натрия, в воду для разбавления наполовину, перемешивают при комнатной температуре, экстрагируют 4 раза 25 мл этилацетата. Промывают каждый экстракт 125 мл раствора кислого карбоната натрия, насыщенного и разбавленного наполовину. Соединяют все основные водные азы, доводят их до нейт.ральногб состояния 2 н. соляной кислотой, кстрагируют .два раза (по 250 мл)
этилацетатом, промывают насыщенным раствором хлористого натрия, снова экстрагируют тётрагидрофураном и опять промывают. Соединяют органические фазы, промывают соленой водой, сушат, выпаривают при пониженном давлении, растирают полученную резину с эфиром, перемешивают при комнатной температуре, обезвоживают, прополаскивают, сушат и получают 1,020 г белого порошка, т.пл. 24бС(с разложением), Rif 0,37 (этилацетат:уксусная кислота: вода ,80:15:5),
: Пример 5. З-Карбамоилоксиметил-7- 2-(2-амино-4-тиазолил)-2-{метоксиимино) ацетамидо цеф-З-ем ;4-карбоновая кислота.
Смешивсют 500 мг продукта, полученного в примере 1, и 5 мл 8%-ной уксусной кислоты в воде. Перемешив:ают 2 ч 30 мин при 50°С, охлаждак1Т до комнатной температуры и осаждак)т добавлением 40 мл эфира. Обезвоживают, промьшают эфиром и получак1Т 290 мг твердого загрязненного креМа.
Растворяют ,270 JMr предыдущего ародукта в 4мл-8%-ного .раствора уксусной кислоты в воде. Добавляют 4 мл этилацетата, фильтруют, промывают смесью 8%-ной уксусной кислоты в воде:этилацетате (1:1), перемешивают фильтрат с 270 мг двуокиси кремния „ После фильтрования и про-мывки осаждают добавлением эфира, дбезвоживают и промывают эфиром. Получают 136 мг продукта, т.пл. 260°С, Rf 0,35 {этилацетат:этанол : вода 6:2:2) .,
Пример 6. 3-Карбамоилоксиметил 7 2-(2-амино-4-тиазолил)-2-(метоксиимино)ацетамидо цеф-З-ем-4-карбоновая кислота, син-изомер,. Берут 950 мг продукта, полученч кого на ;предшествующей стадии, , и 171 мг тиомочевины в 2 мл дистиллированной воды. Помещают в ледян по баню и вводят за несколько раз 190 мг кислого карбоната калия. Массу выдерживают до получения комнатной температуры и оставляют на 5 ч 30 .мин при перемешивании, затем добавляют 6,7 мл воды и добавляют муравьиную кислоту до нейтральной реакции. Растирают в ледяной баяе, с безвоживают, промывают 3,8 мл воды С 10% муравьиной кислоты, поглоща1Ш 5,7 мл воды, выдерживают на льду и добавляют триэтиламин для лучшего растворения. Вводят 0,6 мл муравьиной кислоты, обезвоживаиот при помощи 3,8 мл во;с;ы с 10% муравьиной кислоты за 2 раза и удаляют темно-коричневую резину. Соединяют водные фазы, обрабатывают и 10,25 г сульфата аммония, обезвоживают осадок, замешивают в воде, затем в эфире, сушат и получают 470 м наскщая маточные растворы сульфатом аммония, получают дополнительно 52 мг.
Продукт очищают следующим образом. Перемешивают 2 ч при комнатной температуре 46 мг сырого про- дукта, содержащего муравьиную кислоту, и 0,12 мл абсолютного этанола с 0,1 ммоль пиридина. Обезвоживают, промывают абсолютным этанолом, сушат и получают 32 мг очищенного белого порошка,
Ядерный магнитный резонанс (60 Мгд, диметилсульфоксид) jrpm 6,75 протонов в тиазоловом , 6,58 группы OCONH2.
Пример 7. Натриевая соль З-карбамоилоксиметил-7- 2-(2-амино-4-тиазолил)-2-(метоксиимино) ацетамидо цеф-З-ем - 2-карбоновой кислоты, син-изомера.
Вводят 92 мг 3-карбамоилоксиметил-7-С2-(2-амино-4-тиазолил)-2-(метоксиимино)ацетамидоДцеф-З-ем-4-карбоновой кислоты, синизомера, полученного в примере 5, в О,2 мл дистиллированной воды. Повторно добавляют небольшими количествами 12 мг кислого карбоната натрия. Раствор постепенно растворяется. Поглощает его 2,4 мл ацетона и растирают. Наблюдается образование резины, которую декантиру,ют и поглощают 2,4 лл ацетона, растирают и перемешивают 10 мин при комнатной температуре. Получают фрацию А. Добавляют 2,4 мл ацетона к маточным растворам, растирают и перемешивают 10 мин при комнатной температуре. Получают фракцию Б. Соединяют фракции Д и Б и последовательно замешивают с 0,2 Г4л этанола, 0,2 МП изопропилового эфира и 0,2 мл ацетона. Помещают в сушильный шкаф до достижения постоянного веса и получают 65 мг белого порошка, т.пл. 272С, R 0,16 (элюен :этилацетат:уксусная кислота:вода 80;15:5) .
Формула изобретения
Способ получения ПрОИЗВОДНЕЛХ
З-карбамоилоксиметил-7-аминотиазолилацетамидоцеф-3-ем-4-карбоновойкислоты общей формулы
.«е
s-S
Т Н-Р™/ Х
N
сл,ос-)н
О
2 „ г
OR,
СО,Л
О
виде син-иэомеров,
е R.j- алкильный радикал, насыщенный или ненасыщенный, имеющий 1-4 атома уг-лг-рода;
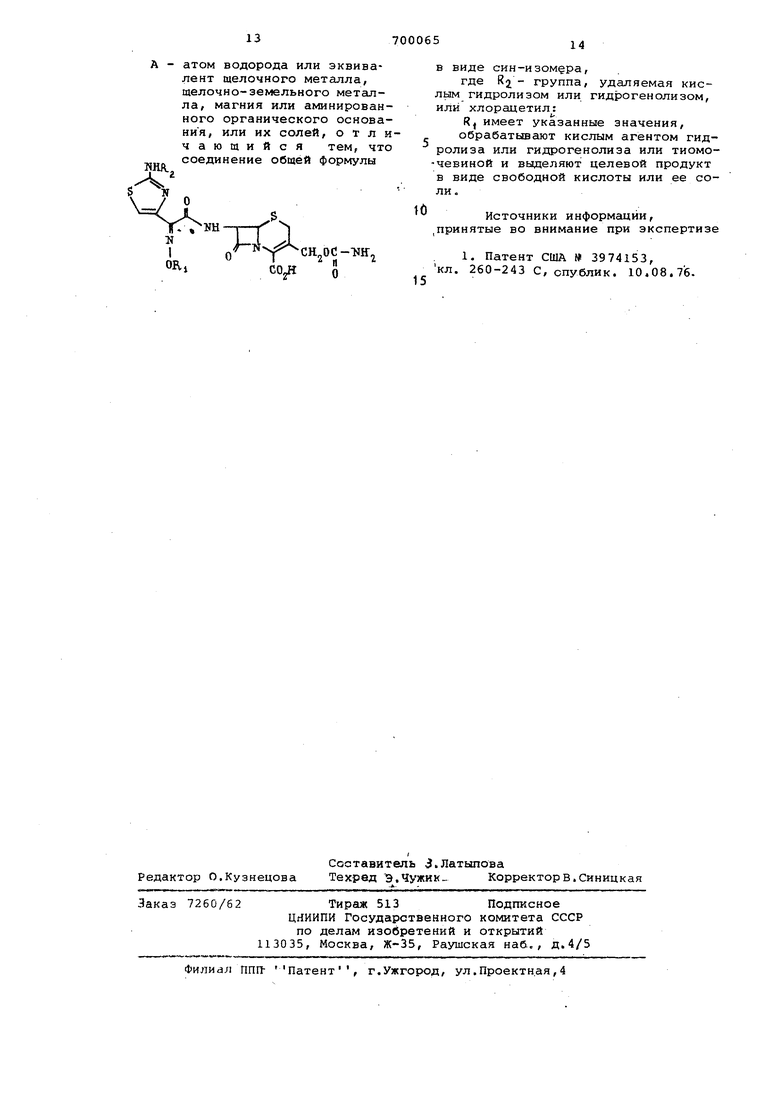
А - атом водорода или эквивалент щелочного металла, щелочно-земельного металла, магния или аминированного органического основания, или их солей, отличающийся тем, что соединение общей формулы
тя
™тгГ1
Jf 1
0 СН„ОС-11Н-,
п о
OR, CO,jH
в виде син-изом§ра,
где Rj - группа, удаляемая кислым гидролизом или гидрогенолизом, или хлорацетил:
R, имеет указанные значения, обрабатывают кислым агентом гидролиза или гидрогенолиза или тиомо-чевиной и выделяют целевой продукт в виде свободной кислоты или ее соли.
Источники информации,
,принятые во внимание при экспертизе
1. Патент США 3974153, кл. 260-243 С, опублик. 10.08.76.
15







Авторы
Даты
1979-11-25—Публикация
1977-08-16—Подача