о
S
сд
со
т
707153 Иэоб1 ётение относится к новым п йзвбдным бициклогептёна, конкретно к 5-НИТРО-7-СИН-(З-оксоокт-1-транс еНил)-вицикло-(2,2,1) -геПл--2-ену ( г - hOj yjcagaHHoe с{3единёнйе является Ьромёжуточным в полном синтезе про станландинов (ПГ) - биологически активных природных соединений. 5-Нитро-7-син- (з-окСоокт-1-тран енил -бицикло-(2,2,1)-гепт-2-ен, ,; ejpo CBQfiCTBa и способ получения - Штёратьфе не описаны. Струйтурным аналогом данного со fiHUCr crt5rtcr/arr«CT л -vrf/-Kri- -ttMatlr - 7- , является 5-хлор-5-ц1 ано-7син-(з-оксоокт-1-транс-енил)-бицик ло-(2,2,1)-гепт-2-ен (И) (1) . J Соединение (11) также является полупродуктом полного сйнггёза простагйайдинрв по схеме Корн-Вроуна H-BuLi (АеО)jP(0)CKjC sHll -с И ()2P(0)CHCCgH i (Ш) л U®; . . П р и мер. По луйёние 5-нйтро7-син- (з-окссокт-1-транс-енил)-бицикло-(2,2,1)-гепт-2-ена. Раствор 7,45 г (О,О34 моль) СВё жепе ёгнанного диметил-2-оксогептилфлсфоната в 70 мл абсолютирован гр Диметоксиэтана охлаждаиот смесью лbjia с хлористым кальцием до -20°С и добаЪляют за 15 мин 35 мл (о,О35 моль) 1н. раствора Нтиляития в гексане. Реакционную емёсь перемешивают 15 мин, затем добавляют 3,4 г (0,024 моль) 5-нитрО-7-син-формил-бицикло- (2,2, 1 .гМа в 40 мл абсолютированного диметрксиэтана при . rip Окончании прибавления смесь ; пёреМешивайт еще 14 ч, постепенно првыйая тёмпе ратурУ ДР крмнатнрй, : нейтрализуют воДныМ раствором уксу ной Йй&лоты,УпЙ| ивают в вакууме и остаток распределяют между 120 мл тЩЙё 8 1э;Метилена мл,насы ; й й Нй«
..
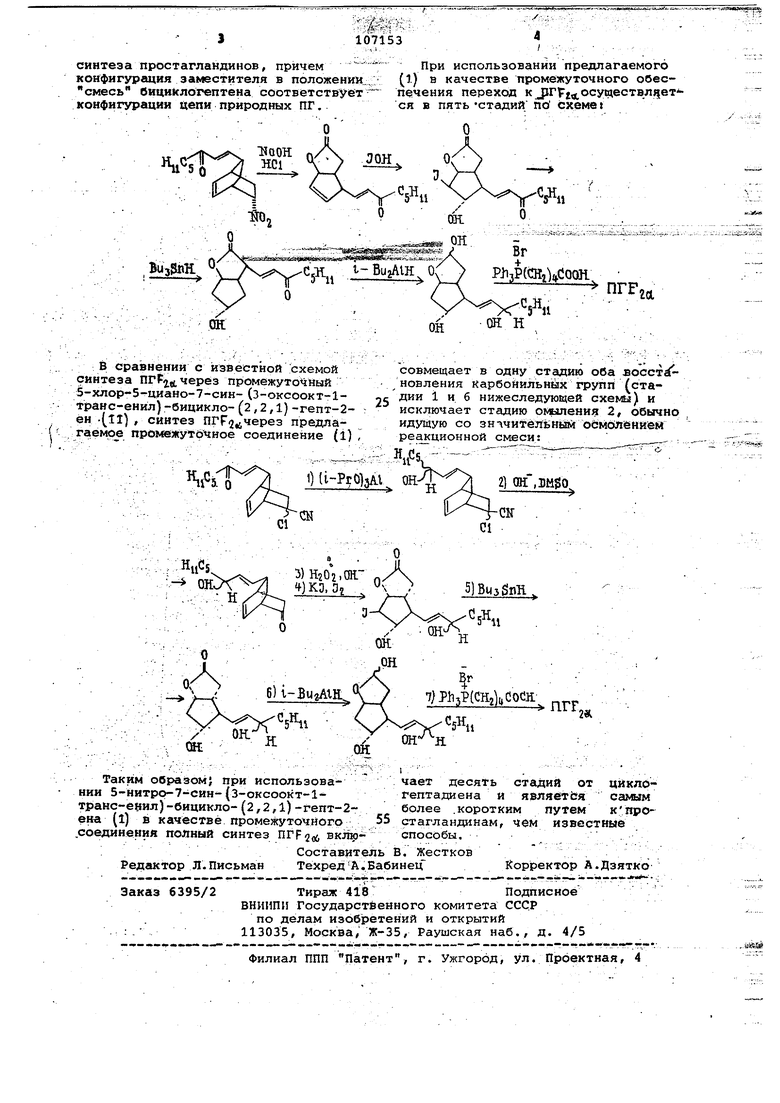
:jJ-i4 e.) иобеспечивает переход к природному простагландйну семь стадий., Цель изобретения - расширение ассортимента полупролуктов пЬлного Синтеза простагландинов и их анало-: гов, позволйювдих упростить схему полного синтеза простагландиЬов, , Цель Достигается 5-нитро-7-синУ-рксоокт-1-транс-енил)-6ир1ИКло- 2, 2,1 -гёпт-2-енбМ формулы Г11. По сравнению с известным 5-хлор-5-циаНО-7-СИН-(З-рксоокт -1-транс-енил)бицикло-(2,2Д)-гепт-2-еном (II) лТредлагаемое соединение обеспечиваё.т б(ЗЛеё переход к биологи40cj H активН1Ф1 ПГ. Кроме того, по ЬравнеИию с синтезом аналога (и) из циклопентадиена, синтез предлагаемого соединения (1) из того же исходного вещества осуществляется с препаративным выходом ив услови,i --w«- i -. - --;-..i: . l я1с, легко, рёализуегллх в препаратив- i ном и прс олшленном масштабе (нетоксичные реагенты, те ературы, близкие к комнатным. Спасоб попученяя 5-нитро-7-син(з-оксоокт-1-Транс-енил)-бицикло(2,2,1)-гепт-2-ена (1) основан на известной реа1сции присоединения диметил-2-б1КЙ6гёптилфосфоната (111) . по SHfTHry-XopiHepy к карбонильному среДинению,В данном случае, ,к 5-нитро-7-син-фЪрмилбицикЛр-(2,2,1) гёпт-2-ену (1У)23. Процесс осуществляют по схеме . V5 О «енНого раствора хлористого натрия. водйую чгасть ёкдтрагируют хлористым ь№ТИйейсмУ ты ванйя И упар11«айия хроматографиpj на силикагеле Л 100/160 (И , продукт смесью растворите-: лей 6 соотнсшёнии хлористый метилен: гексан-1:3 с 50% ацетона. Весь синтез прбйодят в атмосфере аргона. После очистки получают 3,0 г (бО%) хроматографически чистого 5-нйтрр-7-син-(3-оксо(Экт-1-трансен л бицикло-(2,2,1)-гепт-2-ена (l) , RI 0,66 (пластинки Силуфол, система гексан:ацетон 5:1). ИК-спектр, CM-V984(5c.cTpcbic 1385, 1548 () i675(y ) , 3072() {Моя.вес (масс-спектррметрически 263. Вычислено для С15 263. 5-Нитрр-7-снн-(3-оксоокт-1-трансенил) -бицикло- (2, 2,1) -гепт-2-ен является полупродуктом прлногь
5-НИТРО-7-СИН-
| Печь для непрерывного получения сернистого натрия | 1921 |
|
SU1A1 |
| Brown Е.'б | |||
| , LMley T.J | |||
| Кипятильник для воды | 1921 |
|
SU5A1 |
Авторы
Даты
1983-02-15—Публикация
1978-09-20—Подача